An ideal test to evaluate the inflammatory burden in ulcerative colitis is still an unmet need. Fecal calprotectin (FCP) and C-reactive protein (CRP) have significant limitations. Plasma calprotectin (PC) seems to be promising in inflammatory diseases, but its value in IBD is still to be determined. Our aim was to assess whether PC correlates with inflammatory activity in UC.
MethodsProspective single center cohort study. Consecutive patients previously diagnosed with UC undergoing endoscopy were included (June 2021–September 2022). Demographic, clinical, analytical (CRP, PC and FCP), endoscopic and histologic data was collected at the time of colonoscopy. PC was assessed with Gentian Calprotectin Immunoassay and, in a subgroup of patients, also with QUANTA Flash Circulating Calprotectin from INOVA.
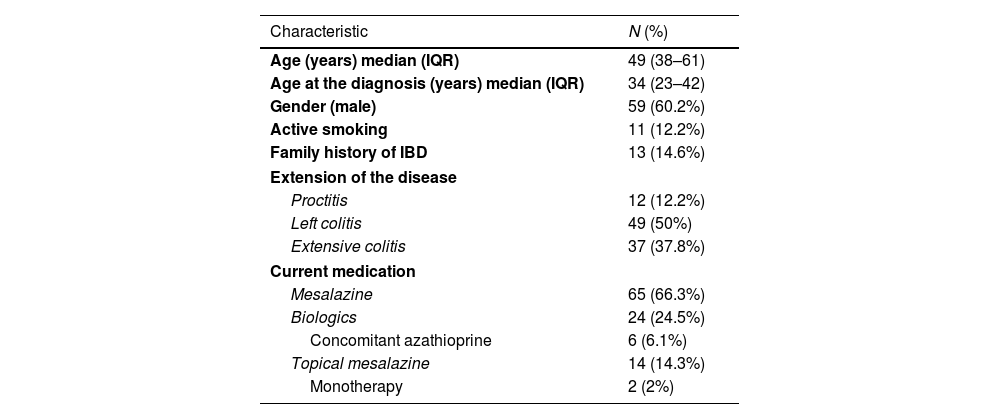
ResultsInclusion of 98 patients (60.2% male) with a median age 49 (38–61) years. The extent of colitis was distal in 12 (12.2%), left-sided in 49 (50%), and extensive in 37 (37.8%). Mesalazine was taken by 65 (66.3%) patients, with biologic monotherapy used in 24 (24.5%) and combination therapy in 6 (6.1%). Clinical, endoscopic and histological remission were detected, in 56 (57.1%), 48 (49%) and in 55 (56.1%) patients, respectively.
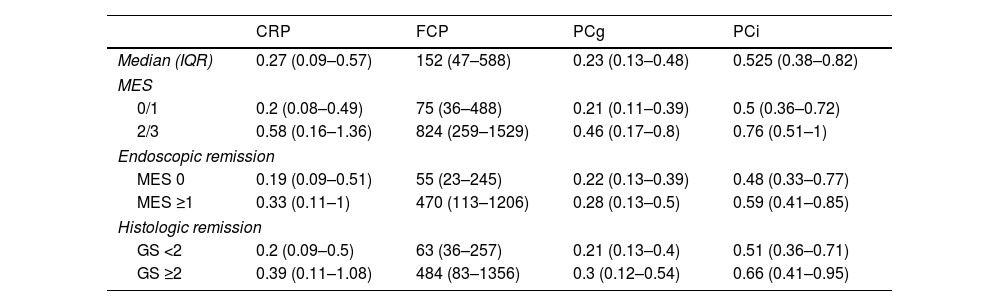
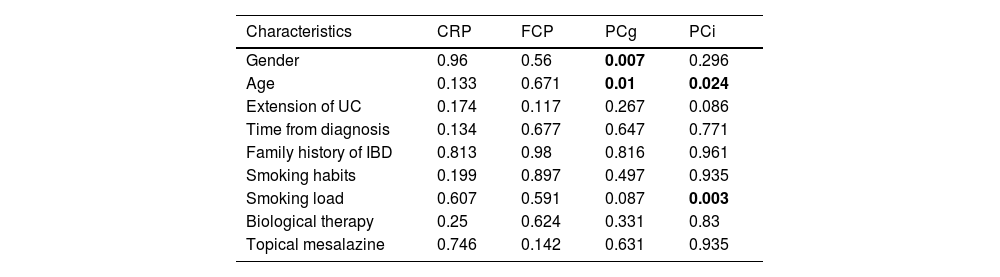
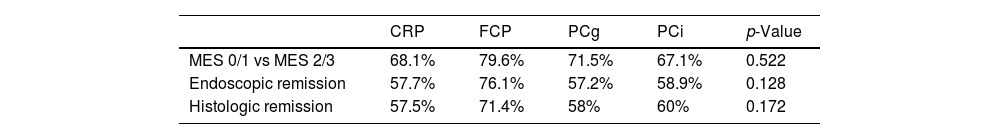
Comparing MES 0/1 vs MES 2/3, a statistically significant difference was found with PC, CRP and FCP. Concerning endoscopic (MES=1) and histological (GS<2) remission, FCP was the only biomarker able to detect these outcomes. PC (Gentian) and PCi (INOVA) were highly correlated with CRP.
ConclusionPC has low value in distinguishing patients in remission from patients with endoscopic or histologic activity in UC. This essential role must continue be played by FCP.
Existe la necesidad de disponer de un examen ideal para evaluar la carga inflamatoria en la colitis ulcerosa (CU). La calprotectina fecal (FCP) y la proteína C reactiva (PCR) presentan limitaciones significativas. La calprotectina plasmática (PC) parece prometedora en enfermedades inflamatorias, pero su valor en la enfermedad inflamatoria intestinal aún está por determinarse. Nuestro objetivo fue valuar si la PC se correlaciona con la actividad inflamatoria en la CU.
MétodosEstudio de cohortes prospectivo en un solo centro. Se incluyeron pacientes consecutivos previamente diagnosticados de CU mediante endoscopia (junio 2021-septiembre 2022). Se recopilaron datos demográficos, clínicos, analíticos (PCR, PC y FCP), endoscópicos e histológicos en el momento de la colonoscopia. Se evaluó la PC con el inmunoensayo de calprotectina Gentian y, en un subgrupo de pacientes, también con QUANTA Flash Circulating Calprotectin de INOVA.
ResultadosUn total de 98 pacientes fueron incluidos (60,2% hombres), con una edad media de 49 (38-61) años. La extensión de la colitis fue distal en 12 (12,2%), izquierda en 49 (50%) y extensa en 37 (37,8%). Mesalazina fue tomada por 65 (66,3%) pacientes, con monoterapia biológica en 24 (24,5%) y terapia combinada en 6 (6,1%). Se detectó remisión clínica, endoscópica e histológica, respectivamente, en 56 (57,1%), 48 (49%) y 55 (56,1%) pacientes.
Al comparar MES 0/1 vs. MES 2/3, se encontró una diferencia estadísticamente significativa con PC, PCR y FCP. En cuanto a la remisión endoscópica (MES=1) e histológica (GS≤2), la FCP fue el único biomarcador capaz de detectar estos resultados. PC (Gentian) y PC (INOVA) mostraron una alta correlación con la PCR.
ConclusiónLa PC tiene poco valor para distinguir a los pacientes en remisión de los pacientes con actividad endoscópica o histológica en la CU. Este papel esencial debe seguir siendo desempeñado por la FCP.