Comparar las características de los pacientes con enfermedad de Parkinson avanzada en tratamiento con infusión intestinal continua de levodopa-carbidopa (IICLC) y los datos de efectividad y seguridad de IICLC entre diferentes comunidades autónomas (CC. AA.).
MétodosEstudio longitudinal observacional y retrospectivo. Se incluyeron 177 pacientes de 11 CC. AA. que iniciaron tratamiento con IICLC entre enero de 2006 y diciembre de 2011. Se compararon las características clínicas y demográficas, las variables de efectividad (cambios en el tiempo OFF, ON con y sin discinesias discapacitantes, cambios en la escala de Hoehn y Yahr y puntuación de la Unified Parkinson's Disease Rating Scale, síntomas no motores e Impresión Clínica Global) y seguridad (acontecimientos adversos), y la tasa de suspensión de IICLC.
ResultadosSe hallaron diferencias significativas entre las CC. AA. en diversas variables basales: duración de la enfermedad hasta el inicio de IICLC, tiempo OFF (34,9-59,7%) y ON (con o sin discinesias; 2,6-48,0%), Hoehn y Yahr en ON, Unified Parkinson's Disease Rating Scale-III en ON y OFF, presencia de≥4 síntomas motores y dosis de IICLC. En el seguimiento (>24 meses en 9 de 11 CC. AA.) hubo diferencias significativas en el porcentaje de tiempo OFF, tiempo ON sin discinesias discapacitantes, frecuencia de acontecimientos adversos e Impresión Clínica Global. La tasa de suspensión fue de entre 20-40% en todas las CC. AA., excepto en 2 (78 y 80%).
ConclusionesEste estudio muestra una amplia variabilidad en la selección de los pacientes y en la efectividad y seguridad de IICLC entre las diferentes CC. AA. Podrían influir las características basales de los pacientes, la disponibilidad de un equipo multidisciplinar y la experiencia clínica.
To compare the characteristics of patients undergoing treatment with continuous intestinal infusion of levodopa-carbidopa (CIILC) for advanced Parkinson's disease and the data on the effectiveness and safety of CIILC in the different autonomous communities (AC) of Spain.
MethodsA retrospective, longitudinal, observational study was carried out into 177 patients from 11 CAs who underwent CIILC between January 2006 and December 2011. We analysed data on patients’ clinical and demographic characteristics, variables related to effectiveness (changes in off time/on time with or without disabling dyskinesia; changes in Hoehn and Yahr scale and Unified Parkinson's Disease Rating Scale scores; non-motor symptoms; and Clinical Global Impression scale scores) and safety (adverse events), and the rate of CIILC discontinuation.
ResultsSignificant differences were observed between CAs for several baseline variables: duration of disease progression prior to CIILC onset, off time (34.9-59.7%) and on time (2.6-48.0%; with or without disabling dyskinesia), Hoehn and Yahr score during on time, Unified Parkinson's Disease Rating Scale-III score during both on and off time, presence of≥ 4 motor symptoms, and CIILC dose. Significant differences were observed during follow-up (> 24 months in 9 of the 11 CAs studied) for the percentage of off time and on time without disabling dyskinesia, adverse events frequency, and Clinical Global Impression scores. The rate of CIILC discontinuation was between 20-40% in 9 CAs (78 and 80% in remaining 2 CAs).
ConclusionsThis study reveals a marked variability between CAs in terms of patient selection and CIILC safety and effectiveness. These results may have been influenced by patients’ baseline characteristics, the availability of multidisciplinary teams, and clinical experience.
El tratamiento con levodopa es en la actualidad el gold standard de la terapia farmacológica para la enfermedad de Parkinson (EP)1. La levodopa ha demostrado en múltiples ocasiones un gran beneficio en la autonomía para el desarrollo de las actividades de la vida diaria y la calidad de vida de los pacientes con EP. Por el contrario, uno de los inconvenientes es el desarrollo de fluctuaciones motoras y discinesias a los pocos años de su inicio2–4. Estas complicaciones son difícilmente controlables con los tratamientos convencionales disponibles en la actualidad, deteriorándose enormemente la calidad de vida del paciente5. La infusión intraintestinal continua de gel de levodopa-carbidopa (IICLC) se desarrolló con el objetivo de reducir estos efectos adversos al evitar la estimulación dopaminérgica pulsátil asociada a la levodopa oral6. Diversos estudios han mostrado que la IICLC es una terapia eficaz7,8, efectiva9–11 y segura7–11, que mejora la calidad de vida7–11 y el grado de autonomía7–9 de los pacientes, y constituye en la actualidad una alternativa terapéutica para reducir las complicaciones motoras en pacientes con EP en estado avanzado5,8,9,12.
En España, la IICLC está aprobada desde el año 2006 y, aunque hay guías publicadas13 sobre la implementación y la utilización de esta terapia en los pacientes con EP avanzada, su uso es individualizado y está condicionado por diversos factores como la experiencia del centro y/o el personal, los recursos disponibles, la aplicación de protocolos internos o aspectos de gestión sanitaria (transferida a las comunidades autónomas [CC. AA.]), existiendo probablemente variabilidad en su manejo. Además, existen pocos datos de las características de los pacientes con EP avanzada tratados con IICLC en España y de la efectividad, la seguridad y la tolerabilidad de dicha terapia. La presente investigación constituye un subanálisis del estudio E-DUO14 (estudio retrospectivo multicéntrico de efectividad y seguridad de la IICLC en España), cuyo objetivo fue comparar las características de los pacientes seleccionados para recibir este tratamiento y los datos de efectividad y seguridad de la IICLC entre las diferentes CC. AA. que participaron.
Pacientes y métodosSe realizó un estudio observacional longitudinal, abierto, multicéntrico y retrospectivo en el que participaron 18 hospitales de 11 CC. AA. El estudio fue aprobado por los comités de ética de todos los centros y se llevó a cabo de conformidad con los principios de la Declaración de Helsinki. Se obtuvo el consentimiento informado de todos los sujetos participantes, excepto de los que habían fallecido antes de iniciarse el estudio.
Se incluyeron pacientes consecutivos con diagnóstico de EP de acuerdo con los criterios del MRC London Neurodegenerative Diseases Brain Bank15, en estado avanzado, que hubieran comenzado el tratamiento con IICLC entre enero de 2006 y diciembre de 2011 (siguieran o no en tratamiento en el momento de la inclusión). Los participantes debían haber sido evaluados durante al menos 11 meses por su neurólogo en el mismo centro. Todos los centros participantes debían tener una experiencia mínima con IICLC de≥5 pacientes.
Variables y método de recogida de datosSe define momento basal como aquel en el que el paciente comienza el tratamiento con IICLC, y visita de inclusión (visita V1) como aquella en la que el paciente es incluido en el estudio.
En el momento basal se obtuvieron, a partir de la historia clínica de los pacientes, sus características sociodemográficas, las características de la enfermedad, los tratamientos previos para la EP, los tratamientos concomitantes y la información del tratamiento con IICLC (dosis y horas al día de infusión). El investigador evaluador de cada centro estableció si, a su criterio, el paciente en situación basal podría haber sido candidato a otra terapia de segunda línea. En la visita V1, a través de cuestionarios y una evaluación clínica, se obtuvieron los datos sobre la evolución de la EP, y la efectividad y la seguridad del tratamiento con la IICLC. También en dicha visita se recogió información sobre la dosis y las horas al día de infusión.
Para definir las características de la EP del paciente y la efectividad del tratamiento, se recogieron, en el momento basal y en la visita V1, el estadio de Hoehn y Yahr (H&Y)16 en ON y en OFF, el porcentaje del tiempo diario en ON sin discinesias discapacitantes, en ON con discinesias discapacitantes y el porcentaje de tiempo en OFF aplicando la Unified Parkinson's Disease Rating Scale (UPDRS)17 parte iv, puntuación en la UPDRS parte iii en ON y en OFF, cambio experimentado (en V1 respecto al momento basal V0) en diferentes síntomas motores y no motores mediante escala con 7 opciones (1: gran empeoramiento; 2: empeoramiento moderado; 3: empeoramiento leve; 4: sin cambios; 5: mejoría leve; 6: mejoría moderada; 7: gran mejoría) y cambio en la impresión clínica global (CGI) en V1 respecto al momento basal según el criterio del neurólogo y del paciente.
Para valorar la seguridad se recogieron los acontecimientos adversos (AA) relacionados con el tratamiento y los datos de abandono de la IICLC, si bien los resultados que presentamos se centran en los AA serios. La clasificación de los AA fue realizada por los neurólogos según categorías establecidas: 1) relacionado con LD; 2) relacionado con la técnica, o 3) relacionado con el dispositivo. Si el AA se clasificaba como relacionado con LD, entonces debía indicar la relación de causalidad (definitiva, probable o posible).
Análisis estadísticoEl análisis estadístico de las variables de efectividad se realizó en la población total de pacientes incluidos que seguían en tratamiento con IICLC en la visita V1, mientras que los datos de seguridad se analizaron sobre la población global (incluyendo los que abandonaron el tratamiento antes de la visita V1). Se realizó un análisis descriptivo en el que los datos se expresaron como frecuencias y proporciones en el caso de las variables categóricas y discretas, y como media±desviación estándar o mediana con rango intercuartílico [RIC], según fuera apropiado, en el caso de las variables continuas. Se compararon los estadísticos máximos y mínimos mediante el test exacto de Fisher, el test de Wilcoxon o el de la t de Student, según correspondiera. Se tuvieron en cuenta las 11 CC. AA. participantes en el estudio para establecer las comparaciones entre ellas. Se definió como variable primaria de eficacia con respecto a la efectividad de la IICLC la reducción en la media del porcentaje de tiempo OFF, considerándose para el cálculo la media del rango en el ítem 39 del UPDRS-IV: 1) 0%; 2) 1-25%; 3) 26-50%; 4) 51-75%; 5) 76-100%. El grado de mejoría experimentado en síntomas motores y no motores preseleccionados (escala de 7 puntos) fue expresado de forma simplificada como 1-3 puntos=mejoría, 4=sin cambios o 5-7=empeoramiento. Todos los test fueron de 2 colas y se consideró el valor de p≤0,05 como estadísticamente significativo. Todos los análisis estadísticos se realizaron con el paquete SAS v9.2 (SAS Institute, Cary, NC, EE. UU.).
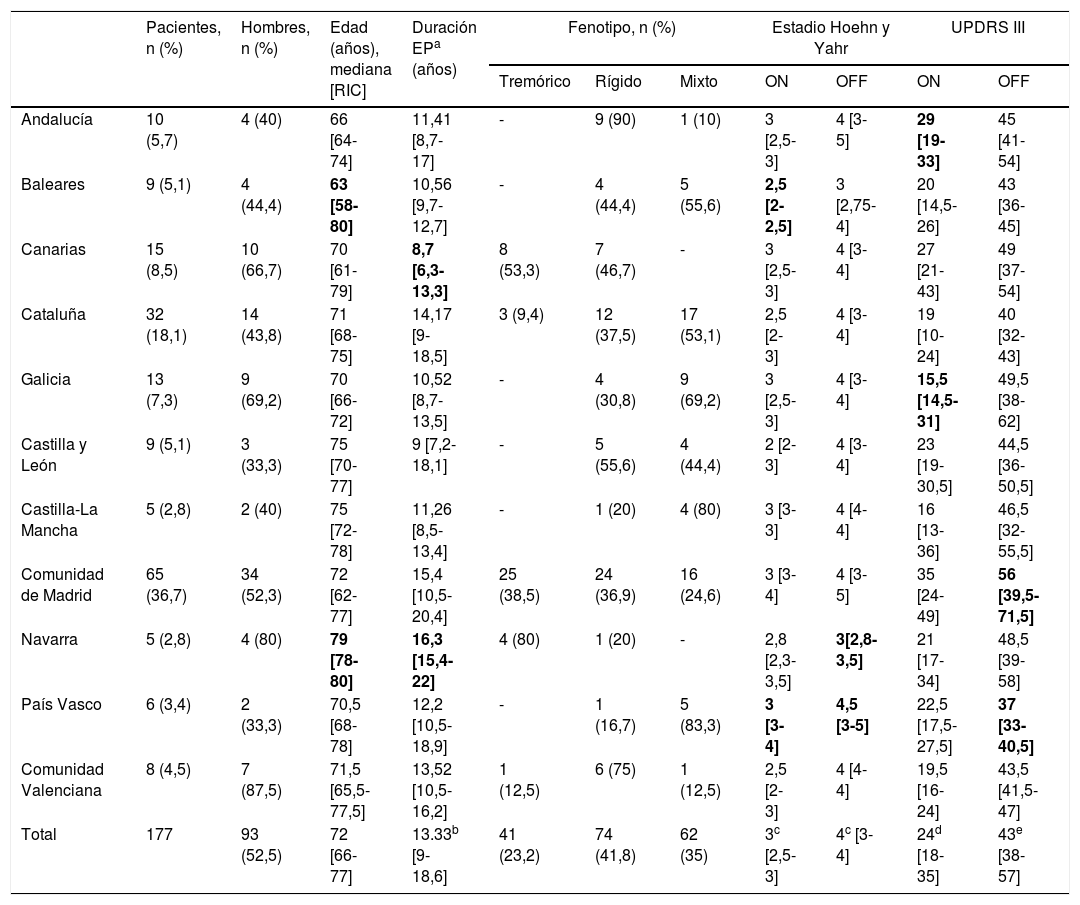
ResultadosSe seleccionaron inicialmente 185 pacientes con EP avanzada, pero 8 fueron excluidos por desviaciones del protocolo. La muestra final se compuso de 177 pacientes evaluables que habían iniciado tratamiento con IICLC en el periodo establecido. En el momento de la selección, los pacientes habían estado en tratamiento con IICLC durante una mediana de 34,7 meses (RIC 18,9-49 meses). La tabla 1 resume la distribución de los pacientes por CC. AA. y las características clínicas y demográficas en el momento basal. Con respecto a la edad, aunque hubo diferencias por CC. AA., no fueron significativas (p=0,204). La mediana de duración de la EP cuando los pacientes iniciaron IICLC fue>10 años en 9 de las 11 CC. AA., observándose diferencias significativas entre Navarra y Canarias (p=0,0015).
Datos clínicos y demográficos en el momento basal de los pacientes en el inicio de la infusión intestinal continua de levodopa-carbidopa
| Pacientes, n (%) | Hombres, n (%) | Edad (años), mediana [RIC] | Duración EPa (años) | Fenotipo, n (%) | Estadio Hoehn y Yahr | UPDRS III | |||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Tremórico | Rígido | Mixto | ON | OFF | ON | OFF | |||||
| Andalucía | 10 (5,7) | 4 (40) | 66 [64-74] | 11,41 [8,7-17] | - | 9 (90) | 1 (10) | 3 [2,5-3] | 4 [3-5] | 29 [19-33] | 45 [41-54] |
| Baleares | 9 (5,1) | 4 (44,4) | 63 [58-80] | 10,56 [9,7-12,7] | - | 4 (44,4) | 5 (55,6) | 2,5 [2-2,5] | 3 [2,75-4] | 20 [14,5-26] | 43 [36-45] |
| Canarias | 15 (8,5) | 10 (66,7) | 70 [61-79] | 8,7 [6,3-13,3] | 8 (53,3) | 7 (46,7) | - | 3 [2,5-3] | 4 [3-4] | 27 [21-43] | 49 [37-54] |
| Cataluña | 32 (18,1) | 14 (43,8) | 71 [68-75] | 14,17 [9-18,5] | 3 (9,4) | 12 (37,5) | 17 (53,1) | 2,5 [2-3] | 4 [3-4] | 19 [10-24] | 40 [32-43] |
| Galicia | 13 (7,3) | 9 (69,2) | 70 [66-72] | 10,52 [8,7-13,5] | - | 4 (30,8) | 9 (69,2) | 3 [2,5-3] | 4 [3-4] | 15,5 [14,5-31] | 49,5 [38-62] |
| Castilla y León | 9 (5,1) | 3 (33,3) | 75 [70-77] | 9 [7,2-18,1] | - | 5 (55,6) | 4 (44,4) | 2 [2-3] | 4 [3-4] | 23 [19-30,5] | 44,5 [36-50,5] |
| Castilla-La Mancha | 5 (2,8) | 2 (40) | 75 [72-78] | 11,26 [8,5-13,4] | - | 1 (20) | 4 (80) | 3 [3-3] | 4 [4-4] | 16 [13-36] | 46,5 [32-55,5] |
| Comunidad de Madrid | 65 (36,7) | 34 (52,3) | 72 [62-77] | 15,4 [10,5-20,4] | 25 (38,5) | 24 (36,9) | 16 (24,6) | 3 [3-4] | 4 [3-5] | 35 [24-49] | 56 [39,5-71,5] |
| Navarra | 5 (2,8) | 4 (80) | 79 [78-80] | 16,3 [15,4-22] | 4 (80) | 1 (20) | - | 2,8 [2,3-3,5] | 3[2,8-3,5] | 21 [17-34] | 48,5 [39-58] |
| País Vasco | 6 (3,4) | 2 (33,3) | 70,5 [68-78] | 12,2 [10,5-18,9] | - | 1 (16,7) | 5 (83,3) | 3 [3-4] | 4,5 [3-5] | 22,5 [17,5-27,5] | 37 [33-40,5] |
| Comunidad Valenciana | 8 (4,5) | 7 (87,5) | 71,5 [65,5-77,5] | 13,52 [10,5-16,2] | 1 (12,5) | 6 (75) | 1 (12,5) | 2,5 [2-3] | 4 [4-4] | 19,5 [16-24] | 43,5 [41,5-47] |
| Total | 177 | 93 (52,5) | 72 [66-77] | 13.33b [9-18,6] | 41 (23,2) | 74 (41,8) | 62 (35) | 3c [2,5-3] | 4c [3-4] | 24d [18-35] | 43e [38-57] |
EP: enfermedad de Parkinson; RIC: rango intercuartílico; UPDRS: Unified Parkinson's Disease Rating Scale.
En negrita se destacan los valores máximos y mínimos de algunas variables.
Dentro del grupo de pacientes que abandonaron la terapia, el tiempo medio hasta su retirada osciló entre una mediana de 39,1 meses en la Comunidad Valenciana (RIC 23,5-60,3] (n=8) y una de 2,8 meses (RIC 2,3-3,3] (n=6) en el País Vasco (p=0,08).
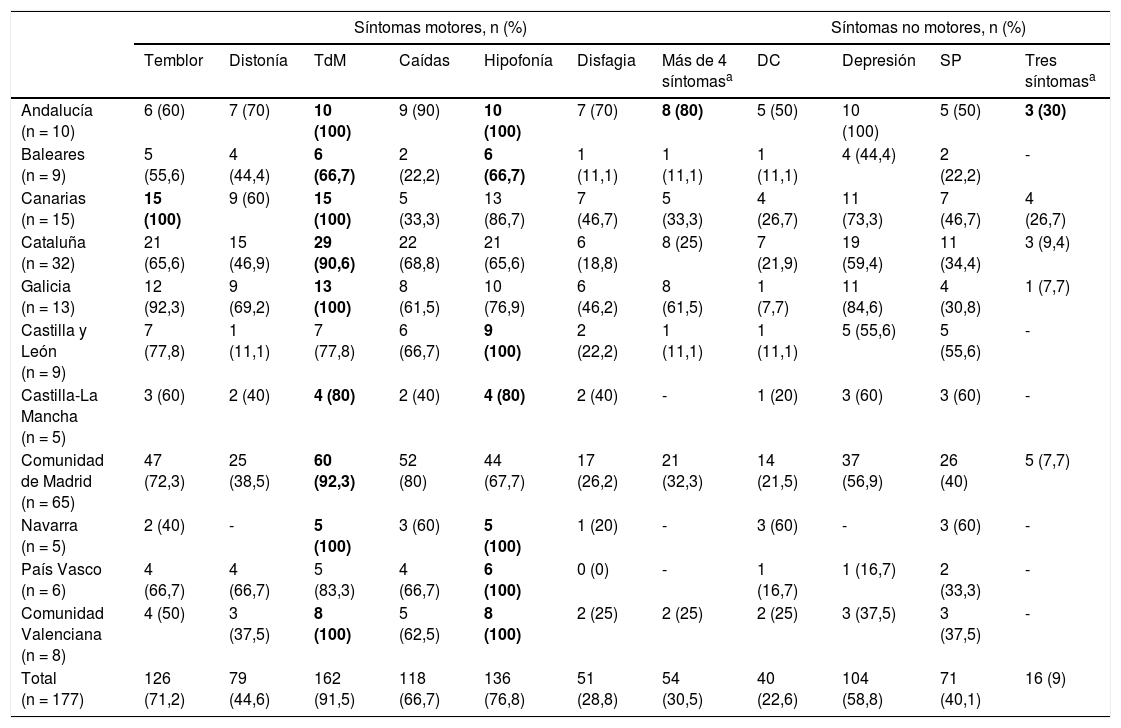
Características clínicas de los pacientes que iniciaron IICLCAl inicio, se observaron diferencias significativas entre las CC. AA. en relación con el H&Y en ON (p = 0,0136) y la escala UPDRS-III tanto en ON como en OFF (p < 0,0001) (tabla 1). Los pacientes con un H&Y más alto en ON y OFF correspondieron al País Vasco. La tabla 2 muestra el porcentaje de pacientes en el momento basal con los síntomas motores y no motores preseleccionados. El 100% de los pacientes de 5 CC. AA. presentaban trastornos de la marcha –síntoma más frecuente en todas las CC. AA.– e hipofonía. Andalucía fue la comunidad con mayor proporción de pacientes que presentaban más de 4 síntomas motores (el 80% de los pacientes), diferenciándose significativamente (p = 0,0325) de Baleares, que fue la comunidad con menos (11,1%). Andalucía fue también la comunidad donde más pacientes presentaban los 3 síntomas no motores recogidos en el momento basal (deterioro cognitivo, depresión y síntomas psiquiátricos). En todas las CC. AA. los pacientes habían recibido un mínimo de 3 fármacos orales antes de iniciar la IICLC (mediana 3, RIC 3-4; tabla suplementaria S1), y la causa más frecuente de inicio de dicha terapia fue el incremento del tiempo OFF (media 85,9%), seguido de la falta de respuesta al tratamiento oral (media 63,3%). Un porcentaje muy variable de pacientes cumplían criterios para ser tratados también con apomorfina o estimulación cerebral profunda (tabla suplementaria S1). Las dosis medias de IICLC a nivel global no experimentaron variaciones destacables entre el momento basal y la visita V1, pero sí existieron diferencias significativas entre CC. AA. La dosis basal media osciló entre los 91,5 ± 25,7ml en Navarra y los 61,1 ± 17,3ml en Castilla y León (p=0,0277), y la dosis final, entre los 92,7 ± 23,9ml en Navarra y los 65,1 ± 10,5ml en Castilla y León (p = 0,0459).
Síntomas motores y no motores basales antes de iniciar la infusión intestinal continua de levodopa-carbidopa
| Síntomas motores, n (%) | Síntomas no motores, n (%) | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Temblor | Distonía | TdM | Caídas | Hipofonía | Disfagia | Más de 4 síntomasa | DC | Depresión | SP | Tres síntomasa | |
| Andalucía (n = 10) | 6 (60) | 7 (70) | 10 (100) | 9 (90) | 10 (100) | 7 (70) | 8 (80) | 5 (50) | 10 (100) | 5 (50) | 3 (30) |
| Baleares (n = 9) | 5 (55,6) | 4 (44,4) | 6 (66,7) | 2 (22,2) | 6 (66,7) | 1 (11,1) | 1 (11,1) | 1 (11,1) | 4 (44,4) | 2 (22,2) | - |
| Canarias (n = 15) | 15 (100) | 9 (60) | 15 (100) | 5 (33,3) | 13 (86,7) | 7 (46,7) | 5 (33,3) | 4 (26,7) | 11 (73,3) | 7 (46,7) | 4 (26,7) |
| Cataluña (n = 32) | 21 (65,6) | 15 (46,9) | 29 (90,6) | 22 (68,8) | 21 (65,6) | 6 (18,8) | 8 (25) | 7 (21,9) | 19 (59,4) | 11 (34,4) | 3 (9,4) |
| Galicia (n = 13) | 12 (92,3) | 9 (69,2) | 13 (100) | 8 (61,5) | 10 (76,9) | 6 (46,2) | 8 (61,5) | 1 (7,7) | 11 (84,6) | 4 (30,8) | 1 (7,7) |
| Castilla y León (n = 9) | 7 (77,8) | 1 (11,1) | 7 (77,8) | 6 (66,7) | 9 (100) | 2 (22,2) | 1 (11,1) | 1 (11,1) | 5 (55,6) | 5 (55,6) | - |
| Castilla-La Mancha (n = 5) | 3 (60) | 2 (40) | 4 (80) | 2 (40) | 4 (80) | 2 (40) | - | 1 (20) | 3 (60) | 3 (60) | - |
| Comunidad de Madrid (n = 65) | 47 (72,3) | 25 (38,5) | 60 (92,3) | 52 (80) | 44 (67,7) | 17 (26,2) | 21 (32,3) | 14 (21,5) | 37 (56,9) | 26 (40) | 5 (7,7) |
| Navarra (n = 5) | 2 (40) | - | 5 (100) | 3 (60) | 5 (100) | 1 (20) | - | 3 (60) | - | 3 (60) | - |
| País Vasco (n = 6) | 4 (66,7) | 4 (66,7) | 5 (83,3) | 4 (66,7) | 6 (100) | 0 (0) | - | 1 (16,7) | 1 (16,7) | 2 (33,3) | - |
| Comunidad Valenciana (n = 8) | 4 (50) | 3 (37,5) | 8 (100) | 5 (62,5) | 8 (100) | 2 (25) | 2 (25) | 2 (25) | 3 (37,5) | 3 (37,5) | - |
| Total (n = 177) | 126 (71,2) | 79 (44,6) | 162 (91,5) | 118 (66,7) | 136 (76,8) | 51 (28,8) | 54 (30,5) | 40 (22,6) | 104 (58,8) | 71 (40,1) | 16 (9) |
DC: deterioro cognitivo; SP: síntomas psiquiátricos; TdM: trastornos de la marcha.
En negrita se destacan los síntomas de mayor frecuencia por comunidad autónoma.
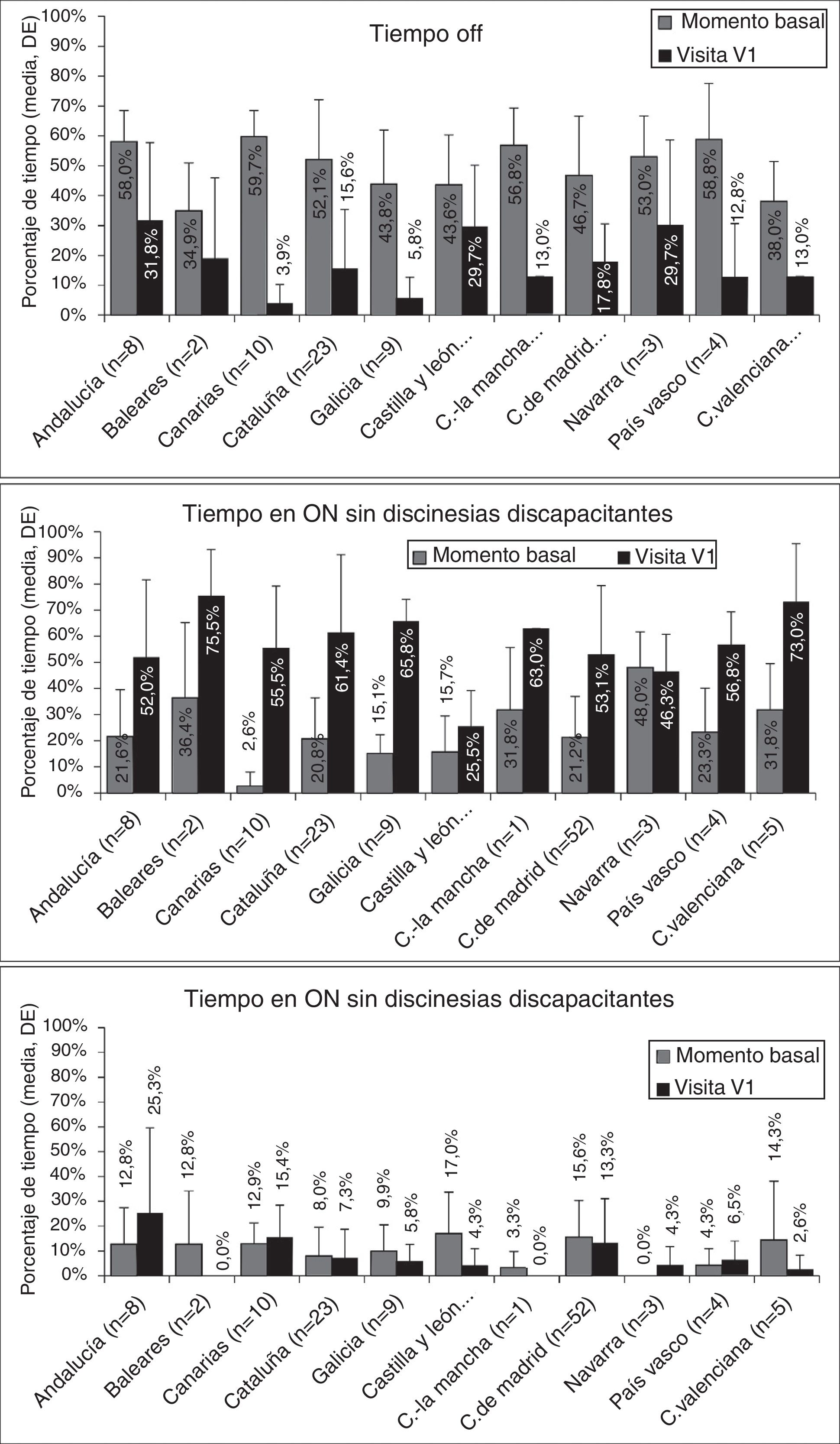
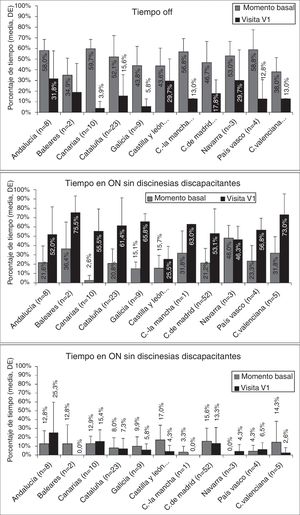
En el momento basal, la media de tiempo OFF superaba en todas las CC. AA. el 33%, con diferencias significativas entre las CC. AA. con datos más extremos (p=0,0024; fig. 1). Igualmente, también se observaron diferencias significativas en cuanto al tiempo medio ON sin discinesias discapacitantes y con discinesias discapacitantes.
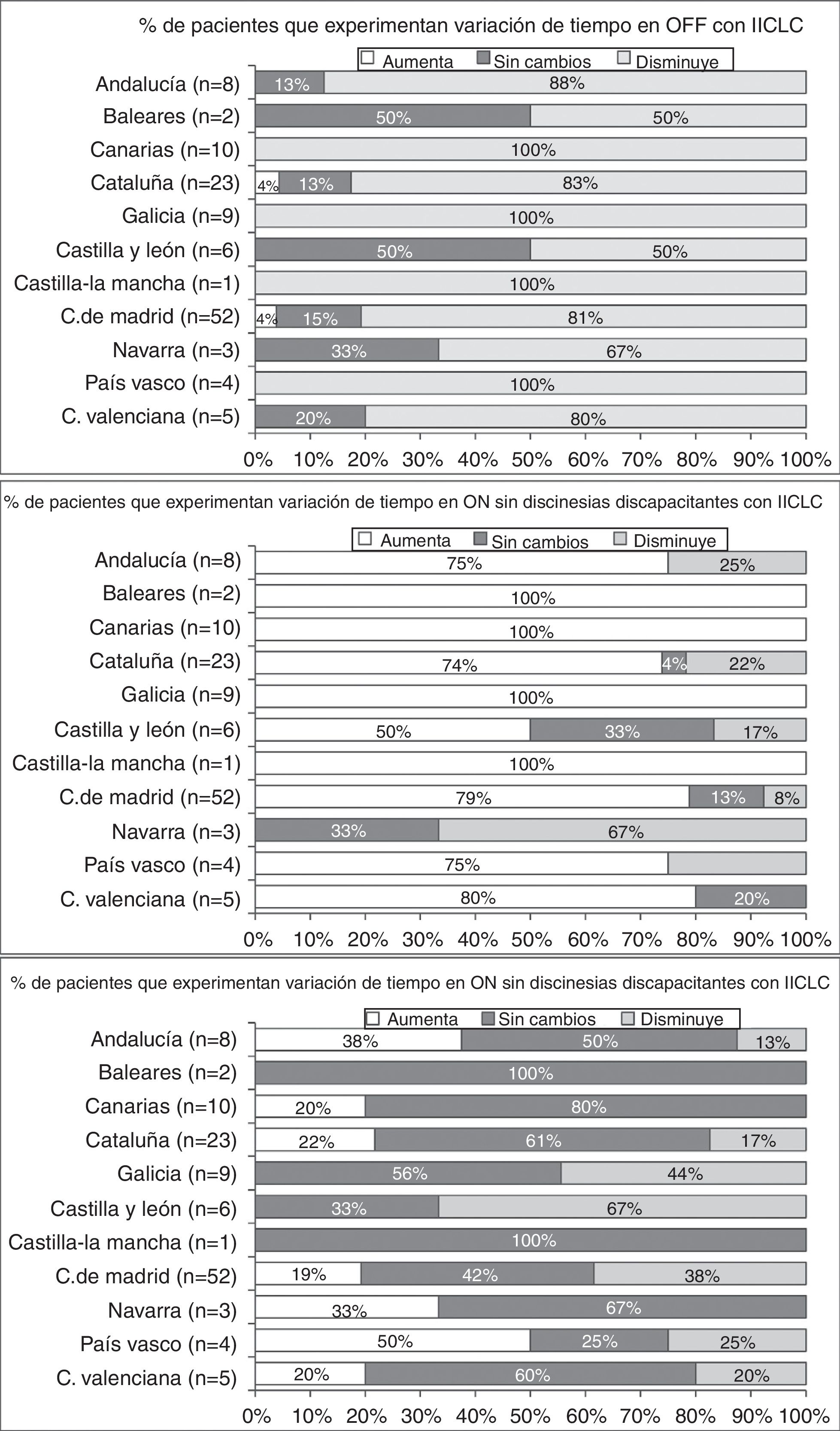
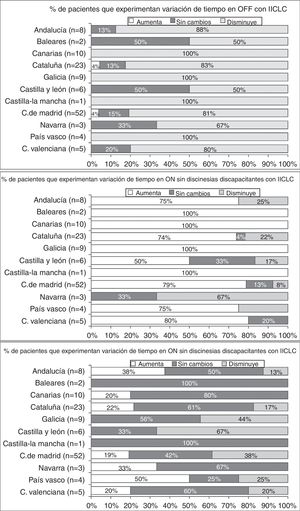
Efectividad de IICLCEn la visita V1, se observó una reducción en el porcentaje de tiempo medio OFF en todas las CC. AA., que se acompañó también (excepto en Navarra) de un incremento en el tiempo medio ON sin discinesias discapacitantes (fig. 1). En la visita V1 hubo diferencias entre CC. AA. en cuanto a la media del tiempo OFF (p=0,0068) y ON (p=0,005). La mayoría de los pacientes experimentaron una reducción del tiempo OFF y un aumento del tiempo ON sin discinesias discapacitantes (fig. 2). Sin embargo, el efecto sobre el tiempo medio ON con discinesias discapacitantes fue más variable (fig. 2), observándose una reducción en 7 CC. AA. y un incremento en el resto (fig. 1, panel inferior).
Con respecto al H&Y (figura suplementaria S1), los pacientes que no presentaron cambios en ON o en OFF fueron mayoría en más de la mitad de las CC. AA. (6/11). La puntuación en la UPDRS-III en ON aumentó en la mayor parte de los pacientes de 7 CC. AA., y la puntuación en OFF disminuyó en la mayoría de los pacientes de otras 7 (figura suplementaria S2). Las tablas suplementarias S2 y S3 muestran el porcentaje de pacientes que presentaron una mejoría, ningún cambio o un empeoramiento para determinados síntomas motores y no motores evaluados, respectivamente, en las diferentes CC. AA.
Finalmente, el CGI, tanto a criterio del neurólogo como del paciente, mostró mejoría en la mayoría de los pacientes de todas las CC. AA., excepto Navarra y Baleares, con una valoración de mejoría por parte del neurólogo en 109 pacientes de 123 de los que se disponía el dato y, por parte del paciente, en 106 (figura suplementaria S3).
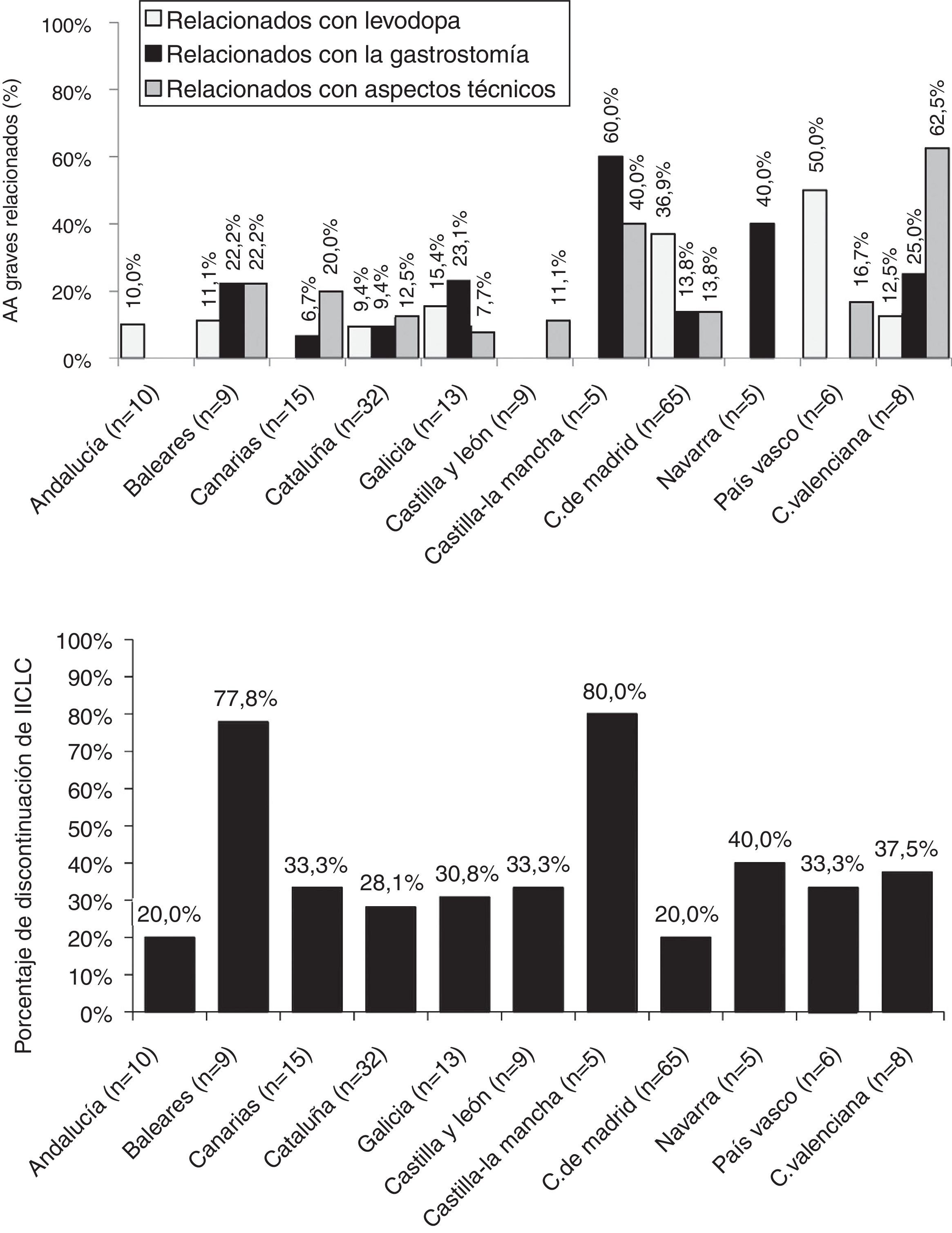
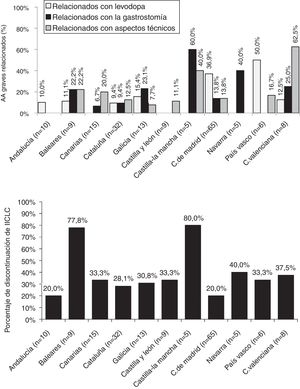
Análisis de seguridadEl porcentaje de AA serios por CC. AA. relacionados con la levodopa o el método de administración fue variable y se muestra en la figura 3. Las tasas de interrupción fueron similares entre las CC. AA., excepto para Baleares y Castilla-La Mancha, en donde resultaron mayores (fig. 3). Los motivos de interrupción prematura de IICLC se detallan en la tabla suplementaria S4.
DiscusiónLa presente investigación constituye un subanálisis del estudio E-DUO, que representa hasta la fecha el que tiene un mayor número de pacientes tratados con IICLC en España14, y muestra en general una variabilidad significativa en cuanto a la selección del candidato, el manejo, la efectividad y la seguridad entre los centros participantes agrupados por CC. AA. Se trata igualmente del primer estudio en el que se analiza el manejo de estos pacientes según la comunidad autónoma a la que pertenece cada centro participante. Esto resulta relevante a la hora de poder comparar resultados y aplicar en el futuro los criterios de manejo que tuvieron resultados más beneficiosos en aquellas CC. AA. en las cuales los pacientes no experimentaron tanto beneficio.
El tratamiento de la EP avanzada es complejo. El agravamiento de los síntomas y la aparición de complicaciones exigen realizar una evaluación minuciosa y plantear la posibilidad de considerar alternativas de tratamiento más intensivas, que no son apropiadas para todos los pacientes18–22. Diversos aspectos que influyen en el éxito del tratamiento comprenden la selección de la alternativa más adecuada para el paciente, la disponibilidad de un equipo de atención multidisciplinar, la experiencia técnica del centro y la curva de aprendizaje. Hay también aspectos de gestión sanitaria, características poblacionales o influencias en la práctica clínica (condicionadas por proximidad geográfica o las sociedades científicas). Todo ello justifica la comparativa entre CC. AA. en el presente estudio.
Una de las primeras cuestiones que no está totalmente aclarada en la actualidad es la clasificación de EP avanzada20 y en qué momento el paciente debe considerarse un candidato adecuado a recibir tratamiento no convencional, ya sea cirugía o infusión continua mediante bomba. Los resultados aquí observados en cuanto al tiempo de evolución están en concordancia con los de otros estudios de enfermos de párkinson tratados con IICLC. En estos, muchos pacientes presentan una duración de la enfermedad de más de 10 años7–11,23–27, aunque llama la atención un tiempo de evolución muy prolongado (mediana de más de 15 años) en Madrid y Navarra. La edad al inicio del tratamiento con IICLC fue superior a la habitualmente reportada en la literatura28, y especialmente elevada (5 pacientes con RIC entre 78 y 80 años) en Navarra. En relación con esto, un subanálisis de esta misma cohorte mostró que los pacientes con un tiempo de evolución menor de 10 años al inicio del tratamiento con IICLC experimentaron una reducción significativamente mayor en el porcentaje del tiempo OFF diario y una menor incidencia de AA serios29. Algunos autores han descrito que una mayor edad se asocia a una mayor tasa de abandonos24,30 y se ha propuesto un inicio más precoz de la terapia con IICLC21,24,30–33, con el objetivo de conseguir mayores beneficios. De hecho, en el presente estudio, en Navarra (pacientes más mayores y con mayor tiempo de evolución) los resultados objetivos (tiempo OFF/ON) y subjetivos (CGI) fueron peores. Sin embargo, el tiempo desde el diagnóstico no necesariamente se correlaciona con la edad, y la duración no siempre se correlaciona con la gravedad de la enfermedad. En el reciente análisis de las características basales de la muestra de pacientes del estudio abierto de fase iii7 (307 pacientes), los pacientes mostraron mejoría independientemente de su edad y de la duración de la enfermedad en el inicio34. Por otra parte, muchos presentaban deterioro cognitivo, depresión u otros síntomas neuropsiquiátricos, dato indicativo de que la IICLC podría, frente a otras alternativas, ofrecer menos restricciones en cuanto a su indicación35,36. De hecho, parte de los pacientes en las diferentes CC. AA. presentaron mejoría en diferentes síntomas motores y no motores, como ya se ha reportado en la literatura. Esto en parte podría deberse a que, con la IICLC, habitualmente se consigue monoterapia (levodopa/carbidopa), y también al mecanismo de acción del fármaco a nivel del sistema nervioso central37–40. Por otro lado, aunque probablemente hay algunos pacientes que se pueden beneficiar de este tratamiento con contraindicación para estimulación cerebral profunda o infusión de apomorfina, una mayor puntuación en el inventario neuropsiquiátrico de Cummings se ha asociado a un mayor riesgo de abandono de la terapia21. En este sentido, Castilla-La Mancha y Navarra (60% de los pacientes con síntomas neuropsiquiátricos, también relacionados con la mayor edad) presentaron la primera y tercera tasa de abandonos. En España, a diferencia de otros estudios de práctica clínica con metodología similar24, la IICLC no fue considerada como la última alternativa por detrás de la estimulación cerebral profunda o la infusión de apomorfina, y esto considerando que un porcentaje importante de pacientes habrían podido recibir otra terapia, según el criterio del neurólogo evaluador.
Se observó mejoría de las complicaciones motoras en todas las CC. AA., excepto Navarra (los pacientes experimentaron una reducción del tiempo OFF, pero no un incremento del tiempo ON sin discinesias discapacitantes), y estos hallazgos están en línea con otros estudios sobre eficacia y/o efectividad de la IICLC7–12,23–25,27,28. Igualmente, un porcentaje muy alto de pacientes y neurólogos reportaron mejoría subjetiva (CGI) con la IICLC: se consideró aproximadamente en 3 de cada 4 de mejoría moderada a gran mejoría. Esto no fue observado en Navarra, donde se registró una menor mejoría objetiva.
Con respecto a la seguridad de la IICLC, un 16% de los pacientes presentaron algún AA serio, con gran variabilidad entre las diferentes CC. AA. Otros estudios han demostrado una buena tolerabilidad a la levodopa administrada en infusión41. El porcentaje de AA relacionados con la medicación (levodopa) fue bajo, excepto en el País Vasco y Madrid. El resto de las complicaciones (relacionadas con la gastrostomía y aspectos técnicos) fueron más frecuentes y variables entre las diferentes CC. AA., algo probablemente condicionado por el nivel de experiencia del equipo o su composición multidisciplinar. En cuanto a la tasa de abandonos, en la mayoría de las CC. AA. esta estaba en un rango similar al descrito en estudios previos (20-30%)24,30,40,42. Finalmente, las mayores tasas de AA serios relacionados con la gastrostomía se dieron en las 2 CC. AA. con los pacientes de mayor edad (Navarra y Castilla-La Mancha).
El presente estudio tiene limitaciones importantes inherentes a su metodología, incluyendo su diseño retrospectivo con periodos de seguimiento variados. Por otra parte, aunque el tamaño muestral global es importante, es pequeño en muchas CC. AA., y esto condiciona los resultados. El fenotipo no fue definido de acuerdo con la literatura43, sino según la percepción del neurólogo investigador. Los datos son del año 2011 y es posible que el manejo haya cambiado debido a una mayor experiencia en España con esta terapia. Finalmente, en algunas CC. AA. había centros con diferente nivel de experiencia (aplicación de protocolos, equipo multidisciplinar, experiencia del neurólogo, gastroenterólogo, etc.) y categoría asistencial (segundo y tercer nivel) u otras características (como el sistema de derivación de pacientes o la mayor presencia de áreas rurales frente a urbanas, etc.) que podrían condicionar los resultados por CC. AA., pero que abren la puerta a plantear otro análisis en función de estos criterios y a conocer las necesidades particulares para alcanzar la mejor calidad asistencial.
En conclusión, el presente estudio muestra una gran variabilidad en cuanto a la selección, el manejo y la respuesta de los pacientes con Parkinson tratados con IICLC en España. En algunas CC. AA. donde la experiencia ha sido menos positiva, es posible que la edad en el inicio fuera un factor a tener en cuenta, pero son necesarios más análisis prospectivos con un mayor número de pacientes.
FinanciaciónAbbVie Spain, S. L. U. financió este estudio, fue responsable del diseño y coordinó la recogida de datos. Asimismo, facilitó el apoyo profesional para el análisis estadístico y el apoyo editorial para la preparación del manuscrito.
AutoríaTodos los firmantes tuvieron acceso sin restricciones a los datos, contribuyeron a su interpretación, revisaron y contribuyeron de forma significativa en el artículo y aprobaron la versión final del manuscrito.
Conflicto de interesesD. Santos-García ha recibido honorarios en el último año de AbbVie, UCB, Zambon, KRKA y Lundbeck para presentaciones formativas, y también ha recibido honorarios de AbbVie por coordinación de ensayos clínicos y en actividades de asesoría. M. J. Catalán ha recibido honorarios de AbbVie y Merz por servicios de consultoría, asesoría, presentaciones e investigación. V. Puente ha recibido honorarios de AbbVie, UCB y Lundbeck por dar cursos y de AbbVie por su participación en actividades de asesoría. F. Valldeoriola ha recibido honorarios de AbbVie, Medtronic y Boston Scientific por actividades de asesoría y charlas. I. Regidor ha recibido ocasionalmente de Medtronic, Boston Scientific y AbbVie la devolución de gastos de viaje y honorarios para charlas en reuniones científicas. P. Mir ha recibido de AbbVie, UCB, Zambon, Allergan y Merz honorarios por actividades de asesoría y charlas. J. M. Arbelo ha recibido honorarios de AbbVie y UCB por actividades de asesoría y charlas. J. C. Parra es empleado de AbbVie y posee acciones u opciones de AbbVie. F. Grandas ha recibido de Merz, AbbVie, UCB y GE Healthcare honorarios por charlas y de AbbVie por su participación en actividades de asesoría.
Los autores agradecen a la Dra. Blanca Piedrafita, de Medical Statistics Consulting, su apoyo editorial en la preparación de este manuscrito.
Parte de los datos de este trabajo se presentaron en forma de póster en la LXVI Reunión Anual de la Sociedad Española de Neurología, en 2014.