Las lesiones arteriales ocultas son frecuentes en casos de traumatismos y los diferentes conflictos militares han permitido observar la evolución de su corrección. En la actualidad se utilizan venas autólogas y politetrafluoroetileno (PTFE) como parches para traumatismos arteriales. Sin embargo, a menudo no se dispone de una vena adecuada en pacientes politraumatizados, y el PTFE tiende a infectarse en las heridas de combate contaminadas. El objetivo de este estudio consiste en evaluar Permacol, un colágeno dérmico porcino, y Alloderm, dermis acelular de cadáver, como alternativas válidas al PTFE con la ventaja potencial de ser utilizados en las heridas contaminadas. La arteriotomía carotídea común en conejos New Zealand White se utilizó como modelo para comparar la corrección mediante parches de Permacol (n=12), Alloderm (n=11) y PTFE (n=13). Se examinó la formación de trombina utilizando un ensayo ELISA para el complejo trombina-antitrombina. Se obtuvieron muestras histológicas para analizar el área de la luz vascular, el diámetro del vaso, el espesor de la íntima, y el grosor de la media. Se llevaron a cabo los estudios anatomopatológicos para comparar las tasas de hiperplasia de la íntima, aneurisma, permeabilidad y formación de trombos. El grupo con Permacol mostró tasas equivalentes de trombos, aneurisma y permeabilidad en comparación con el PTFE. En el grupo con Permacol también se observó un aumento del área luminal, 0,344mm2 (p=0,02) en comparación con el grupo PTFE, 0,204mm2. Así mismo, éste presentó una menor incidencia de hiperplasia de la íntima en comparación con el grupo PTFE, 50,0 frente al 92% (p<0,05). El grupo con Alloderm presentó tasas más elevadas de formación de aneurisma, 63,6% (p=0,004) en comparación con los grupos con PTFE, 0,0%, y Permacol, 8,3%. Además, éste presentó un aumento del grosor de la íntima en la zona del parche, 0,076mm (p=0,18), en comparación con los grupos con PTFE, 0,026mm, y Permacol, 0,024mm. El diámetro del vaso en la zona del parche en el grupo con Alloderm, 1,87mm (p=0,004), fue significativamente mayor que el de los grupos con Permacol, 1,41mm, y PTFE, 1,28mm. Así mismo, el grupo con Alloderm presentó migración leucocitaria alrededor del parche. El ELISA del complejo trombina-antitrombina solamente estuvo elevado en el grupo con PTFE durante el 7.° día del postoperatorio, pero no difirió de forma estadísticamente significativa respecto a los otros grupos. Permacol tiene características que lo hacen una alternativa eficaz frente al PTFE para la corrección mediante arteriotomía con parche en nuestro modelo animal. Son necesarios estudios adicionales para investigar el potencial de Permacol en los traumatismos vasculares. Alloderm no es una alternativa adecuada al PTFE para la corrección mediante arteriotomía con parche.
Las lesiones arteriales ocultas son frecuentes en tiempos de guerra y en traumatismos civiles y se ha observado la evolución de su tratamiento a lo largo del tiempo. En la actual guerra de Irak, los traumatismos vasculares mayores siguen siendo las lesiones principales de los soldados americanos en el campo de batalla1. Estas lesiones suelen ser básicamente traumatismos penetrantes secundarios a artefactos explosivos improvisados y heridas por proyectiles de gran velocidad2. Los traumatismos penetrantes representaron el 90% de los traumatismos vasculares en un amplio informe epidemiológico sobre un importante centro de traumatismos de EE. UU3. Es necesaria una corrección satisfactoria de estas lesiones arteriales traumáticas para lograr el cese de la hemorragia y para facilitar el flujo sanguíneo distal a las extremidades. Los pacientes politraumatizados generalmente necesitan un tiempo de intervención más corto para facilitar la reanimación y la normalización de la hipotermia, la coagulopatía y la acidosis metabólica. El tiempo necesario para reparar formalmente una lesión vascular mediante injerto con interposición de vena safena invertida imposibilita que ésta sea una buena opción debido a la fisiología debilitada y a los tiempos de intervención que necesariamente deben reducirse. En la actualidad, la vena autóloga es el material de elección aceptado como parche para lesiones arteriales en las extremidades inferiores. Sin embargo, en los pacientes con lesiones críticas debe sopesarse la lesión fisiológica producida durante la extracción de la vena frente al uso de un parche alternativo. En los pacientes gravemente lesionados con extremidades destrozadas, es posible que no se disponga de vena para corrección. Con el objeto de reducir los tiempos de intervención, un conducto biológico podría ser la solución en un campo potencialmente contaminado. Este estudio evalúa las propiedades vasculares de dos materiales biológicos como parches vasculares.
Se han utilizado diferentes materiales tisulares como parches arteriales, y todos tienen varias características que los hacen adecuados como material para parches vasculares. Las sustancias inertes populares, como el Dacrón tejido y el politetrafluoroetileno (PTFE), han demostrado ser alternativas seguras a los injertos de venas autólogas. Además, una reciente revisión Cochrane ha demostrado que estos dos tipos de implantes sintéticos tienen una tasa menor de formación de pseudoaneurismas en comparación con los injertos de venas autólogas en las correcciones de la arteria carótida4. Sin embargo, el PTFE se ha asociado con peores resultados en casos de traumatismos, como consecuencia de infecciones y trombosis siendo necesarias, con frecuencia, intervenciones adicionales2. El PTFE debe retirarse en caso de infección activa ya que prolongará la infección de la herida.
El Permacol, colágeno dérmico porcino, es una matriz de colágeno acelular procedente de una fuente de colágeno dérmico porcino que se trata de forma enzimática para retirar los componentes celulares y las proteínas no estructurales, dejando solamente el colágeno y la elastina nativos5. Este entramado se ha utilizado con éxito en correcciones de defectos de tejidos blandos sin que se hayan producido reacciones citotóxicas, genotóxicas, piógenas o de hipersensibilidad6. No se han realizado estudios previos con Permacol como alternativa al PTFE en casos de traumatismo sin temer una futura retirada secundaria a la infección de la herida ya que se ha demostrado que es seguro y eficaz en casos de heridas con infecciones graves7. Como sucede con el PTFE, Permacol puede almacenarse y utilizarse fácilmente, y sus características de manipulación son comparables.
Alloderm, un producto de tejido cutáneo acelular humano, está fabricado mediante un procedimiento patentado que elimina los materiales celulares de la piel de cadáver. Este proceso retiene los componentes de la matriz dérmica intacta, como la elastina, las fibras de colágeno, los proteoglicanos y el entramado vascular8. Alloderm ha demostrado ser un injerto seguro y duradero en reconstrucciones complejas de la pared abdominal y puede utilizarse en heridas contaminadas9,10. Los estudios realizados en animales han demostrado la formación de neovascularización y el crecimiento de tejido con los injertos Alloderm11. Permacol y Alloderm presentan una ventaja clara frente al PTFE en situaciones de campos contaminados, como en el caso de traumatismos o infecciones. Alloderm debe refrigerarse pero, dejando este aspecto de lado, sus características de manipulación son comparables a las de Permacol y PTFE.
Materiales y métodosTodos los procedimientos fueron revisados y autorizados por el Animal Care and Use Committee del centro y se llevaron a cabo en una instalación acreditada por la Association for the Assessment and Accreditation of Laboratory Animal Care, International. La investigación se realizó cumpliendo con los preceptos del Animal Welfare Act y otros estatutos y regulaciones federales en relación con la experimentación animal.
En este estudio se utilizaron un total de 36 conejos macho New Zealand White (Myrtles Rabbitry, Thompson Station, TN) con un peso aproximado de 3,5-4,5kg. Se alojaron en una sala con temperatura controlada y un ciclo lumínico de 12h de luz/oscuridad y fueron alimentados con un pienso estándar para conejos y agua ad libitum. Tras la cirugía fueron alojados de forma individual.
Intervención quirúrgicaSe realizó un abordaje longitudinal de 4cm en el borde anterior del músculo esternoclavicular. Los músculos infrahioideos se retrajeron lateralmente para exponer la vaina carotídea. Se logró la anticoagulación sistémica gracias a la administración de heparina (100 U/kg) en bolos intravenosos antes de la colocación del clampaje y se administró una segunda dosis (50 U/kg) 45min después de su colocación. Tras la anticoagulación, la carótida común se aisló y clampó, y se creó una arteriotomía de 5mm. Este defecto fue reparado mediante un parche de 2 x 5mm de PTFE (Gore Medical, Flagstaff, AZ; n=13), Alloderm (Lifecell, Branchburg, NJ; n=11), o Permacol (Tissue Science Laboratory, Andover, MA; n=12) (fig. 1). Se realizó una sutura continua de doble aguja con Prolene 6-0 empezando por el vértice superior del parche hasta el vértice inferior asegurando bilateralmente el borde del parche al borde del abordaje del vaso. Se realizó una segunda intervención a los 60 días para extraer la arteria carótida y evitar la formación de trombos intraarteriales durante la extracción de la muestra.
ELISA para la formación de trombos sistémicosSe obtuvieron muestras de sangre durante el preoperatorio, varias horas antes de la cirugía, y 7 y 60 días después de la intervención inicial. Se obtuvieron 5ml de sangre periférica en tubos con citrato sódico (3,8%) y se colocaron en hielo. El plasma se separó de los glóbulos rojos mediante centrifugación a 6.000g durante 10min y las alícuotas se almacenaron a –80°C hasta que se analizó el complejo trombina-antitrombina (Enzygnost TAT Micro; Behring Diagnostic, Inc.), un marcador específico y sensible de formación de trombos sistémicos12. En cada muestra se realizaron dos pruebas ELISA.
Estudio histológico y de imagen, análisis patológicoEl parche arterial se fijó en formalina al 10% en la segunda intervención utilizando un catéter de 25-gauge, gracias a una presión constante de 100 mmHg determinada mediante esfigmomanómetro, que permitió infundir formalina durante varios minutos. La muestra se transfirió posteriormente a un contenedor con formalina al 10%. Se obtuvieron cortes transversales de la arteria en la zona del parche, y 2mm distales y 2 proximales a la corrección, y se tiñeron con azul tricrómico y hematoxilina-eosina (figs. 2 y 3). Se realizó el análisis computarizado de los gráficos de la imagen mediante el programa ImageCost (University of Texas Health Science Center de San Antonio, San Antonio, TX). Se midió el diámetro vascular (mm), el área de sección transversal del vaso (mm2), el grosor de la íntima (mm) y de la media (mm) (fig. 4). El grosor de la íntima y de la media se midió en la arteria nativa adyacente a la corrección con parche, no directamente debajo de ella. La formación de trombos se consideró positiva si la muestra presentó cualquier cantidad de trombos organizados en la luz vascular en cualquiera de los cortes transversales obtenidos en la zona del parche, o proximal o distal a él. La muestra se consideró positiva para la hiperplasia de la íntima si alguno de los cortes presentó hiperplasia sobre la lámina elástica interna en alguna de las muestras transversales obtenidas en la zona del parche, o proximal o distal a él (fig. 5). La muestra se consideró aneurismática si el diámetro en la zona del parche fue mayor que el área de la arteria proximal a él como mínimo 1,5 veces. Las muestras se consideraron permeables si como mínimo un 10% de la luz no resultó ocluida por trombos o por la hiperplasia de la íntima.
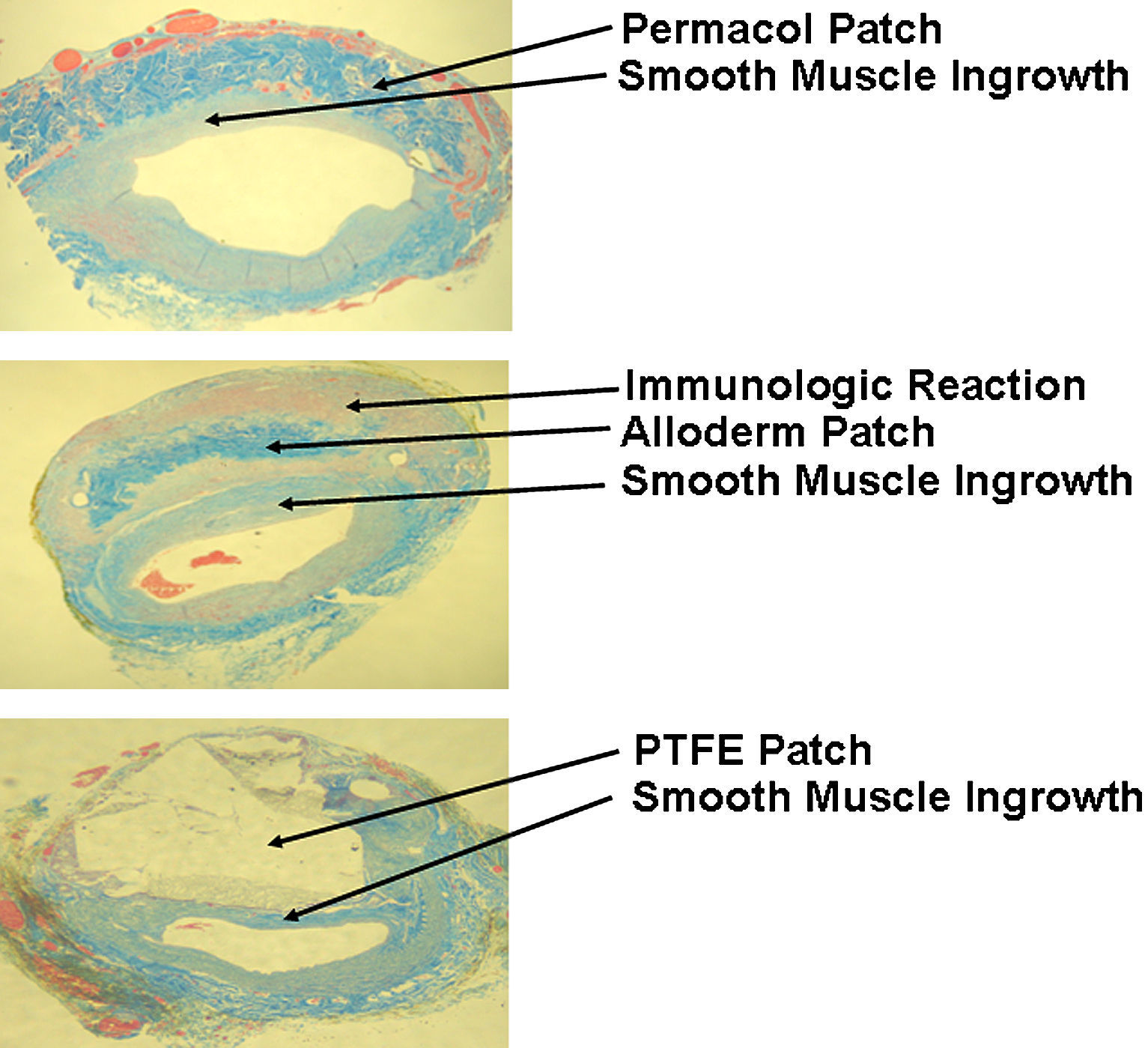
Preparaciones de azul tricrómico de los cortes histológicos de la zona del parche. El parche de Permacol se observa como colágeno azul con crecimiento de músculo liso bajo el parche. El parche de Alloderm se observa como colágeno azul con zonas de infiltración eosinofílica a su alrededor. El parche de PTFE se observa como una zona traslúcida con crecimiento de músculo liso. Alloderm Patch: parche de Alloderm; Immunologic Reaction: reacción inmunológica; Permacol Patch: parche de Permacol; PTFE Patch: parche de politetrafluoroetileno; Smooth Muscle Ingrowth: crecimiento de músculo liso.
Representaciones histológicas de las mediciones tomadas para el análisis de las imágenes. Se midió el diámetro (mm), el área de la sección transversal de la luz (mm2), y el grosor de la íntima y la media (mm). Diameter: diámetro; Intimal Thickness: grosor de la íntima; Medial Thickness: grosor de la media; Vessel Lumen Area: área de la luz vascular.
Preparaciones histológicas de las muestras. La imagen de la izquierda muestra el infiltrado eosinofílico alrededor del parche Alloderm con la formación de centros germinales. Este infiltrado leucocitario se observó solamente con el parche Alloderm. La hiperplasia de la íntima y la formación de trombos organizados común a todos los grupos se aprecian en las imágenes de la derecha. Eosinophilic Infiltration: infiltrado eosinofílico; Germinal Centers: centros germinales; Internal Elastic Lamina: lámina elástica interna; Intimal Hyperplasia: hiperplasia de la íntima; Organized Thrombus: trombos organizados.
Los resultados de los análisis de las imágenes histológicas se presentan como distancias promedio en mm o área de sección transversal en mm2±EEM. Los resultados del complejo trombina-antitrombina III se presentan en mg/l±EEM. Se utilizó el análisis de varianza (ANOVA) para comparar los grupos control y tratamiento. Los resultados del estudio patológico se presentan como diferencias entre grupos utilizando el análisis χ2. La significancia estadística se estableció en p<0,05.
ResultadosELISA para el complejo trombina-antitrombina IIILas muestras obtenidas antes de la cirugía muestran una concentración indetectable del complejo en cada grupo y no existen diferencias entre grupos. Las mediciones tempranas realizadas 7 días después de la intervención muestran una elevada formación de trombos sistémicos en el grupo PTFE, 5,27mg/l, que no es estadísticamente diferente de los otros grupos. La formación diferida de trombos determinada 60 días después de la intervención muestra un nivel significativamente elevado de la prueba en el grupo Permacol, 2,57mg/l (p=0,002) en comparación con las concentraciones indetectables en los grupos PTFE, –1,55mg/l, y Alloderm, –0,95mg/l (fig. 6). Este resultado, no obstante, está dentro del intervalo de referencia normal (1-4mg/l) para esta prueba. A los 60 días, los datos se estratificaron entre grupos con muestras cuyo examen patológico evidenció la presencia de trombos. Este análisis no mostró diferencias estadísticamente significativas entre grupos. Los resultados de Permacol fueron de 0,407mg/l en comparación con los de Alloderm, –1,463mg/l, y PTFE, –1,370mg/l. Todas estas cifras representan concentraciones indetectables del complejo trombina-antitrombina. Además, los grupos que presentaron oclusión en el examen patológico a los 60 días presentaron un aumento de Permacol, 2,173mg/l, en comparación con Alloderm, –1,655mg/l, y PTFE, –0,058mg/l. Sin embargo, no se observaron diferencias estadísticamente significativas entre grupos.
Gráfico que muestra los resultados del ELISA para el complejo trombina-antitrombina. Los resultados a los 7 días de la intervención del grupo PTFE muestran una elevación estadísticamente no significativa en comparación con el resto de los grupos. Los resultados a los 6 días de la intervención muestran un aumento estadísticamente significativo del complejo en el grupo Permacol (p=0,002) en comparación con los grupos PTFE y Alloderm. No obstante, este resultado estuvo dentro del intervalo de referencia normal (1-4mg/l). ELISA Thrombin/Antithrombin: ELISA para el complejo trombina-antitrombina; PTFE: politetrafluoroetileno; Time Points in Days: FALTA TRADUCCIÓN.
El área de la luz vascular fue significativamente mayor en los grupos Alloderm, 0,374mm2 (p=0,008), y Permacol, 0,344mm2 (p=0,02), en comparación con el grupo PTFE, 0,204mm2, en la arteria proximal. El área de la sección transversal en la zona del parche del grupo Alloderm, 0,432mm2 (p=0,005), fue mayor que en el grupo PTFE, 0,204mm2. No se observaron diferencias estadísticamente significativas entre grupos en la arteria distal (fig. 7). El diámetro del vaso en la zona del parche del grupo Alloderm, 1,87mm (p=0,004), fue significativamente mayor que el de los grupos Permacol, 1,41mm, y PTFE, 1,28mm (fig. 8). La íntima del grupo Alloderm, 0,076mm (p=0,018), fue significativamente más gruesa que la de los grupos PTFE, 0,026mm, y Permacol, 0,022mm, en la zona del parche (fig. 9a). No se observaron diferencias estadísticamente significativas con respecto al grosor de la íntima entre los grupos en las arterias proximal y distal. Esta hiperplasia de la íntima se observó en la arteria nativa yuxtapuesta al parche. El grosor de la media no fue estadísticamente diferente entre grupos en ninguno de los cortes histológicos (fig. 9b). La hiperplasia de la media se observó en la arteria nativa yuxtapuesta al parche.
Gráfico que muestra el área de la luz vascular de las 3 muestras de la arteria proximal, el parche y la arteria distal. El área de la luz de la arteria proximal muestra un aumento estadísticamente significativo en el grupo Permacol (p=0,008) y el grupo Alloderm (p=0,02) en comparación con el grupo PTFE. El área de la zona del parche está aumentada en el grupo Alloderm (p=0,005) en comparación con el grupo PTFE. No se observaron diferencias estadísticamente significativas en la arteria distal. Cross Sectional Area (sq mm): FALTA TRADUCCIÓN; Distal Artery: arteria distal; Patch: parche; Proximal Artery: arteria proximal; PTFE: politetrafluoroetileno; Vessel Lumen Area: área de la luz vascular.
a Gráfico que muestra la hiperplasia de la íntima en la zona del parche de las muestras. El grupo Alloderm (p=0,018) presentó un aumento del grosor de la íntima en comparación con los grupos Permacol y PTFE. No todas las muestras del grupo Alloderm presentaron hiperplasia de la íntima; sin embargo, en los casos en que sí existió, los efectos fueron muy destacados. b Gráfico que muestra el grosor de la media de los 3 segmentos en cada grupo. No se observaron diferencias estadísticas entre los grupos respecto a cada sección. Distal Artery: arterial distal; Intimal Thickness: grosor de la íntima; Medial Thickness: grosor de la media; Patch: parche; Proximal Artery: arteria proximal; PTFE: politetrafluoroetileno.
Los resultados no muestran diferencias estadísticamente significativas entre grupos respecto a la formación de trombos organizados. El grupo con PTFE (p=0,03) mostró una mayor incidencia de hiperplasia de la íntima en comparación con el grupo Permacol, 92 frente a 50,0%. El grupo con Alloderm (p=0,009) presentó una mayor incidencia de formación de aneurismas, 63,6%, en comparación con los grupos con PTFE, 0,0%, y Permacol, 8,3%. No se observaron diferencias estadísticamente significativas entre grupos en cuanto a la permeabilidad de la luz arterial (tabla I).
Examen de los cortes histológicos de los grupos de parches
| Tipo de parche | Trombos | Hiperplasia de la íntima | Aneurisma | Permeabilidad |
| PTFE, n=13 | 8/13=61,5% | 12/13=92,0%a | 0/13=0,0% | 11/13=84,6% |
| Permacol, n=12 | 6/12=50,0% | 6/12=50,0% | 1/12=8,3% | 8/12=66,7% |
| Alloderm, n=11 | 6/11=54,50% | 6/11=54,50% | 7/11=63,6%b | 9/11=81,8% |
PTFE: politetrafluoroetileno.
No se observaron diferencias entre grupos en cuanto a la formación de trombos y la permeabilidad.
Este estudio trató de encontrar alternativas adecuadas al PTFE en casos de traumatismos arteriales. A menudo el PTFE debe retirarse tras la corrección del traumatismo con parche debido a la existencia de infección o trombosis2. En la actualidad, la vena autóloga es el patrón de referencia para la corrección con parche de los traumatismos arteriales. Un parche biosintético resistente a la infección, prescindiendo de una segunda intervención definitiva con injerto venoso, supondría una clara ventaja en el tratamiento actual de los traumatismos vasculares. Se escogieron los parches Alloderm y Permacol por su potencial para poder ser utilizados en heridas muy contaminadas7,9,10. Además, estos materiales pueden almacenarse fácilmente y tienen unas características de manipulación comparables a las del PTFE. Este estudio mostró que, en este modelo, Permacol fue equivalente al PTFE en la corrección de la arteriotomía con parche. Alloderm no fue una alternativa adecuada al PTFE.
El ELISA para el complejo trombina-antitrombina ha demostrado ser un marcador sensible de la formación de trombos sistémicos así como una prueba diagnóstica precoz de reoclusión vascular12,13. Spanier et al14 midieron con éxito el complejo trombina-antitrombina en conejos New Zealand White tras la corrección de la aorta infrarrenal mediante parche de PTFE utilizando el factor XII activado. Adicionalmente, Sugatani et al15 midieron el aumento del complejo trombina-antitrombina en ratones C57BL/6 tras la inoculación intravenosa de lipopolisacáridos. Este estudio demostró que los grupos control y de tratamiento no sirven como foco para la formación de trombos sistémicos. Solamente el PTFE demostró una elevación por encima del intervalo de referencia a los 7 días, pero no de forma significativa en comparación con los grupos tratamiento. Las mediciones de Permacol fueron significativamente mayores que las de PTFE y Alloderm a los 60 días de la intervención, pero se situaron en el intervalo no detectable respecto a la formación de trombos sistémicos.
Permacol ha demostrado con anterioridad su eficacia en la corrección de heridas abdominales en campos infectados7. Esta resistencia a la infección hace que sea una alternativa ideal para la corrección con parche en casos de traumatismos. La mortalidad, la formación de trombos organizados, la formación de aneurismas y los índices de permeabilidad fueron similares entre grupos. Además, el grupo con Permacol presentó una incidencia de hiperplasia de la íntima estadísticamente menor que el grupo PTFE. El área de sección transversal de la luz vascular del grupo con Permacol tendió a ser mayor en comparación con el grupo con PTFE en la zona del parche. El área de sección transversal proximal al parche fue significativamente mayor que en el grupo con PTFE, posiblemente debido al aumento de la distensibilidad del material. Este aumento de la distensibilidad, sin embargo, no indujo la formación de aneurismas en comparación con los grupos PTFE y Alloderm. Con anterioridad se había probado el injerto de submucosa de intestino delgado porcino, Surgisis, en la arteria carótida canina de forma satisfactoria en comparación con los implantes de PTFE16. El injerto de submucosa de intestino delgado porcino se estudió como conducto vascular en presencia de contaminación por microorganismos grampositivos y mostró resistencia a la colonización bacteriana17. No obstante, los intentos por utilizar el injerto de submucosa de intestino delgado porcino en humanos para la corrección mediante parche de la endarterectomía carotídea no fueron satisfactorios debido a la formación temprana de pseudoaneurismas18. Solamente una muestra fue aneurismática en el grupo tratado con Permacol. En los cortes histológicos se apreció el crecimiento de músculo liso y la formación de neoíntima. Permacol no inició una respuesta inmunitaria frente al injerto en el animal hospedador.
Alloderm demostró ser una pobre alternativa al PTFE en este estudio. La incidencia de formación de aneurismas fue más elevada en el grupo Alloderm que en los grupos PTFE y Permacol. El tamaño de la luz fue mayor que en el grupo PTFE en la zona del parche, pero este efecto probablemente sea secundario a la formación de aneurisma. A diferencia de Permacol, el aumento del área de la luz vascular condujo a la formación de aneurismas. Si bien el porcentaje global de hiperplasia de la íntima fue similar al del PTFE, su efecto sobre la incidencia de hiperplasia fue especialmente marcado. El promedio del grosor de la íntima fue aproximadamente el triple con Alloderm que con Permacol y PTFE. Históricamente, Alloderm se describe como un material que no causa reacciones inmunitarias ya que se usa habitualmente en la corrección de hernias complejas9,10. Sin embargo, observamos una respuesta inmunitaria con infiltración eosinofílica y formación de centros germinales alrededor del material del parche.
En resumen, Permacol fue equivalente al PTFE para la corrección mediante parche de la arteriotomía en este modelo animal. Permacol tiene potencial para ser una alternativa al PTFE en casos de traumatismos vasculares. Este estudio no apoya el uso de Alloderm como alternativa al PTFE debido a la formación de aneurismas, al notable aumento del grosor de la íntima, y al desencadenamiento de una respuesta inmunitaria. Los estudios futuros deberán incluir sistemas de animales de mayor tamaño con mediciones hemodinámicas intraoperatorias y el uso de parches biosintéticos en campos contaminados.
Agradecemos a Major Julie Stephens-DeValle, Dr. J. Malcolm Kling, Mr. Eugene Cauley, Mr. David Robinson, y Ms. Leticia Simon su ayuda con el cuidado de los animales y la cirugía. También agradecemos la ayuda en la revisión patológica de la Dra. Julie Lemmon.
La investigación fue financiada por una beca interna del Dwight David Eisenhower Army Medical Center, Department of Clinical Investigations.
El PTFE fue suministrado por Gore Medical para su evaluación en este estudio. Los autores no tienen relación económica o interés alguno con los fabricantes de Goretex, Permacol o Alloderm.
Las opiniones de los autores no tienen por qué reflejar la posición del Deparment of the Army o del Department of Defense (párrafo 4-3), AR 360-5.