El síndrome de robo vascular es una complicación poco frecuente después de los accesos vasculares para hemodiálisis. Las opciones de tratamiento incluyen la ligadura de la fístula, banding y revascularización distal con ligadura intermedia (RDLI). La plicatura es otra técnica que es simple aunque apenas se han publicado datos sobre el procedimiento. Hemos adoptado esta técnica como procedimiento de elección para el síndrome del robo tras la colocación de una fístula arteriovenosa (FAV) autóloga. Describimos a siete pacientes tratados mediante plicatura. En todos se obtuvo la resolución inmediata de los síntomas (Tabla 1). En el seguimiento, todas las FAV estaban permeables y continuaban utilizándose para la hemodiálisis. No obstante, un paciente experimentó recidiva de los síntomas y precisó una nueva plicatura. En conclusión, este procedimiento para la FAV autóloga representa una alternativa simple del tratamiento del síndrome del robo.
Después de la colocación de una fístula arteriovenosa (FAV) para hemodiálisis, se considera que la mayoría de los pacientes desarrollan cierto grado de robo fisiológico debido a una alteración de la hemodinamia local y la derivación de sangre de la circulación arterial distal hacia el lado venoso de baja resistencia1-3. El robo patológico es una complicación poco frecuente pero devastadora de los accesos vasculares en la extremidad superior con una incidencia estimada del 1-9%4-7. Las opciones de tratamiento incluyen ligadura de la FAV, banding y revascularización distal con ligadura de intervalo (RDLI). Este último procedimiento se considera el tratamiento de elección de este síndrome. No obstante, esta intervención requiere la creación de un nuevo bypass. Aunque casi no se han publicado artículos sobre el procedimiento, una alternativa de la RDLI es la plicatura. Hemos adoptado esta técnica como tratamiento de elección del robo tras la creación de FAV autóloga. En el presente estudio describimos los resultados de siete pacientes.
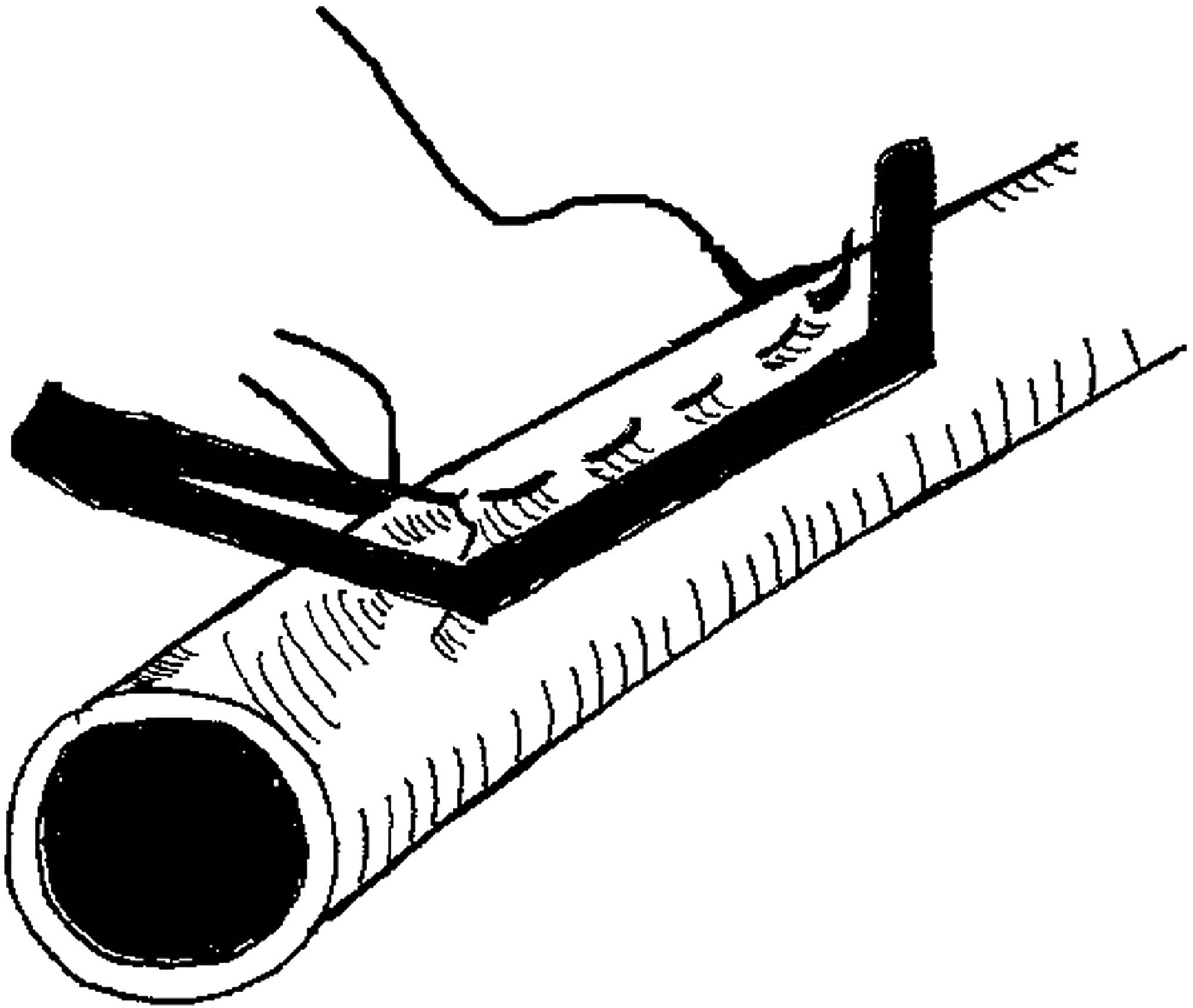
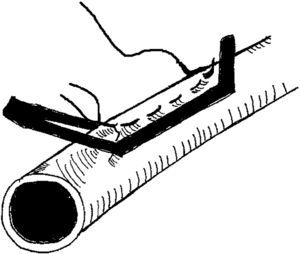
PacientesDespués de la creación de FAV nativa como acceso vascular para hemodiálisis, siete pacientes, cuatro hombres y tres mujeres, presentaron síntomas de robo vascular (Tabla 1). La edad media fue de 51 años (límites 33-68). Dos pacientes tenían antecedentes de diabetes mellitus y seis de hipertensión arterial. En cinco pacientes se creó una FAV de arteria humeral a vena cefálica y en dos de arteria humeral a vena basílica, todas en la fosa antecubital. Los síntomas incluyeron parestesias, frialdad y dolor en la mano y los dedos. Ninguno presentó ulceraciones. Los hallazgos de la exploración física incluyeron ausencia de pulsos distales, retraso del llenado capilar y señales del eco-Doppler monofásicas en las arterias radial y cubital distales. El diagnóstico de robo se confirmó mediante compresión manual de la fístula, que dio lugar a una mejora considerable del llenado capilar; una mejora de las señales Doppler en la muñeca; en seis de siete pacientes, una reanudación de pulso arterial radial palpable. En un paciente en el que no se obtuvo la reanudación del pulso radial con la compresión de la fístula se efectuó arteriografía, ya que se sospechaba arteriopatía oclusiva subyacente. El estudio reveló una arteria radial permeable pero estenosada, arteriopatía aterosclerótica oclusiva grave en la arteria cubital y falta de circulación colateral en la mano. Todos los pacientes se sometieron a la plicatura de la FAV, lo que incluyó la plicatura de la vena proximal a la anastomosis usando una sutura de polipropileno 6-0 para una longitud de alrededor de 1 cm, como puede observarse en la figura 1. La reanudación de un pulso palpable o un cambio de la señal Doppler arterial distal de monofásica a bifásica determinaron la extensión de la plicatura. Cuando la señal Doppler no mejoró, se redujo todavía más el diámetro mediante nueva aplicación de un clampaje de Satinsky en la misma área, al mismo tiempo que garantizábamos que sobre el abordaje persistía el frémito. En el postoperatorio, en seis de siete pacientes se observó la reanudación de un pulso radial palpable con una mejora del llenado capilar y de la señal Doppler bifásica en la muñeca. El séptimo paciente (el mismo con la arteriopatía distal grave, observada en la arteriografía) manifestó una mejora destacada de los síntomas y de la señal Doppler sin un pulso distal claramente palpable. En la primera semana postoperatoria, una paciente presentó un hematoma sobre el lugar del abordaje y edema del brazo. Fue tratada de forma conservadora y sus síntomas se resolvieron al cabo de pocos días.
Siete casos de síndrome del robo tratados con plicatura de la vena nativa
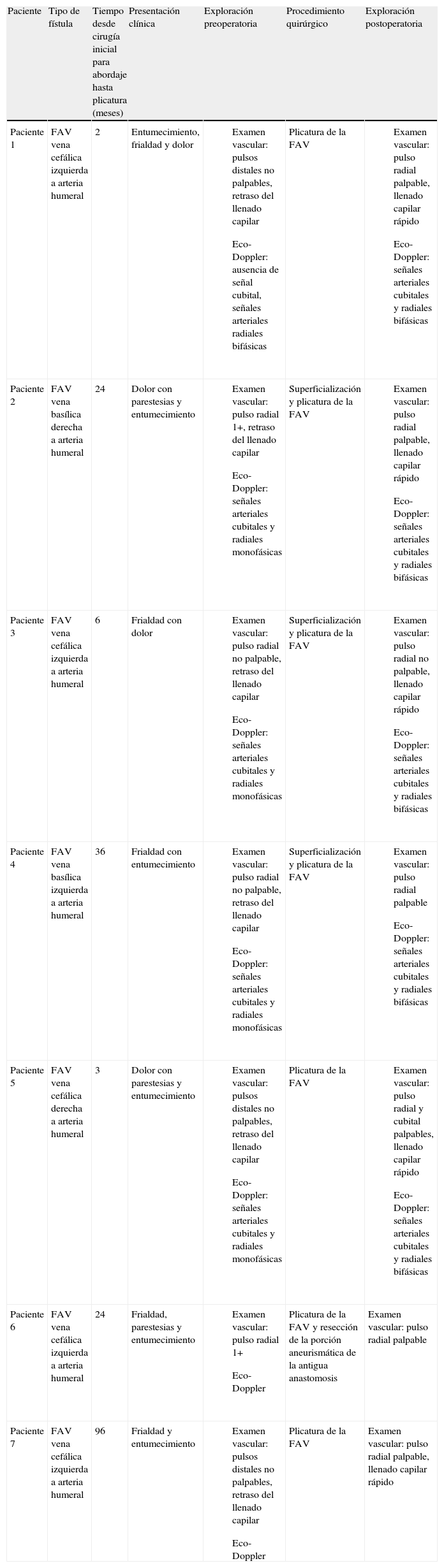
| Paciente | Tipo de fístula | Tiempo desde cirugía inicial para abordaje hasta plicatura (meses) | Presentación clínica | Exploración preoperatoria | Procedimiento quirúrgico | Exploración postoperatoria |
| Paciente 1 | FAV vena cefálica izquierda a arteria humeral | 2 | Entumecimiento, frialdad y dolor |
| Plicatura de la FAV |
|
| Paciente 2 | FAV vena basílica derecha a arteria humeral | 24 | Dolor con parestesias y entumecimiento |
| Superficialización y plicatura de la FAV |
|
| Paciente 3 | FAV vena cefálica izquierda a arteria humeral | 6 | Frialdad con dolor |
| Superficialización y plicatura de la FAV |
|
| Paciente 4 | FAV vena basílica izquierda a arteria humeral | 36 | Frialdad con entumecimiento |
| Superficialización y plicatura de la FAV |
|
| Paciente 5 | FAV vena cefálica derecha a arteria humeral | 3 | Dolor con parestesias y entumecimiento |
| Plicatura de la FAV |
|
| Paciente 6 | FAV vena cefálica izquierda a arteria humeral | 24 | Frialdad, parestesias y entumecimiento |
| Plicatura de la FAV y resección de la porción aneurismática de la antigua anastomosis | Examen vascular: pulso radial palpable |
| Paciente 7 | FAV vena cefálica izquierda a arteria humeral | 96 | Frialdad y entumecimiento |
| Plicatura de la FAV | Examen vascular: pulso radial palpable, llenado capilar rápido |
FAV: fístula arteriovenosa.
En conjunto, el período medio de seguimiento fue de 9 meses (límites 4-18). En el seguimiento a los 13 meses, un paciente (el mismo en el que no se reanudó el pulso) experimentó recidiva de los síntomas. Cabe destacar que en la mano contralateral presentaba pulsos no palpables junto con una disminución de la perfusión. Debido a los hallazgos del examen y a la anatomía arterial, se trasladó al paciente al quirófano, donde se sometió a una nueva plicatura con la mejora de los síntomas. A pesar de que se consideró una RDLI, en la arteria humeral y la arteria radial proximal se detectaron calcificaciones densas, por lo que se descartó la tentativa de bypass. De nuevo, el paciente refirió una mejora de los síntomas sin que se restableciera el pulso distal.
DiscusiónEl síndrome de robo vascular es una complicación excepcional, pero potencialmente devastadora, del abordaje AV para hemodiálisis, con una incidencia estimada del 1-8%4,8-11. En los estudios previos se ha descrito una mayor incidencia de este síndrome en pacientes con injertos AV (IAV) en comparación con aquellos con FAV autólogas. Su incidencia es mayor para las fístulas más proximales. Otros factores de riesgo conocidos del síndrome incluyen la edad avanzada, el sexo femenino, diabetes, hipertensión arterial, aterosclerosis, y múltiples procedimientos previos de creación de acceso vascular en el mismo brazo12,13.
La etiología del robo se basa en la alteración de la hemodinámica local. La baja resistencia en el lado venoso de la fístula da lugar a la derivación del flujo sanguíneo arterial en la vena. La presión en la arteria distal disminuye, al igual que la perfusión distal. Si el grado de disminución de la resistencia en el lado venoso es suficiente, puede producirse una inversión del flujo sanguíneo arterial distal en la vena, lo que exacerba todavía más la perfusión distal14. Se considera que alrededor del 80% de los pacientes con un abordaje AV funcional presentan un robo fisiológico, que es asintomático desde un punto de vista clínico1-3. En general, el desarrollo de colaterales arteriales y la vasodilatación distal compensan el robo fisiológico1. No obstante, si estos mecanismos son insuficientes para mantener una presión de perfusión distal adecuada, se origina un síndrome del robo isquémico.
El tratamiento clínico de este síndrome se basa en la gravedad de los síntomas. Inicialmente, los de carácter leve pueden tratarse mediante observación. Con frecuencia, el mecanismo compensador natural de la dilatación proximal del vaso de entrada resolverá los síntomas al cabo de pocos días a semanas. Si los síntomas persisten o se agravan, está indicado un tratamiento quirúrgico. Éste debe dirigirse tanto a mantener la permeabilidad del abordaje AV como a la resolución de los síntomas isquémicos. Por lo tanto, la simple ligadura del abordaje AV es subóptima9. El banding de la salida venosa se ha descrito principalmente en los IAV y se basa en la premisa de que la mayor resistencia de la fístula aumentará la perfusión de la extremidad distal hasta el origen de la fístula. Sin embargo, debido a la trombogenicidad de los IAV, con frecuencia, esta estrategia da lugar a la trombosis del injerto15-19. Los malos resultados del banding dieron lugar al concepto de RDLI en 198820. Se ha descrito que este procedimiento se asocia a una tasa de eficacia del 83-100%. Las ventajas incluyen el salvamento del abordaje AV al mismo tiempo que se proporciona un restablecimiento fiable del flujo en la extremidad isquémica y la eliminación de las vías potenciales de reaparición del síndrome. Sin embargo, esta técnica requiere otro bypass.
Previamente se ha descrito el uso de la plicatura en el tratamiento de este síndrome. Rivers et al21 usaron el procedimiento en cinco pacientes con el síndrome y en los cinco obtuvieron la resolución de los síntomas isquémicos y mantuvieron el abordaje funcionante. En el presente estudio obtuvimos hallazgos similares; no obstante, en un paciente los síntomas recurrieron, por lo que requirió una nueva plicatura. Es probable que la recidiva se deba a la arteriopatía aterosclerótica distal grave subyacente. Una limitación del presente estudio es que no usamos una variable objetiva, como los registros del volumen del pulso, para determinar el grado de plicatura necesario. En su lugar, usamos el examen con Doppler directo para observar un cambio hasta una señal bifásica y en seis de siete pacientes se observó el restablecimiento de los pulsos distales. El hecho de que en todos los pacientes se obtuviera una mejora de los síntomas y se mantuviera la permeabilidad de la fístula sugiere que es una estrategia aceptable. De forma parecida, Khalil y Livingston18 no usaron criterios de valoración objetivos para determinar el grado de plicatura en pacientes con IAV. Esto contrasta con el estudio de Rivers et al21, que usaron los registros del volumen del pulso como guía de la plicatura y observaron que, para mejorar los síntomas isquémicos, fue necesario un aumento de, como mínimo, 5 mm en los registros del volumen del pulso. En 2006, Zanow et al22 efectuaron un estudio retrospectivo en 95 pacientes (78 con isquemia y 17 con insuficiencia cardíaca) que se sometieron a reducción del flujo entre 1999 y 2005. La reducción del flujo se obtuvo mediante una sutura continua de estrechamiento de tipo huso cerca de la anastomosis y la colocación final de un parche de politetrafluoroetileno al mismo tiempo que, para la determinación intraoperatoria del flujo de abordaje, se usó un medidor de flujo. Se observó la resolución completa de los síntomas a largo plazo en el 86% de los pacientes con isquemia y en el 96% de aquellos con insuficiencia cardíaca. Más recientemente, también se ha descrito la derivación proximal del flujo de entrada arterial como alternativa a la RDLI para tratar el síndrome23.
Tras la creación de una FAV autóloga, el momento del robo parece diferir del de un IAV. Tras la implantación de un IAV, en general, el síndrome de robo se manifiesta precozmente, de inmediato después de la cirugía o al cabo de pocos días. Esto se explica por el hecho de que inmediatamente después de su creación, se produce el hiperaflujo máximo de la fístula. Al contrario, con una FAV nativa, hay un aumento gradual del flujo de la fístula a medida que se dilata la salida venosa12. En el presente estudio se destaca esta diferencia, ya que cinco de siete pacientes desarrollaron síntomas de robo meses a años después de la intervención quirúrgica.
En conclusión, el síndrome del robo es una complicación poco frecuente, pero grave, después de la creación de un acceso vascular para hemodiálisis. Tras la implantación de un IAV, en general, su inicio es inmediato y la RDLI ha irrumpido como el procedimiento de elección ya que las tentativas de banding del injerto con frecuencia dan lugar a trombosis. No obstante, es posible que la RDLI no sea necesaria para las fístulas arteriovenosas14 ya que la fisiopatología y el momento de la presentación pueden diferir. En el presente estudio, siete pacientes con síndrome del robo después de la creación de FAV autólogas fueron tratados satisfactoriamente con plicatura de la vena nativa, con la resolución de los síntomas, al igual que la mejora de la perfusión distal. Creemos que las FAV autólogas son subsidiarias de una plicatura con éxito porque la vena nativa es menos trombogénica que el injerto. Ninguno de los siete pacientes desarrolló trombosis de la fístula. Debido al seguimiento relativamente breve de la cohorte del presente estudio, y el hecho de que un paciente presentó recidiva de los síntomas, es posible que esta técnica no proporcione resolución en todos ellos, en particular, si la compresión preoperatoria de la fístula no da lugar al restablecimiento de un pulso palpable en la muñeca, lo que sugiere arteriopatía aterosclerótica distal. La plicatura parece servir de opción alternativa a la RDLI en pacientes con fístulas arteriovenosas autólogas.