Evaluamos los resultados a corto y medio plazo de la reparación endovascular de aneurismas (REVA) aórticos micóticos. Revisamos a todos los pacientes sometidos a tratamiento quirúrgico en nuestro hospital. Para que la investigación fuera concordante con los estudios publicados, se incluyeron los pacientes con aortoentérica o bronquialaortoentérica o bronquialfístula aortoentérica o bronquial asociada. Se revisaron la localización del aneurisma, demografía, hallazgos clínicos, eficacia de la REVA, morbilidad y mortalidad a corto (< 30 días) y largo plazo. Desde 2000 a 2007, 326 pacientes se sometieron a REVA. En nueve de ellos (3%) se efectuó el tratamiento por aneurisma micótico. La edad media fue de 72 años (límites 53-86), y siete eran hombres. De los aneurismas, cuatro se localizaban en la aorta torácica, dos en la aorta abdominal, y tres en la aorta toracoabdominal. Se presentaron con hemorragia gastrointestinal cuatro pacientes, dos con hemoptisis, uno con hemotórax, y dos con fiebre. Las etiologías fueron: endocarditis e infección de catéter central con bacteriemia, erosión de aneurismas anastomóticos a partir de cirugía aórtica previa o endoprótesis implantada previamente como tratamiento de úlcera en aorta torácica, erosión de una úlcera penetrante con pseudoaneurisma, corrección aórtica infectada, empiema torácico izquierdo, y desconocida en un paciente. En el 56% de los pacientes la única bacteria aislada fue Staphylococcus aureus meticilín resistente. La REVA excluyó satisfactoriamente el aneurisma o la fístula en los nueve pacientes; sin embargo, cinco experimentaron, como mínimo, una complicación postoperatoria. Fallecieron al cabo de 30 días dos pacientes; después de 30 días, fallecieron otros cuatro pacientes; tres de estas muertes se relacionaron con el procedimiento o el aneurisma. De los tres supervivientes, durante el seguimiento medio de 257 días (límites 60-417), una paciente ha requerido la resección de la endoprótesis infectada con un injerto mediante bypass extraanatómico pero, en la actualidad, sigue viva y se encuentra en buen estado general. Los tres pacientes supervivientes y dos de los cuatro que fallecieron después de 30 días habían recibido antibióticos postoperatorios a largo plazo. A pesar de que la mortalidad hospitalaria fue del 22,2%, la REVA puede usarse para tratar las complicaciones agudas de los aneurismas micóticos y las aortoentéricas o bronquialaortoentéricas o bronquialfístulas aortoentéricas o bronquiales asociadas, como la hemorragia gastrointestinal, hemoptisis o inestabilidad hemodinámica. Como tratamiento definitivo, esta corrección sigue siendo problemática y ha de considerarse un procedimiento provisional mientras se espera el momento apropiado de la corrección quirúrgica abierta.
Durante la última década, el tratamiento de los aneurismas aórticos ha evolucionado, y la reparación endovascular (REVA) ha llegado a ser la opción primaria en muchos contextos clínicos. Debido a su eficacia, los cirujanos vasculares han extendido sus aplicaciones al tratamiento de patología aórtica diversa, como las disecciones, lesiones traumáticas, pseudoaneurismas y, en ocasiones, aneurismas micóticos1. Sin embargo, debido a la naturaleza infrecuente de dichos aneurismas, los datos sobre su tratamiento con reparación endovascular (EV) se han basado en unos pocos casos clínicos y series de casos publicados. En una revisión publicada por Kan et al2, los autores sólo identificaron 48 casos entre los estudios publicados. Los resultados han sido variables y apenas se dispone de datos de la evolución tardía, en particular comparado con las intervenciones abiertas. Describimos los hallazgos a corto y medio plazo en una serie de pacientes con aneurismas micóticos y aortoentérica o bronquial asociada tratados con REVA.
MétodosRevisamos a todos los pacientes que, entre 2000 y 2007, se sometieron en nuestro centro a reparación EV de la aorta (torácica, toracoabdominal o infrarrenal) por aneurisma micótico. Éstos se definieron por la presencia de sepsis (como mínimo dos de los siguientes criterios: fiebre, leucocitosis, taquipnea o taquicardia) asociada a aneurisma con cualquiera de las características siguientes: hallazgos radiológicos compatibles con aorta infectada, presencia de una fístula aortoentérica (FAE), o presencia de una fístula aortobronquial (FAB). La ausencia de fiebre y de hemocultivos positivos no se usó como criterio de exclusión. Se revisaron la localización del aneurisma, demografía de los pacientes, presentación, etiología, bacteriología, pauta antibiótica, eficacia de la REVA, morbilidad, mortalidad a corto plazo (< 30 días), mortalidad intermedia y necesidad de una reintervención.
ResultadosEn nuestro hospital, la REVA es el método de elección para tratar la patología aórtica dentro de limitaciones anatómicas y en pacientes que no son candidatos quirúrgicos apropiados. En los casos de aneurisma micótico, la REVA es de elección sobre la corrección abierta debido a su naturaleza menos cruenta y la capacidad de estabilizar rápidamente a los pacientes que presentan una hemorragia aguda. Durante un período de 7 años, 326 pacientes se sometieron a reparación EV de la aorta. De ellos, nueve (3%) presentaban aneurismas micóticos y son aquellos cuyas características se resumen en la tabla I. En cuatro pacientes los aneurismas se localizaban en la aorta torácica, en tres en la región toracoabdominal, y en dos en posición infrarrenal. La edad media fue de 72 años (límites 52-86), y siete pacientes eran hombres. De los nueve, siete tampoco se consideraron candidatos apropiados para la corrección abierta debido a la presencia de enfermedad pulmonar obstructiva crónica (n = 4), insuficiencia renal (n = 1), o deterioro a partir de una intervención quirúrgica reciente (n = 2). Presentaron hemorragia gastrointestinal (HGI) cuatro pacientes, dos hemoptisis, uno hemotórax y otros dos fiebre.
Resumen de los pacientes, presentaciones y desenlaces
| Paciente | Sexo/edad (años) | Presentación | Etiología | Fiebre | Microorganismo (localización) | Localización | Reintervención (DPO) | Mortalidad (DPO) | Seguimiento (DPO) | Duración tratamiento antibióticoa |
| 1 | Hombre/65 | Fiebre | Sepsis a partir de catéter central | Sí | Staphylococcus aureus resistente a meticilina (hemocultivo) | Toracoabdominal-celíaco cubierto | No | No | 60 | 3 meses antes cirugía y todavía tratado |
| 2 | Mujer/72 | Fiebre y dolor abdominal | Desconocida rotura contenida de aneurisma | Sí | No | Toracoabdominal | Colecistitis (5), corrección de perforación esofágica (11) | Síb (61) | – | Postoperatorio hasta su muerte |
| 3 | Hombre/86 | Hemorragia gastrointestinal | Aneurisma con fistula aortoentérica a partir de foco de endocarditis | Sí | Staphylococcus aureus resistente a meticilina (hemocultivo) | Abdominal, aorto-uniilíaco con bypass femorofemoral | No | Sí (2) | – | Postoperatorio hasta su muerte |
| 4 | Hombre/72 | Hemorragia gastrointestinal | Rotura de pseudoaneurisma a partir de corrección previa de aorta torácica descendente | No | No | Torácica | Desbridamientos mediastínicos (¿?) | Síb (102) | – | Ninguno en el momento del alta |
| 5 | Hombre/73 | Hemorragia gastrointestinal | Fístula aortoentérica tras pseudoaneurisma a partir de úlcera penetrante con hematoma intramural | No | No | Torácica | No | No | 295 | 6 semanas postoperatorias |
| 6 | Mujer/78 | Hemorragia gastrointestinal | Fístula aortoentérica a partir de pseudoaneurisma de la corrección de un AAA previo | No | No | Abdominal, uniilíaco con injerto mediante bypass femorofemoral | Exploración laparoscópica negativa para peritonitis (1) bypass/resección axilofemoral de endoprótesis (111/118) | No | 417 | 4 semanas postoperatorias |
| 7 | Hombre/67 | Hemoptisis | Fístula aortobronquial después de tres REVAT previas con fugas en tórax en postoperatorio, transformadas en empiema | No | Staphylococcus aureus resistente a meticilina (cultivo de esputo) | Torácica | Toracotomía para hemotórax (2) | Sí (2) | – | Postoperatorio hasta su muerte |
| 8 | Hombre/84 | Hemoptisis | Erosión de pseudoaneurisma tras fuga de corrección previa con endoprótesis de una úlcera penetrante | No | Staphylococcus aureus resistente a meticilina (cultivo de esputo) | Torácica, con debranching del cayado aórtico | No | Síb (48) | – | Ninguno en el momento del alta |
| 9 | Hombre/52 | Hemotórax | Corrección de lesión aórtica infectada tras esofagectomía | No | Staphylococcus aureus resistente a meticilina (hemotórax) | Torácica | No | Sí (69) | – | Postoperatorio hasta su muerte |
AAA: aneurisma aórtico abdominal; DPO: día postoperatorio.
La etiología de la infección fue variable. Entre los dos pacientes con fiebre, en uno no se evidenció foco séptico y en el otro se identificó bacteriemia debida a infección de un catéter central. De los pacientes con fístulas aortoentérica o bronquial asociada, todos presentaban erosión de pseudoaneurismas con diferente origen, incluida bacteriemia debida a endocarditis, endoprótesis implantada previamente para una úlcera aórtica torácica, pseudoaneurisma causado por una úlcera penetrante con hematoma intramural, dos a partir de pseudoaneurismas anastomóticos después de una corrección aórtica abierta previa y, en el último, tras una REVA torácica, persistía la fuga, lo que causaba un hemotórax que se transformó en empiema. El último caso fue el de un paciente con corrección aórtica, utilizando pledget durante la esofagectomía, presentando un hemotórax que se infectó y se transformó en pseudoaneurisma.
En el 56% de los pacientes del presente estudio, pudimos aislar la bacteria causal; en todos los casos, el patógeno infeccioso fue Staphylococcus aureus meticilín resistente (SAMR). En dos pacientes se identificó a partir del hemocultivo, en otros dos en el esputo de pacientes con FAB, y en un hemotórax infectado del quinto. En todos los pacientes, en los que se estableció el diagnóstico de aneurisma o fístula micóticos, se administró tratamiento antibiótico en el período perioperatorio. Cuando se administraron, se seleccionó antibioterapia a largo plazo en función de los cultivos y las sensibilidades. Si no se aislaron bacterias, la pauta antibiótica se basó en las recomendaciones a partir de la consulta efectuada con expertos en enfermedades infecciosas. De los cinco pacientes con SAMR, cuatro recibieron tratamiento antibiótico a largo plazo con linezolid (tabla I, paciente 1) o vancomicina (tabla I, pacientes 3, 7 y 9). En los tres pacientes en los que no se identificaron bacterias, la pauta antibiótica incluyó levofloxacino, metronidazol y caspofungina (tabla I, paciente 2); levofloxacino, metronidazol y fluconazol (tabla I, paciente 5); o vancomicina, piperacilina-tazobactam y fluconazol (tabla I, paciente 6). En el momento del alta, dos pacientes no recibían antibióticos debido a la preferencia del médico responsable (tabla I, pacientes 4 y 8).
En los nueve pacientes se obtuvo la exclusión EV satisfactoria del aneurisma o fístula con la endoprótesis Excluder o TAG (W. L. Gore, Flagstaff, AZ). En una reparación EV torácica se requirió el debranching del cayado aórtico para proporcionar una zona de anclaje proximal. En las correcciones aórticas infrarrenales, fue necesaria la implantación de una endoprótesis aorto-uniilíaca con bypass femoro-femoral debido a: la oclusión de rama del injerto preexistente en un paciente y después de que la pata contralateral de la endoprótesis no se abriera en el otro.
Cinco pacientes experimentaron como mínimo una de las complicaciones hospitalarias postoperatorias siguientes: fibrilación auricular (n = 2), trombosis venosa profunda (n = 1), neumonía (n = 1), colecistitis (n = 1) y perforación esofágica con sepsis (n = 1). Fallecieron al cabo de 30 días dos pacientes (22%). Uno era portador de aneurismas micóticos desarrollados a partir de bacteriemia y endocarditis. Presentó una hemorragia gastrointestinal a partir de la erosión de una fístula aortoduodenal que se excluyó con la REVA, sobre la base de la angiografía intraoperatoria, pero en el postoperatorio la hemorragia continuó y, por último, falleció. El otro presentó una rotura del aneurisma de la aorta torácica descendente que se corrigió con una endoprótesis pero las endofugas persistieron en el tórax y se transformaron en empiema que causó FAB. Después de una cuarta intervención EV, en el postoperatorio, desarrolló un hemotórax masivo y fue trasladado al quirófano para efectuar una toracotomía de urgencia, identificándose una dehiscencia aórtica secundaria a infección y falleció.
En total, fallecieron seis pacientes (67%). Después de 30 días, cuatro de los siete supervivientes (57%) fallecieron en el transcurso de una media de 74,5 días (límites 48-102); tres de estas muertes se relacionaron con el procedimiento/aneurisma. La primera paciente presentó fiebre y se observó la rotura contenida del aneurisma micótico de aorta torácica descendente. Su curso postoperatorio se complicó debido a una colecistitis aguda que requirió colecistectomía abierta, y, 11 días después de la REVA, desarrolló una perforación esofágica que requirió su corrección quirúrgica. Durante ésta se determinó que la persistencia de la infección del saco del aneurisma había dado lugar a una perforación esofágica y se observaba la endoprótesis a través de un orificio en la aorta. Puesto que la paciente se encontraba demasiado inestable para una corrección definitiva, se efectuó desbridamiento, se colocó un drenaje y se efectuó corrección esofágica con flap. Tras sobrevivir a la hospitalización inicial, pudo ser dada de alta, pero falleció de sepsis 2 meses más tarde (fig. 1). El segundo paciente presentaba un pseudoaneurisma anastomótico de una corrección abierta previa de un aneurisma de aorta torácica descendente que provocó una erosión en el esófago. La reparación EV excluyó la FAE pero falleció 3 meses más tarde tras requerir desbridamientos mediastínicos por infección persistente. El tercer paciente presentó hemoptisis tras la implantación previa de una endoprótesis para una úlcera penetrante que erosionó los bronquios izquierdos. Esta FAB se trató con la implantación de otra endoprótesis pero, debido a la persistencia de la infección a su alrededor, 48 días más tarde, el paciente presentó hemoptisis masiva y falleció (fig. 2). El cuarto paciente falleció de la progresión de un cáncer de esófago metastásico preexistente en el día 69 postoperatorio. De estos cuatro pacientes, sólo la primera y el último recibieron antibióticos postoperatorios a largo plazo.
La paciente 2 (tabla I) presentó fiebre y se observó que presentaba una rotura contenida de aneurisma micótico de la aorta torácica descendente (izquierda, flecha negra). La exclusión del aneurisma con implantación de endoprótesis fue satisfactoria (centro), pero, en el postoperatorio, desarrolló perforación esofágica por infección (derecha, flecha blanca, que muestra la presencia de aire alrededor de la endoprótesis). La paciente se sometió a drenaje esofágico y corrección con flap y pudo ser dada de alta, pero falleció 2 meses más tarde.
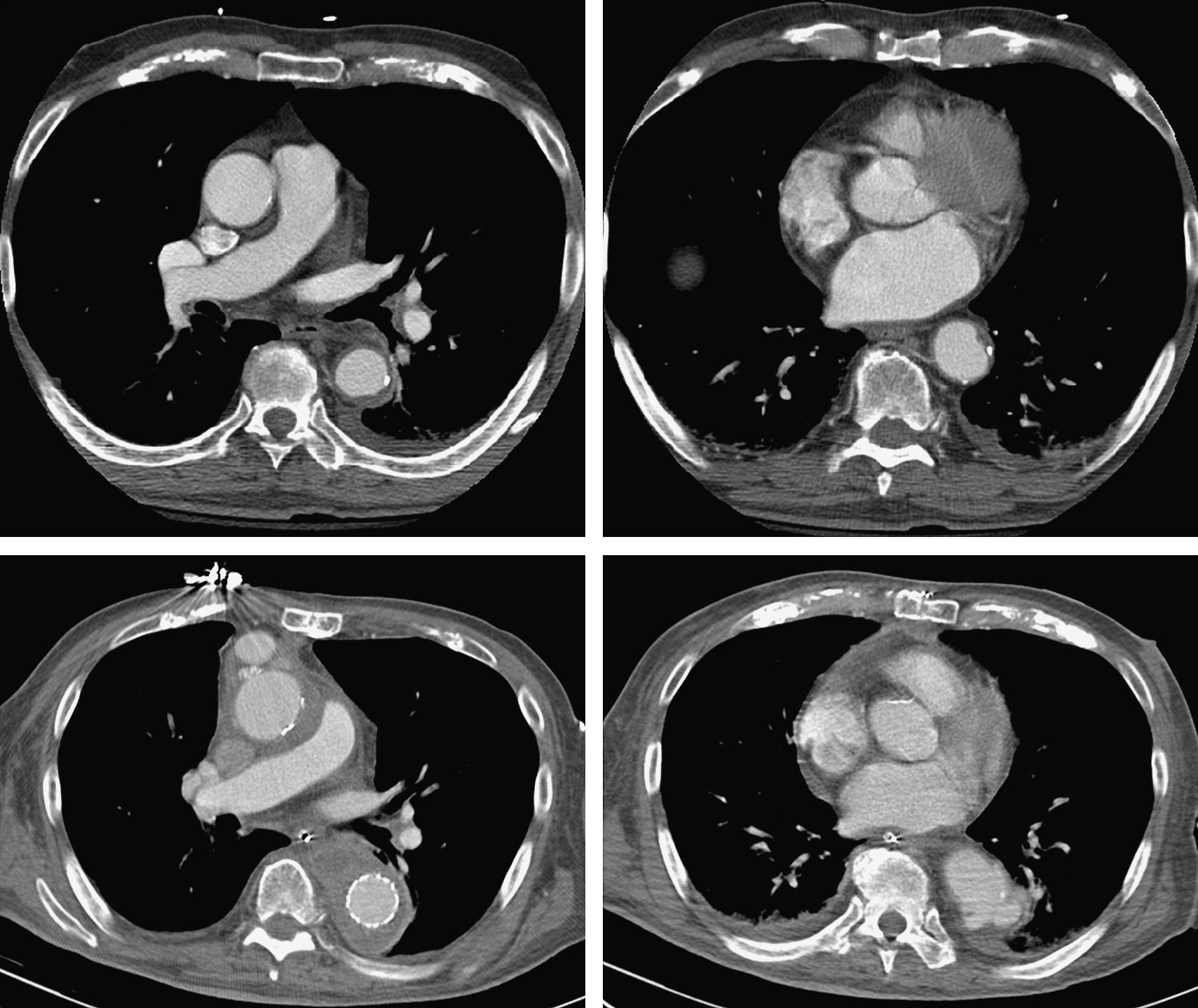
Paciente 8 (de la tabla I). Las imágenes superiores son cortes seriados del TC correspondientes a un paciente que presentó primariamente una úlcera penetrante. Fue tratado con el implante de una endoprótesis pero presentó de nuevo con hemoptisis secundaria a la erosión de un pseudoaneurisma alrededor de la endoprótesis. Una segunda endoprótesis excluyó la fístula aerobronquial, pero el paciente presentó infección persistente alrededor de la endoprótesis, observada en las imágenes correspondientes (parte inferior). Finalmente desarrolló una hemoptisis masiva que le produjo la muerte.
Durante el seguimiento medio de 257 días (límites 60-417), tres pacientes sobrevivieron. Todos recibieron antibióticos postoperatorios a largo plazo, durante 4-6 semanas. En dos no se habían identificado bacterias y fueron dados de alta con tratamiento antibiótico, que incluyó levofloxacino, metronidazol y fluconazol (tabla I, paciente 5) y vancomicina, piperacilina-tazobactam y fluconazol (tabla I, paciente 6). En el tercero se identificó Staphylococcus aureus resistente a meticilina en el hemocultivo y fue tratado con linezolid (tabla I, paciente 1). De los supervivientes, sólo un paciente requirió reintervención. Éste presentó melenas a partir de una fístula aortointestinal debido a la erosión de un pseudoaneurisma anastomótico de un bypass aortobifemoral previo (fig. 3). La rama izquierda del injerto de bypass previo estaba ocluida, y se usó una endoprótesis uniilíaca con bypass femoro-femoral para tratar satisfactoriamente la fístula y el aneurisma (fig. 4). A los 4 meses, el paciente se presentó de nuevo con una infección de la endoprótesis (Fig. 3). Tras el explante y la implantación de un bypass extraanatómico, el paciente sigue vivo y en buen estado general. El segundo superviviente desarrolló bacteriemia y aneurismas micóticos a partir de un catéter central infectado (fig. 5), mientras que el tercero era portador de una fístula aortoentérica secundaria a la erosión de un pseudoaneurisma por úlcera penetrante. En ambos pacientes la reparación endovascular fue satisfactoria y en el seguimiento presentan buen estado general.
Paciente 6 (de la tabla I). Reconstrucción TC (izquierda) y corte axial TC (derecha, parte superior) de un pseudoaneurisma anastomótico que erosionó el tracto gastrointestinal causando una hemorragia digestiva. Corte axial TC (derecha, parte inferior) 4 meses después de la exclusión endovascular, que muestra la endoprótesis infectada; obsérvese la presencia de aire en la luz del injerto (flecha blanca). El paciente fue tratado mediante bypass extraanatómico y explante de la endoprótesis, en el seguimiento presenta buen estado general.
Angiografía intraoperatoria de un pseudoaneurisma anastomótico (flecha blanca) en la porción proximal de injerto previo (bypass aortobifemoral) en el paciente 6 (izquierda). Sólo estaba permeable la rama derecha (flecha negra). Reparación EV con endoprótesis aorto-uniilíaca desde la aorta nativa a la rama derecha del bypass (derecha). La arteria ilíaca común izquierda nativa se ha ocluido con coils.
Paciente 1 (de la tabla I). TC (izquierda) y angiografía (centro) de un aneurisma micótico toracoabdominal. Exclusión del aneurisma con una endoprótesis (derecha) y cobertura del tronco celíaco (flecha blanca). Durante el seguimiento el paciente ha permanecido en buen estado general.
Los aneurismas micóticos son entidades poco frecuentes.
En la presente serie de casos encontramos que el 3% de las reparaciones aórticas EV correspondieron a esta indicación, y que en las diferentes series se encuentra en el extremo superior de las incidencias descritas del 0,8-3,4%3-6. El tratamiento conservador de este proceso consiste en el desbridamiento del tejido infectado y las técnicas de corrección en la aorta torácica incluyen angioplastia con parche in situ y bypass aortoaórtico. En la aorta abdominal pueden utilizarse bypass in situ o extraanatómicos en función de la gravedad de la infección. En 1999, Soravia-Dunand et al efectuaron una de las revisiones a mayor escala e identificaron 136 casos de infecciones aórticas por Salmonella durante los 50 últimos años7. En 52 pacientes el tratamiento consistió en antibioterapia exclusiva y la tasa de mortalidad global fue del 96% comparado con el 38% en los otros 84 pacientes tratados con cirugía abierta y antibióticos. En esta serie hubo una incidencia del 14% de fístula aortoentérica o bronquial asociada.
En las series más contemporáneas, destaca una con 33 pacientes que se sometieron a un procedimiento abierto con una tasa de mortalidad global a los 30 días del 36%, y no se identificaron diferencias estadísticamente significativas en esta variable cuando se dividió a los pacientes en un grupo de corrección extraanatómica comparado con in situ (50% frente al 32%, respectivamente), torácica comparado con abdominal (38% frente al 36%, respectivamente), o roturas (incluyendo contenidas y fístulas) comparado con aneurismas sin rotura8 (63% frente a 28%, respectivamente). Otro estudio efectuado en 35 pacientes refirió una tasa más baja de mortalidad hospitalaria (11%) (4/35) pero no documentaron el número de fístulas aortoentérica o bronquial; los pacientes supervivientes fueron seguidos una mediana de 27 meses, y la tasa de mortalidad tardía fue del 17%9 (6/35). En otra serie de 43 pacientes y con un seguimiento medio de 4,3 años se encontró una tasa de supervivencia a los 5 años del 50%; a los 9 años, ya no se identificó diferencia en la supervivencia entre las correcciones aórticas abiertas en pacientes con aneurisma infectado comparado con no infectado10. En comparación con las series de corrección abierta de aneurisma micótico, nuestras tasas de mortalidad a los 30 días (22%) y tardía (44%) se encuadran en las descritas del 11-36% y 17-50%.
En una revisión reciente sobre tratamiento endovascular en aneurismas micóticos, Kan et al2 recogieron 48 pacientes de 22 estudios. Tras revisar individualmente todos los trabajos, encontraron dos muertes omitidas del estudio de Ting et al11, lo que modificaba la supervivencia de la revisión. La mortalidad global fue del 25%, con una tasa a los 30 días del 10% y una tasa de mortalidad tardía del 15% durante un período medio de seguimiento de 20 meses (límites 0-96). En relación con estos resultados, las tasas de mortalidad global del presente estudio, a los 30 días y tardía fueron mayores: 67%, 22% y 44%, respectivamente (tabla II). Una posible explicación de esta discrepancia es la elevada incidencia de fístula aortoentérica o bronquial identificadas de nuestra serie (6/9, 67%), comparada con la de revisión (13/48, 27%). Para los portadores de fístulas aortoentéricas y bronquiales de nuestro estudio las tasas de mortalidad global, a los 30 días y tardía fueron muy similares, del 33%, 33% y 67% en nuestra serie (tabla II) y del 15%, 39% y 54% en la revisión.
Mortalidad por criterios
| Total | Rotura | Fístula | Antibióticos | Cultivo positivo | |||||
| Mortalidad | (N = 9) (%) | Sía (n = 8) (%) | No (n = 1) (%) | Síb (n = 6) (%) | No (n = 3) (%) | Síc (n = 7) (%) | No (n = 2) (%) | Síd (n = 5) (%) | No (n = 4) (%) |
| 30 días | 2 (22%) | 2 (25%) | 0 | 2 (33%) | 0 | 2 (29%) | 0 | 2 (40%) | 0 |
| Tardía | 4 (44%) | 4 (50%) | 0 | 2 (33%) | 2 (67%) | 2 (29%) | 2 (100%) | 2 (40%) | 2 (50%) |
| Total | 6 (67%) | 6 (75%) | 0 | 4 (67%) | 2 (67%) | 4 (57%) | 2 (100%) | 4 (80%) | 2 (50%) |
La comparación de los resultados del tratamiento de aneurismas micóticos mediante procedimiento EV y abierto puede ser difícil debido a la variabilidad de la presentación, etiología de la infección y comorbilidades de los pacientes individuales, que se observa en las diferentes series. Además, también es posible que esté presente un sesgo de selección entre los que se someten a tratamiento endovascular. En función de nuestra experiencia, la reparación endovascular es una técnica razonable a corto plazo para tratar la hemorragia gastrointestinal aguda, hemoptisis o inestabilidad hemodinámica debida a rotura de aneurismas. No obstante, como se observa en nuestra serie, el 71% (5/7) de los que sobrevivieron 30 días requirieron el explante de la endoprótesis o fallecieron secundariamente por las complicaciones de la infección aórtica inicial y/o de la REVA. A pesar del tratamiento antibiótico, la contaminación bacteriana del saco aneurismático puede persistir tras la exclusión mediante endoprótesis. En el caso de las fístulas aortoentérica o bronquial asociadas esto se agrava por la conexión persistente entre el tracto aerodigestivo y el saco del aneurisma12. En pacientes con aneurismas micóticos la reparación endovascular inicial ha de considerarse un procedimiento provisional mientras se espera el momento apropiado de la corrección quirúrgica abierta, una vez el paciente se ha estabilizado.
La duración de la pauta antibiótica postoperatoria recomendada por la mayor parte de los autores varía desde algunas semanas hasta un tratamiento de por vida. En nuestra serie, el 71% (5/7) de todos los pacientes que sobrevivieron al alta recibieron antibioticoterapia a largo plazo y su duración varió a discreción del médico responsable. Es importante mencionar que, en este estudio, los tres supervivientes fueron tratados a largo plazo. Sin embargo, debido al tamaño de la muestra, no pudimos extraer conclusiones estadísticamente significativas sobre diferencias de mortalidad entre los tratados (57%) y los no tratados (100%) con antibióticos (tabla II).
Históricamente, la Salmonella ha sido el microorganismo identificado con mayor frecuencia en los aneurismas micóticos, pero la prevalencia de Staphylococcus aureus meticilín resistente es cada vez mayor y es el origen de la infección en diversos casos clínicos y series de casos publicados sobre tratamiento quirúrgico abierto y endovascular3,12-14. Se ha destacado la virulencia asociada a las infecciones por este patógeno, que se asocia a una supervivencia significativamente menor comparado con las infecciones por especies de Salmonella9,10. En el 56% de los pacientes, SAMR fue la única bacteria identificada en el cultivo y en ellos observamos un aumento de la mortalidad (80%), respecto de los que no la presentaron (50%) (tabla II). Cuando se aísla un patógeno, la antibioticoterapia ha de basarse en los cultivos y sensibilidades. En muchos casos, no se identificará ningún microorganismo (56% en el presente estudio), por lo que es preciso seleccionar antibióticos de amplio espectro que no sólo cubran bacterias grampositivas, gramnegativas y anaeróbicas, sino también hongos. Por último, debido a la virulencia y prevalencia de Staphylococcus aureus meticilín resistente, es preciso considerar el uso añadido de linezolid o vancomicina.
ConclusionesEl aneurisma micótico es una entidad compleja con resultados muy variables del tratamiento quirúrgico debido a la población heterogénea de pacientes. En la presente investigación, abordamos un alto porcentaje de roturas de estos aneurismas y, en particular, los asociados a fístulas aortoentéricas o bronquiales, que dieron lugar a peores resultados comparado con otras series publicadas sobre tratamiento endovascular. No obstante, comparado con cirugía abierta, la mortalidad a 30 días y tardía fue similar. Para mejorar los resultados del tratamiento endovascular de esta patología, esta técnica ha de considerarse un procedimiento provisional mientras se espera el momento apropiado para la corrección quirúrgica abierta, más definitiva.