Puntos clave
- •
El test del sudor es el método por excelencia para el diagnóstico de fibrosis quística (FQ).
- •
El único test del sudor aceptado para el diagnóstico es la determinación de la concentración de cloro en una muestra de sudor estimulado por iontoforesis por pilocarpina.
- •
El test del sudor consta de 3 fases: estimulación del sudor, recogida de la muestra y análisis de la misma.
- •
El sistema más utilizado es el denominado Macroduct®.
- •
Concentraciones de cloro en sudor > 60mmol/l, en 2 muestras, son indicativas de FQ. Valores entre 30 y 60mmol/l son dudosos y por debajo de 30mmol/l es poco probable el diagnóstico de FQ.
La fibrosis quística (FQ) es la enfermedad hereditaria letal más frecuente en las poblaciones caucásicas. La prevalencia en estas se sitúa entre 1/2.000–1/4.000 recién nacidos vivos1. El test del sudor fue descrito por Gibson y Cooke en el año 1959 y continúa siendo en la actualidad el método de diagnóstico principal de la FQ. Los avances en genética molecular ayudan al diagnóstico y existen test comerciales que cubren un 70% de las mutaciones genéticas, pero aproximadamente un 10% de los pacientes de FQ no tienen ninguna mutación conocida y existe una regular relación entre fenotipo y genotipo2.
Epidemiología, Clínica y Diagnóstico de la Fibrosis QuísticaLa FQ es una enfermedad genética, de herencia autosómica recesiva, con una incidencia en nuestro medio de alrededor de 1/4.500 recién nacidos vivos; se calcula que aproximadamente una de cada 25 personas es portadora heterocigota sana de alguna de las mutaciones de la enfermedad3.
La enfermedad está causada por mutaciones en un gen que se localiza en el brazo largo del cromosoma 7, que codifica una proteína que regula el paso de iones a través de las membranas, denominada cystic fibrosis transmembrane conductance regulador (CFTR). Hay más de 1.600 mutaciones conocidas, siendo la más frecuente la denominada ΔF508, que afecta aproximadamente al 60–75% de los pacientes.
La clínica o los denominados rasgos fenotípicos de la FQ4 incluyen 4 grupos: enfermedad sinopulmonar crónica, alteraciones gastrointestinales y nutricionales, cuadros producidos por las pérdidas excesivas de sal por el sudor y ausencia bilateral de conductos deferentes en los varones. Tradicionalmente, se ha considerado que la FQ era una enfermedad severa que producía síntomas graves desde los primeros meses de vida, pero en la actualidad se sabe que existe un amplio abanico de formas de presentación clínica, con afectación muy variable y de manifestación en cualquier edad, por lo que el diagnóstico de la enfermedad a través de los distintos métodos diagnósticos, fuera de la clínica, se convierte en más importante. Aunque el estudio genético está cada vez más desarrollado, todavía existe un 10% de los pacientes que no tienen una mutación conocida, por lo que la demostración de la concentración de cloro en sudor sigue siendo el método fundamental para el diagnóstico.
Los criterios diagnósticos actuales de FQ4, según el último consenso de la European Cystic Fibrosis Society, diferencian 2 tipos de diagnóstico:
- –
FQ clásica: uno o más rasgos fenotípicos característicos junto a una concentración de cloro en sudor mayor o igual de 60mmol/l.
- –
FQ no clásica o atípica: uno o más rasgos fenotípicos, más prueba del sudor con resultado dudoso (entre 30–60mmol/l), más identificación de 2 mutaciones causantes de la enfermedad y/o una diferencia de potencial transepitelial nasal anormal.
La Cystic Fibrosis Foundation de Estados Unidos5,6, establece, en su último consenso, que en los lactantes, se debe considerar resultado dudoso entre 30–59mmol/l y en pacientes de más edad entre 40–59mmol/l; valores indicio de FQ en cualquier edad > 60mmol/l. En la última revisión conjunta de un grupo de trabajo europeo y americano se han definido los denominados cuadros relacionados con alteraciones en la CFTR, como aquellos donde se manifiesta una alteración de la CFTR, pero sin cumplir los criterios diagnósticos de FQ.
Test Del SudorEl test del sudor fue descrito por primera vez en 1959 por Gibson y Cook7 y se basa en la medición de la concentración de cloro en el sudor, estimulado mediante iontoforesis con pilocarpina. El único método que se reconoce en la actualidad como válido para el diagnóstico de FQ es la medición bioquímica de la concentración de cloro4,8 y, si es posible, también de sodio en el sudor, después de la estimulación del sudor con pilocarpina. Es lo que se denomina «test cuantitativo de iontoforesis por pilocarpina» o QPIT. Se necesitan al menos 2 QPIT positivos para el diagnóstico de FQ. Es conveniente realizarlo a partir del mes de vida para obtener resultados fiables. Los resultados obtenidos por otros métodos de recogida o de análisis (como la conductividad eléctrica, determinación de la osmolaridad, cristalización del sudor) solo son aceptables como cribado, no para el diagnóstico. El test se debe realizar por personal experimentado en la técnica y en Estados Unidos se exige una acreditación de los laboratorios que lo realizan para considerar fiable el resultado. El QPIT tiene 3 fases4:
- 1.
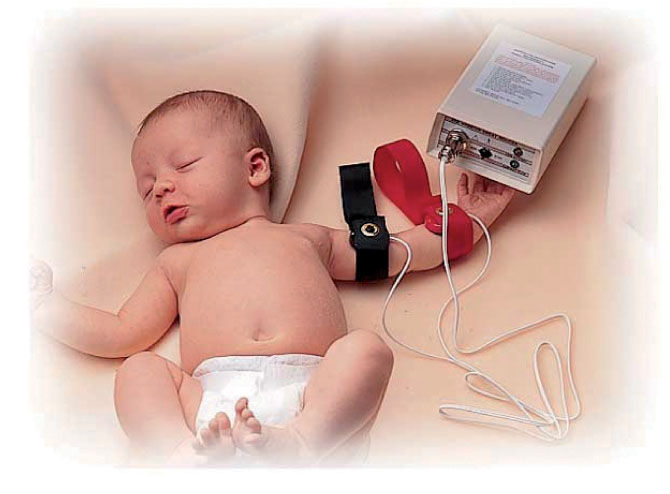
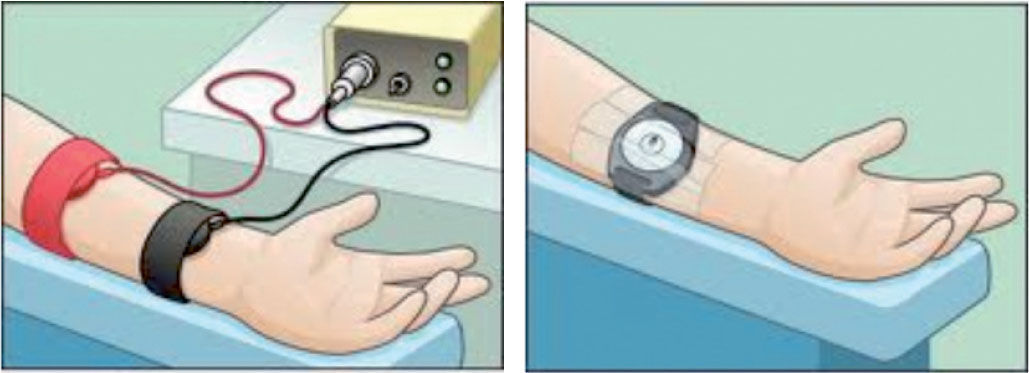
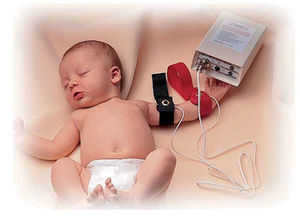
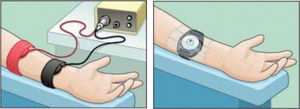
Estimulación del sudor. Se lava el antebrazo con agua destilada y alcohol. Se colocan 2 electrodos, con un reactivo de pilocarpina, en el brazo del niño (véase la fig. 1), que aplican una corriente de 1,5mA durante 5min, controlada de manera automática. Al final de la estimulación, se quitan los electrodos, se lava de nuevo la piel con agua destilada y se seca. La zona de la piel donde se realiza debe estar sana, sin procesos inflamatorios y/o infecciosos. Existe un riesgo pequeño de urticaria en la zona, irritación o quemadura (si se sobrepasa un voltaje de 4mA o por mal estado de los electrodos), que ocurre en < 1% de las pruebas realizadas.
- 2.
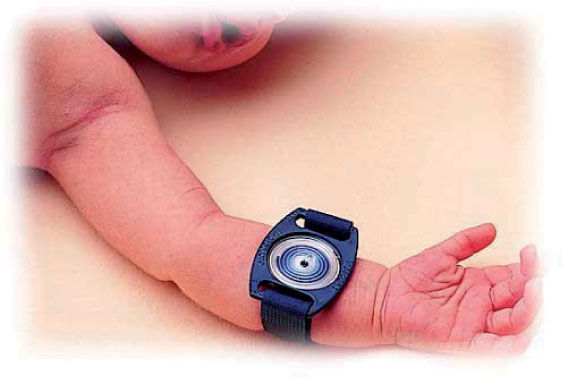
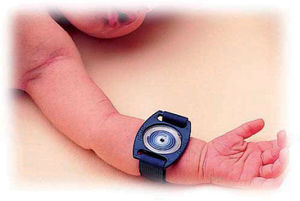
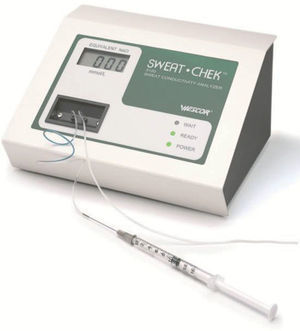
Recogida de la muestra. Se puede realizar con el método clásico de Gibson y Cook, a través de un papel de filtro o gasas prepesados, o la manera más habitual es a través del sistema denominado Macroduct®. La muestra mínima de sudor debe de ser de 75mg con el método clásico o 15μl con Macroduct®. El Macroduct® Sweat Collection System (Wescor Inc.) consiste en un disco de plástico, ligeramente cóncavo, con un agujero en el centro y un tubo de plástico que desde el agujero se enrosca en espiral (véanse las figs. 2 y 3). Tiene una pequeña cantidad de colorante azul que permite, simplemente por inspección visual, comprobar si la cantidad de sudor obtenida es correcta.
El periodo de recogida no debe superar los 30min. No se debe prolongar el tiempo de recogida para aumentar el volumen de sudor, porque se asocia al aumento de falsos negativos, por proceder de glándulas estimuladas subóptimamente. Si la cantidad de sudor obtenida es inferior a 15μl no se debe procesar la muestra. El volumen necesario es de 15–50μl, dependiendo de los métodos de cuantificación y de si sólo se mide cloro o también sodio.
De momento, no está validado para el diagnóstico de FQ el sistema denominado Nanoduct®, creado en principio para obtener muestras muy pequeñas en recién nacidos.
- 3.
Análisis de la muestra. La muestra se debe analizar en un laboratorio, determinándose la concentración de cloro mediante un cloridómetro. La técnica utilizada suele ser la coulombimetría o titulación del cloruro de plata formado por la exposición de un electrodo de plata a una solución con cloro. La concentración de sodio se puede analizar mediante fotómetro de llama.
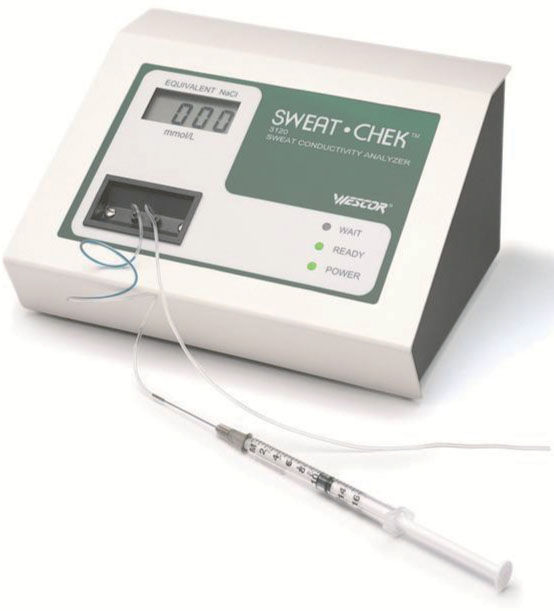
La muestra se recoge con aguja y jeringa del tubo desenrollado. Se puede analizar, como primera aproximación, a través de la célula de medición de conductividad que incorpora el aparato («sweat check», fig. 4). Según el fabricante, tests con conductividad > 95mmol/l son positivos y de 80–95mmol/l son dudosos. La Cystic Fibrosis Foundation de EE. UU. y el Grupo de Trabajo de la Sociedad de Neumología de España aconsejan realizar el QPIT si el resultado de conductividad es > 50mmol/l. Posteriormente, la muestra se transfiere a unos recipientes cónicos que facilita el fabricante, para su paso al laboratorio, para la determinación bioquímica de la concentración de cloro y sodio. Se guardan en nevera hasta el análisis, que debe ser siempre antes de 48h desde la recogida.
Interpretación de los resultados9–12. Un valor de cloro > 60mmol/l tiene una sensibilidad y especificidad cercanas al 100% para el diagnóstico de FQ. Expresado de otra manera, el 98–99% de los pacientes con FQ tienen test del sudor con valores de cloro > 60mmol/l, 1–2% tiene valores entre 40–60mmol/l y menos de 1/1.000 pacientes con FQ tienen valores < 40mmol/l. En los lactantes, los valores de cloro en sudor son menores, y 40mmol/l representa aproximadamente 3 desviaciones estándar por encima de la media para este grupo de edad, por lo que los últimos consensos consideran dudoso el test a partir de 30mmol/l en lactantes (menores de 6 meses). Valores por encima de 160mmol/l aconsejan repetir la prueba, porque son sugestivos de errores de laboratorio.
La sensibilidad y la especificidad de los valores de la medición de sodio son menores, especialmente en adultos, ya que los niveles de sodio en sudor aumentan con la edad. De todas formas, se consideran como positivos niveles de Na > 60mmol/l, y en pacientes con valores de cloro dudosos, una relación entre Cl/Na > 1, se considera muy indicativa de FQ.
Las causas que pueden alterar los resultados del test, produciendo falsos positivos o negativos, se especifican en la tabla 1, y hay que tenerlas en cuenta a la hora de la interpretación de los resultados. De todas formas, la mayoría de las causas de falsos negativos y positivos del test son metodológicas, por error o método inadecuado en alguno de los pasos del test2,3.
Causas de falsos positivos y negativos en el test del sudor.
| Falsos positivos | Falsos negativos |
| Seudohipoaldosteronismo congénito | Errores técnicos |
| Insuficiencia suprarrenal no tratada | Edema de la zona estimulada |
| Hipotiroidismo no tratado | Hipoproteinemia |
| Dermatitis atópica | Recién nacido en primeros días |
| Síndrome nefrótico | |
| Síndrome de Down | |
| Anorexia nerviosa | |
| Sida | |
| Malnutrición proteico-calórica | |
| Hipoparatiroidismo | |
| Síndrome de Klinefelter | |
| Mucopolisacaridosis tipo I | |
| Diabetes insípida nefrogénica | |
| Glucogenosis tipo I | |
| Déficit de glucosa-6-fosfato deshidrogenasa | |
| Fucosidosis | |
| Colestasis familiar (enfermedad de Byler) | |
| Síndrome de Mauriac | |
| Infusión de PG E-1 a largo plazo | |
| Hipogammaglobulinemia | |
| Displasia ectodérmica | |
| Disautonomía familiar | |
| Deprivación ambiental (retraso crecimiento psicosocial) | |
| Errores técnicos |
Los autores declaran no tener ningún conflicto de intereses.
Anexo 1Información al paciente
- –
El test del sudor es un prueba que se realiza para el diagnóstico de una enfermedad genética denominada fibrosis quística.
- –
La fibrosis quística es una enfermedad que afecta de manera muy diferente a distintos niños y que les puede producir síntomas respiratorios, nutricionales y digestivos.
- –
El test del sudor es una prueba indolora, donde se recoge una cantidad pequeña de sudor del niño. La piel de la zona donde se realiza la prueba debe estar sana.
- –
Primero le colocarán a su hijo unos discos (electrodos) con unas cintas para la estimulación de la producción del sudor y posteriormente un recipiente para su recogida, como se ve en los siguientes dibujos
- –
No precisa ninguna preparación previa y su duración es de alrededor de una hora.
- –
De manera excepcional, la prueba puede producir irritación o alergia en la zona de realización.