Analizar los efectos del clampaje suprarrenal (CSR) frente al clampaje infrarrenal (CIR) en la evolución de la función renal en la cirugía del aneurisma de aorta abdominal (AAA).
Material y métodoEstudio de cohortes retrospectivo de los AAA tratados mediante cirugía abierta electiva entre 1998 y 2011. Se analizó la creatinina sérica (mg/dl) preoperatoria y a las 24, 48, 72, 96h postoperatorias y al alta. Se definió deterioro de la función renal como una creatinina > 2mg/dl en los pacientes con una creatinina basal normal o un aumento del doble de la creatinina basal en los pacientes con IRC previa. Se definió deterioro del filtrado glomerular (FG) como una disminución > 25%. Análisis multivariable de la evolución de la función renal.
ResultadosSe analizaron 464 AAA, 359 (77,4%) con CIR y 105 (22,6%) con CSR. La prevalencia de IRC preoperatoria fue similar entre ambos grupos. El tipo de clampaje no se asoció a deterioro de la función renal (CSR=8,6% vs. CIR=4,7%; p=0,13) y sí al deterioro del FG (CSR=27,6% vs. CIR=13,4%; p=0,001). El tiempo de clampaje, la pérdida sanguínea y la IRC preoperatoria fueron factores de riesgo independientes para deterioro de la función renal. El tipo de clampaje aumentó el riesgo de deterioro de la función renal a partir de los 30min (p=0,001), asociándose a deterioro del FG (OR 2,04; IC 95% 0,94-4,47) de forma independiente.
ConclusiónCon CSR inferiores a 30min, en pacientes con creatinina normal, no es previsible un deterioro de la función renal. Con IRC previa o si se espera un CSR prolongado, es esperable un deterioro de la función renal, por lo que deberían valorarse métodos de protección renal.
To analyse the effects of suprarenal cross-clamping (SC) as opposed to the infrarenal position (IC) in the evolution of the renal function abdominal aorta aneurysm (AAA) surgery.
Material and methodA retrospective cohort study of AAAs treated by elective open surgery between 1998 and 2011. The preoperative level of serum creatinine (mg/dL) was determined and compared to postoperative level at 24, 48, 72 and 96hours, and on discharge. A deterioration in the renal function was defined as a creatinine > 2mg/dL in patients with a normal baseline creatinine level or an increase of double the baseline creatinine in patients with a previous chronic renal insufficiency (CRI). A deterioration of the glomerular filtrate (GF) was defined as a > 25% decrease. Multivariable analysis was performed on the evolution of the renal function.
ResultsA total of 464 AAA's were analysed, 359 (77.4%) with IC, and 105 (22.6%) with SC. The prevalence of preoperative CRI was similar in both groups. The type of clamp was not associated with a deterioration in the renal function (SC=8.6% vs. IC=5.7%; p=.13) but was associated with a deterioration of the GF (SC=27.6% vs. IC=13.4%; p=.001). The time the clamp was in place, the blood loss, and the preoperative CRI were independent risk factors for the deterioration of the renal function. The type of clamp increased the risk of deterioration of the renal function beyond 30minutes (p=.001), being independently associated with a deterioration in the GF (OR 2.04; 95% CI: 0.94-4.47).
ConclusionWith SC less than 30min, in patients with a creatinine level, a deterioration in the renal function is not foreseeable. With prior CRI, or if a prolonged SC is foreseen, a deterioration in the renal function can be expected, thereby making it necessary to evaluate methods for renal protection.
Los aneurismas yuxtarrenales (AYR) representan un 15% de los aneurismas de aorta abdominal (AAA)1 y, por definición, no disponen de un cuello infrarrenal de suficiente longitud para poder colocar un clamp, realizar una anastomosis protésica o garantizar el soporte de una endoprótesis.
Desde que en 1991 se introdujera el tratamiento endovascular de los aneurismas de aorta abdominal (EVAR), se ha producido un gran cambio en el tipo de tratamiento de esta enfermedad. Actualmente se estima que alrededor de un 70% de los AAA se tratan mediante esta técnica2. La creciente utilización del EVAR está produciendo un cambio en la demografía de los pacientes que se intervienen mediante cirugía abierta. Diferentes publicaciones han destacado la mayor complejidad técnica de los pacientes que se intervienen mediante cirugía abierta, siendo preciso un clampaje suprarrenal hasta en un 60% de los casos3, lo cual implica un mayor riesgo de deterioro de la función renal y de hemodiálisis. En la era endovascular y con el desarrollo de endoprótesis fenestradas y ramificadas existen numerosos estudios que demuestran que el clampaje suprarrenal (CSR) no conlleva un aumento significativo en cuanto a complicaciones renales y mortalidad perioperatoria respecto al clampaje infrarrenal (CIR), por lo que concluyen que la cirugía abierta del AYR se debe considerar el gold-standard actualmente1,4,5.
El objetivo del presente estudio es evaluar los resultados del tratamiento quirúrgico electivo de los AYR y analizar la evolución de la función renal tras el CSR.
Material y métodosSe diseñó un estudio de cohortes retrospectivo en el que se incluyeron los AAA tratados mediante cirugía abierta electiva entre 1998 y 2011 y se dividieron en 2 grupos en función del tipo de clampaje realizado. El tipo de clampaje se determinó en función de la distancia entre el aneurisma y las arterias renales y la presencia de calcio o trombo mural a ese nivel. Se excluyeron los casos con clampaje supravisceral, aneurismas pararrenales, toracoabdominales tipo iv y aquellos en los que se realizase algún procedimiento simultáneo de revascularización de una arteria renal.
Se registraron los datos referentes a la demografía, incluida edad y sexo, el diámetro máximo del AAA, factores de riesgo cardiovascular y comorbilidad asociada. La función renal preoperatoria normal se definió con una creatinina sérica menor de 1,5mg/dl. Se registraron las variables intraoperatorias incluido el tipo de abordaje, el tipo de bypass, el tiempo de clampaje suprarrenal, la sección de vena renal y las pérdidas hemáticas según los valores recogidos en el autotransfusor que se utilizó de forma sistemática.
Se registraron los valores de creatinina sérica a las 24, 48, 72 y 96h postoperatorias y al alta y se calculó el filtrado glomerular (FG) según la fórmula MDRD que aplica la ecuación GFR=186×creatinina sérica−1,154×edad−0,203×0,742 (si mujer)×1,21 (si afroamericano). Se definió como deterioro de la función renal un aumento de la creatinina por encima de los 2mg/dl en pacientes con una función renal preoperatoria normal y un aumento del doble de la creatinina basal en pacientes con insuficiencia renal preoperatoria. Además, se definió el riesgo de deterioro de la función renal como un descenso mayor del 25% del FG basal. Estos criterios se definieron según la clasificación RIFLE publicada en 20046. Se registraron las complicaciones postoperatorias y la mortalidad a los 30 días. Se analizaron los resultados en términos de morbimortalidad precoz, estancia hospitalaria y mortalidad durante el seguimiento.
Las variables cualitativas se describen con su distribución de frecuencias y las cuantitativas con su media y desviación estándar o mediana y rango intercuartílico en caso de asimetría. La comparación basal entre el tipo de clampaje se realizó en variables cualitativas con el test de ji al cuadrado y las cuantitativas con la t de Student o test no paramétricos en caso de que fuera necesario. Se ajustó un modelo de propensity score para evaluar la confusión de las variables significativas en el análisis univariable entre los tipos de clampaje. El propensity score identifica aquellas variables que pueden afectar a los resultados o producir confusión en estudios no aleatorizados en los que los grupos a estudio no son homogéneos. Se ajustaron modelos de regresión logística sobre las variables de resultado (deterioro de función renal, deterioro del FG, mortalidad precoz y tardía) en función de tipo de clampaje y ajustado por el propensity score. Se calcularon curvas ROC para determinar el punto discriminativo en las variables cuantitativas que predecía el deterioro de función renal en el seguimiento. Para evaluar la mortalidad se realizó un análisis de supervivencia por curvas de Kaplan-Meier y la hazard ratio con un modelo de Cox. Para todas las pruebas se aceptó un valor de significación del 5%. El procesamiento y análisis de los datos se realizó mediante el paquete estadístico SPSS 15.0.
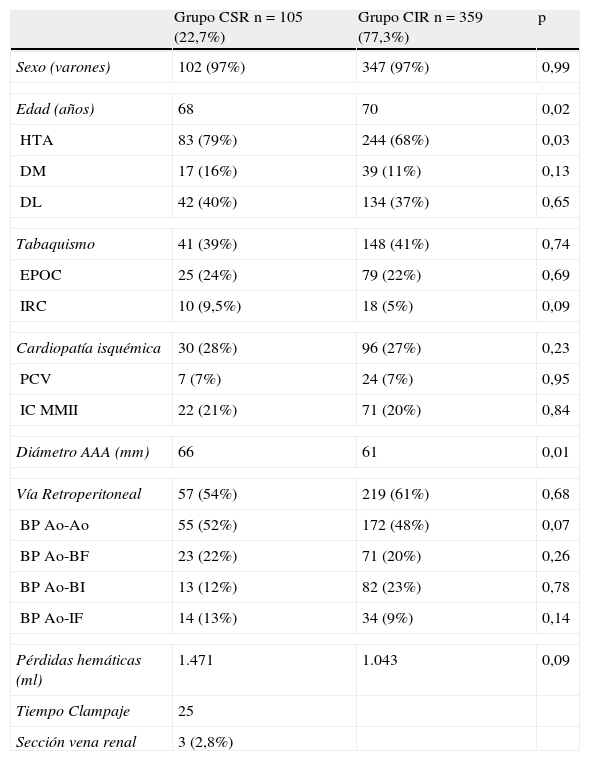
ResultadosSe incluyeron 464 AAA de los cuales en un 77% se realizó un CIR y en un 23% CSR. La media de edad del grupo con CSR fue 68 años, siendo significativamente menor respecto al grupo infrarrenal, mientras que el porcentaje de pacientes hipertensos fue significativamente mayor en el grupo con CSR. El diámetro medio de los aneurismas con CSR fue de 66mm con un tiempo medio de CSR de 25min. Las pérdidas hemáticas medias en este grupo fueron de 1.470 ml existiendo una tendencia que no alcanzó la significación estadística respecto al grupo con CIR (tabla 1). El propensity score demostró que la probabilidad de pertenecer al grupo de clampaje suprarrenal se podía ver influida por la edad (p=0,002), la HTA (p=0,03) y el diámetro del aneurisma (p=0,01). Los resultados de este modelo se incluyeron posteriormente en el análisis multivariable.
Demografía, factores de riesgo cardiovascular y variables intraoperatorias
| Grupo CSR n=105 (22,7%) | Grupo CIR n=359 (77,3%) | p | |
| Sexo (varones) | 102 (97%) | 347 (97%) | 0,99 |
| Edad (años) | 68 | 70 | 0,02 |
| HTA | 83 (79%) | 244 (68%) | 0,03 |
| DM | 17 (16%) | 39 (11%) | 0,13 |
| DL | 42 (40%) | 134 (37%) | 0,65 |
| Tabaquismo | 41 (39%) | 148 (41%) | 0,74 |
| EPOC | 25 (24%) | 79 (22%) | 0,69 |
| IRC | 10 (9,5%) | 18 (5%) | 0,09 |
| Cardiopatía isquémica | 30 (28%) | 96 (27%) | 0,23 |
| PCV | 7 (7%) | 24 (7%) | 0,95 |
| IC MMII | 22 (21%) | 71 (20%) | 0,84 |
| Diámetro AAA (mm) | 66 | 61 | 0,01 |
| Vía Retroperitoneal | 57 (54%) | 219 (61%) | 0,68 |
| BP Ao-Ao | 55 (52%) | 172 (48%) | 0,07 |
| BP Ao-BF | 23 (22%) | 71 (20%) | 0,26 |
| BP Ao-BI | 13 (12%) | 82 (23%) | 0,78 |
| BP Ao-IF | 14 (13%) | 34 (9%) | 0,14 |
| Pérdidas hemáticas (ml) | 1.471 | 1.043 | 0,09 |
| Tiempo Clampaje | 25 | ||
| Sección vena renal | 3 (2,8%) | ||
BP Ao-Ao: bypass aorto-aórtica; BP Ao-BF: bypass aorto-bifemoral; BP Ao-BI: bypass aorto-bilíaco; BP Ao-IF: bypass aorto-iliofemoral; CIR: clampaje infrarrenal; CSR: clampaje suprarrenal; DL: dyslipidemia; DM: diabetes mellitus; EPOC: enfermedad pulmonar obstructiva crónica; HTA: hipertensión arterial; ICMMII: isquemia crónica de miembros inferiores; IRC: insuficiencia renal crónica.
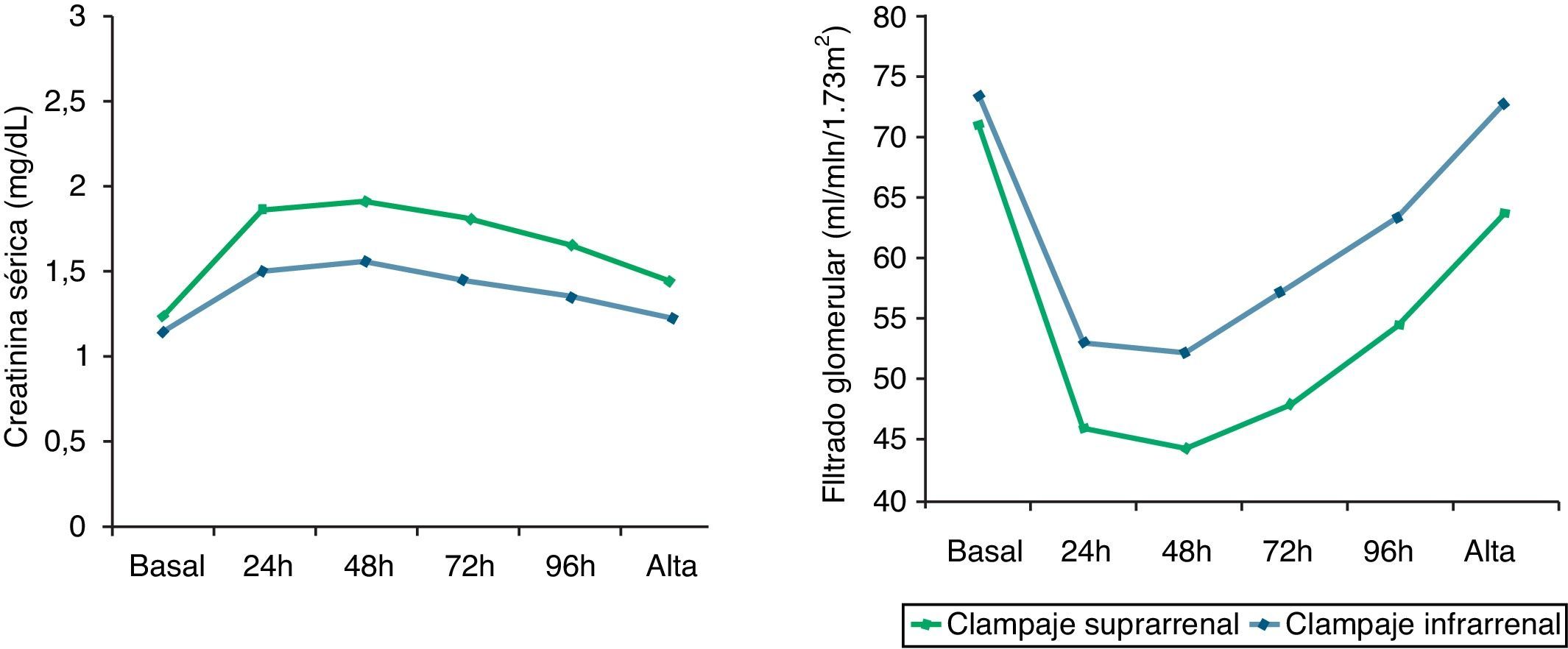
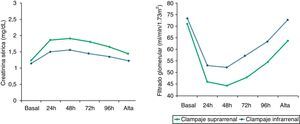
Las cifras de creatinina ascendieron en ambos grupos durante el postoperatorio inmediato, presentando las cifras más altas a las 48h de la cirugía en ambos grupos. El ascenso de creatinina fue mayor en el grupo con CSR con un pico cercano a 1,9mg/dl, disminuyendo de forma paralela hasta alcanzar unas cifras similares a las basales en el momento del alta. La diferencia de creatinina sérica basal fue de 0,09mg/dl entre ambos grupos (p=0,5), mientras que al alta fue de 0,22mg/dl (p<0,01). De igual forma, las cifras de FG descendieron bruscamente en las primeras 24h del postoperatorio y alcanzaron las cifras menores a las 48h. El grupo con CIR normalizó totalmente las cifras de FG en el momento del alta mientras que el grupo con CSR presentó unos valores medios levemente menores, aunque estadísticamente significativos, a los basales en el momento del alta (FG al alta CSR 63,8ml/min vs. CIR 72,9ml/min; diferencia ambos grupos FG al alta 9,1ml/min, p<0,01) (fig. 1).
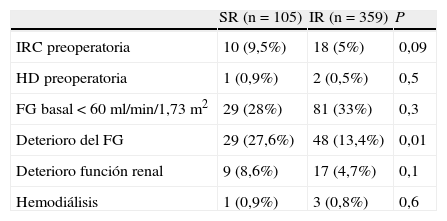
No hubo diferencias en la función renal basal entre ambos grupos. Tampoco hubo diferencias significativas en cuanto al deterioro de la función renal en el postoperatorio. El 8,6% de los pacientes del grupo con CSR sufrió un deterioro de la función renal y tan solo un paciente precisó diálisis definitiva. En cuanto al FG, el grupo con CSR presentó un 27% de pacientes con disminución > 25% del filtrado glomerular (riesgo de deterioro de la función renal), siendo este porcentaje significativamente mayor respecto al grupo infrarrenal (tabla 2).
Evolución de la función renal
| SR (n=105) | IR (n=359) | P | |
| IRC preoperatoria | 10 (9,5%) | 18 (5%) | 0,09 |
| HD preoperatoria | 1 (0,9%) | 2 (0,5%) | 0,5 |
| FG basal < 60ml/min/1,73 m2 | 29 (28%) | 81 (33%) | 0,3 |
| Deterioro del FG | 29 (27,6%) | 48 (13,4%) | 0,01 |
| Deterioro función renal | 9 (8,6%) | 17 (4,7%) | 0,1 |
| Hemodiálisis | 1 (0,9%) | 3 (0,8%) | 0,6 |
FG: filtrado glomerular; HD: hemodiálisis; IR: infrarrenal; IRC: insuficiencia renal crónica; SR: suprarrenal.
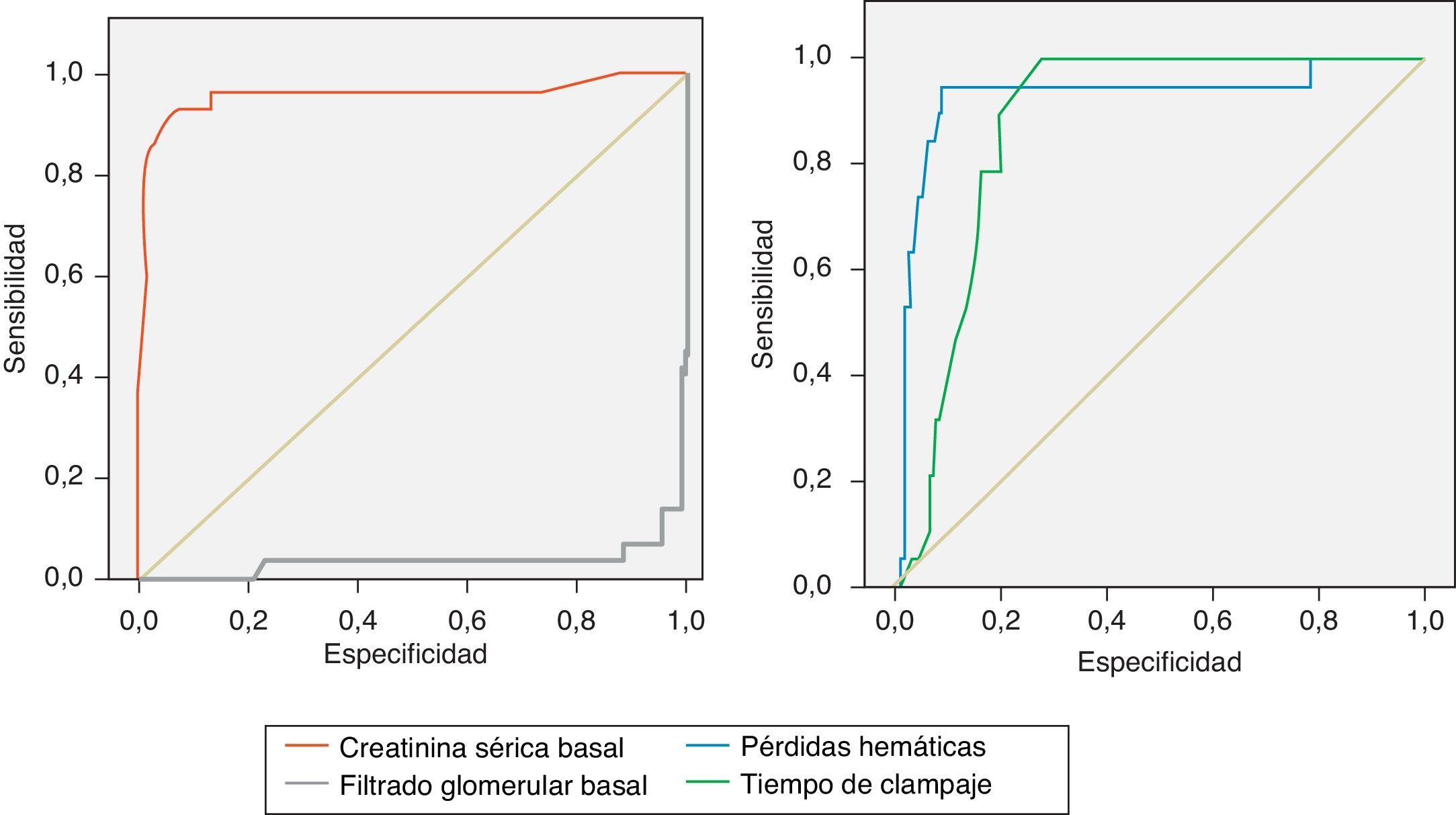
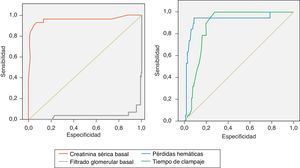
Se realizaron curvas ROC en la serie global para determinar los valores predictivos de deterioro de la función renal de las variables cuantitativas. En el caso de las pérdidas hemáticas se obtuvo una sensibilidad y especificidad para el punto de corte de 1.600 ml del 95 y 90%, respectivamente. En el caso del tiempo de clampaje, se obtuvo una sensibilidad del 100% y una especificidad del 73% para el punto de corte de 30 min. Las curvas ROC de cada grupo según el tipo de clampaje revelaron unos resultados parecidos a los de la serie global. La creatinina sérica basal obtuvo unos valores de sensibilidad y especificidad inferiores respecto al FG, con una sensibilidad del 98 y especificidad del 86% en el punto de corte de 40ml/min (fig. 2).
El análisis multivariable ajustado por el propensity score objetivó que el clampaje suprarrenal (OR 2,1; IC 95% 1-4,5; p=0,03) como el FG basal (OR 2,3; IC 95% 1,2-4,3; p=0,007), las pérdidas hemáticas mayores de 1.600 ml (OR 8,3; IC 95% 1,1-64; p=0,005) y el tiempo de clampaje suprarrenal mayor de 30min (OR 2,8; IC 95% 1,4-5,6; p=0,001) fueron factores de riesgo independientes para deterioro del filtrado glomerular > 25% (riesgo de deterioro de la función renal) Mientras que al analizar el deterioro de la función renal, se confirmó que la creatinina sérica basal (OR 2,7; IC 95% 1,8-8,3; p=0,003), las pérdidas hemáticas mayores de 1.600 ml (OR 2,3; IC 95% 1,2-4,6; p=0,01) y el tiempo de clampaje suprarrenal mayor de 30 min (OR 7,2; IC 95% 2,6-19,6; p=0,01) se comportaban como factores de riesgo independientes mientras que el clampaje suprarrenal no fue un factor de riesgo independiente para deterioro de la función renal (OR 0,97; IC 95% 0,5-1,7; p=0,7).
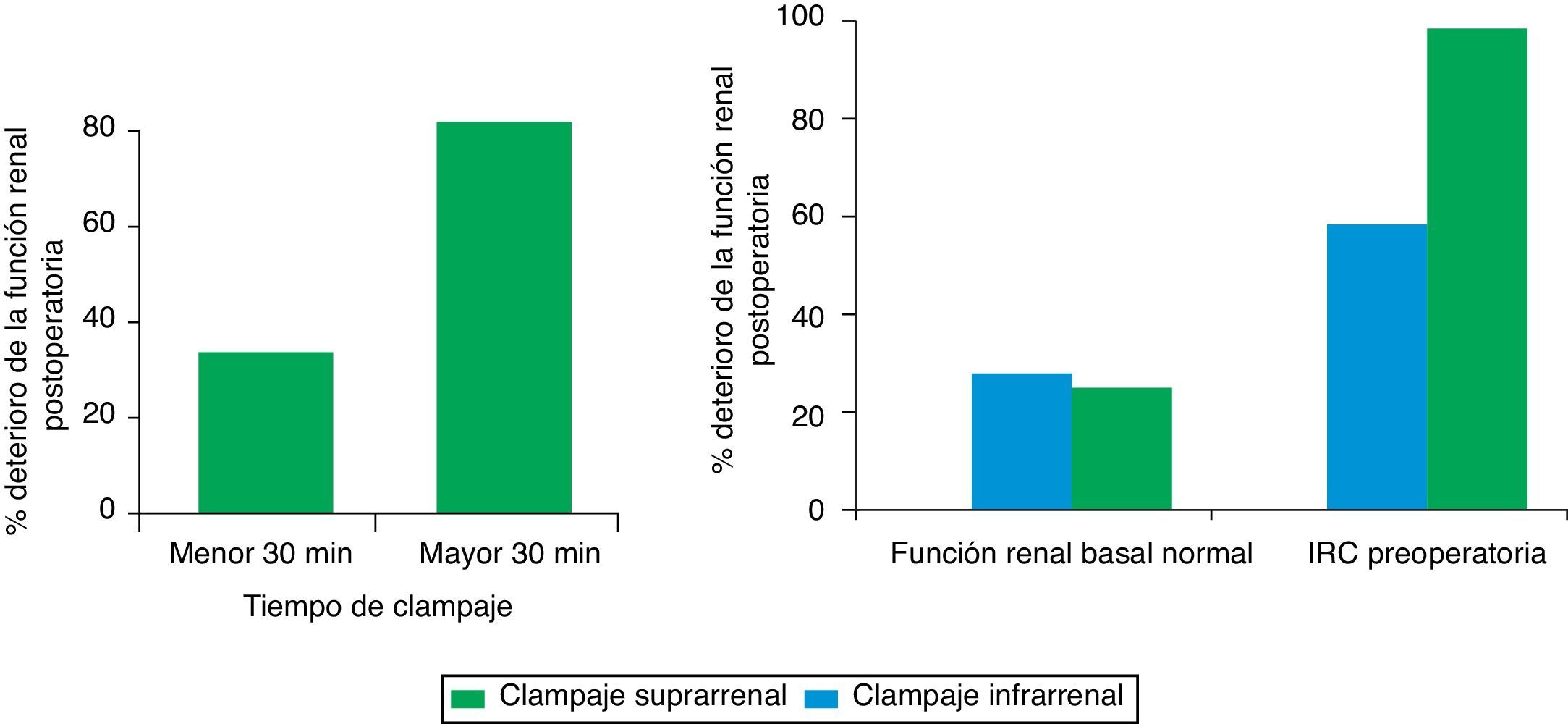
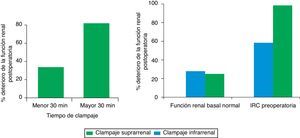
En el análisis por subgrupos se confirmó que el efecto del clampaje suprarrenal en el deterioro de la función renal dependía del tiempo de clampaje, existiendo diferencias significativas por encima de los 30 min respecto al clampaje infrarrenal (OR 7,94; IC 95% 2,64-23,68; p=0,001) y de la función renal preoperatoria, con un riesgo de 1,7 veces superior de deterioro de la función renal en los pacientes con una creatinina sérica mayor de 1,5mg/dl (fig. 3).
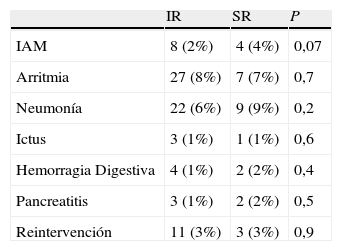
La estancia mediana fue similar para ambos grupos (estancia mediana [días], CSR 7 [RI 7-11] vs. CIR 7 [RI 6-8]; p=0,09) y no hubo diferencias significativas en cuanto a la morbilidad perioperatoria entre ambos grupos (tabla 3). La mortalidad precoz en el grupo CSR fue del 3,8% vs. CIR 2,5%; p=0,5. El análisis multivariable demostró que el CSR no aumentó el riesgo de mortalidad precoz (OR 1,05; IC 95% 0,3-4,4; p=0,83) mientras que las pérdidas hemáticas mayores a 1.600 < ml doblaron el riesgo de mortalidad aunque no de forma significativa (OR 2,05; IC 95% 0,5-7; p=0,31).
Morbilidad Perioperatoria
| IR | SR | P | |
| IAM | 8 (2%) | 4 (4%) | 0,07 |
| Arritmia | 27 (8%) | 7 (7%) | 0,7 |
| Neumonía | 22 (6%) | 9 (9%) | 0,2 |
| Ictus | 3 (1%) | 1 (1%) | 0,6 |
| Hemorragia Digestiva | 4 (1%) | 2 (2%) | 0,4 |
| Pancreatitis | 3 (1%) | 2 (2%) | 0,5 |
| Reintervención | 11 (3%) | 3 (3%) | 0,9 |
IR: infrarrenal, SR: suprarrenal, IAM: infarto agudo de miocardio.
El seguimiento mediano fue similar para ambos grupos (clampaje suprarrenal 42 [RI 10-90] meses vs. infrarrenal 52 [RI 14-85] meses) con unas cifras de supervivencia a los 5 años del 74% para el grupo suprarrenal y del 83% para el infrarrenal (p=0,8). Mediante el modelo de Cox se evidenció que el clampaje suprarrenal no aumentaba el riesgo de mortalidad a largo plazo (HR 0,98; IC 95% 0,63-1,52; p=0,94).
DiscusiónDebido a los excelentes resultados del EVAR recogidos en numerosos estudios se ha producido un cambio en el tipo de tratamiento de los AAA. No obstante, estudios posteriores han demostrado que los resultados del EVAR dependen en gran medida de la calidad del cuello infrarrenal entre otros factores, comprobando que en cuellos con una longitud menor de 15mm, excesiva angulación o calcificación se producen mayores tasas de endofugas y migración7–9. Así, numerosos estudios resaltan la mayor complejidad técnica de la cirugía aórtica abierta en la era del EVAR precisando un mayor número de CSR, desde el 6% en la era pre-EVAR hasta el 20% en 20044. En estudios más recientes este porcentaje aumenta hasta el 60% de las cirugías por AAA3. En nuestro centro, actualmente se precisa un CSR en un 34% de las cirugías aórticas.
Los resultados de la cirugía abierta de los AYR han experimentado una clara mejoría a lo largo de las últimas décadas desde la publicación por Crawford et al.10 en 1986 de la primera serie de cirugía aórtica con clampaje suprarrenal. En esta serie la mortalidad precoz fue del 7,9% con una tasa de diálisis postoperatoria del 8%. En 2002, Sarac et al. publican los resultados de la Cleveland Clinic con una serie de 138 casos, una mortalidad precoz del 5% y una tasa de diálisis postoperatoria cercana al 6%11. West publicó en 2008 la experiencia de la Clínica Mayo con 247 casos, una mortalidad del 2,7% y un 3,7% de necesidad de diálisis postoperatoria12. Jongkind et al. han publicado recientemente un metaanálisis en el que analizan los resultados de la cirugía del aneurisma yuxtarrenal en 21 estudios desde 1986 a 2008 con un total de 1.256 pacientes. La mortalidad perioperatoria fue del 2,9% con una tasa de diálisis del 3,3%1. Estos resultados coinciden con las cifras de mortalidad precoz y hemodiálisis de nuestra serie.
Uno de los problemas fundamentales a la hora de analizar los resultados de la cirugía con CSR es la falta de consenso a la hora de definir el fracaso renal agudo (FRA) en estos pacientes. Según Jongkind et al.1, se utiliza una definición distinta de FRA en cada estudio, por lo que el porcentaje de deterioro de la función renal postoperatoria varía ampliamente desde el 0 hasta el 39% en algunas series con un deterioro mediano del 18%. Por esta razón, en este estudio se han seguido las recomendaciones de Jongkind en las que propone seguir los criterios diagnósticos de fracaso renal de la clasificación RIFLE publicada en 2004 para evitar la amplia variedad de resultados en el futuro. En dicha clasificación se define el FRA según el filtrado glomerular/creatinina sérica y por otro lado según la diuresis. El deterioro del GFR basal > 25% es el criterio más sensible para detectar aquellos pacientes en riesgo de desarrollar un FRA mientras que un aumento al doble de la creatinina sérica basal es criterio de fracaso renal establecido6.
El grupo de Belkin publicó en 2009 un artículo en el que compararon los resultados de la cirugía aórtica con clampaje infrarrenal y con clampaje suprarrenal, utilizando unos criterios similares a los propuestos por el estudio RIFLE, obteniendo unos excelentes resultados con un 7% de deterioro de la función renal, un 0,6% de hemodiálisis postoperatoria y una mortalidad menor del 2% en el grupo con CSR. El autor concluye que el CSR se puede realizar con una morbimortalidad similar al CIR y que debe considerarse el gold-standard actual en la cirugía del aneurisma yuxtarrenal. Nuestros resultados son similares a los del grupo de Belkin et al.13. En ambos estudios destaca la gran importancia de la función renal preoperatoria, del tiempo de CSR y de las pérdidas hemáticas para poder identificar aquellos pacientes con un mayor riesgo de deterioro de la función renal. Es interesante destacar que el deterioro del FG ha sido un criterio más sensible, capaz de identificar aquellos pacientes en riesgo de sufrir un fracaso renal agudo. En nuestra serie un FG basal <40ml/min obtuvo una sensibilidad del 98% y una especificidad del 86% para predecir el fracaso renal agudo postoperatorio. Por lo tanto, creemos que es de gran importancia unificar los criterios de fracaso renal para poder obtener en el futuro estudios con un mayor rigor científico.
Cambria et al.14 publicarán próximamente un artículo en el que analizan los resultados a largo plazo de 199 aneurismas yuxtarrenales con un seguimiento mediano de 56 meses, una tasa de deterioro de la función renal del 10% y una mortalidad a 5 años del 74%. Este estudio servirá como punto de referencia en el futuro cuando se publiquen los resultados a largo plazo de las técnicas endovasculares. Nuestra serie tiene una mortalidad a largo plazo similar y el análisis de la función renal durante el seguimiento será motivo de futuras investigaciones.
ConclusionesEn función de estos resultados, podemos concluir que con clampajes suprarrenales inferiores a 30 min, en pacientes con creatinina normal, no es previsible un deterioro de la función renal, mientras que en pacientes con insuficiencia renal previa o si se espera un clampaje suprarrenal prolongado, es esperable un deterioro de la función renal, por lo que deberían valorarse métodos de protección renal.
El filtrado glomerular basal ha demostrado una excelente sensibilidad y especificidad en el deterioro de la función renal postoperatoria, por lo que podría ser de utilidad en futuros estudios en los que deberían utilizarse criterios diagnósticos unificados.
El clampaje suprarrenal se puede realizar de forma segura, sin existir diferencias significativas respecto al clampaje infrarrenal en cuanto a deterioro de la función renal, estancia hospitalaria, morbimortalidad precoz y durante el seguimiento.
Por lo tanto, las técnicas endovasculares deberán acreditar sus resultados para ofrecer un beneficio respecto a la cirugía aórtica con clampaje suprarrenal.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.