Introducción
Las denominadas vías de la coagulación forman uno de los ejes centrales en la formación de trombos tanto arteriales como venosos. Por ello, en los últimos 50 años los anticoagulantes han salvado tantas vidas y extremidades. En la actualidad, millones de pacientes en todo el mundo utilizan anticoagulantes para la prevención o el tratamiento de una gran variedad de problemas cardiovasculares.
El progreso de la medicina en general y de la farmacología en particular permite la aparición en la escena científica de nuevos anticoagulantes. Por ello, recientemente numerosas revistas médicas de impacto se hacen eco a través de editoriales o revisiones 1-12 de los nuevos anticoagulantes orales. Este hecho, ser activos por vía oral, los hace enormemente atractivos tanto en determinados procesos agudos como crónicos.
Perspectiva histórica de los anticoagulantes
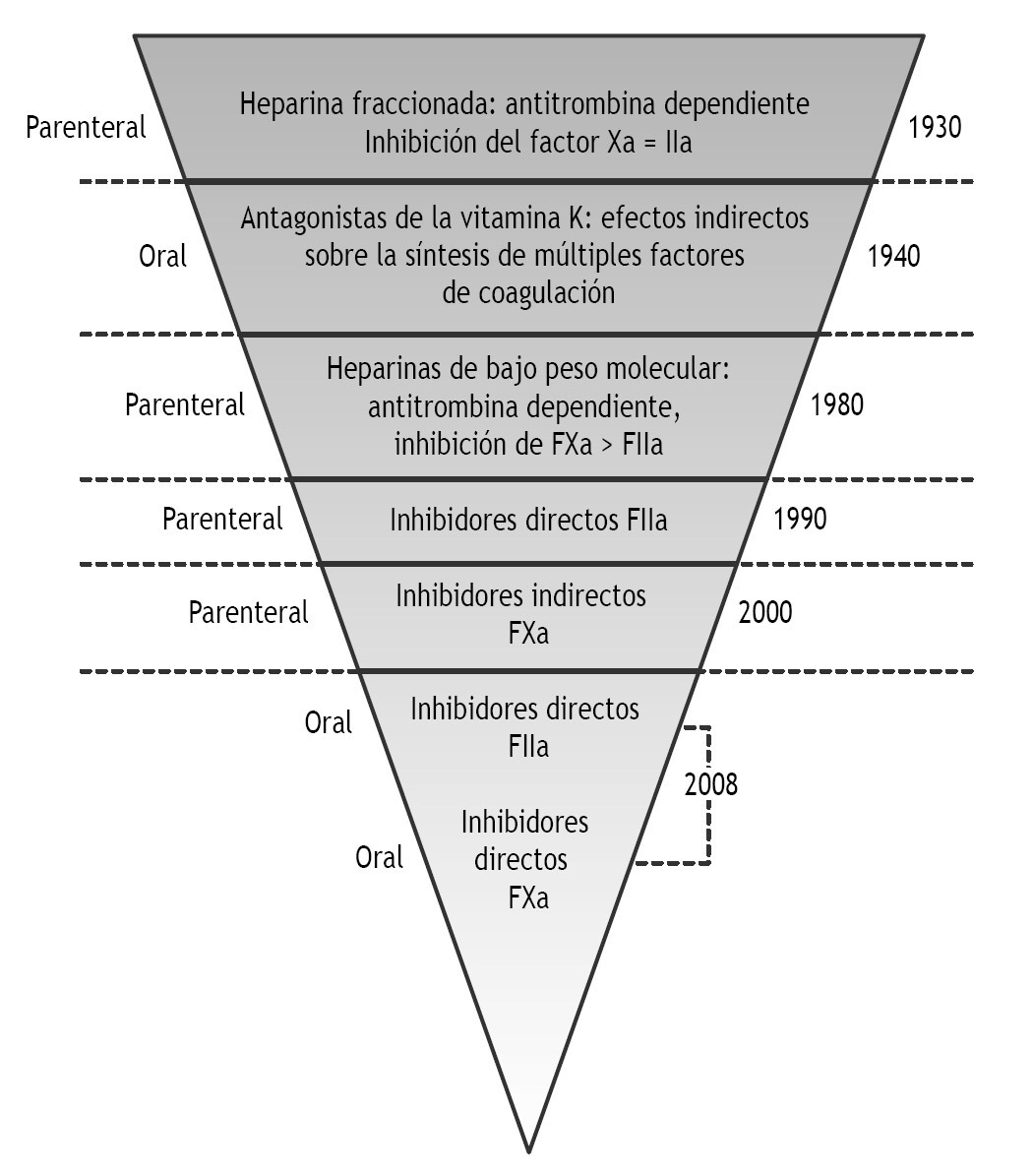
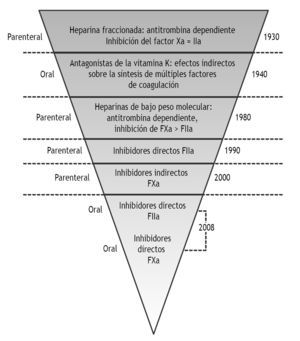
En la práctica clínica actual, por orden de su descubri miento, empleamos los siguientes anticoagulantes: a) la heparina convencional o no fraccionada (HNF); b) los anticoagulantes orales o antagonistas de la vitamina K (AVK), y c) las heparinas de bajo peso molecular (HBPM), incluida su mínima expresión o pentasacárido (fig. 1) 13.
Figura 1 Historia de los anticoagulantes. Modificada de Alban 13.
La historia de la heparina está llena de anécdotas. En el año 1918, Jay Mclean, por entonces estudiante de medicina en la Universidad Johns Hopkins (Baltimore), descubre la heparina. Su maestro, el profesor de Farmacología William Henry Howell (1918), fue quien la estudió y describió. Se denominó heparina por su abundancia en el hígado.
Charles Best (Toronto 1929), Schmitz y Fischer (Copenhague 1933) y Jorpes (Estocolmo 1935) fueron los responsables de su purificación y caracterización. Gordon Murray (1937), que trabajaba en el hospital de Best, fue el primero en realizar estudios experimentales al respecto. Por su parte Jorpes animó al cirujano Crafoord (1939) para emplear heparina en humanos. Por otro lado, en 1939, Brinkhous et al evidenciaron que la actividad anticoagulante de la heparina precisaba para su actuación de un cofactor plasmático. Ese cofactor era la antitrombina III (Abildgaard, 1968).
En 1959, Sevitt y Gallager usaron heparina profiláctica en pacientes con fractura de cadera, y en 1960 Sharnoff inicia la pauta de inyectar heparina subcutánea dos horas antes de la operación. Años más tarde Kakkar (1975) demuestra la efectividad profiláctica de la HNF a baja dosis.
El descubrimiento de los dicumarínicos o AVK se remonta a una historia acaecida en ciertas regiones del medioeste norteamericano y de Alberta, en Canadá, cuando los ganaderos de estas zonas observan cómo sus vacas fallecen a causa de una enfermedad hemorrágica (1920). Posteriormente se descubre que parte de la alimentación de este ganado consistía en un trébol "dulce" que contenía dicumarol. El descubrimiento de esta sustancia se debe a Karl Paul Link y Wilhelm Schoeffel (Universidad de Wisconsin). Dicho producto se comercializó en 1941. Posteriormente, la búsque da de un raticida permitió la síntesis de la warfarina, que fue aprobada para uso médico en 1954.
La aparición de las HBPM en la década de 1980 revolucionó tanto la profilaxis como el tratamiento de numerosas entidades clínicas. En 1978, un equipo del Instituto Choay fue el primero que concibió un nuevo medicamento constituido por fragmentos de HBPM con el objetivo de mantener las propiedades antitrombóticas de la heparina y desarrollar una actividad anticoagulante reducida, y así se emprendió el aislamiento de una fracción que poseía las propiedades buscadas.
En 1985 se realizó el lanzamiento de la primera HBPM (nadroparina). En 1987 se comercializó la enoxaparina, cuya numerosa investigación clínica hace de esta HBPM el estándar del grupo. Posteriormente han aparecido nuevas HBPM (bemiparina, dalteparina, tinzaparina, etc.). Las HBPM se empleaban de forma rutinaria en Europa y EE.UU. desde 1990 y 1995, respectivamente.
En 1981 surge el pentasacárido (Jean Choay), que representa la más pequeña porción de la heparina con actividad anti-Xa. Posteriormente colaboradores de Choay (Maurice Petitou y Jean Claude Lormeau, entre los más significativos) desarrollarán numerosas investigaciones sobre el pentasacárido (producción sintética del mismo, 1983 —fondaparinux—; caracterización y búsqueda de análogos, 1995; etc.).
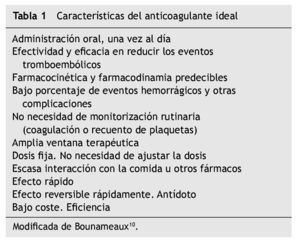
La búsqueda del anticoagulante ideal (tabla 1) continúa. La presente revisión aporta una aproximación a dicho objetivo.
Problemas y limitaciones de los actuales anticoagulantes
La HNF es un fármaco de administración parenteral, con un inicio de efecto rápido, como también lo es la supresión del mismo tras la interrupción (T1/2 aproximadamente 2 h). Posee un antídoto rápido y eficaz (sulfato de protamina).
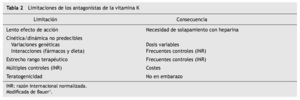
Por su parte, las AVK son de administración oral y de inicio y parada lentos (varios días). Ambas familias de fármacos poseen un elevado grado de variabilidad intra e interindividual. Ello, asociado al hecho de poseer una ventana terapéutica estrecha, evidenció la necesidad de monitorización analítica. Otros inconvenientes de las AVK se aprecian en la tabla 2; ello es importante dado que el arsenal terapéutico actual para tratamientos prolongados sigue limitado prácticamente a las AVK, como ha sido durante más de medio siglo.
La aparición de las HBPM cambió la estrategia terapéutica de muchos pacientes. Una biodisponibilidad estable y cercana al 100 % tras la administración subcutánea y una farmacocinética altamente predecible permitieron el ajuste de dosis según el peso sin necesidad de monitorización. Ello, unido a una vida media (3-5 h) algo mayor a la de la HNF, posibilitó la administración domiciliaria por vía subcutánea cada 12/24 h. Pero la HBPM presenta tres problemas importantes, como son el efecto acumulativo en la insuficiencia renal, la no disponibilidad de un antídoto plenamente eficaz y, aunque con menor frecuencia que la HNF, su implicación en la trombocitopenia inmune inducida por heparina.
Finalmente, la irrupción de fármacos de administración parenteral de diana específica (anti-Xa o antitrombina) como el pentasacárido, los derivados de la hirudina o el argatroban no han supuesto una modificación radical en la terapia anticoagulante por diversos motivos, entre otros por la sospecha de un perfil de seguridad inferior a las HBPM.
Nuevos anticoagulantes
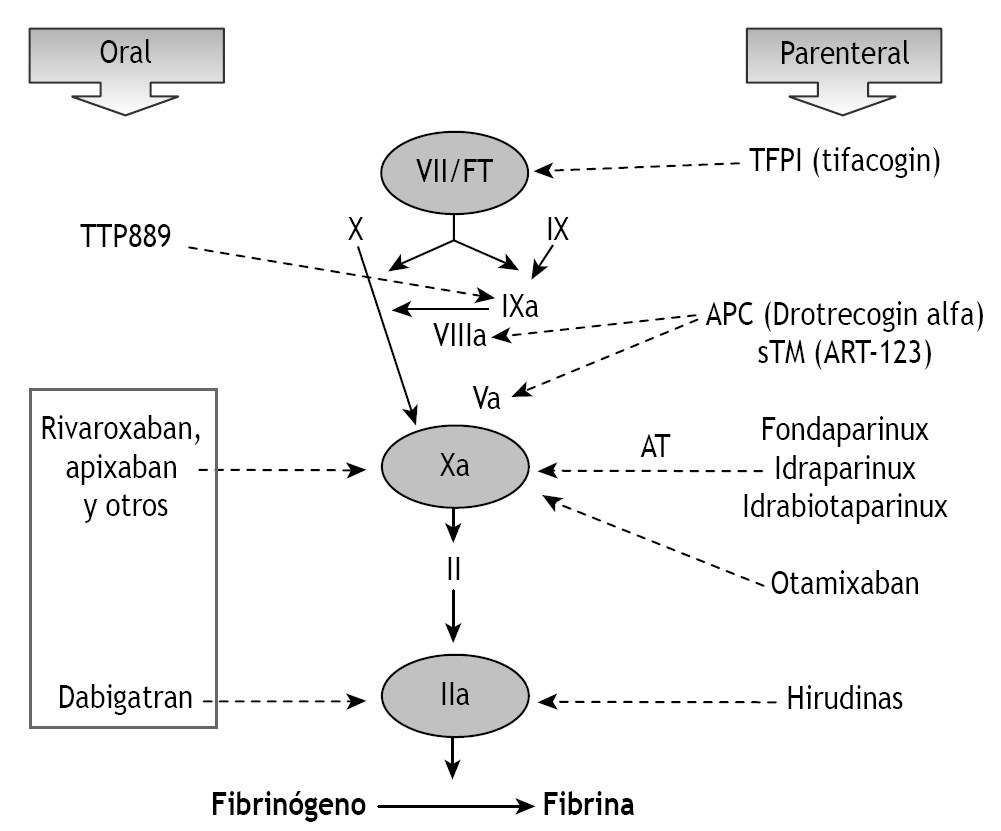
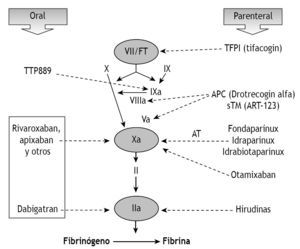
Siguiendo a Weitz et al 9,14 se clasifican en (fig. 2):
Figura 2 Mecanismo de acción (diana) de los nuevos fármacos anticoagulantes orales y parenterales. Adaptada de Weitz y Bates 14.
1. Inhibidores del inicio de la coagulación: actúan sobre el complejo factor VIIa/factor tisular. En condiciones fisiológicas este complejo es un activador del factor X y, en menor medida, de la vía intrínseca mediante su unión al factor IX. Están constituidos por fármacos de acción inhibidora directa que se administran por vía parenteral. Dos fármacos representan a este grupo: el inhibidor de la vía del factor tisular (TFPI) o tifacogin, y el NAPC2 (nematode anticoagulant peptide 2).
2. Inhibidores del factor Va: son productos en diferentes fases de estudio, tales como el drotrecogin alfa (IV) y el ART 123 (subcutáneo).
3. Inhibidores de la propagación de la coagulación. Dos grupos:
3.1. Inhibidores del factor IXa: RB006 (IV) y TTP889 (oral; fase II suspendida).
3.2. Inhibidores del factor Xa: el factor X en la encrucijada de las dos vías de la coagulación, siendo un punto clave en la regulación del sistema hemostático. Se subdividen en:
3.2.1. Inhibidores directos: a este grupo pertenecen, entre los más desarrollados, rivaroxaban y apixaban. La mayoría de ellos se administra por vía oral.
3.2.2. Inhibidores indirectos: ejercen su función inhibitoria sobre el factor Xa mediante su unión a la antitrombina. Se trata del pentasacárido sintético (fondaparinux), su análogo molecular idraparinux y un derivado de este último, el idrabiotaparinux (que posee un antídoto). Todos son de administración subcutánea.
4. Inhibidores de la trombina: este factor de la coagulación está situado en la vía común de la cascada de la coagulación y es el responsable de la activación del fibrinógeno para convertirlo en fibrina. Se dividen en:
4.1. Inhibidores directos: se unen de modo directo a la trombina, bloqueando su acción en la formación del coágulo y en la regulación de la activación de la vía intrínseca y de los anticoagulantes naturales (antitrombina, proteínas C y S). Sus principales exponentes son las hirudinas (desirudina, lepirudina) y el dabigatran etexilate (de administración oral). También pertenecen a este subgrupo el megalatran y ximegalatran, que fueron retirados por problemas de seguridad (toxicidad hepática). Un nuevo derivado del ximelagatran de bajo riesgo hepatotóxico, el AZD0837, se encuentra en fase II.
4.2. Inhibidores indirectos: inhiben la trombina mediante la potenciación del efecto inhibidor sobre la antitrombina y no mediante la unión directa a la misma. Estarían constituidos por las heparinas (que también inhiben el factor Xa) y, por tanto, fuera del contexto de este apartado sobre nuevos agentes antitrombóticos.
Nuevos anticoagulantes orales
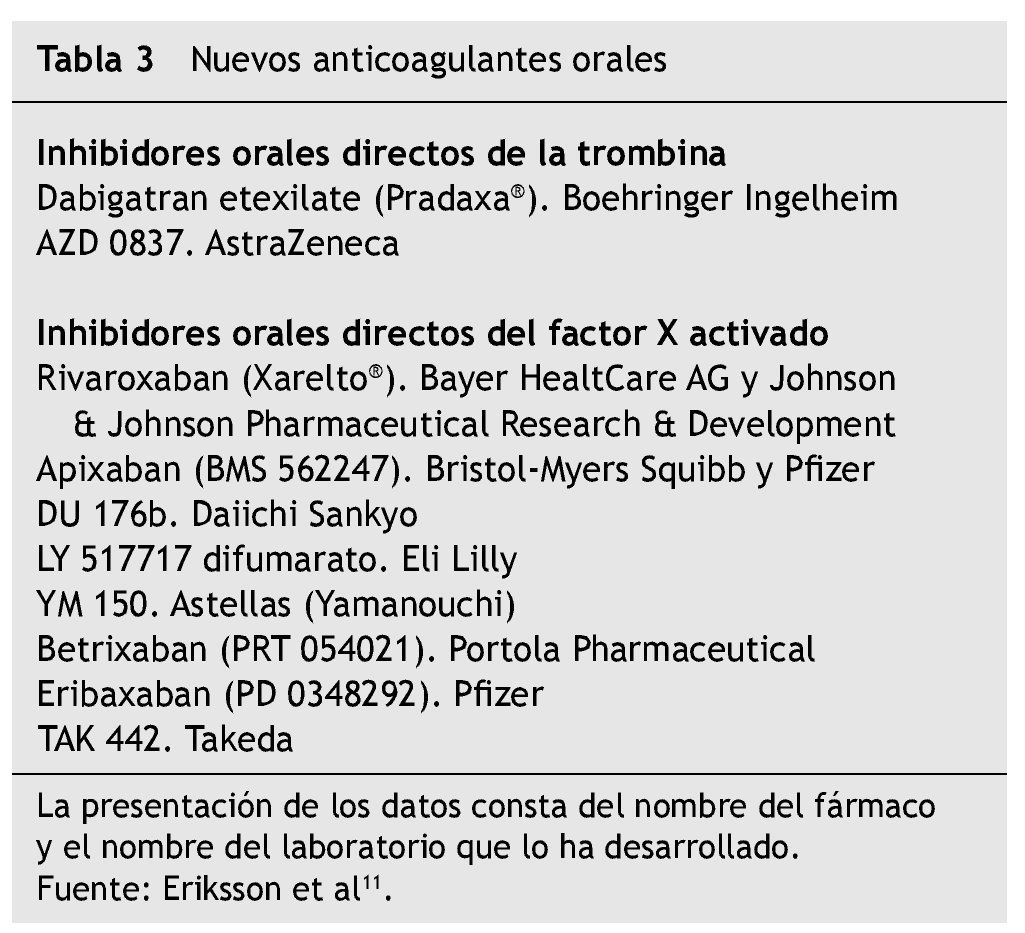
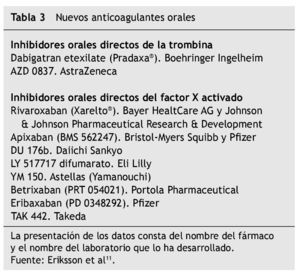
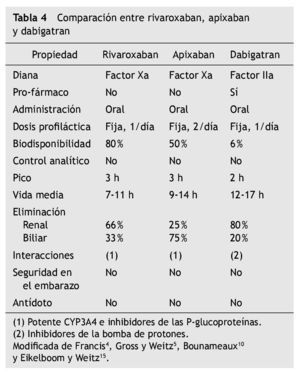
Una apuesta importante de la industria farmacéutica son los anticoagulantes de administración oral, inicio de actividad precoz y una diana específica y directa anti-Xa o anti-IIa (tabla 3).
Los productos que poseen el desarrollo clínico más avanzado son dabigatran etexilato y rivaroxaban. Apixaban es el tercero, pero con ensayos más retrasados respecto de los anteriores.
Poseen una biodisponibilidad estable al ser administrados por vía oral, una farmacocinética altamente predecible y no precisan de monitorización habitual. Ello los hace candidatos claros a sustituir a las AVK en las indicaciones duraderas, sin necesidad de combinarlos en la fase inicial con HBPM dado su inicio rápido de actividad (Tmáx 2-4 h). Son también candidatos a sustituir a las HBPM en los tratamientos domiciliarios. Poseen una vida media superior a la de las HBPM (8-17 h) y una fracción de los mismos se elimina por vía renal (25-80 %). No disponen de antídoto por el momento.
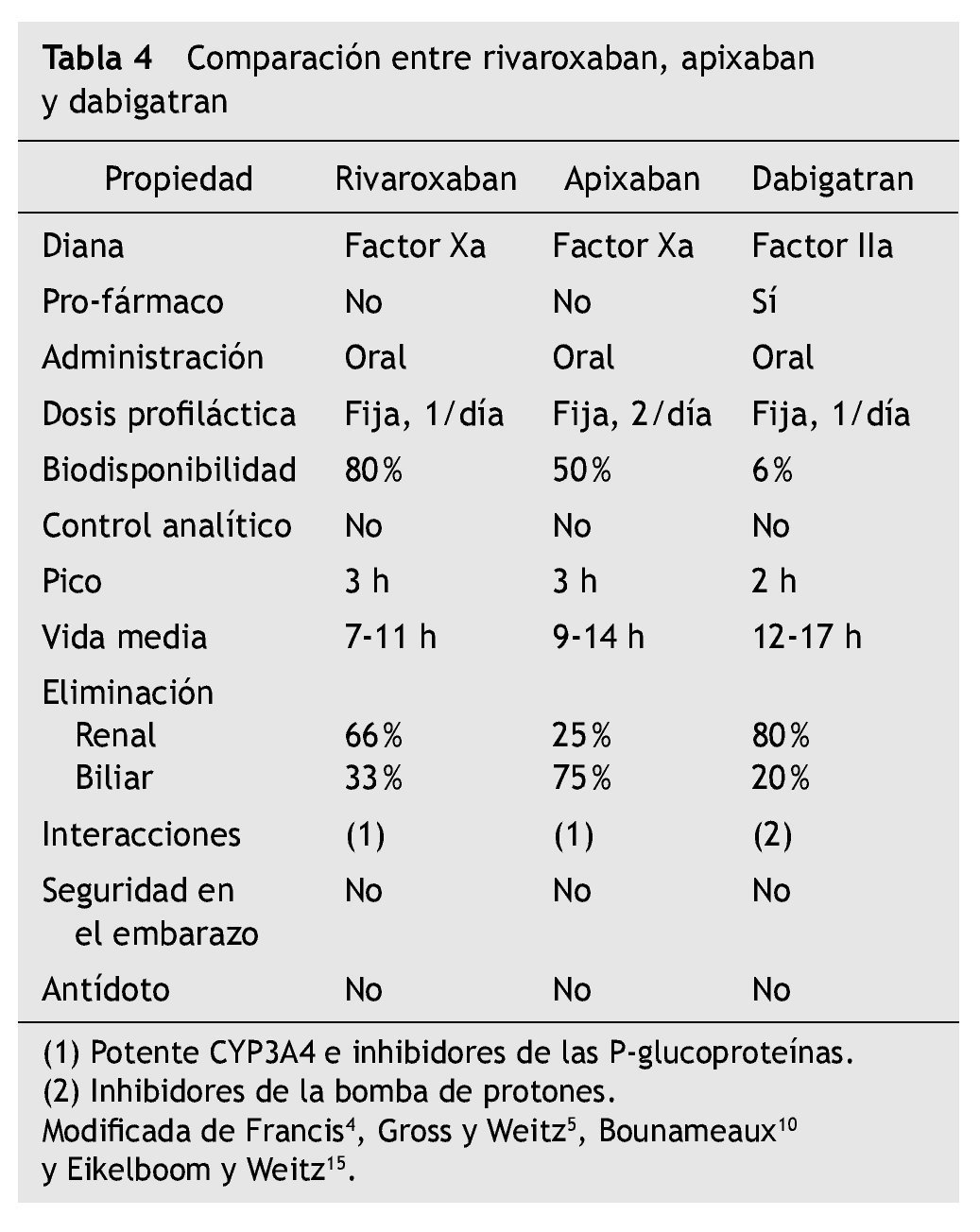
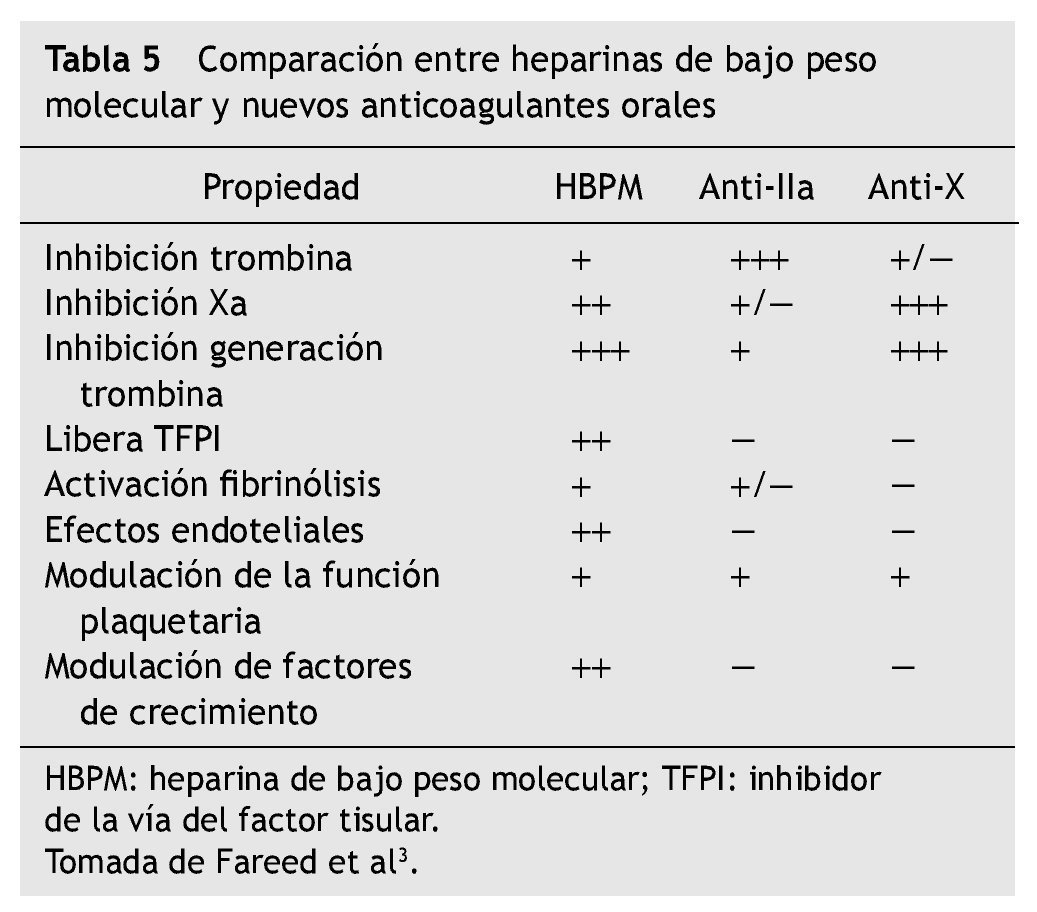
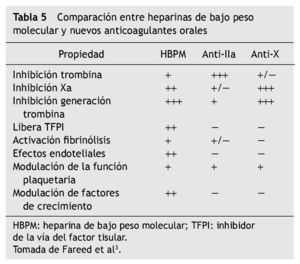
En las tablas 4 y 5 se aprecian las características comparativas entre estos nuevos anticoagulantes orales.
Los estudios publicados hasta el momento generan buenas expectativas en indicaciones tales como el tratamiento y la profilaxis de la enfermedad tromboembólica venosa, la profilaxis cardioembólica en la fibrilación auricular o el tratamiento del síndrome coronario agudo. Está por ver si su perfil de eficacia/seguridad abrirá nuevas expectativas terapéuticas, como la profilaxis tromboembólica venosa permanente en pacientes de alto riesgo. Evidencias sobre la eficacia en algunas indicaciones como las prótesis valvulares mecánicas tardarán más en aparecer. Más difícil todavía será disponer de información de eficacia y seguridad en pacientes habitualmente excluidos de los estudios, como son los afectos de insuficiencia renal, de insuficiencia hepática o las embarazadas. Probablemente serán opciones terapéuticas muy interesantes en pacientes afectos de trombocitopenia inducida por heparina, como ya demostró la lepirudina. Su actividad directa sobre el factor Xa o IIa, tanto en su forma libre como la localizada en el interior del trombo, los hace interesantes en pacientes en los que se ha evidenciado fracaso a las actuales estrategias antitrombóticas.
Un aspecto fundamental será cómo abordar el seguimiento de los pacientes tratados para evitar problemas de adhesión o errores en la toma de estos fármacos, puesto que la no necesidad de monitorización deja obsoleta la actual estructura de control del tratamiento anticoagulante. También será importante establecer, en caso de necesidad, cuál es el mejor método analítico de control y cuáles son los niveles óptimos de tratamiento. Un aspecto controvertido de los nuevos anticoagulantes es la inexistencia de antídoto, aspecto complicado en aquellos de vida media larga. Por último, decir que será importante confirmar para cada una de estas moléculas la inexistencia de efectos secundarios graves inesperados. El coste del fármaco será un aspecto que seguramente tendrán muy en cuenta los gestores de salud.
En resumen, estos nuevos productos aportan la posibilidad de administrarlos por vía oral, una vez al día, sin monitorización ni ajustes de dosis, lo que mejorará la aceptación por parte de los pacientes, sobre todo cuando se requiera un tratamiento prolongado. De hecho, estos fármacos podrían sustituir en el futuro a los clásicos anticoagulantes orales en numerosas indicaciones.
Dabigatran etexilate
Se trata de un fármaco que ejerce una inhibición selectiva de la trombina (FII), siendo conocidos como inhibidores directos de la trombina. Ha sido evaluado en tres ensayos en fase III, en pacientes sometidos a cirugía ortopédica de la rodilla y cadera (RE-MODEL, RE-NOVATE y RE-MOBILIZE). Los resultados, ya publicados, muestran no inferioridad con respecto a enoxaparina, con las ventajas de inicio postoperatorio y la administración oral del fármaco. Se encuentra comercializado en España con el nombre de Pradaxa®, precisamente con la indicación de profilaxis de la enfermedad tromboembólica venosa en la cirugía ortopédica mayor referida.
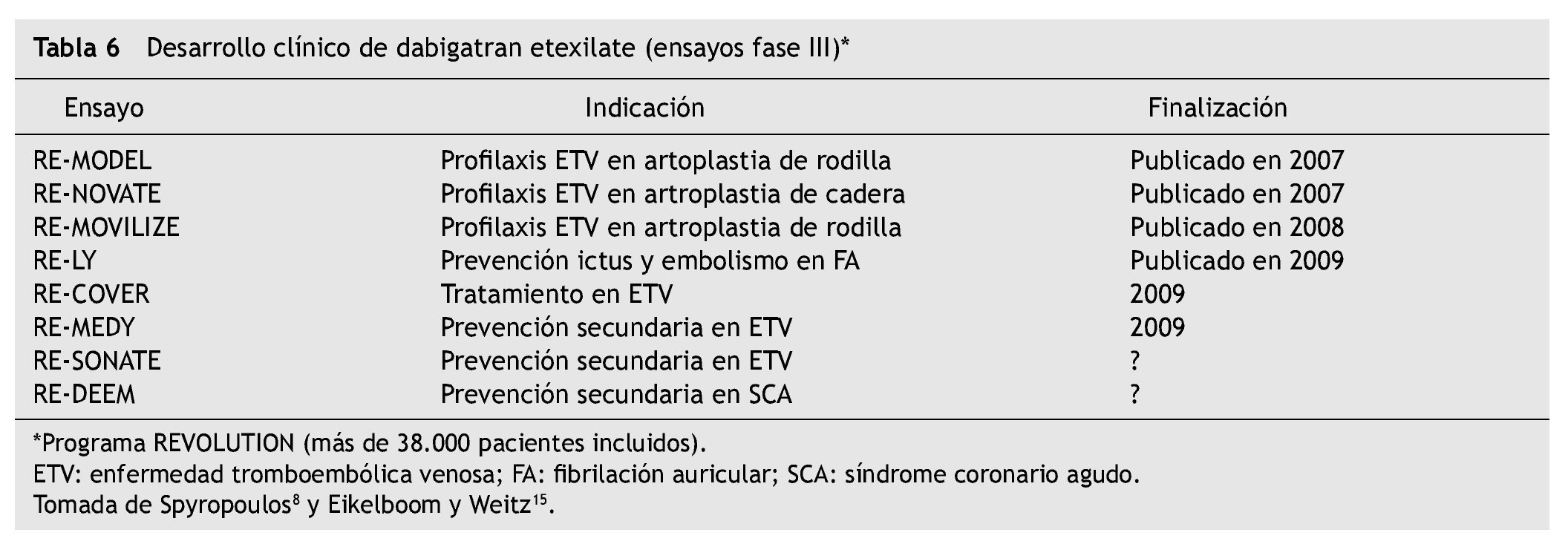
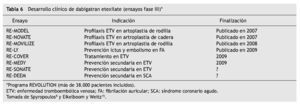
Existen estudios en curso sobre otras indicaciones, cuyos resultados iniciales se esperan para finales de este año (tabla 6) 15,16.
Ribaroxaban y otros inhibidores directos del factor Xa
Existen numerosos fármacos inhibidores selectivos directos del factor Xa: otamixaban, razaxaban, apixaban, rivaroxaban, etc., cuyas características se pueden ver en revisiones específicas al respecto 11. Otamixaban es el único que se administra por vía intravenosa (no oral, como el resto de los fármacos del grupo) y sus investigaciones están poco avanzadas. Razoxaban fue evaluado en fase II (tromboprofilaxis en la artroplastia de rodilla) pero el estudio fue detenido por los elevados porcentajes de hemorragia. Apixaban es una variante de razoxaban pero con mejores propiedades farmacológicas. Existen en curso dos ensayos (rodilla) y otro (cadera) en fase III, que lo compara con enoxaparina.
Rivaroxaban es un derivado oxazolidónico, potente y selectivo inhibidor del factor Xa, activo por vía oral. Es el fármaco del grupo con un desarrollo clínico más avanzado. Posee investigaciones publicadas en el mismo escenario que dabigatran y se comercializa en España (junio 2009) con el nombre de Xarelto®. Recientemente se han publicado 4 ensayos fase III (RECORD 1-4), realizados en cirugía ortopédica (cadera y rodilla), que han demostrando la superioridad del nuevo fármaco frente a enoxaparina, con igual seguridad (hemorragias) que el control.
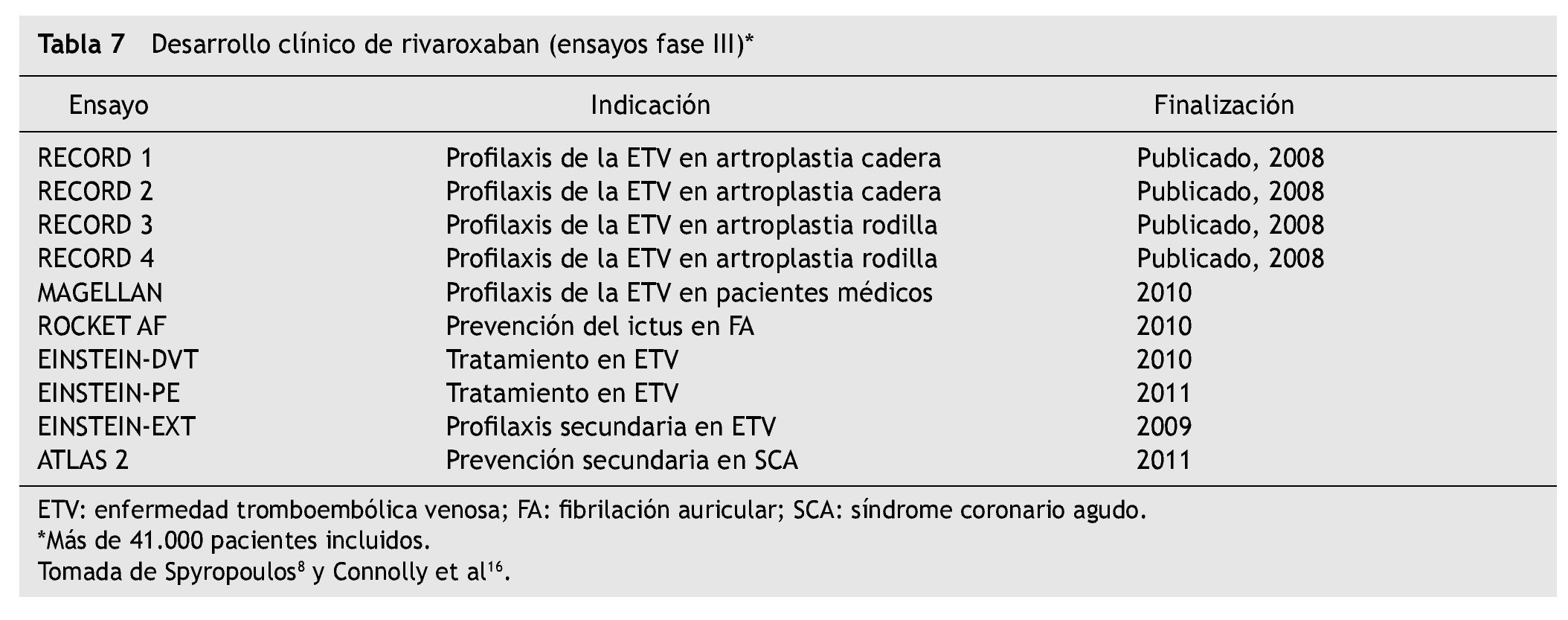
Adicionalmente existen más indicaciones clínicas en fase de ensayo III, cuyos resultados estarán disponibles a partir de los próximos dos años (tabla 7) 17.
Conclusiones
Los nuevos anticoagulantes orales presentan un enorme potencial de mercado, al pretender cubrir numerosas indicaciones clínicas. Por otro lado, parece claro que simplifican el tratamiento: dosis única, fija, oral y sin controles. No presentan las limitaciones de las AVK, lo que puede optimizar el tratamiento si se cuida el cumplimiento (adherencia al tratamiento), y finalmente presentan ventajas para pacientes y facultativos.
Los estudios iniciales con estos nuevos anticoagulantes orales se han centrando excesivamente en la profilaxis en cirugía ortopédica de alto riesgo, posiblemente porque en ella pueden encontrar las mayores diferencias con los fármacos de referencia (HBPM). Las expectativas potenciales y las nuevas oportunidades tienen que justificar 5 principios: efectivo, sencillo, económico, sin riesgos considerables y aplicable a muchos pacientes. De momento el coste de la mayoría de estos productos es superior al de las HBPM, pero ello puede cambiar a lo largo de los años, cuando se amortice la inversión en investigación.
En resumen, aunque los nuevos anticoagulantes orales son muy atractivos por diversas razones, todavía no sabemos cuándo reemplazarán a los anticoagulantes convencionales. Cada potencial indicación específica requerirá de nuevas y numerosas investigaciones.
Agradecimientos
A los doctores Pere Doménech y Jordi Fontcuberta, por sus enseñanzas especializadas a través de informes personales.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
*Autor para correspondencia.
Correo electrónico:lozano@usal.es (F.S. Lozano).
Recibido el 14 de enero de 2010;
aceptado el 18 de enero de 2010