Introducción. La fístula aortocava secundaria a rotura de aneurisma de aorta abdominal es una complicación muy poco frecuente con elevada morbimortalidad. Caso clínico. Varón de 71 años de edad que presentaba aneurisma de aorta abdominal infrarrenal roto y fistulizado a cava inferior. Se realizó una intervención urgente mediante endoprótesis aortouniilíaca derecha e injerto femorofemoral. Como complicación, endofuga tipo II por arteria mesentérica inferior que presurizaba el saco aneurismático y mantenía permeable la fístula. En un segundo tiempo se implantó una endoprótesis en la cava inferior y se embolizó el saco con Onyx ® mediante punción translumbar ecoguiada. En el postoperatorio, hubo mejoría hemodinámica, pero la endofuga y la fístula seguían permeables. Al mes se realizó una nueva intervención por persistencia de la fístula aortocava con débito elevado y pseudoaneurisma femoral derecho de gran tamaño, con explantación de la endoprótesis aórtica, cierre de la comunicación aortocava, reparación del seudoaneurisma femoral e interposición de prótesis aortobifemoral. La endoprótesis cava ayudó a atenuar la hemorragia intraoperatoria. Control evolutivo a los dos años: paciente asintomático con endoprótesis cava permeable. Conclusión. Las complicaciones de la cirugía endovascular de la fístula aortocava parecen frecuentes y pueden requerir reconversión abierta si ésta fracasa. [ANGIOLOGÍA 2008; 60: 439–43]
Introduction. An aortocaval fistula secondary to rupture of an abdominal aortic aneurysm is a very rare complication with high morbidity and mortality rates. Case report. A 71-year-old male who presented an infrarenal abdominal aorta aneurysm that was ruptured and fistulised to the inferior cava. Urgent surgery was performed involving a right aortouniiliac stent and a femorofemoral graft. The situation was complicated by a type II endoleak via the inferior mesenteric artery that put pressure on the aneurysmal sac and kept the fistula patent. Later, a stent was placed in the inferior cava and the sac was embolised with Onyx ® by means of ultrasound-guided translumbar puncture. In the post-operative period a haemodynamic improvement was observed, but the endoleak and the fistula remained patent. At one month, a second operation was performed due to persistence of the aortocaval fistula with a high debit and a large right femoral pseudoaneurysm, with explantation of the aortic stent, closure of the aortocaval communication, repair of the femoral pseudo-aneurysm and placement of an aortobifemoral stent. The caval stent helped to reduce intraoperative bleeding. A control visit was carried out at two years and the patient was found to be asymptomatic and the caval stent was patent. Conclusions. Complications of endovascular surgery carried out to treat aortocaval fistulas seem to be frequent and may require open restructuring if endovascular techniques fail. [ANGIOLOGÍA 2008; 60: 439–43]
Las técnicas endovasculares se han aplicado con éxito en el tratamiento de las fístulas arteriovenosas y traumatismos vasculares en los últimos años [1]. Por otro lado, el tratamiento de los aneurismas rotos de aorta abdominal mediante endoprótesis vasculares es factible en casos seleccionados, con resultados similares al mejor tratamiento quirúrgico abierto convencional [2]. Sin embargo, la experiencia endovascular en fístulas aortocava (FAC) es mucho más limitada.
Caso clínicoVarón de 71 años de edad que acude a urgencias por dolor abdominal de tres días de evolución, que se había intensificado en la últimas horas, acompañado de aumento de su disnea habitual. En su historial destacaba ser fumador activo con enfermedad pulmonar obstructiva crónica (EPOC) moderada y dislipidemia. En la exploración física presentaba una masa abdominal pulsátil y un soplo periumbilical 'en maquinaria'; las extremidades inferiores estaban bien perfundidas, no edematosas y con pulsos presentes a todos los niveles. La diuresis estaba mantenida y la presión arterial sistólica era de 80mmHg.
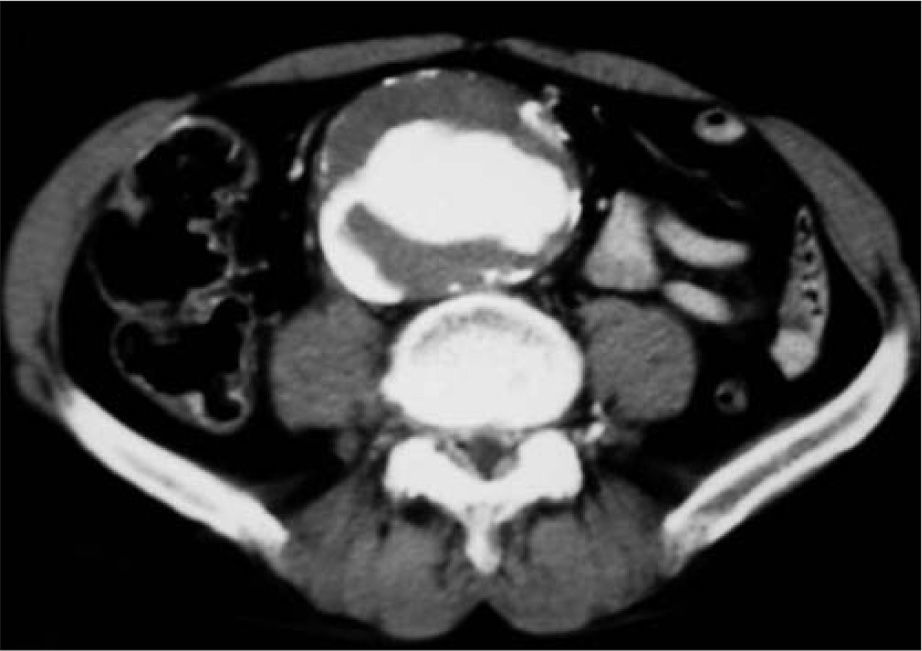
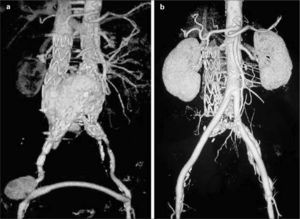
Entre las pruebas complementarias, la cifra de hemoglobina era de 14g/dL con hematocrito del 40%, coagulación normal y función renal levemente alterada con creatinina de 1,30mg/dL. El electrocardiograma mostraba taquicardia sinusal a 125 pulsaciones por minuto, sin signos de isquemia miocárdica. La radiografía de tórax, signos radiológicos de EPOC e incipientes de insuficiencia cardíaca. En la angiotomografía computarizada (angio-TC) se observaba un aneurisma de aorta abdominal (AAA) infrarrenal de 75mm de diámetro con morfología sacular, fisurado y fistulizado a vena cava inferior (relleno precoz de vena cava en fase arterial), con cuello proximal de 25mm de diámetro y 35mm de longitud, e ilíacas ectásicas menores de 20mm (Fig. 1).
Una vez valoradas la comorbilidad del paciente y las características anatómicas del AAA que eran aptas para el tratamiento endovascular, se decidió realizar una reparación urgente al disponer de endoprótesis del tamaño adecuado. Bajo anestesia general, se disecaron ambas arterias femorales comunes, se realizó una arteriografía intraoperatoria que confirmó la FAC y se implantó una endoprótesis aortouniilíaca derecha Talent® (Medtronic) de 2816C170X (28 proximal, 16 distal, 170 longitud), con extensión ilíaca de 1812C80X y cobertura simple de la hipogástrica. Tras colocar el oclusor en la ilíaca común izquierda y balonear proximal y distalmente con balón Reliant ® (Medtronic) se observó una endofuga tipo II que mantenía permeable la FAC. Después de balonear otra vez, persistía la endofuga, aunque con menor intensidad. Se completó la intervención con un injerto femorofemoral cruzado protésico (Dacron ® de 8mm). Nada más colocar la endoprótesis, las cifras de presión arterial aumentaron y disminuyó la presión venosa central de 30 a 11mmHg. En el postoperatorio, el paciente se mantuvo hemodinámicamente estable, sin ayuda inotrópica. Estancia en la UCI de 24 horas.
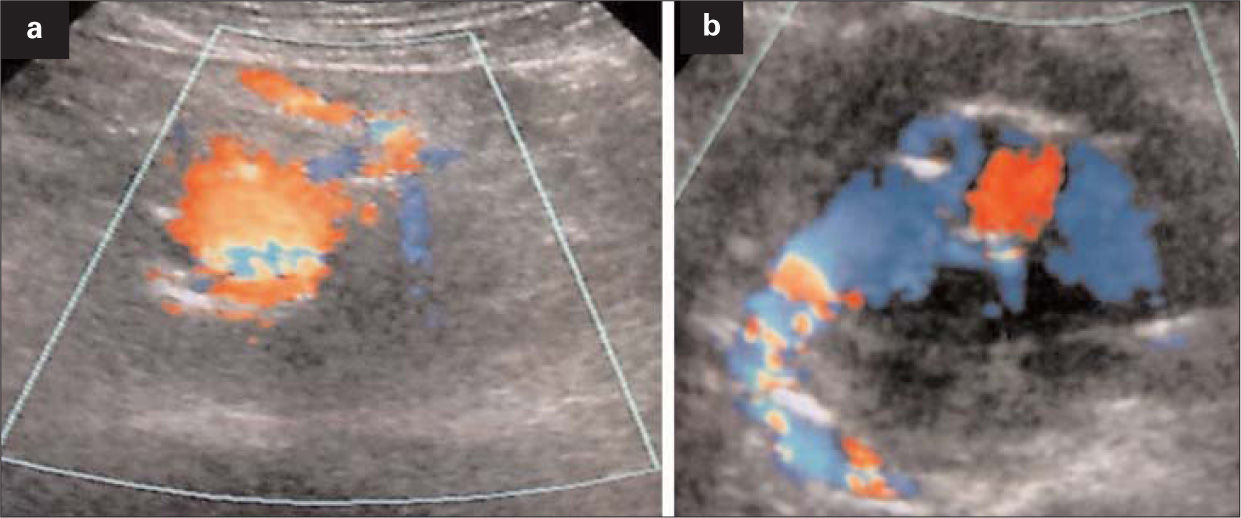
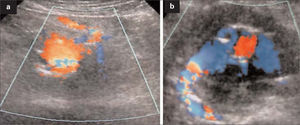
En la angio-TC de control realizada a las 48 horas se observaba una posición correcta de la endoprótesis pero con persistencia de la endofuga y de la FAC. Al cuarto día se realizó una eco-Doppler que confirmaba la endofuga tipo II por flujo retrógrado de la arteria mesentérica inferior (AMI) que presurizaba el saco aneurismático y mantenía permeable la FAC (Fig. 2). El ecocardiograma mostraba una función sistólica hiperdinámica (fracción de eyección, 79%), cavidades derechas dilatadas, insuficiencia tricuspídea III/IV, presión venosa central de 10–15mmHg e hipertensión pulmonar moderada de 55–60mmHg.
Ante la persistencia de la FAC y los signos clínicos, ecocardiográficos y radiológicos ya avanzados de insuficiencia cardíaca por hiperdinamia, se planteó un nuevo tratamiento quirúrgico, de nuevo endovascular: tras disecar la vena safena interna derecha a nivel inguinal, se introdujo a través de ésta una endoprótesis Valiant® (Medtronic) de 2626C100X (22 Fr), que se desplegó en la vena cava infrarrenal para intentar excluir la fístula. El diámetro de la endoprótesis se eligió en base al diámetro de la vena cava con la maniobra de Valsalva en la eco-Doppler preoperatoria y con la cavografía intraoperatoria sobredimensionando un 10%. En el mismo acto se colocó al paciente en decúbito prono y se realizó una punción translumbar ecoguiada del saco aneurismático; a través de un microcatéter compatible con dimetilsulfóxido se embolizó el saco aneurismático con Onyx® (EV3), con el objetivo de trombosar el saco y el origen de la AMI; sin embargo, no fue posible cateterizar selectivamente ésta. El volumen de Onyx introducido fue de 3mL. Ambos procedimientos se realizaron con anestesia local.
En la angio-TC postoperatoria se continuaba visualizando la endofuga y la FAC permeables; no obstante, el paciente fue dado de alta sin signos de insuficiencia cardíaca, y esperó una resolución espontánea de la endofuga y de la fístula.
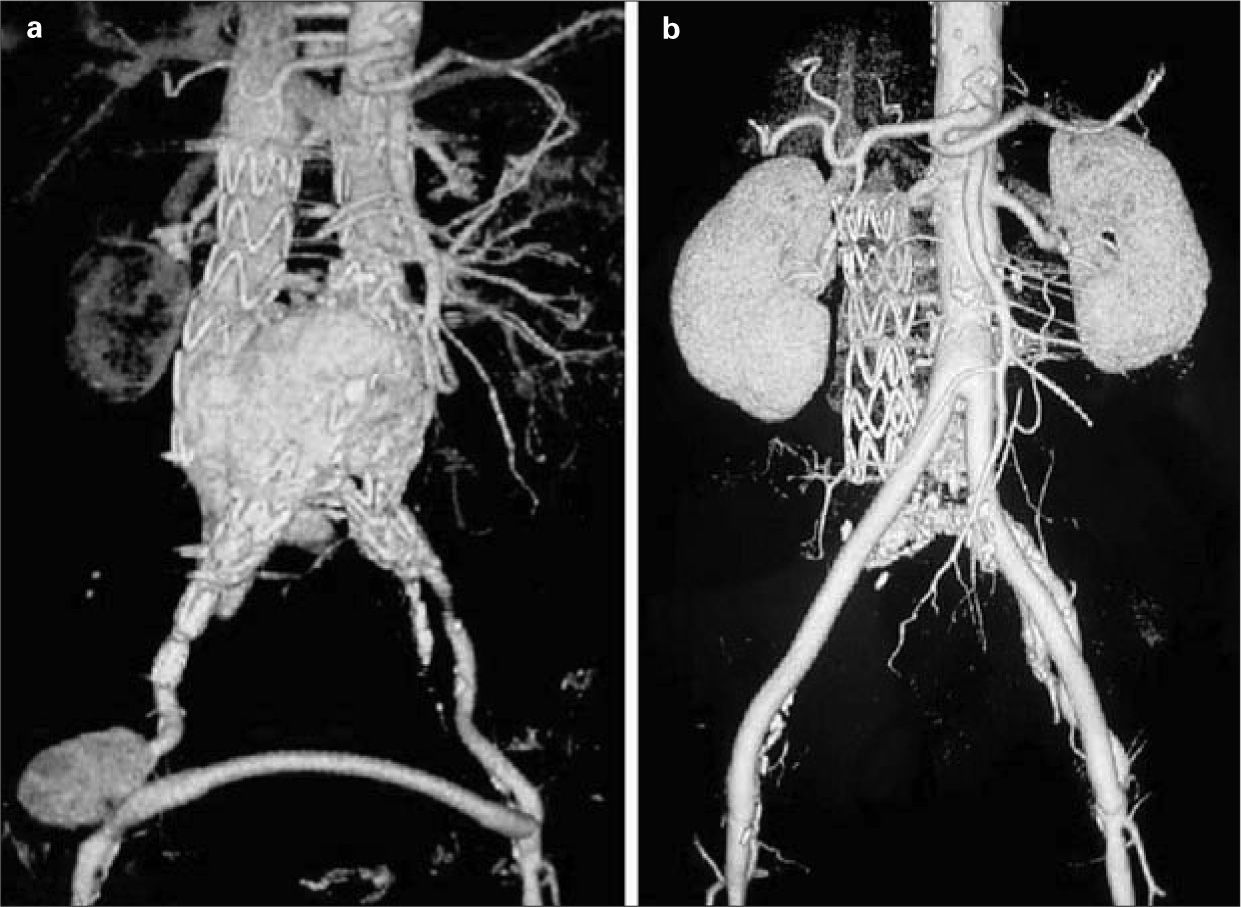
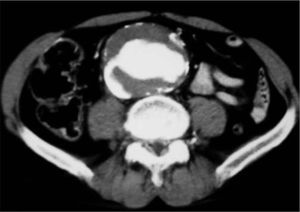
Al mes, reingresa por masa pulsátil inguinal derecha e inestabilidad hemodinámica. La angio-TC urgente mostraba un pseudoaneurisma femoral derecho de gran tamaño (6 × 4cm) y además la FAC continuaba permeable y con débito elevado (Fig. 3a). El tratamiento realizado fue el siguiente: laparotomía media xifopubiana (se comprueba in situ la pulsatilidad del aneurisma con FAC permeable), pinzamiento infrarrenal, aneurismorrafia longitudinal (se comprueba reflujo intenso por lumbares prominentes que se suturan), ligadura de la AMI, cierre del desgarro longitudinal de la cava (4cm de longitud) mediante puntos de Prolene ® '0' apoyados en la endoprótesis (la presencia de ésta atenuó la hemorragia), explantación de la endoprótesis aortomonoilíaca, reparación del pseudoaneurisma femoral (dehiscencia de la sutura), retirada del bypass femorofemoral e interposición de una prótesis bifurcada aortobifemoral Dacron-rifampicina (16 × 8mm) (Fig. 3b). Pérdida sanguínea: 6.500cm3. Estancia en la UCI de 48 horas, y precisó politransfusión. Hubo una buena recuperación, de manera que el alta
En el control evolutivo a los dos años el paciente se encuentra asintomático, en tratamiento con clopidogrel y con el bypass aortobifemoral y la endoprótesis cava permeables en la ecografía-Doppler.
DiscusiónEl 2-4% de los AAA rotos se complican con FAC [3]. El 80% se trata de aneurismas ateroscleróticos que erosionan espontáneamente la vena. Otras causas incluyen traumatismos, iatrogenia e infecciones aórticas. La mayoría de los casos se presenta como masa abdominal pulsátil, soplo sistodiastólico en mesogastrio e insuficiencia cardíaca hiperdinámica. También se ha documentado su presentación como fallo renal agudo, congestión venosa pélvica, edema de miembros inferiores [4] o embolismo pulmonar. Frecuentemente, el diagnóstico es intraoperatorio al intervenir un AAA roto.
La cirugía abierta suele conllevar una mortalidad alta (equiparable al del aneurisma roto), superior al 30% [3], debido a las pérdidas hemorrágicas muy importantes que se suelen producir. Además, si la fístula es de larga evolución, la disección suele ser más dificultosa y la hemorragia cuantiosa es inevitable debido a la arterialización del sistema venoso.
Las publicaciones de tratamiento endovascular de la FAC [4–7] son muy escasas, y, aunque sea una técnica menos agresiva, no está exenta de complicaciones. En el caso de Lau et al [5], se produjo la trombosis de la endoprótesis aortouniilíaca en el postoperatorio y la FAC se mantuvo permeable por un endoleak distal. Otra complicación posible es una endofuga tipo II que mantenga permeable la fístula, como en el caso de Burke et al [6], en el que una endofuga por AMI fue tratada con endoprótesis cava y embolización líquida del saco aneurismático. En nuestro caso, optamos también, en primer lugar, por excluir la fístula desde el lado venoso mediante una endoprótesis y, a continuación, mediante punción translumbar, rellenar el saco aneurismático con el sistema de embolización líquido Onyx, que ya ha demostrado su eficacia en el tratamiento de las endofugas tipo II [8], aunque, en este caso, no se consiguió el objetivo, debido probablemente al débito elevado de la fístula, al gran volumen del saco aneurismático y a que técnicamente no fue posible cateterizar de forma selectiva la AMI. Además, intraoperatoriamente se constató la presencia de numerosas lumbares con reflujo importante, que también contribuyeron al mantenimiento de la fístula.
La implantación de endoprótesis vasculares en laceraciones de la vena cava y en hemorragias inaccesibles de la vena cava retrohepática ha sido publicada [9]. En este caso implantamos la endoprótesis cava para intentar excluir completamente el flujo venoso del saco aneurismático, aunque es probable que la adaptación a la pared venosa no fuera completa o la sobredimensión no del todo adecuada; además, pudo influir la variabilidad del diámetro con los movimientos respiratorios, lo que dificulta la medición exacta. Sin embargo, la endoprótesis fue de vital importancia para disminuir la hemorragia durante la cirugía abierta y facilitó el cierre quirúrgico de la fístula. Se han descrito otras técnicas endovasculares para tratar de atenuar la hemorragia, como la colocación de balones de oclusión proximal y distal a la fístula dentro de la vena cava a través de un abordaje femoral bilateral [10].
Otro punto importante de la discusión es si estaba indicada la explantación de la endoprótesis y el cierre quirúrgico de la fístula. Lo cierto es que las técnicas endovasculares empleadas fracasaron en su objetivo y la fístula continuaba permeable con débito elevado y con el saco aneurismático pulsátil, por lo que optamos por la reconversión abierta y la reparación del pseudoaneurisma al mismo tiempo.
Si bien el tratamiento endovascular de la fístula aortocava puede llegar a ser atractivo por su carácter mínimamente invasivo, debemos tener presentes las posibles complicaciones que pueden surgir y que son un auténtico quebradero de cabeza para el cirujano, e incluso pueden requerir una reconversión abierta.