Los marcadores de inflamación son reactantes de fase aguda que se elevan en procesos inflamatorios como la isquemia crítica del miembro inferior (ICMI). La proteína C reactiva de alta sensibilidad (PCR-hs) ha sido el más utilizado para predecir eventos cardiovasculares en pacientes con ateroesclerosis. El objetivo de este estudio es conocer el valor pronóstico de la PCR-hs preoperatoria en pacientes con ICMI tratados mediante revascularización.
Material y métodosEstudio prospectivo de 100 pacientes con ICMI, incluidos de forma consecutiva y tratados mediante revascularización. En todos se realizó PCR-hs previa al procedimiento. La evaluación durante el año siguiente incluyó: mortalidad, eventos cardiovasculares (coronarios, neurológicos y en miembros inferiores) y restenosis arterial ecográfica.
ResultadosSe intervinieron 100 pacientes, 67 varones y 33 mujeres, con mediana de 76 años (rango intercuartílico [RIC] 65–83). Las categorías Rutherford eran: 4 (n = 29), 5 (n = 63) y 6 (n = 8). La mediana de la PCR-hs era 1,5 mg/dl (RIC 0,5–3). El índice tobillo-brazo preoperatorio era 0,3 (RIC 0,19–0,45). Las modalidades de tratamiento fueron: endovascular (n = 45), quirúrgico (n = 43) e híbrido (n = 12). No hubo mortalidad perioperatoria. El seguimiento fue de 11,7 meses (RIC 9,3–13,6). Fallecieron 20 pacientes y ocurrieron 90 eventos cardiovasculares en 70 pacientes. Se detectaron restenosis ecográfica > 70 % y/u obstrucción arterial en 39 pacientes. Había mayor probabilidad de mortalidad al año cuando la PCR-hs preoperatoria era > 3 mg/dl (p = 0,022; odds ratio [OR] = 6,15; intervalo de confianza [IC] 95 % 1,30–29,14).
ConclusiónValores elevados de PCR-hs (> 3 mg/dl) en el preoperatorio de pacientes con ICMI se relacionan con una mayor mortalidad al año.
Acute-phase reactants are inflammatory markers that increase during inflammatory events such as critical limb ischaemia (CLI). High-sensitivity C-reactive protein (hsCRP) is the most useful marker to predict cardiovascular events in patients with atherosclerosis. We investigated whether baseline levels of hsCRP predict mid-term clinical outcome in patients with CLI.
MethodsWe prospectively studied 100 consecutive patients with CLI who were treated by revascularization. All the patients had hsCRP samples taken prior to the intervention. During the first year the following endpoints were evaluated: mortality, cardiovascular events (coronary, neurological and lower limb) and echographic restenosis.
ResultsA total of 100 patients were intervened (67 males and 33 females). The median age was 76 years (interquartile range [IQR] 65-83). Rutherford categories were: 4 (n = 29), 5 (n = 63) and 6 (n = 8). The median preoperative hsCRP was 1.5 mg/dl (IQR 0.5–3). Baseline ankle-braquial index was 0.3 (IQR 0.19–0.45). Treatment modalities were: endovascular (n = 45), surgical (n = 43) and hybrid (n = 12). There was no perioperative mortality. Median follow-up was 11.7 months (IQR 9.3–13.6). During the first year, 20 patients died and there were 90 cardiovascular events in 70 patients. There were 39 patients with echographic restenosis > 70 % or obstruction. There was a higher probability of death when preoperative hsCRP was > 3 mg/dl (p = 0.022; odds ratio [OR] = 6.15; 95 % confidence interval [CI] 1.30–29.14).
ConclusionCLI patients with preoperative values of PCR-hs > 3 mg/dl are associated with death during the first year after treatment.
La ateroesclerosis es una enfermedad inflamatoria en constante evolución, responsable de la mayoría de muertes en los países desarrollados. Se caracteriza por la formación de placas lipídicas en la capa íntima de las arterias, que estrechan su luz y producen trombosis1. La isquemia crítica de miembro inferior (ICMI) es la forma más grave de enfermedad arterial periférica y presenta una incidencia anual de 50 casos por cien mil habitantes2.
Los marcadores de la inflamación son reactantes de fase aguda que se elevan en procesos inflamatorios como la ICMI. De todos ellos, la proteína C reactiva de alta sensibilidad (PCR-hs) es el más importante y se ha utilizado en la práctica clínica para predecir eventos cardiovasculares en pacientes con ateroesclerosis3.
ObjetivoEl objetivo de nuestro estudio es conocer el valor predictivo de la PCR-hs en la supervivencia, incidencia de eventos cardiovasculares y restenosis arterial, al año del tratamiento revascularizador, en pacientes con ICMI.
Material y métodosEstudio prospectivo de 100 pacientes con ICMI, incluidos de manera consecutiva, que recibieron tratamiento revascularizador, con cirugía y/o terapia endovascular, en el periodo comprendido entre marzo de 2007 y diciembre de 2008.
El estudio fue aprobado por la Comisión de Investigación del Hospital Montecelo de Pontevedra, e incluía un consentimiento informado personalizado con la firma de cada paciente.
Todos estos pacientes reunían los criterios diagnósticos de ICMI, según la Society for Vascular Surgery y la TASC II4,5. Se excluyeron los pacientes con isquemia aguda (clínica de menos de 14 días), aquellos que tenían ICMI con asociada patología aneurismática aortoiliaca y/o femoropoplítea, y los que se intervinieron por ICMI en miembro inferior y del territorio arterial visceral o carotídeo simultáneamente.
En una base de datos del programa Excel, de Microsoft Office 2003, se incluyeron:
- 1.
Datos de identificación de cada paciente, incluidos edad y sexo.
- 2.
Datos preoperatorios: factores de riesgo cardiovascular, índice tobillo-brazo (ITB), clasificación por categorías de Rutherford y parámetros analíticos, incluida la PCR-hs.
- 3.
Tratamiento revascularizador realizado.
- 4.
Datos de seguimiento, que se explican más adelante.
El trabajo que presentamos forma parte de un estudio más amplio de revascularización en pacientes con isquemia crítica, el cual continúa hasta obtener un tamaño muestral mayor.
Definición de variables- 1.
Fumador: fumador habitual o exfumador de menos de un año.
- 2.
Broncopatía crónica: tos productiva crónica durante al menos tres meses consecutivos durante dos años, o que estén a tratamiento previo con inhaladores.
- 3.
Hipertensión arterial: tensión arterial sistólica > de 140mmHg o con tratamiento antihipertensivo.
- 4.
Diabetes mellitus: glucemia basal > 110mg/dl o HbA1c > 7 %. Los pacientes con diabetes insulinodependiente son los que reciben insulina, y los no insulinodependientes, los que no necesitan insulina para su control.
- 5.
Dislipidemia: con tratamiento hipolipemiante o cifras de colesterol > 240mg/dl, triglicéridos > 150mg/dl o ratio HDL/LDL < 0,3.
- 6.
Enfermedad arterial coronaria: historia de angina de pecho, infarto agudo de miocardio o revascularización miocárdica quirúrgica o endoluminal.
- 7.
Insuficiencia renal: valores de creatinina > 1,5mg/dl.
- 8.
Enfermedad cerebrovascular: antecedente de ictus, ataque isquémico transitorio o revascularización carotídea previa, quirúrgica o endoluminal.
- 9.
Intervenciones vasculares previas: antecedentes de intervención vascular homolateral o contralateral.
Se realizaron análisis preoperatorios, incluida la PCR-hs, a toda la serie. Para el análisis de la PCR-hs se siguió el protocolo del Laboratorio de Bioquímica del Hospital Montecelo (Pontevedra): extracción de sangre venosa periférica y obtención del suero mediante centrifugación a 1.200rpm y a 4°C, durante 10 minutos. Conservación de la muestra a –20°C hasta su análisis mediante técnica de inmunoensayo turbidimétrico, siguiendo las recomendaciones del fabricante (Flex reagent cartridge. Dimension clinical chemistry system. Siemens Healthcare Diagnostics, USA).
Esta prueba cumple las recomendaciones de la American College of Cardiology/American Heart Association (ACC/AHA) para detectar pacientes con alto riesgo de enfermedades cardiovasculares. El rango de medición analítica está entre 0,05 y 25mg/dl. Los valores esperados para individuos sanos son < 0,3mg/dl.
SeguimientoConcluido el postoperatorio, se remitía cada paciente a su centro de Atención Primaria, bajo tratamiento antiagregante y una estatina, y con corrección de los principales factores de riesgo cardiovascular (hipertensión arterial, diabetes mellitus y dislipidemia), susceptibles de tratamiento médico. Los casos con stents implantados recibían doble antiagregación durante los tres primeros meses (clopidogrel 75mg/día más ácido acetilsalicílico [AAS] 100mg/día).
Se hacían tres revisiones en nuestras consultas externas:
- 1.
Al mes de la intervención, para evaluación directa de la morbimortalidad y de la permeabilidad de la intervención.
- 2.
A los tres meses, para realizar eco-doppler e ITB de control. Se recogían todas las incidencias ocurridas (reintervenciones o pérdida de extremidad, cuando las hubo), complicaciones coronarias o neurológicas y el cambio postoperatorio según escala de Rutherford. Cuando no acudía el paciente, también se recababa información de las incidencias y mortalidad a través de contacto telefónico.
- 3.
Al año, se repetía lo mismo que a los tres meses.
Se consideraba evento cardiovascular cualquiera de los siguientes supuestos:
- 1.
Reintervención por estenosis u oclusión en la extremidad operada.
- 2.
Restenosis > 70 %, todavía no tratada, en la extremidad operada.
- 3.
Empeoramiento de al menos una categoría en la escala de cambio clínico de Rutherford en la extremidad intervenida.
- 4.
Cualquier intervención en la extremidad contralateral.
- 5.
Eventos coronarios o ictus cerebrovasculares.
- 6.
Exitus letalis de cualquier origen.
La eco-doppler fue realizada con ecógrafo Philips HD11. Se consideraba la estenosis como hemodinámicamente significativa cuando era > 70 % del diámetro del vaso, y se consideraba como obstrucción la ausencia de flujo.
En el control ecográfico de una angioplastia-stent se consideraba estenosis > 70 % cuando la ratio entre la velocidad pico sistólica (VPS) de la estenosis y la VPS de la arteria sana proximal era > 36.
Se consideraban bypass en riesgo (failing graft), ya fueran con injerto protésico o venoso, cuando a la estenosis > 70 % se asociaba: VPS en un segmento determinado del bypass > 300cm/seg, o ratio entre la VPS de la estenosis y la VPS proximal a la estenosis > 3 y/o VPS en el trayecto del injerto < 45cm/seg7,8.
Todas las ecografías fueron realizadas por el mismo médico, con amplia experiencia en ecografía, en el laboratorio vascular de nuestro servicio. En aquellos casos en los que se planteaba reintervención vascular, se confirmaban los hallazgos ecográficos con arteriografía intraoperatoria.
Análisis estadísticoSe realizó con el programa Statistical Package for Social Sciencies (SPSS), versión 15.0 en castellano. Se consideró estadísticamente significativa una p < 0,05.
Las variables cualitativas se expresan como porcentajes y frecuencias absolutas. Las variables cuantitativas se indican con la media y la desviación típica si seguían distribución normal, o con la mediana y el rango intercuartílico (RIC) si resultaban no gaussianas. Como pruebas de normalidad se emplearon la de Kolmogorov-Smirnov y la de Shapiro-Wilk.
Se evaluó el valor predictivo de la PCR-hs en cuanto a la aparición de diversos eventos cardiovasculares, restenosis arterial y exitus letalis en el año de seguimiento. Para ello se realizaron tres puntos de corte para la PCR-hs, que fueron la mediana (1,5mg/dl) y el RIC (0,5-3mg/dl) y se analizó la probabilidad de ocurrencia de los eventos antes definidos en función de los valores de la PCR-hs. Se utilizó la prueba de la Chi2 para comparar proporciones en cada punto de corte.
Para estudiar la posible asociación entre las diferentes variables y la supervivencia anual o con los eventos cardiovasculares anuales se empleó la prueba de la Chi2 para las variables dicotómicas y para las variables categóricas de más de dos categorías; en el caso de variables continuas, las pruebas de la t de Student para datos independientes, previa aplicación de la prueba de Levene para igualdad de varianzas, en las que seguían distribución normal, y la U de Mann-Whitney en las no gaussianas.
Todas las variables que en el análisis univariante de supervivencia anual y de eventos cardiovasculares anuales tuvieron una p < 0,1 (para obtener así un mejor ajuste de posibles variables de confusión) se analizaron de forma multivariada, mediante un modelo de regresión logística por el método introducir, calculándose la odds ratio (OR) ajustada y su intervalo de confianza (IC) del 95 %. Se realizó un análisis de calibración de modelo mediante las pruebas de bondad de ajuste y medida del estadístico de Chi 2 de Hosmer-Lemeshow.
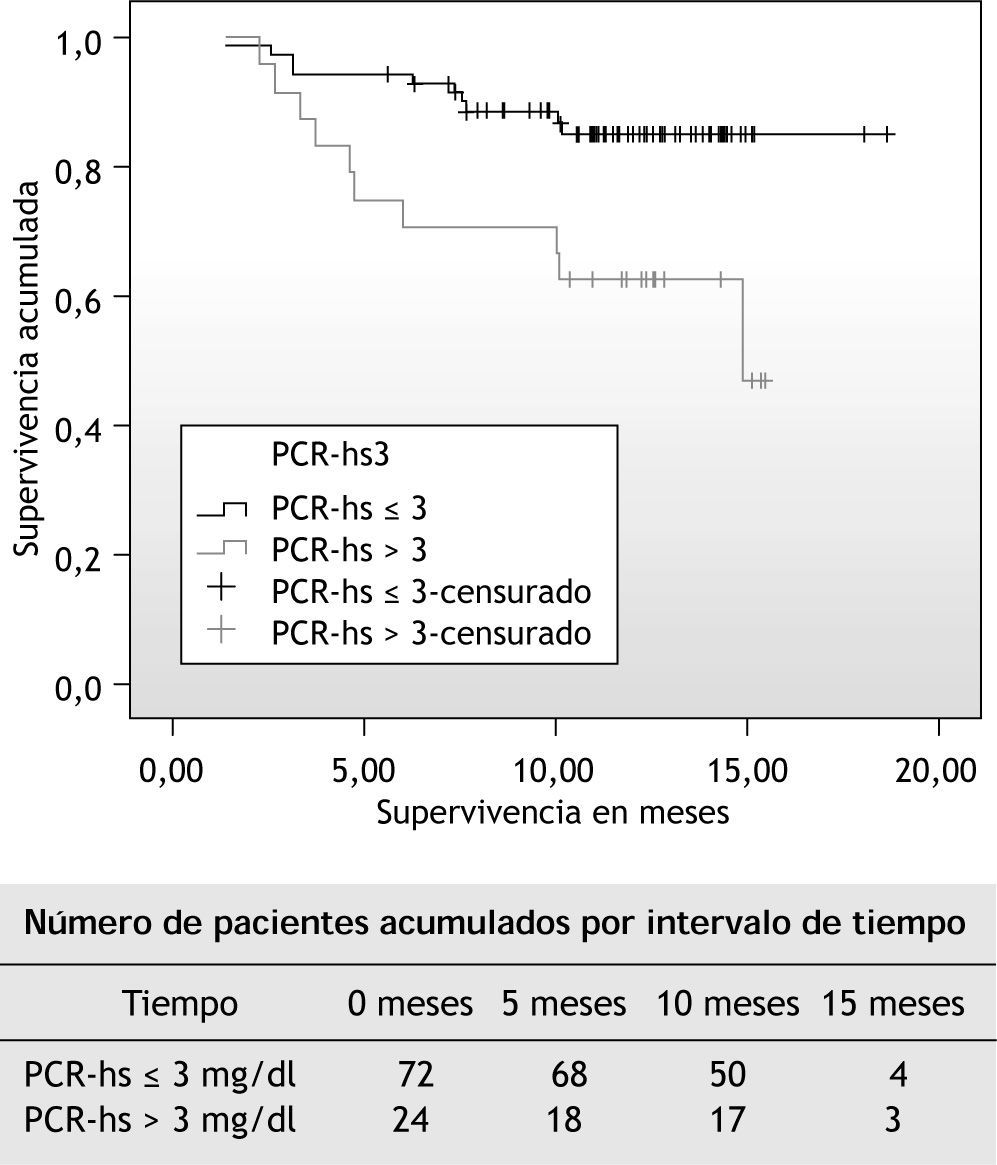
Se realizó análisis de supervivencia mediante curva de Kaplan-Meier para valorar la supervivencia de los grupos con valores de PCR-hs > 3mg/dl y < 3mg/dl.
ResultadosSe excluyó del estudio a 4 pacientes con ICMI: dos tenían asociado aneurisma poplíteo en la extremidad homolateral y otros dos porque se operaron simultáneamente de endarterectomía femoral y angioplastia renal y de bypass femorofemoral y stenting carotídeo.
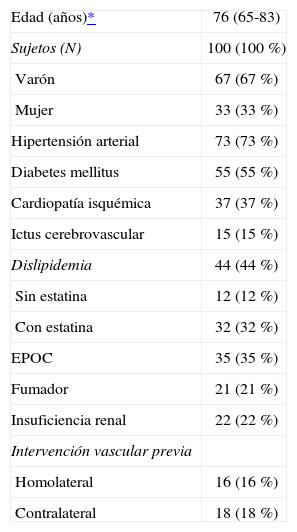
Se intervinieron 100 pacientes con mediana de edad de 76 años (65-83). Había 67 varones y 33 mujeres. Destacaban en la serie, como principales factores de riesgo: hipertensión arterial, diabetes mellitus y enfermedad cardiovascular (tabla 1).
Datos demográficos y factores de riesgo cardiovascular
| Edad (años)* | 76 (65-83) |
| Sujetos (N) | 100 (100 %) |
| Varón | 67 (67 %) |
| Mujer | 33 (33 %) |
| Hipertensión arterial | 73 (73 %) |
| Diabetes mellitus | 55 (55 %) |
| Cardiopatía isquémica | 37 (37 %) |
| Ictus cerebrovascular | 15 (15 %) |
| Dislipidemia | 44 (44 %) |
| Sin estatina | 12 (12 %) |
| Con estatina | 32 (32 %) |
| EPOC | 35 (35 %) |
| Fumador | 21 (21 %) |
| Insuficiencia renal | 22 (22 %) |
| Intervención vascular previa | |
| Homolateral | 16 (16 %) |
| Contralateral | 18 (18 %) |
Variables categóricas expresadas por frecuencias absolutas y porcentajes.
EPOC: enfermedad pulmonar obstructiva crónica.
Dentro de la clasificación por categorías de Rutherford, los pacientes se distribuían en: categoría 4 (n = 29), 5 (n = 63) y 6 (n = 8).
La mediana del ITB preoperatorio era de 0,3 (RIC 0,19-0,45).
Las modalidades del tratamiento revascularizador fueron: endovascular (n = 45), quirúrgico (n = 43) e híbrido (n = 12). Las lesiones suprainguinales se trataron de manera endovascular y quirúrgica por igual. En el sector infrainguinal las lesiones TASC A y B se trataron de manera endovascular preferentemente (74 %), y las C y D, de manera quirúrgica o híbrida (80 %).
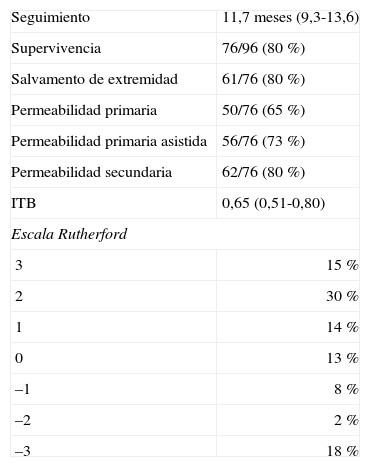
El seguimiento fue de 11,7 meses de mediana (9,3-13,6). La supervivencia, el salvamento de la extremidad, la permeabilidad, el ITB y la escala de cambio clínico de Rutherford al año del procedimiento se detallan en la tabla 2.
Supervivencia, salvamento de la extremidad, permeabilidad, índice tobillo-brazo y escala de cambio clínico de Rutherford al año de seguimiento
| Seguimiento | 11,7 meses (9,3-13,6) |
| Supervivencia | 76/96 (80 %) |
| Salvamento de extremidad | 61/76 (80 %) |
| Permeabilidad primaria | 50/76 (65 %) |
| Permeabilidad primaria asistida | 56/76 (73 %) |
| Permeabilidad secundaria | 62/76 (80 %) |
| ITB | 0,65 (0,51-0,80) |
| Escala Rutherford | |
| 3 | 15 % |
| 2 | 30 % |
| 1 | 14 % |
| 0 | 13 % |
| –1 | 8 % |
| –2 | 2 % |
| –3 | 18 % |
ITB: índice tobillo-brazo.
La mediana de la PCR-hs preoperatoria era 1,5mg/dl (RIC 0,5-3). Los valores totales estaban comprendidos entre 0,1 (mínimo) y 18,6mg/dl (máximo). Los valores extremos fueron: 5 % superior (> 11mg/dl): 5 pacientes, y 5 % inferior (≤ 0,1mg/dl): 5 pacientes.
El análisis del valor predictivo de la PCR-hs se hizo con 96 pacientes del total de la serie. Se excluyó del análisis a 4 pacientes: tres porque aunque tenían la determinación hecha no fue posible aprovecharla, al no poder hacerles el seguimiento al año, y la cuarta paciente porque se perdió la muestra para PCR-hs, aunque se le hizo seguimiento completo al año.
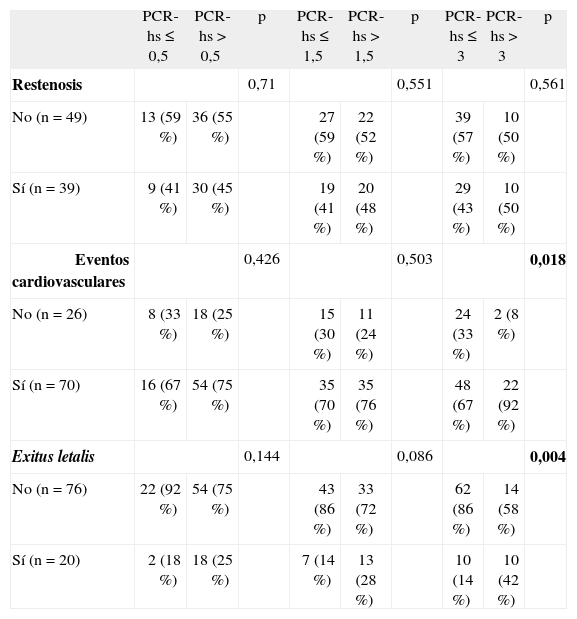
Se evaluó el valor predicivo de PCR-hs al año de seguimiento, según los eventos cardiovasculares, la restenosis arterial ecográfica y la mortalidad. Se tomó como punto de corte (cut-off) la mediana (1,5mg/dl) y el RIC (0,5-3mg/dl). El valor esperado para individuos sanos en nuestro Laboratorio de Bioquímica es < 0,3mg/dl (tabla 3).
Valores de PCR-hs en pacientes con restenosis vascular, eventos cardiovasculares y exitus letalis
| PCR-hs ≤ 0,5 | PCR-hs > 0,5 | p | PCR-hs ≤ 1,5 | PCR-hs > 1,5 | p | PCR-hs ≤ 3 | PCR-hs > 3 | p | |
| Restenosis | 0,71 | 0,551 | 0,561 | ||||||
| No (n = 49) | 13 (59 %) | 36 (55 %) | 27 (59 %) | 22 (52 %) | 39 (57 %) | 10 (50 %) | |||
| Sí (n = 39) | 9 (41 %) | 30 (45 %) | 19 (41 %) | 20 (48 %) | 29 (43 %) | 10 (50 %) | |||
| Eventos cardiovasculares | 0,426 | 0,503 | 0,018 | ||||||
| No (n = 26) | 8 (33 %) | 18 (25 %) | 15 (30 %) | 11 (24 %) | 24 (33 %) | 2 (8 %) | |||
| Sí (n = 70) | 16 (67 %) | 54 (75 %) | 35 (70 %) | 35 (76 %) | 48 (67 %) | 22 (92 %) | |||
| Exitus letalis | 0,144 | 0,086 | 0,004 | ||||||
| No (n = 76) | 22 (92 %) | 54 (75 %) | 43 (86 %) | 33 (72 %) | 62 (86 %) | 14 (58 %) | |||
| Sí (n = 20) | 2 (18 %) | 18 (25 %) | 7 (14 %) | 13 (28 %) | 10 (14 %) | 10 (42 %) | |||
Se resaltan en negrita los valores de p < 0,05.
PCR-hs: proteína C reactiva de alta sensibilidad.
Dos pacientes (2 %) estaban siendo tratados antes de la intervención con corticoides, a baja dosis, para control de lupus eritematoso en un caso y de polimialgia reumática en el otro, pero en el momento de la intervención, en ninguno de los dos su enfermedad sistémica se encontraba activa. El primero tenía PCR-hs de 2,1mg/dl y el segundo de mg/dl, y los dos presentaban categoría 5 de Rutherford. Al año de seguimiento ambos estaban vivos, el último con la extremidad amputada.
Otros dos pacientes (2 %) presentaron problemas concomitantes antes de la intervención vascular. Un caso había sido intervenido de hemicolectomía por diverticulitis hacía 15 días y otro tuvo una hemorragia digestiva en el preoperatorio. Tenían valores preoperatorios de PCR-hs de mg/dl y 11,2mg/dl, respectivamente, y ambos pacientes, con categoría 6, fallecieron al año, con la extremidad amputada.
Eventos cardiovascularesOcurrieron 90 eventos cardiovasculares en 70 pacientes durante el primer año: vasculares periféricos en la extremidad intervenida (n = 43; 48 %), vasculares periféricos en la extremidad contralateral, que precisaron intervención (n = 7; 8 %), eventos coronarios (n = 16; 18 %), ictus (n = 4; 4 %) y exitus letalis (n = 20; 22 %).
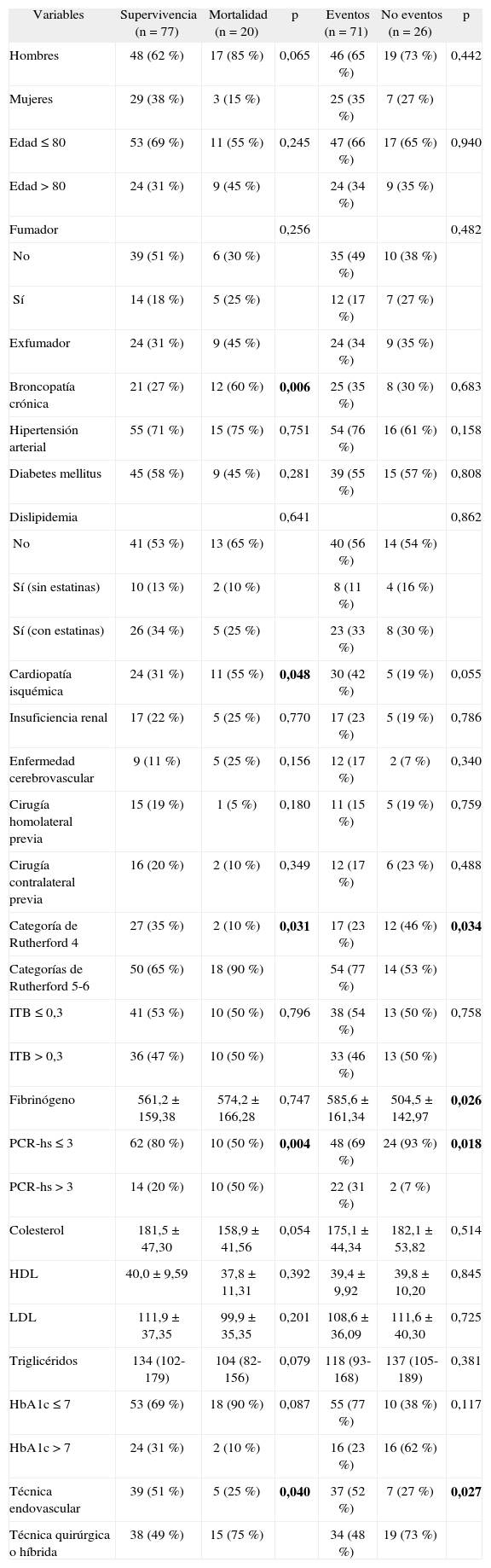
Las variables de eventos cardiovasculares al año, en el análisis univariante con significación estadística, eran: categorías Rutherford 5 y 6 (p = 0,034), valores elevados de fibrinógeno (p = 0,026), PCR-hs > 3mg/dl (p = 0,018) y técnica endovascular (p = 0,027) (tabla 4).
Asociación entre variables de pacientes, mortalidad y eventos cardiovasculares al año. Análisis univariante
| Variables | Supervivencia (n = 77) | Mortalidad (n = 20) | p | Eventos (n = 71) | No eventos (n = 26) | p |
| Hombres | 48 (62 %) | 17 (85 %) | 0,065 | 46 (65 %) | 19 (73 %) | 0,442 |
| Mujeres | 29 (38 %) | 3 (15 %) | 25 (35 %) | 7 (27 %) | ||
| Edad ≤ 80 | 53 (69 %) | 11 (55 %) | 0,245 | 47 (66 %) | 17 (65 %) | 0,940 |
| Edad > 80 | 24 (31 %) | 9 (45 %) | 24 (34 %) | 9 (35 %) | ||
| Fumador | 0,256 | 0,482 | ||||
| No | 39 (51 %) | 6 (30 %) | 35 (49 %) | 10 (38 %) | ||
| Sí | 14 (18 %) | 5 (25 %) | 12 (17 %) | 7 (27 %) | ||
| Exfumador | 24 (31 %) | 9 (45 %) | 24 (34 %) | 9 (35 %) | ||
| Broncopatía crónica | 21 (27 %) | 12 (60 %) | 0,006 | 25 (35 %) | 8 (30 %) | 0,683 |
| Hipertensión arterial | 55 (71 %) | 15 (75 %) | 0,751 | 54 (76 %) | 16 (61 %) | 0,158 |
| Diabetes mellitus | 45 (58 %) | 9 (45 %) | 0,281 | 39 (55 %) | 15 (57 %) | 0,808 |
| Dislipidemia | 0,641 | 0,862 | ||||
| No | 41 (53 %) | 13 (65 %) | 40 (56 %) | 14 (54 %) | ||
| Sí (sin estatinas) | 10 (13 %) | 2 (10 %) | 8 (11 %) | 4 (16 %) | ||
| Sí (con estatinas) | 26 (34 %) | 5 (25 %) | 23 (33 %) | 8 (30 %) | ||
| Cardiopatía isquémica | 24 (31 %) | 11 (55 %) | 0,048 | 30 (42 %) | 5 (19 %) | 0,055 |
| Insuficiencia renal | 17 (22 %) | 5 (25 %) | 0,770 | 17 (23 %) | 5 (19 %) | 0,786 |
| Enfermedad cerebrovascular | 9 (11 %) | 5 (25 %) | 0,156 | 12 (17 %) | 2 (7 %) | 0,340 |
| Cirugía homolateral previa | 15 (19 %) | 1 (5 %) | 0,180 | 11 (15 %) | 5 (19 %) | 0,759 |
| Cirugía contralateral previa | 16 (20 %) | 2 (10 %) | 0,349 | 12 (17 %) | 6 (23 %) | 0,488 |
| Categoría de Rutherford 4 | 27 (35 %) | 2 (10 %) | 0,031 | 17 (23 %) | 12 (46 %) | 0,034 |
| Categorías de Rutherford 5-6 | 50 (65 %) | 18 (90 %) | 54 (77 %) | 14 (53 %) | ||
| ITB ≤ 0,3 | 41 (53 %) | 10 (50 %) | 0,796 | 38 (54 %) | 13 (50 %) | 0,758 |
| ITB > 0,3 | 36 (47 %) | 10 (50 %) | 33 (46 %) | 13 (50 %) | ||
| Fibrinógeno | 561,2 ± 159,38 | 574,2 ± 166,28 | 0,747 | 585,6 ± 161,34 | 504,5 ± 142,97 | 0,026 |
| PCR-hs ≤ 3 | 62 (80 %) | 10 (50 %) | 0,004 | 48 (69 %) | 24 (93 %) | 0,018 |
| PCR-hs > 3 | 14 (20 %) | 10 (50 %) | 22 (31 %) | 2 (7 %) | ||
| Colesterol | 181,5 ± 47,30 | 158,9 ± 41,56 | 0,054 | 175,1 ± 44,34 | 182,1 ± 53,82 | 0,514 |
| HDL | 40,0 ± 9,59 | 37,8 ± 11,31 | 0,392 | 39,4 ± 9,92 | 39,8 ± 10,20 | 0,845 |
| LDL | 111,9 ± 37,35 | 99,9 ± 35,35 | 0,201 | 108,6 ± 36,09 | 111,6 ± 40,30 | 0,725 |
| Triglicéridos | 134 (102-179) | 104 (82-156) | 0,079 | 118 (93-168) | 137 (105-189) | 0,381 |
| HbA1c ≤ 7 | 53 (69 %) | 18 (90 %) | 0,087 | 55 (77 %) | 10 (38 %) | 0,117 |
| HbA1c > 7 | 24 (31 %) | 2 (10 %) | 16 (23 %) | 16 (62 %) | ||
| Técnica endovascular | 39 (51 %) | 5 (25 %) | 0,040 | 37 (52 %) | 7 (27 %) | 0,027 |
| Técnica quirúrgica o híbrida | 38 (49 %) | 15 (75 %) | 34 (48 %) | 19 (73 %) |
Variables continuas expresadas con la media y la desviación típica si siguen distribución normal y con la mediana y el rango intercuartílico si son no gaussianas. Se resaltan en negrita los valores de p < 0,05.
HbA1c: hemoglobina glucosilada; HDL: colesterol ligado a lipoproteínas de alta densidad; ITB: índice tobillo-brazo; LDL: colesterol ligado a lipoproteínas de baja densidad; PCR-hs: proteína C reactiva de alta sensibilidad.
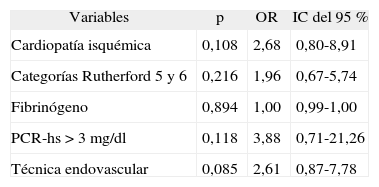
Ninguna de estas variables fue significativa en el análisis multivariante (tabla 5).
Eventos cardiovasculares al año y factores de riesgo. Análisis multivariante
| Variables | p | OR | IC del 95 % |
| Cardiopatía isquémica | 0,108 | 2,68 | 0,80-8,91 |
| Categorías Rutherford 5 y 6 | 0,216 | 1,96 | 0,67-5,74 |
| Fibrinógeno | 0,894 | 1,00 | 0,99-1,00 |
| PCR-hs > 3mg/dl | 0,118 | 3,88 | 0,71-21,26 |
| Técnica endovascular | 0,085 | 2,61 | 0,87-7,78 |
IC: intervalo de confianza; OR: odds ratio ajustada; PCR-hs: proteína C reactiva de alta sensibilidad.
Para evaluar la restenosis u obstrucción vascular en la extremidad afecta al año de la intervención se realizó un estudio de eco-doppler a los 76 pacientes vivos. Se incluyeron, además, otros 12 pacientes que fallecieron antes del año, pero a los que se pudo realizar una eco-doppler de control previa a la fecha del exitus.
En total fueron estudiados 88 pacientes de la serie y se detectaron alteraciones en 39: restenosis > 70 % de la luz (n = 15) y obstrucción total del vaso (n = 24).
MortalidadFallecieron 20 pacientes, todos a partir del segundo mes de la intervención. Las causas fueron: infarto agudo de miocardio (n = 12), neumonía (n = 5), cetoacidosis diabética (n = 1), gangrena de la extremidad (n = 1) y autolisis supuesta (n = 1).
Las variables que alcanzaban significación estadística en el análisis univariante de mortalidad al año eran: pacientes con enfermedad pulmonar obstructiva crónica (p = 0,006), cardiopatía isquémica (p = 0,048), categorías Rutherford 5 y 6 (p = 0,031), valores de PCR-hs > 3mg/dl (p = 0,004) y los intervenidos con cirugía o técnica híbrida (p = 0,040), según se recoge en la tabla 4.
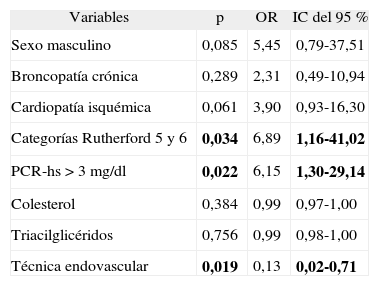
En el análisis multivariante (tabla 6), eran significativas de mortalidad al año las siguientes variables: categorías Rutherford 5 y 6 (p = 0,034) y PCR-hs > 3mg/dl (p = 0,022). La técnica endovascular era significativa de menor mortalidad (p = 0,019).
Mortalidad anual y factores de riesgo. Análisis multivariante
| Variables | p | OR | IC del 95 % |
| Sexo masculino | 0,085 | 5,45 | 0,79-37,51 |
| Broncopatía crónica | 0,289 | 2,31 | 0,49-10,94 |
| Cardiopatía isquémica | 0,061 | 3,90 | 0,93-16,30 |
| Categorías Rutherford 5 y 6 | 0,034 | 6,89 | 1,16-41,02 |
| PCR-hs > 3mg/dl | 0,022 | 6,15 | 1,30-29,14 |
| Colesterol | 0,384 | 0,99 | 0,97-1,00 |
| Triacilglicéridos | 0,756 | 0,99 | 0,98-1,00 |
| Técnica endovascular | 0,019 | 0,13 | 0,02-0,71 |
Se resaltan en negrita los valores de p < 0,05.
IC: intervalo de confianza; OR: odds ratio ajustada; PCR-hs: proteína C reactiva de alta sensibilidad.
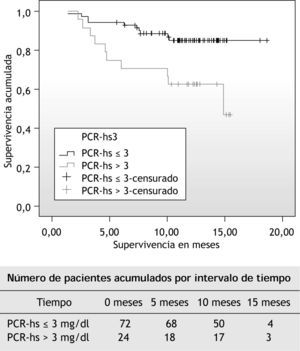
También se hizo una curva de Kaplan-Meier de supervivencia acumulada por encima y por debajo del cuartil superior de PCR-hs (3mg/dl) (fig. 1).
DiscusiónEn la práctica clínica, la PCR-hs es el principal marcador inflamatorio que aparece relacionado con eventos cardiovasculares, en pacientes ateroesclerosos3.
Los primeros estudios con este biomarcador se hicieron en el territorio coronario, donde se encontró un mayor número de eventos cardiovasculares postoperatorios y de restenosis tras cirugía aortocoronaria y angioplastia, en los pacientes con niveles más altos de PCR-hs basal9-11.
En el territorio carotídeo, los niveles elevados de PCR-hs se relacionan con la progresión de la estenosis en controles ecográficos, la inestabilidad de la placa y la aparición de eventos neurológicos tras intervención carotídea12-15.
Eventos cardiovascularesEn la enfermedad arterial periférica, la PCR-hs presenta valores basales más elevados en los pacientes con ICMI que en los que tienen claudicación intermitente16.
Owens et al realizaron un estudio prospectivo con 91 pacientes afectos de enfermedad arterial periférica (EAP), que habían sido incluidos en una lista para realizar bypass femoropoplíteo con vena autóloga, y de la que habían sido excluidos los que tenían infecciones agudas (celulitis y osteomielitis) o graves procesos concomitantes. Fueron intervenidos aproximadamente la mitad de la lista por ICMI. En este grupo predominaba la categoría 4 de Rutherford y la mediana de niveles de PCR-hs era de 0,68mg/dl (RIC 0,2-2). La otra mitad operada, que no tenía isquemia crítica, daba una mediana de niveles de PCR-hs mucho más baja, de 0,2 (RIC 0,1-0,4). Los pacientes con niveles elevados de PCR-hs tenían un mayor riesgo de eventos cardiovasculares al año3.
En nuestra serie, con un mayor número de casos, todos los pacientes tenían ICMI de mayor nivel de gravedad, ya que las dos terceras partes tenían categorías 5 y 6 de Rutherford. En consecuencia, era esperable que la mediana de nuestros niveles de PCR-hs fuera mucho más alta (1,5mg/dl). Y todavía contribuía más a la elevación de los parámetros inflamatorios que la mayoría de nuestros pacientes tenían heridas sobreinfectadas en la extremidad, en el preoperatorio, y que más del 50 % tenían diabetes mellitus, a menudo descompensada, y que solo la tercera parte del total de los pacientes tomaba estatina al ingreso, fármaco que contribuye a la disminución de la inflamación y, por tanto, de la PCR-hs17.
La ateroesclerosis puede evolucionar con distintos niveles de gravedad en los pacientes con EAP. Niveles elevados de PCR-hs están relacionados con eventos cardiovasculares en diferentes territorios arteriales18. Matzke et al encontraron que los casos con amputación secundaria a fracaso precoz del bypass femoropoplíteo por ICMI presentaban niveles más altos de PCR-hs19.
En nuestro estudio, los eventos cardiovasculares ocurrieron en más del 70 % de los casos y con mayor frecuencia en pacientes con valores de PCR-hs por encima del cuartil superior (> 3mg/dl), aunque no encontramos significación estadística en el análisis multivariante. Esto puede deberse al insuficiente tamaño muestral, de solo 100 casos, ya que forma parte de un estudio más amplio de revascularización de pacientes con isquemia crítica, actualmente en curso.
Restenosis arterialLa PCR-hs como marcador de inflamación puede encontrarse más elevada también en los pacientes con hiperplasia intimal. Schillinger et al encontraron, en sus estudios de angioplastia femoropoplítea y de arterias tibiales, que la restenosis a los 6 meses se producía con mayor frecuencia en los pacientes que tenían niveles elevados de PCR-hs antes de la intervención y 48 horas después, aunque en su estudio muchos de los pacientes tenían claudiación intermitente20,21.
Nosotros no hemos encontrado relación entre los valores de PCR-hs y las restenosis al año de seguimiento. La posible explicación de esta discordancia debe ser que la mitad de nuestros pacientes se trataron con cirugía clásica, que es la que da lugar a menos restenosis22.
MortalidadLa PCR-hs elevada también se relaciona con la mortalidad de pacientes con EAP, tanto en su evolución natural como en los intervenidos por ICMI. Vainas et al observaron que los valores más altos de PCR-hs en pacientes con EAP se asociaban a una mayor mortalidad a los dos años de seguimiento16. Sultan et al, en un grupo de pacientes con ICMI tratados con angioplastia y cirugía revascularizadora, encontraron que la PCR-hs tenía un efecto negativo en la supervivencia a los 5 años23.
La mortalidad de nuestra serie fue de 20 casos, incluidas todas las causas de muerte, siguiendo en este punto la opinión de Owens et al3, basada en que la mayoría de las causas naturales no tienen verificación postmortem. Preferimos incluir en la mortalidad global un caso de supuesta autolisis, según información familiar a través de contacto telefónico, al no disponer de la confirmación de los datos.
En nuestro estudio de pacientes revascularizados por ICMI y seguimiento de un año, los valores prequirúrgicos de PCR-hs > 3mg/dl se asociaban, en el análisis multivariante, con el aumento de la mortalidad al año. También hemos encontrado en el análisis multivariante que los pacientes con categorías 5 y 6 de Rutherford, puesto que presentan mayor evolución y gravedad de su enfermedad, tenían también mayor mortalidad al año. Sin embargo, los tratados con técnica endovascular tenían menor mortalidad, probablemente por tratarse de lesiones infrainguinales menos complejas.
Deben añadirse algunas consideraciones en nuestro estudio. En primer lugar, la AHA considera pacientes de alto riesgo cardiovascular los que tienen valores de PCR-hs por encima de 0,3mg/dl. Nuestros pacientes tenían cifras mucho más elevadas, ya que había casos de ateroesclerosis avanzada, con gran afectación tisular del pie, así como con reagudizaciones de otros problemas médicos. Todas estas condiciones es sabido que se acompañan de cifras altas de marcadores inflamatorios y pueden haber influido en los resultados de nuestra serie. Además, solo un tercio de nuestros casos tomaba estatina al ingreso, que disminuye la respuesta inflamatoria y la PCR-hs17.
ConclusiónEn nuestra experiencia, los valores elevados de PCR-hs (> 3mg/dl) en el preoperatorio de pacientes con ICMI se relacionan con una mayor mortalidad al año.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
El presente artículo forma parte de la tesis doctoral: “Evaluación del tratamiento endovascular y quirúrgico en la isquemia crítica de miembros inferiores: Influencia de los biomarcadores de inflamación en el resultado y calidad de vida”, de la que es autor Ignacio Hernández-Lahoz Ortiz.