El colesterol es un esteroide precursor de hormonas, componente esencial de la membrana celular, sin embargo, alteraciones en la regulación de la síntesis, absorción y excreción del colesterol predisponen al desarrollo de enfermedades cardiovasculares de origen aterosclerótico. De esta manera, reconociendo los acontecimientos históricos desde hace 200 años, con Michel Chevreul que le dio el nombre «colesterina», más tarde Lobstein que acuñó el término aterosclerosis y Marchand que lo introduce, Anichkov que identifica el colesterol en las placas de ateroma, y el descubrimiento del receptor LDL por Brown y Goldstein; además de la aparición de los diferentes fármacos que han surgido desde los fibratos, las estatinas y en esta década cetrapibs, muy prometedores para aumentar el HDL, en forma más reciente, ezetimibe y anti-PCSK9 para inhibir el proceso de degradación del receptor LDL; no obstante, estos avances no han sido suficientes para disminuir la morbilidad en enfermedades cardiovasculares.
Cholesterol is a precursor of steroid hormones and an essential component of the cell membrane, however, altered regulation of the synthesis, absorption and excretion of cholesterol predispose to cardiovascular diseases of atherosclerotic origin. Despite, the recognition of historical events for 200 years, starting with Michel Chevreul naming «cholesterol»; later on, Lobstein coining the term atherosclerosis and Marchand introducing it, Anichkov identifying cholesterol in atheromatous plaque, and Brown and Goldstein discovering LDL receptor; as well as the emerging of different drugs, such as fibrates, statins and cetrapibs this decade, promising to increase HDL and the most recent ezetimibe and anti-PCSK9 to inhibit the degradation of LDL receptor, however morbidity has not been reduced in cardiovascular disease.
«Al seguir un camino pocos pueden predecir el lugar al que llegarán, hasta que alcanzan su final» JRR Tolkien (1892-1978)
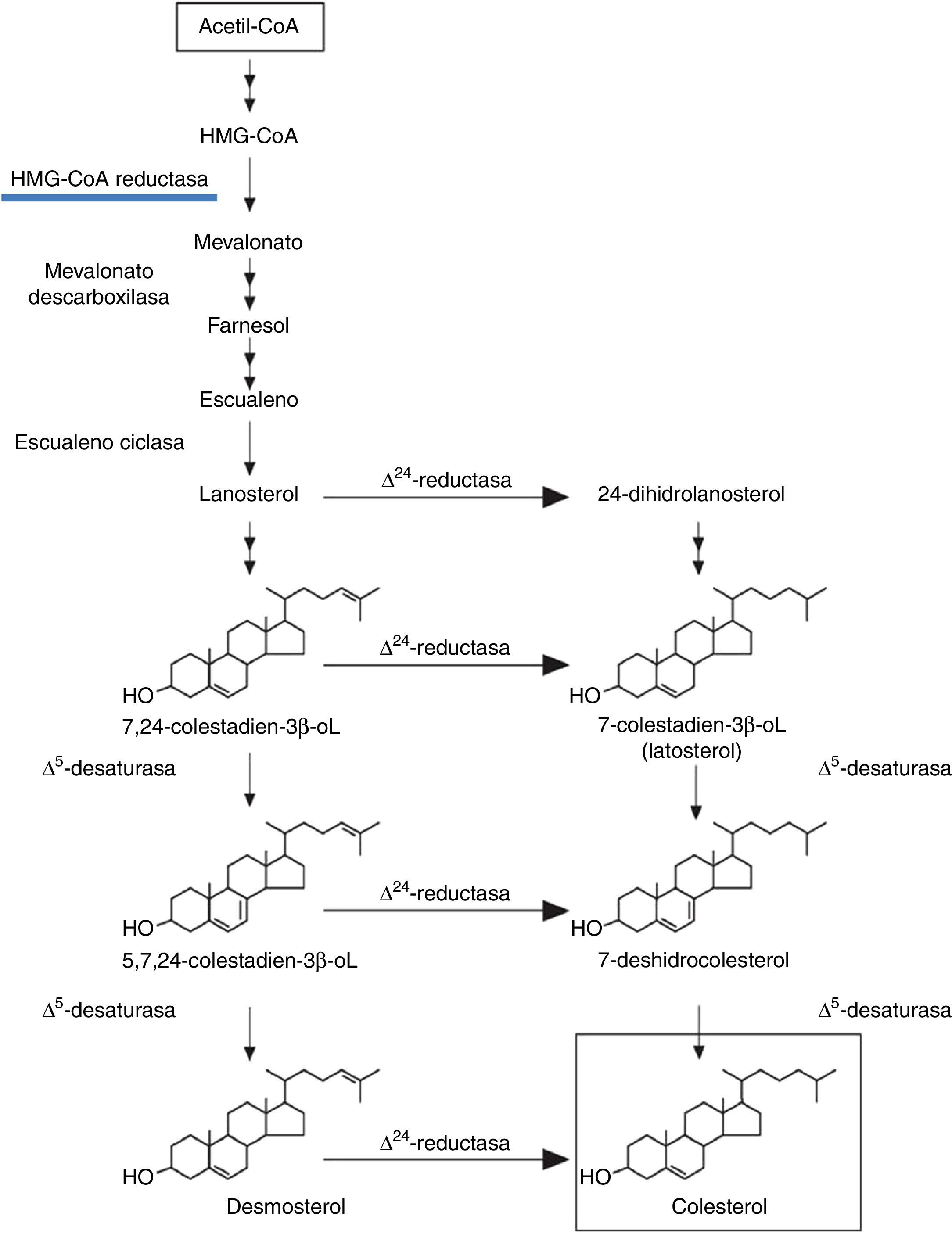
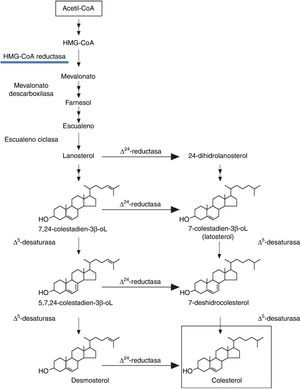
El colesterol es un esteroide que constituye el componente esencial de la membrana celular y es precursor de las hormonas esteroideas, varias vitaminas y la bilis (fig. 1). También es el componente esencial de la mielina que recubre a los nervios y de esta manera permite la conducción del impulso eléctrico para asegurar la correcta respuesta por parte de los tejidos efectores. Una fracción del colesterol se obtiene de los alimentos, pero la mayor proporción se sintetiza en el hígado y de allí pasa a la circulación general, siendo transportado por las lipoproteínas, las cuales son de diferente peso molecular1. El colesterol fue descubierto por François Poulletier de la Salle en 1769 como la porción «aceitosa» de la bilis obtenida de la vesícula biliar extraída de cadáveres; sin embargo, hasta 1815 no se consiguió separar ese contenido aceitoso de la bilis por el químico francés Michel-Eugéne Chevreul (1786-1889) (fig. 2) quien le dio el nombre de «colesterina» y después se cambió a colesterol (del griego: chole, bilis; stereos, sólido). Más tarde, en 1833, F. Boudet demostró que el colesterol también se encontraba en la circulación. Cerca de un siglo después, en 1904 Felix Jacob Marchand (1846-1928) demostró que el colesterol se encontraba y era uno de los componentes principales de la placa ateromatosa y en consecuencia en la génesis de la aterosclerosis. La estructura molecular del colesterol fue descubierta por Heinrich O. Wieland (1877-1957) por lo cual recibió el Premio Nobel de Química en 1927; asimismo, Adolf O. Reinhold Windaus (1876-1959) demostró que la placa ateromatosa en la arteria aorta contenía cristales de colesterol y por ello recibió el Nobel de Química en 19282. Más adelante se otorgó el Premio Nobel de Fisiología y Medicina en 1964 a George J. Popjak (1914-1998), Konrad E. Bloch (1912-2000) y Feodor F. Lynen (1911-1979) por demostrar que el acetato es el precursor en la síntesis del colesterol. El mevalonato ocupa un lugar especial en la cadena enzimática porque cuando se impide experimentalmente su formación mediante la enzima hidroxi-metil-glutaril-CoA reductasa (HMG-CoA reductasa) no progresa más allá la síntesis de colesterol, y por ello se le otorgó el Premio Nobel de Química 1975 a John W. Cornforth (1917-2013)3. Otra investigación fundamental fue el descubrimiento del receptor celular hepático para el acoplamiento de la lipoproteína de baja densidad (r-LDL) realizada por Michael S. Brown (1941-) y Joseph L. Goldstein (1940-) por lo cual determina un proceso clave en el metabolismo del colesterol; por ello fueron merecedores del Nobel de Fisiología y Medicina en 1985 (tabla 1)3–5 (fig. 3). Ante este panorama y tomando en cuenta que el colesterol contribuye a la aterosclerosis se buscaba una manera farmacológica para bloquear la síntesis de dicha molécula. En 1973 Akira Endo encontró que en el cultivo de una especie de hongo se producía una sustancia que tenía la capacidad de inhibir HMG-CoA reductasa y en consecuencia impedía la formación de colesterol. En semejanza con lo que ocurrió en el caso de la obtención de penicilina por Fleming, surgió la idea de obtener un producto farmacológico que pudiera ser utilizado en la clínica para el tratamiento de la hipercolesterolemia. Este producto tuvo inicialmente el nombre de compactina, así el estudio de fármacos similares han sido conocidos como estatinas lo cual significó un avance impresionante en la terapéutica; por estos hallazgos Endo recibió el Premio Lasker en 20086,7.
Investigadores que han recibido el Premio Nobel por sus descubrimientos científicos relacionados con el estudio del colesterol
| • Heinrich Otto Wieland por la composición de los ácidos biliares recibió el Nobel de Química en 1927 • Adolf Otto Windaus describe en sus estudios sobre ateromas formados de cristales de colesterol por ello le fue otorgado el Nobel de Química en 1928 • A Konrad Bloch y Feodor Lynen por sus estudios de la vía de biosíntesis del colesterol les fue otorgado el Nobel de Fisiología y Medicina en 1964 • Michael S. Brown y Joseph L. Goldstein, por sus estudios sobre el metabolismo de colesterol les fue otorgado el Nobel de Fisiología y Medicina en 1985 |
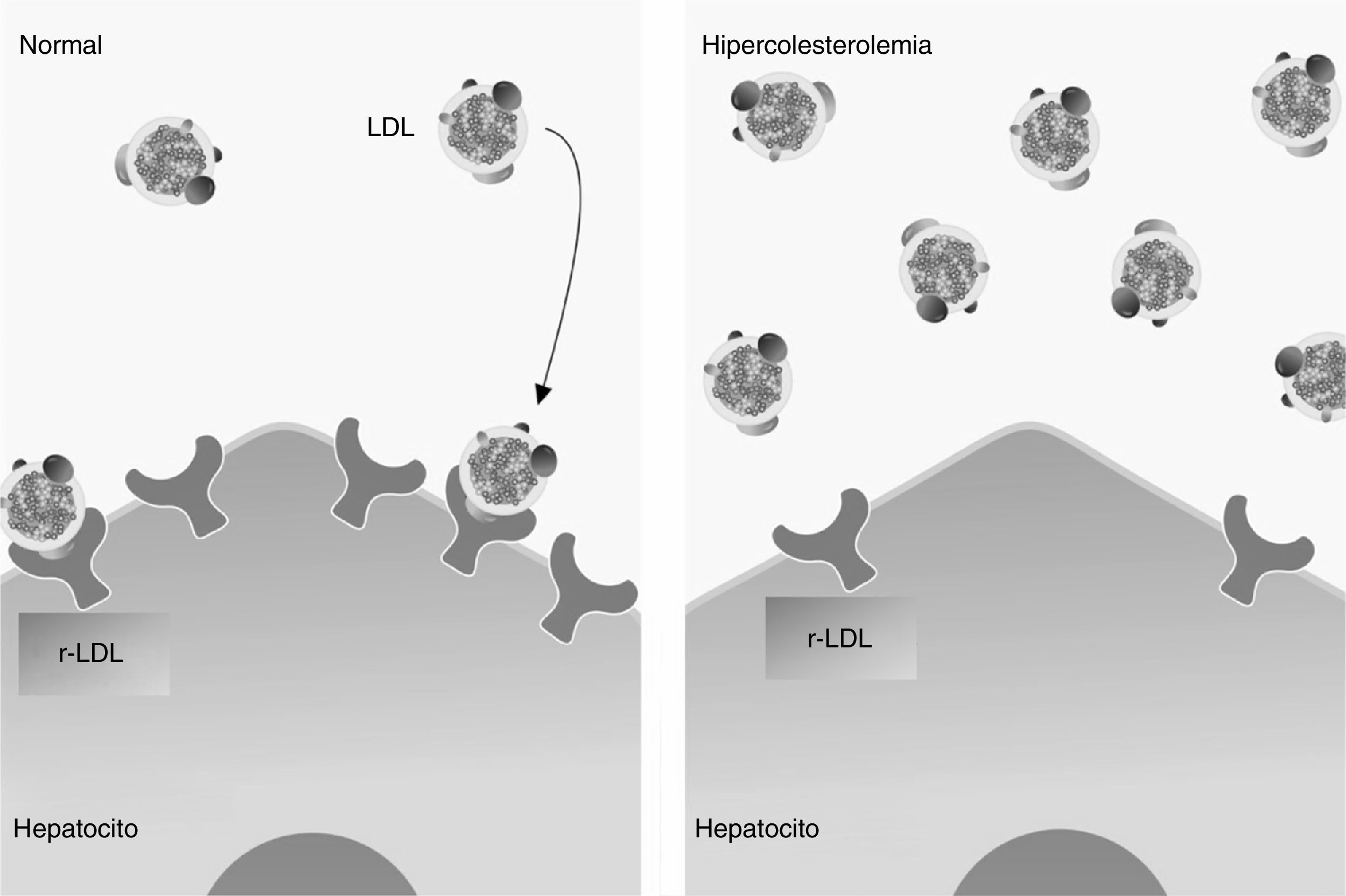
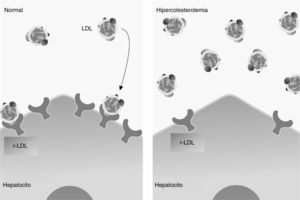
Representación esquemática de la captura de LDL por los receptores específicos localizados transmembranalmente en el hepatocito en condiciones normales (lado izquierdo). En el lado derecho se nota una reducción importante del receptor, lo cual causa un exceso circulante de colesterol, debido a que el colesterol no es degradado por permanecer en la circulación.
El colesterol circulante requiere ser transportado por lipoproteínas ya que es insoluble; los quilomicrones son transportadores, pero también existen la lipoproteína de baja densidad (LDL), de muy baja densidad y alta densidad (HDL). La principal fuente de colesterol proviene de la síntesis interna que comprende entre 800-1,500mg diarios, a la cual se suman aproximadamente 300mg proveniente de la alimentación; en otras palabras, los alimentos contribuyen en menor cantidad del colesterol circulante. En el intestino delgado se absorbe cerca del 40% del total de grasas que recorren el tubo digestivo y estas son empaquetadas simultáneamente con los triglicéridos, en forma de quilomicrones que son de una menor densidad y tamaño mayor (contiene apoproteína A, B y E)8.
Por otra parte, en el hepatocito se realiza la síntesis del colesterol endógeno que de inmediato se une a las diferentes lipoproteínas para de esta manera ingresar a la circulación general en 2 formas principales que son la lipoproteína de alta densidad (HDL) y la de baja densidad (LDL). Estas lipoproteínas regresan al hígado en donde se acoplan a los 2 tipos de receptores específicos r-LDL y r-HDL que se encuentran en la membrana de los hepatocitos en donde son metabolizados. HDL, conocido genéricamente como «colesterol bueno» contribuye a la formación de las sales biliares; en contraste, LDL conocido como «colesterol malo» es transportado por el r-LDL al interior de la célula8,9. Este receptor compuesto de 839 aa captura e internaliza LDL en donde es hidrolizado por los lisosomas para degradar al colesterol, entonces r-LDL se recicla para repetir su función a partir de la membrana del hepatocito (fig. 3). De esta manera se explica que la ausencia del gene encargado de la expresión de r-LDL, como ocurre en algunas familias, se produce hipercolesterolemia, la cual se conoce como la variedad familiar. Esta enfermedad es rara y se presenta generalmente en una familia homocigota. El otro tipo de hipercolesterolemia es la adquirida, la cual aparece en individuos mayores de 20 años. El descubrimiento y función del r-LDL por Brown y Goldstein (fig. 4) significó un avance seminal en el entendimiento de la hipercolesterolemia4,9.
Desarrollo del ateromaEl primero que utilizó el término arteriosclerosis fue Johann Friedrich Lobstein en 1829, fue quien identificó mediante el análisis macroscópico el endurecimiento de la pared vascular; pasaron 75 años entre Lobstein y Marchand en 1904, para el empleo de los 2 términos: arteriosclerosis y aterosclerosis, términos originados en la Universidad de Estrasburgo. Años después los médicos rusos Ignatowsky y luego Nikolai Anichkov realizaron por primera vez la inducción de aterosclerosis en conejos sometidos a una dieta abundante en contenido de colesterol3,10. El análisis de la aorta de los animales mostraba la presencia de las placas blanco-grisáceas semejantes a las que se encontraban en la autopsia de personas fallecidas por enfermedad cardiovascular. Por otra parte, Anichkov propuso que además de la hipercolesterolemia deberían existir otros factores para la formación de la placa ateromatosa11 y la causa de la muerte en el humano, mencionándose entre los riesgos la edad, la historia familiar, el sedentarismo, la obesidad, el tabaquismo, la hipertensión arterial y la diabetes. Más adelante, en 1938, Carl Müller describió la hipercolesterolemia familiar como una enfermedad autosómica dominante asociada con xantomas en varios sitios del cuerpo y la aparición precoz de enfermedad coronaria3,10,12.
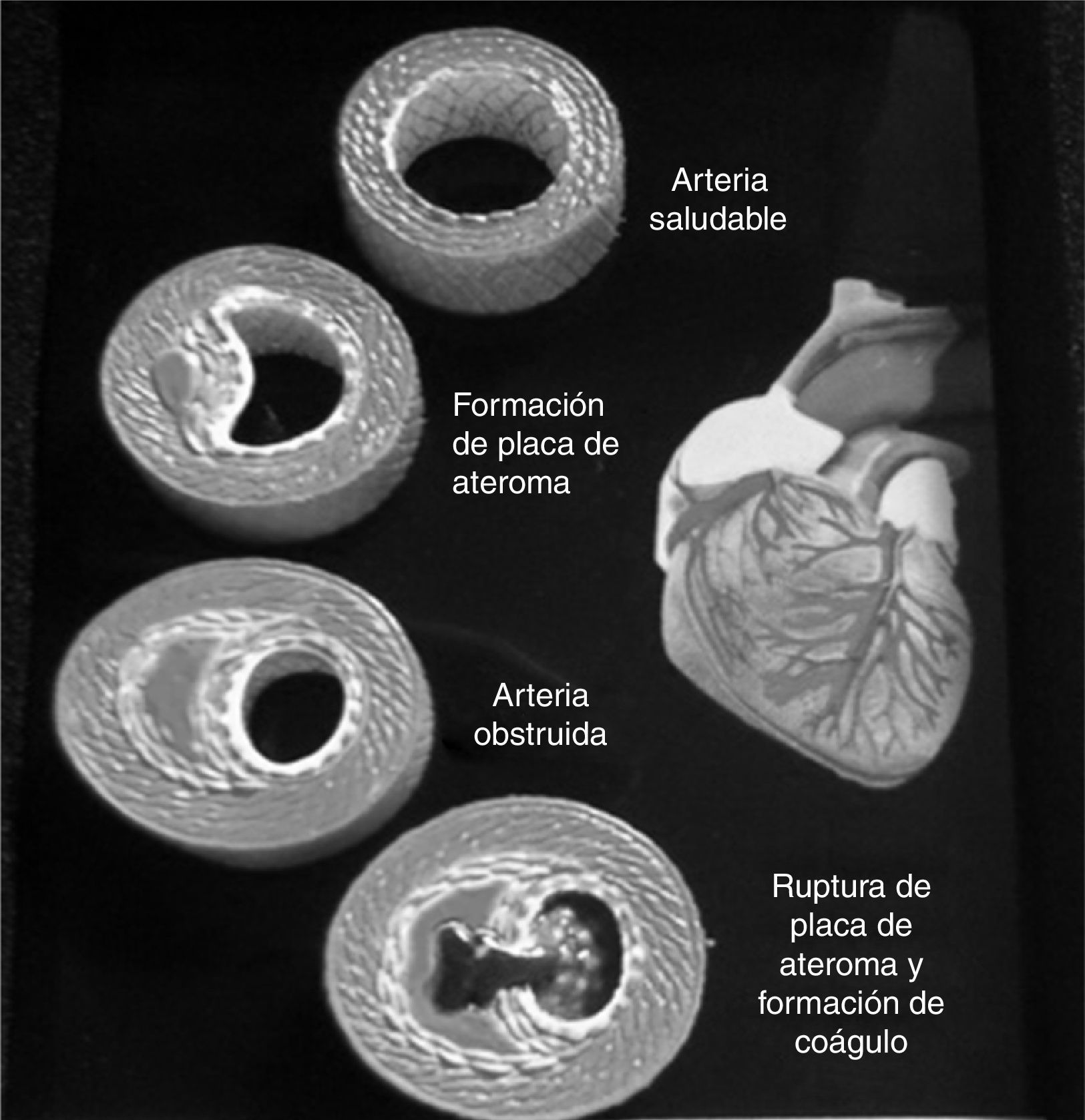
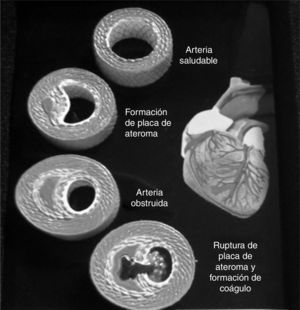
Estudios posteriores mostraron que la aterosclerosis no solo era provocada por el acúmulo del colesterol en la capa interna de las arterias resultando en la obstrucción de la corriente circulatoria, sino que simultáneamente se desarrollaba un proceso inflamatorio causante de una disfunción endotelial compleja acompañada de alteración en la coagulación con la formación de trombos que terminaba en la fatal rotura de la placa ateromatosa13–16 (fig. 5).
Tratamiento de la hipercolesterolemiaLa aterosclerosis permanece como la primera causa de mortalidad, aparentemente debido a la prolongación de la expectativa de vida, la obesidad, el sedentarismo, el tabaquismo, y el incremento de comorbilidad en la que destaca la diabetes mellitus, la dislipidemia y la hipertensión arterial. Históricamente el reconocimiento de la importancia del desarrollo de aterosclerosis se considera uno de los avances más importantes para esclarecer la fisiopatogenia; asimismo, el conocimiento de la participación del colesterol en la formación de la placa ateromatosa abrió un caudal de maniobras diagnósticas y terapéuticas para ayudar a prevenir la ocurrencia de aterosclerosis y enfermedad cardiovascular17,18.
Una de las primeras medidas implementadas para disminuir el colesterol circulante se dirigió a la reducción dietética de alimentos grasos; sin embargo, pronto surgió la hipótesis de que el problema no era simplemente mecánico, es decir un bloqueo producido por la acumulación de colesterol, sino que se antojaba que fuera multifactorial. El avance tecnológico facilitó establecer que coincidían con un proceso inflamatorio que promovía una disfunción endotelial y trastorno hemostático, lo cual en conjunto inducía la rotura de la placa ateromatosa y el desprendimiento trombótico. Continúa aceptándose la conveniencia de establecer una alimentación con contenido muy bajo en grasas en particular saturadas y evitar la obesidad. Asimismo, se debe controlar la hiperglucemia, la hipertensión arterial y la dislipoproteinemia. En esta revisión se hace énfasis en esta última porque desde hace varios años se ha tratado de encontrar el fármaco óptimo y ha sido el motivo de recurrentes controversias16–18.
Entre los primeros fármacos se encuentra el clofibrato que desde 1962 mostró su efecto principal sobre la hipertrigliceridemia, así como una reducción modesta sobre LDL y pobre incremento sobre HDL circulante; por ello se consideró magro su utilidad en la prevención y el tratamiento de la enfermedad cardiovascular. Además, los fibratos se relacionaron con malestar indeseable tanto en el aparato gastrointestinal como en el muscular. También se ha utilizado el ácido nicotínico que aunque origina pocos efectos indeseables su efectividad terapéutica es incluso inapreciable19,20.
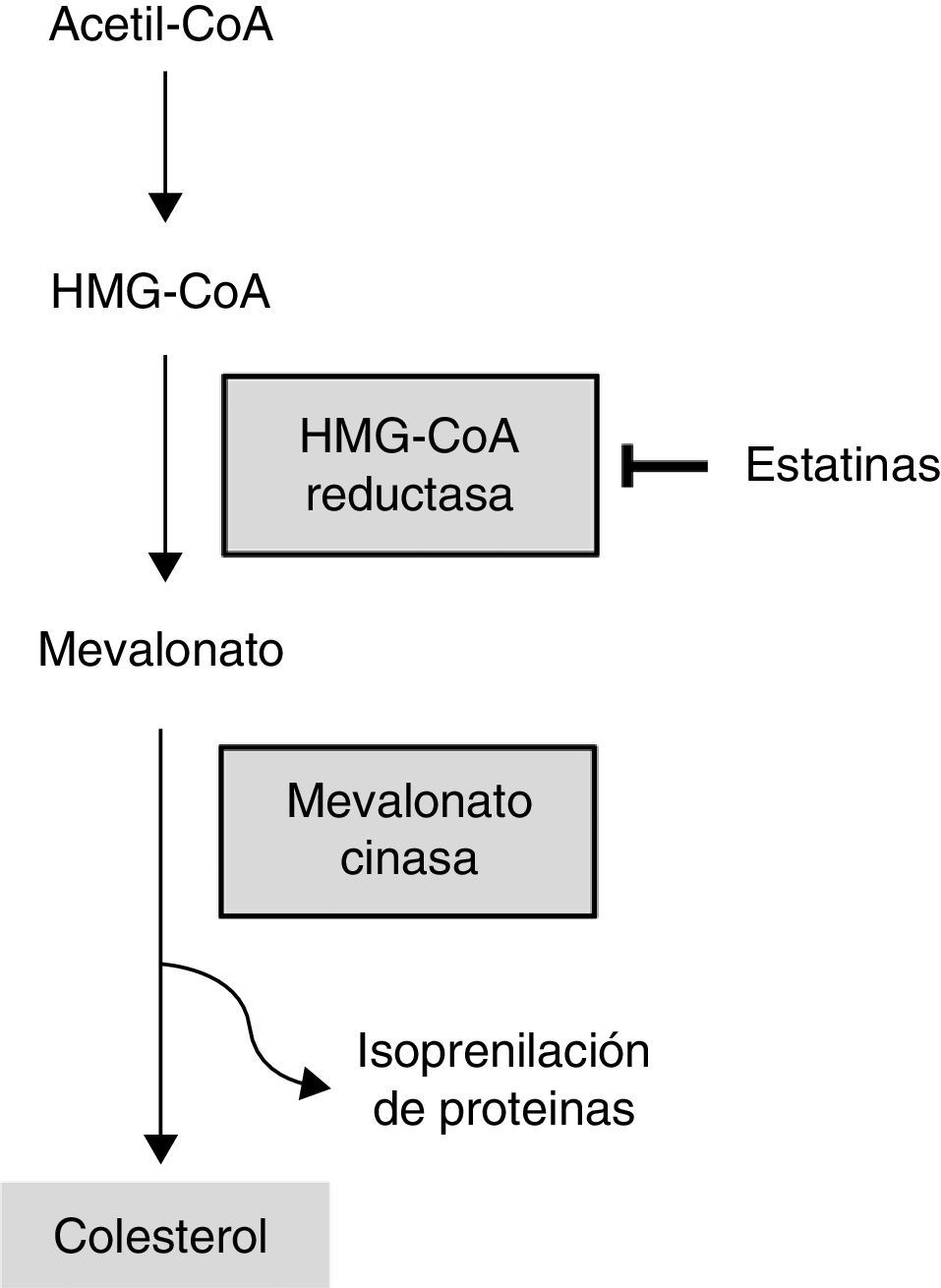
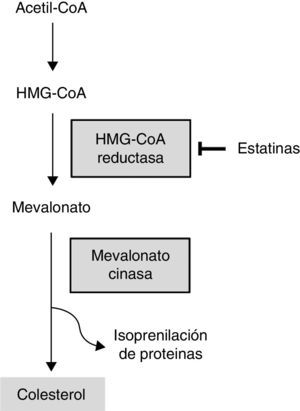
El descubrimiento seminal de las estatinas por Akira Endo (fig. 6) consistió en aislar 3,800 cepas de hongos encontrando que una de ellas, Penicillium citrinum, tenía la propiedad de inhibir el efecto de una enzima clave en la cadena de síntesis de colesterol; de esta manera, bloqueando artificialmente a la enzima HMG-CoA reductasa se anulaba la producción de mevalonato que era necesario para alcanzar la formación de colesterol (fig. 7). Este producto del hongo recibió el nombre de compactina, la cual se incluyó en la industrialización farmacéutica con el nombre de Mevastatina marcando el principio de las estatinas6. Las pruebas clínicas de inmediato confirmaron la magnífica utilidad de las estatinas para reducir los niveles elevados de colesterol circulante y de esta manera ofrecer un recurso efectivo en la prevención de la enfermedad cardiovascular7. En esa época las estatinas ocupan uno de los primeros lugares en el consumo de la farmacoterapia, pero al utilizarse a un grado masivo en la población general aparecieron algunos efectos indeseables, principalmente oculares, musculares y gastrointestinales. Esto llevó a la aparición de nuevas modalidades como fueron la atorvastatina y la simvastatina; así como, por otro lado, situaciones de controversia en cuanto, el efecto hipocolesterolemiante y su lugar en la prevención de efectos cardiovasculares20,21. Las estatinas poseen un racimo de efectos biológicos complejos que incluye mejorías en la disfunción endotelial, incremento de la biodisponibilidad de óxido nítrico, propiedades antioxidantes e inhibición de proceso inflamatorio que es separado del efecto lipoproteico, y todo ello podría explicar el mecanismo protector de las estatinas22.
La terapéutica para reducir solamente el nivel del colesterol total circulante no era suficiente ya que era necesario tomar en cuenta la concentración de LDL en relación con su receptor específico localizado en el hepatocito confirmando la teoría propuesta por Goldstein y Brown demostrando que el r-LDL capturaba LDL circulante para internalizarlo y degradar al colesterol por los lisosomas; y posteriormente el receptor se reciclaba para repetir la captura de LDL4,23.
Por otra parte, se demostró la existencia del gen denominado PCSK9 que se encarga de inhibir la síntesis de r-LDL y por ello se han desarrollado anticuerpos monoclonales que son capaces de bloquear a dicho gen y así inducir la síntesis de una mayor cantidad de r-LDL. En la actualidad se están ensayando clínicamente 2 fármacos, alirocumab y evolocumab, que pueden reducir LDL circulante entre un 50-70%; el efecto se extiende a la prevención de episodios cardiacos y la muerte. Esta novedosa variante terapéutica tiene el inconveniente de la administración por vía parenteral cada 2-4 semanas y seguramente tendrá un costo elevado; además es indispensable realizar estudios a largo plazo y por ahora se restringe su uso experimental en los casos de intolerancia y/o fracaso con las estatinas, en personas con el antecedente de un episodio cardiovascular24,25.
Adicionalmente se han realizado estudios con cetrapibs (torcetrapib, dalcetrapib y anacetrapib) que son inhibidores de la proteína de transferencia del éster de colesterol con el objeto de incrementar HDL que, como se ha mencionado, se considera como la «lipoproteína buena»26. Existe la controversia de asociar una estatina con ezetimiba (Rx Vytorin), que tiene el efecto de reducir la absorción intestinal del colesterol proveniente de los alimentos27,28. El estudio de dicha combinación IMPROVE-IT, que utiliza 40mg de simvastatina y 10mg de ezetimiba, ha mostrado resultados satisfactorios en cuanto al decremento de eventos coronarios y cerebrales29.
FinanciaciónLos autores manifiestan que reciben una beca proporcionada por SNI/CONACYT y están asignados profesionalmente al IMSS (excepto IS).
Conflicto de interesesLos autores declaran no tener conflicto de intereses.