Introducción
En México existe un número considerable de pacientes que se someten a una intervención cardiovascular, con un riesgo operatorio mayor respecto de las décadas anteriores; en consecuencia, es indispensable contar con protocolos de atención que optimicen los resultados posquirúrgicos.
Este capítulo se enfoca en los cuidados posoperatorios del paciente no complicado de la cirugía cardiaca, que se define como aquel individuo extubado en las primeras 12 h del posoperatorio, con índices de oxigenación normales, un sangrado mediastínico perioperatorio < 1 000 ml en las primeras 24 h, un perfil hemodinámico con un índice cardiaco > 2.4 L/m2/s, un gasto urinario ≥ 1 ml/kg/h con requerimientos mínimos de aminas que disminuyen en las primeras 24 h en la unidad de cuidados intensivos cardiovasculares (UCIC) y, por último, nula necesidad de dispositivos externos para mantener un perfil hemodinámico normal.
El manejo posquirúrgico del paciente sometido a una operación cardiovascular es un desafío permanente y complejo; las condiciones biológicas anteriores a la intervención, los desequilibrios producidos por el acto quirúrgico y los efectos secundarios ocasionados por la circulación extracorpórea hacen que cada paciente tenga una evolución particular. El manejo posoperatorio de estos sujetos requiere del conocimiento de la afección cardiovascular y los mecanismos compensatorios que interactúan para establecer la homeostasia, las técnicas quirúrgicas y anestésicas llevadas a cabo en el quirófano y los efectos sistémicos y locales de la circulación extracorpórea (CEC) y sus mecanismos lesivos. Por lo tanto, la intervención oportuna y radical en el tratamiento posoperatorio incide en el control de la morbimortalidad de estos pacientes. Es necesaria una completa vigilancia de diversos parámetros fisiológicos en la UCIC y un control muy dinámico de las medidas de apoyo hemodinámico y respiratorio conforme cambia el estado clínico del enfermo.
Traslado del paciente del quirófano a la UCIC
Una vez que el procedimiento quirúrgico concluye y que el anestesiólogo considera apto al paciente para su trasladado, el equipo en sala debe comunicarse con el equipo de la UCIC para notificar el estado del paciente, los fármacos en infusión y los dispositivos especiales de asistencia (BCIA, DAV, ON, etcétera), de tal forma que el equipo de la UCIC conozca el posible escenario clínico del paciente a su ingreso.
El traslado de estos sujetos representa un riesgo real de muerte, por lo que debe realizarse con un protocolo adecuado, con el personal idóneo y en las condiciones más apropiadas.
Equipo y personal de traslado. El personal mínimo necesario para realizar el traslado es de cuatro individuos: el anestesiólogo, el cirujano designado y dos enfermeras (de anestesia y circulante); en condiciones ideales es posible incluir a un terapista en cuidados respiratorios o un técnico en cuidados intensivos.
Recomendación I, nivel de evidencia A
Ventilación. Los pacientes con ventilación espontánea y saturación por oximetría de pulso > 90% pueden abandonar el quirófano extubados; si la saturación es < 90% a pesar del 02 complementario con mascarilla, no pueden salir extubados y se requiere una nueva intubación para proteger la vía respiratoria. Todas las fuentes de oxígeno deben tener la capacidad de suministrar al paciente por lo menos durante 30 min, por lo que es necesario revisarlas de forma continua.
Recomendación I, nivel de evidencia A
Presión arterial y accesos venosos. Todo paciente sometido a una intervención cardiaca debe salir del quirófano con un acceso arterial y dos venosos (al menos uno de ellos central).
Recomendación I, nivel de evidencia B
Ritmo cardiaco. En una operación cardiaca, el paciente debe tener un marcapaso epicárdico externo; su función es regular la frecuencia cardiaca, así como las arritmias transoperatorias y posoperatorias. Existen diversos tipos de cirugía (como la valvular), que se relacionan con frecuencia con bloqueos auriculoventriculares, lo que hace indispensable el apoyo de un marcapaso externo; asimismo, dado que esta alteración no puede anticiparse con facilidad, es importante colocar un marcapaso en toda persona programada para una intervención cardiaca. En ocasiones, cuando se tratan las arritmias posoperatorias, es deseable disponer de un marcapaso que asegure un ritmo de emergencia en el caso de posibles bloqueos farmacológicos.
Recomendación I, nivel de evidencia A
La frecuencia cardiaca programada en el marcapaso depende de la situación clínica y hemodinámica del enfermo. En situaciones en las que existe un evidente riesgo de bloqueo, se debe dejar el marcapaso a demanda con una frecuencia segura (50 a 60 lpm) o mantener 10 latidos por debajo del ritmo de base de tal modo que se mantenga una adecuada perfusión y presión. Siempre que sea posible, es preferible colocar un marcapaso bicameral para asegurar la contribución auricular en apoyo de la función ventricular.
Recomendación IIa, nivel de evidencia B
Drenajes
Drenajes torácicos. Los pacientes sometidos a toracotomía tienen drenajes pleurales o mediastínicos, según sea el caso, y deben estar permeables y conectados a sistemas cerrados de aspiración.
Recomendación IIa, nivel de evidencia C
Sonda vesical. La sonda vesical debe conectarse a una bolsa colectora cerrada.
Recomendación I, nivel de evidencia A
Traslado
Es aconsejable que el cambio de la mesa de quirófano a la cama de traslado se efectúe directamente a la cama de la UCIC, de tal manera que se eviten las movilizaciones adicionales peligrosas; asimismo, es recomendable que no existan cambios de bomba de infusión y que sean las mismas del quirófano la que se utilicen en la UCIC, ya que la suspensión incluso temporal y rápida de los fármacos (arterenol, adrenalina o dopamina) puede representar un gran riesgo.
Recomendación IIa, nivel de evidencia C
Recepción del paciente en la UCIC
Los cuidados posoperatorios comienzan aún antes de la llegada del paciente a la UCIC; en esta etapa, la preparación de la habitación donde se recibirá al individuo operado está a cargo del jefe de enfermería y el médico intensivista.
Recomendación IIa, nivel de evidencia B
Antes de la recepción
El equipo encargado de recibir al paciente debe preparar los siguientes implementos:
• Ventilador.
• Sistema de monitoreo invasivo y no invasivo.
• Sistemas de aspiración.
• Fármacos requeridos por el paciente de respaldo, de acuerdo con la información del quirófano .
• Carro de paro adecuado para realizar una reanimación cardiopulmonar, si se requiere.
Recepción del paciente
La recepción del paciente exige la transmisión de la información clínica por parte de cirujano y anestesiólogo al equipo médico y de enfermería que atiende al paciente en la UCIC. De manera inicial deben continuarse las medidas terapéuticas instituidas en el quirófano mientras se activan los sistemas de vigilancia y se analiza la situación del sujeto.
Recomendación I, nivel de evidencia A
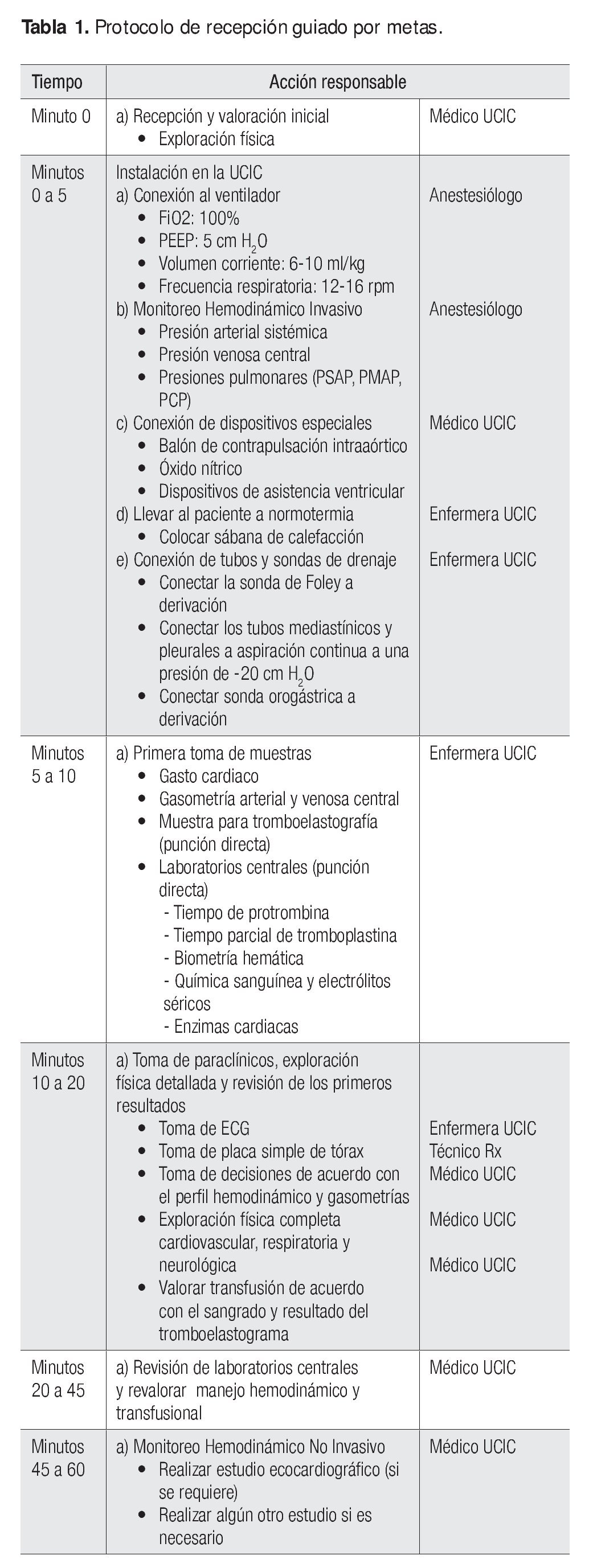
Para la adecuada recepción del paciente es preciso contar con un protocolo pormenorizado de las acciones que lleva a cabo cada integrante del personal asignado; además, es deseable contar con una recepción guiada por objetivos para optimizar el trabajo del personal en la UCIC (Tabla 1).
Atención general
Soluciones
En el posoperatorio, la mayoría de los pacientes experimenta una sobrecarga de volumen, alrededor de 5% de su peso preoperatorio como resultado de la hemodilución en la circulación extracorpórea. Debido a factores secundarios a esta última, como fuga capilar, vasodilatación y disminución de la presión osmótica, este estado puede no reflejarse en las presiones de llenado, las cuales pueden indicar normovolemia o hipovolemia. Asimismo, durante las primeras horas del posoperatorio, algunos sujetos registran volúmenes urinarios elevados, como consecuencia de la administración de manitol, y presiones de llenado bajas (también son posibles volúmenes urinarios bajos). En un estado en el cual se altera la permeabilidad de la membrana por el proceso inflamatorio secundario a la circulación extracorpórea es preferible utilizar soluciones que expandan el espacio intravascular y atenúen la expansión del espacio intersticial.
Se deben suministrar soluciones cristaloides con la finalidad de mantener una adecuada volemia intravascular; los parámetros empleados con frecuencia para tomar esta decisión son la presión venosa central, presión pulmonar en cuña o la variación de la presión arterial invasiva, todas las cuales tienen sus limitaciones.
Recomendación IIa, nivel de evidencia A
Se pueden infundir también soluciones coloides para la reposición y las cargas de volumen.
Recomendación IIb, nivel de evidencia B
Electrólitos
Deben mantenerse en límites normales y su aporte se determina de acuerdo con las pérdidas y necesidades del paciente, en particular potasio y magnesio.
Recomendación I, nivel de evidencia A
Las soluciones cristaloides deben contener potasio, de tal forma que se conserven concentraciones séricas de 3.7 a 5.5 mEq/L para prevenir arritmias ventriculares.
La adición de dosis bajas de magnesio a las soluciones cristaloides es útil para impedir las arritmias supraventriculares y ventriculares (dosis de 2-6 g/día).
Recomendación IIa, nivel de evidencia B
Fármacos
Antiagregantes plaquetarios
Ácido acetilsalicílico
La administración temprana de antiagregantes plaquetarios ha mejorado la permeabilidad de los puentes coronarios y reducido la mortalidad en los pacientes sometidos a una revascularización coronaria. Goldman y colaboradores realizaron un estudio aleatorizado (n = 772) con los siguientes brazos: a) ácido acetilsalicílico, 325 mg cada 24 h; b) ácido acetilsalicílico, 325 mg como dosis única; c) sulfinpirazona, 267 mg; y d) placebo. No encontraron diferencias en la mortalidad en relación con los diferentes antiagregantes, pero sí respecto del grupo control en el cual se identificó un aumento de la mortalidad. Dacey y colaboradores, en un estudio de casos y controles, compararon el uso del ácido acetilsalicílico preoperatorio con la mortalidad intrahospitalaria (n = 8 461). Estos especialistas hallaron que la administración del ácido acetilsalicílico, siete días antes de la operación, disminuía la mortalidad en los sujetos posoperados (RM, 0.55; IC 95%, 0.31-0.98). Mangano, en un estudio de cohorte y prospectivo, investigó el consumo temprano de ácido acetilsalicílico después de la revascularización coronaria (n = 5 065) dentro de las primeras 48 h posoperatorias. Los pacientes que recibieron ácido acetilsalicílico tuvieron una menor mortalidad en comparación con los que no lo recibieron (RM, 0.41; IC 95%, 0.27-0.62; P <0.0001). En consecuencia, debe emplearse este fármaco a dosis de 100 a 325 mg en las primeras 24 h si no hay sangrado; cuanto más temprano mejor, ya que algunos estudios en los que se administró a las 6 h del posoperatorio mostraron una mejoría de la permeabilidad de los puentes y disminución de la mortalidad. Esta terapéutica debe continuarse de manera indefinida.
Recomendación I, nivel de evidencia A
Clopidogrel
El American College of Physicians recomienda el uso del clopidogrel junto con ácido acetilsalicílico en pacientes sometidos a revascularización coronaria luego de un infarto, sin elevación del segmento ST, durante nueve a 12 meses posteriores a la operación. La mayoría de los cirujanos lo utiliza en individuos que requieren revascularización de urgencia y en personas que sufrieron un infarto sin elevación del segmento ST. Sin embargo, esta relación incrementa el riesgo de sangrado y no ha demostrado mayor beneficio que el uso del ácido acetilsalicílico solo.
Recomendación III, nivel de evidencia B
La evidencia se basa en estudios de grupos pequeños, no aleatorizados, no controlados y no doblemente cegados, por lo que se ha concluido que en caso de utilizarse debe administrarse junto con el ácido acetilsalicílico, luego de 48 h, para reducir el riesgo de sangrado y en pacientes que requieren intervenciones de urgencia o luego de un infarto sin elevación del segmento ST.
Analgésicos
Inducir una adecuada analgesia durante el posoperatorio temprano minimiza la ansiedad, el dolor y el estrés hemodinámico que contribuyen a la hipertensión y la isquemia. Los opioides son los analgésicos más usados después de un procedimiento cardiaco (morfina y oxicodona). Sin embargo, no deben administrarse hasta que el paciente manifieste la intensidad del dolor: a pesar de que ofrecen un adecuado alivio del dolor, son susceptibles de producir una sedación prolongada y depresión respiratoria. El objetivo de la analgesia consiste en iniciar un opioide oral dentro de las primeras 24 h posteriores a la intervención. Éste ayuda a facilitar la tolerancia a la vía oral, la movilización del paciente y la realización de la fisioterapia pulmonar.
Recomendación I, nivel de evidencia A
Por su parte, los antiinflamatorios no esteroideos (AINE) son los más administrados para el dolor agudo. En un meta-análisis se demostró el efecto potencial de los AINE para reducir el consumo de opiáceos en cerca del 20%. Aunque su eficacia analgésica está demostrada, sus efectos adversos pueden presentarse, los más comunes de los cuales son gastritis, úlcera péptica, insuficiencia renal, broncoespasmo mediado por leucotrienos y sangrado posoperatorio. En cuanto al uso de los inhibidores de la ciclooxigenasa II, se han vinculado con un mayor índice de trombosis coronaria (valdecoxib/parecoxib). El rafecoxib tiene un claro nexo con mayor trombosis coronaria y cerebrovascular en la analgesia crónica, por lo que debe evitarse al máximo.
La dosis regular de AINE puede atenuar la intensidad del dolor y minimizar el consumo de opioides; no obstante, debido a sus efectos adversos, debe evitarse en sujetos con riesgo de sangrado, úlcera péptica e insuficiencia renal.
Recomendación clase I, nivel de evidencia A
El paracetamol, al igual que los AINE, disminuye hasta en 20% la utilización de los opioides en las primeras 24 h del posoperatorio; su efecto analgésico es mayor con la administración intravenosa.
Recomendación clase IIa, nivel de evidencia A
El tramadol es una buena alternativa cuando la eficacia de los opioides, solos o en combinación con los AINE o paracetamol, no inducen una analgesia eficaz o están contraindicados. Durante el posoperatorio de un procedimiento cardiaco es preferible emplear analgésicos del tipo de los AINE, paracetamol o tramadol, en caso de no obtener una analgesia eficaz o se encuentren contraindicaciones.
Recomendación clase Ia, nivel de evidencia A Antibióticos profilácticos Cobertura para Staphylococcus Las infecciones nosocomiales se desarrollan en un 10% a 20% de los pacientes sometidos a una operación cardiaca; las heridas quirúrgicas son sitios comunes, al igual que el sistema respiratorio y el tracto urinario. El riesgo relativo (RR) de muerte por infecciones en estos individuos se incrementa a 4.0 (95% con intervalo de confianza de 2.7-5.8) y el tiempo de estancia hospitalaria prolongada es tres veces mayor. El régimen antimicrobiano debe incluir cobertura para Staphylococcus y se administra la primera dosis una hora antes de la incisión quirúrgica y durante 48 a 72 h posoperatorias. En caso de alergia se emplea otro antibiótico con la misma cobertura.Recomendación I, nivel de evidencia A
Protección gástrica
Inhibidores H2 e inhibidores de la bomba de prótones
Tanto los inhibidores H2 como los inhibidores de la bomba de protones se han estudiado ampliamente en pacientes críticos y han demostrado su eficacia en la prevención de la úlcera por estrés, neumonía relacionada con el ventilador y mortalidad, sin encontrar diferencias entre ellos. Sin embargo, con los inhibidores H2 la rápida taquifilaxia limita su eficacia.
Recomendación IIa, nivel de evidencia A
Sucralfato
En un meta-análisis de profilaxis de úlcera por estrés en pacientes críticos, la eficacia del sucralfato se comparó con los inhibidores H2 en nueve estudios y con antiácidos en ocho protocolos. El sucralfato fue más eficaz que los inhibidores H2 (RM, 0.532; IC 95%, 0.303 - 0.933) e igual de efectivo que los antiácidos (RM, 0.868; IC 95%, 0.452 -1.667). La aparición de neumonía en estos individuos fue más frecuente con los inhibidores H2 (RM, 0.316 - 0.783) y con los antiácidos (RM, 0.402; IC 95%, 0.235 - 0.687). Pese a ello, existe poca evidencia que sustente con solidez el uso del sucralfato porque los estudios realizados incluyen un número no significativo de pacientes.
Recomendación IIa, nivel de evidencia B
Control glucémico
El control glucémico en los sujetos sometidos a una operación cardiaca es parte integral de los cuidados posoperatorios; su finalidad es disminuir la incidencia de infecciones en tejidos blandos, mediastinitis y mortalidad. El control estricto de la glucosa en estos pacientes todavía es controversial, con un estudio que sugiere una mayor mortalidad
vinculada con hipoglucemia en las personas que utilizan insulina para mantener niveles óptimos de glucosa. Se ha demostrado que la conservación de una glucosa por debajo de 200 mg/dl durante el periodo intraoperatorio reduce la mortalidad y la incidencia de infecciones. El control estricto intraoperatorio de la glucosa se ha acompañado también de una menor morbilidad cardiopulmonar y renal en pacientes diabéticos, mientras que la hiperglucemia durante el bypass cardiopulmonar se ha considerado un factor independiente de una mayor mortalidad. Los niveles intraoperatorios de glucosa deben mantenerse por debajo de 130 mg/dl; en el posoperatorio, el objetivo es preservar una glucosa menor de 110 mg/dl dentro de las primeras 3 h del posoperatorio, con cifras de 90 a 110 mg/ dl, y evitar un descenso de la glucosa por debajo de 90 mg/dl para prevenir el riesgo de hipoglucemia. Se deben realizar determinaciones de la glucemia capilar en el periodo intraoperatorio cada 30 min para ajustar la insulina; en la UCIC se deben tomar determinaciones de glucosa por lo menos cada hora hasta alcanzar los niveles objetivo (90-110 mg/dl) y posteriormente cada 2 h hasta suspender la infusión de insulina y luego cada 4 h durante la estancia en terapia intensiva (es preciso aplicar insulina de acción rápida si la concentración es mayor de 130 mg/dl); en los pacientes que desarrollan hiperglucemia se recomienda mantener glucemias de 90 a 110 mg/dl.
Recomendación clase I, nivel de evidencia A
Profilaxis de arritmias
Las taquiarritmias en las primeras 24 h del posoperatorio son poco comunes en relación con el posoperatorio tardío, ya que pueden presentarse a las 48 h, sobre todo en personas sometidas a intervenciones valvulares. La arritmia auricular más frecuente es la es la fibrilación auricular FA, que se identifica en 20% a 60% de los pacientes (aparece en 40% de los individuos sometidos a revascularización, en 35% a 40% de los tratados con operaciones valvulares y en 60% de los sujetos sometidos a ambas intervenciones). En los pacientes postrasplantados se presenta en 11% a 24%. Las bradiarritmias se han informado en 0.1% a 0.4% de los enfermos y la taquicardia ventricular en un 0.5% a 0.6%; en este último caso la mortalidad en los 30 días posteriores a la operación es mayor.
Bloqueadores β
La eficacia en la disminución de la FA posoperatoria con el uso de los bloqueadores β, solos o en combinación con otros antiarrítmicos (bloqueadores de los canales de calcio y digital), está bien demostrada. Estos fármacos deben administrarse en el perioperatorio, sobre todo en el caso de las personas intervenidas con una revascularización coronaria, si no hay contraindicación para su uso.
Recomendación clase I, nivel de evidencia A
El fármaco más utilizado en los diferentes estudios es el metoprolol; no existe una dosis específica, aunque se han prescrito dosis desde 12.5 mg cada 12 h hasta 100 mg cada 12 h.
Recomendación clase IIa, nivel de evidencia A
Amiodarona
La amiodarona se ha evaluado en numerosos estudios aleatorizados y ha demostrado una disminución de la incidencia de FA (por las vías intravenosa y oral). En un meta-análisis de 10 estudios se confirmó que la amiodarona reduce la incidencia de FA y flúter auricular (riesgo relativo, 0.64; IC 95%, 0.55 a 0.75). En un estudio doble ciego, aleatorizado y controlado, la profilaxis con amiodarona para la prevención de FA (PAPABEAR) demostró una reducción del 40% en aquellos pacientes que recibieron amiodarona (10 mg/kg/día) seis días antes de la operación en comparación con el grupo que recibió placebo.
La amiodarona es una terapéutica profiláctica apropiada para individuos con alto riesgo posoperatorio de FA y contraindicación para el uso de los bloqueadores β.
Recomendación clase IIb, nivel de evidencia A
Antagonistas del calcio y digital
Los antagonistas del calcio no han mostrado disminución de la incidencia de la FA con su uso profiláctico. En dos meta-análisis, la digital no redujo la incidencia de las taquiarritmias posoperatorias en pacientes de revascularización coronaria. Sin embargo, puede administrarse de forma conjunta con los bloqueadores β. La digoxina, al igual que el verapamilo, es de Clase IIa para el control de la frecuencia ventricular. No hay indicación para el uso profiláctico de la digital en la prevención de FA.
Recomendación clase IIb, nivel de evidencia B
Sulfato de magnesio
Se ha estudiado el empleo del magnesio como profiláctico de la FA, pero los resultaos han sido inconsistentes.
Recomendación clase IIb, nivel de evidencia B
Estatinas
Algunos protocolos sobre la administración de las estatinas en el periodo preoperatorio de una intervención cardiaca identificaron una disminución de la incidencia de isquemia/infarto y menor mortalidad. Dotani y colaboradores demostraron en un estudio retrospectivo una reducción de la mortalidad a los 60 días y un año tras la revascularización. Pan y colegas realizaron un estudio de cohorte retrospectivo que incluía a 1 663 pacientes sometidos a revascularización: 943 individuos recibieron estatinas y 920 fueron controles. Una vez realizado el ajuste en las diferencias clínicas y demográficas entre los casos y controles, se demostró una disminución del 50% de la mortalidad por todas las causas a los 30 días. Sin embargo, las publicaciones actuales no son concluyentes en cuanto al efecto benéfico del uso de las estatinas, ya que Subramaniam y colaboradores, así como Ali y Buth, no observaron una reducción de la morbimortalidad (incluidos FA e infarto al miocardio) de los pacientes tratados con revascularización.
Hay muy pocos estudios prospectivos y aleatorizados sobre el uso de las estatinas en la cirugía cardiaca; uno de los más recientes es el de Mannacio en el cual el grupo que utilizó rosuvastatina a 20 mg presentó un bajo pero significativo número de pacientes que elevaron Trop I (35% vs 65%), mioglobina (39% vs 72%) y creatina cinasa (22% vs 40%), en comparación con el grupo control.
Hindler analizó 10 estudios que incluían el consumo de estatinas en la cirugía cardiaca y demostró una disminución de 3% del riesgo de mortalidad en los sujetos que recibieron estatina (1.9% vs 3.1%).
Liakopoulos realizó un meta-análisis que incluyó a 31 000 pacientes y observó una reducción significativa de la mortalidad por todas las causas (2.2 vs 3.7%), así como de presentación de un episodio vascular cerebral (2.1 vs 2.9), no así de la presentación de infarto del miocardio e insuficiencia renal. Las dosis administradas no están estandarizadas, aunque la mínima dosis utilizada en los diferentes estudios es de 20 mg (dosis máxima, 80 mg); si se eligen estos fármacos, es mejor suministrar la dosis de 20 mg.
Los hallazgos están limitados por la naturaleza retrospectiva de los estudios y la falta de protocolización en la medicación, dosis e inicio de tratamiento, además de la estandarización de los resultados.
Recomendación clase IIa, nivel de evidencia B
Alta de la UCIC
La estancia promedio esperada para los pacientes con una evolución satisfactoria en la UCIC es de 48 a 72 h, considerando que el periodo crítico de la recuperación posoperatoria de la mayoría de estos pacientes cardiacos, una vez que abandonan el quirófano, comprende las primeras 24 a 36 h. Durante este tiempo debe restablecerse la estabilidad hemodinámica, disminuir el aporte farmacológico si el paciente lo ha requerido y, por último, retirar la vigilancia invasiva.
Retiro de la vigilancia y procedimientos invasivos
Ventilación mecánica. Por lo general se exige un mínimo de 4 h de asistencia respiratoria mecánica para garantizar una adecuada oxigenación y ventilación en aquellos sujetos que salen de quirófano aún con ventilación mecánica; la desconexión se logra en la mayor parte de los casos en las 8 a 12 h del posoperatorio.
Recomendación clase IIa, nivel de evidencia A
En la actualidad se prefiere todavía en procedimientos quirúrgicos de bajo riesgo trasladar a los pacientes con intubación orotraqueal y luego extubarlos con seguridad en la UCIC, de tal forma que se evitan así riesgos innecesarios.
Recomendación clase IIb, nivel de evidencia B
Accesos. El acceso arterial puede retirarse en cuanto se consiga la estabilidad hemodinámica y, en condiciones ideales, se retira en las primeras 12 a 24 h una vez que el paciente no depende ya de los vasopresores.
Recomendación clase I, nivel de evidencia B
Los accesos venosos periféricos y la sonda vesical se deben retirar en las primeras 24 h.
Recomendación clase I, nivel de evidencia B
Los drenajes mediastínicos los extrae el cirujano y deben obtenerse menos de 100 ml en 8 h, o 50 ml en 5 h, además de que las características de los líquidos deben ser serosas. Se solicita una radiografía de tórax en los pleurales.
Recomendación clase IIa, nivel de evidencia B
Los cables de los marcapasos epicárdicos se pueden retirar en cuanto se encuentre en ritmo estable y estabilidad hemodinámica, sin perder de vista que la falla en el sensado y la captura ocurren aproximadamente al cuarto o quinto días del posoperatorio.
Recomendación clase IIa, nivel de evidencia B
Bibliografía
Aasbo JD, Lawrence AT, Krishnan K, et al. Amiodarone prophylaxis reduces major cardiovascular morbidity and length of stay after cardiac surgery: a meta-analysis. Ann Intern Med 2005;143:327- 336.
Albert MA. HNAE: preoperative evaluation for cardiac surgery. In: Cohn LH, editor. Cardiac surgery in the adult. 3rd ed. New York: McGraw-Hill 2008;261-280.
Ali IS, Buth KJ. Preoperative statin use and outcomes following cardiac surgery. Int J Cardiol 2005;103:12-18.
Ali T, Harty R. Stress - induced ulcer bleeding in critically Ill Patients. Gastroenterol Clin N Am 2009;38:245-265.
Amar D. Prevention and management of perioperative arrhythmias in the thoracic surgical population. Anesthesiol Clin 2008;26:325- 335.
American College of Critical Care Medicine: Critical care delivery in the intensive care unit: Defining clinical roles and the best practical model. Crit Care Med 2001;29:2007-2019.
André A, DelRossi A. Hemodynamic management of patients in the first 24 hours after cardiac surgery. Crit Care Med 2005;3:29.
Aranki SF, Shaw DP, Adams DH, et al. Predictors of atrial fibrillation after coronary artery surgery: current trends and impact on hospital resources. Circulation 1996;94:390-397.
Ascione R, Reeves BC, Santo K, et al. Predictors of new malignant ventricular arrhythmias after coronary surgery. J Am Coll Cardiol 2004;43:1630-1638.
Baron JA, Sandler RS, Bresalier RS. A randomized trial of rofecoxib for the chemoprevention of colorectal adenomas. Gastroenterology 2006;131(6):1674-1682.
Bojar R. Manual of perioperative care in adult cardiac surgery. 4a ed. 2005. Blackwell publishing. p.219-258.
Bombardier C, Laine L, Reicin A, et al. Comparison of upper gastrointestinal toxicity of rofecoxib and naproxen in patients with rheumatoid arthritis. N Engl J Med 2000;343:1520-1528.
Bradley D, Creswell LL, Hogue CWJr, et al. Pharmacologic prophylaxis: American College of Chest Physicians guidelines for the prevention and management of postoperative atrial fibrillation after cardiac surgery. Chest 2005;128:39S-47S.
Braman SS, Dunn SM, Amico CA, et al. Complications of intrahospital transport in critically ill patients. Ann Int Med 1987;107:469-473.
Connolly SJ, Cybulsky I, Lamy A, et al. Beta-Blocker Length of Stay (BLOS) Study. Double-blind, placebo controlled, randomized trial of prophylactic metoprolol for reduction of hospital stay after heart surgery: the beta-Blocker Length of Stay (BLOS) trial. Am Heart J 2003;145:226-232.
Crystal E, Connolly SJ, Sleik K, et al. Interventions on prevention of postoperative atrial fibrillation in patients undergoing heart surgery: a meta-analysis. Circulation 2002;106:75-80.
Dacey LJ, Munoz JJ, Johnson ER, et al. Effect of preoperative aspirin use on mortality in coronary artery bypass grafting patients [see comment]. Ann Thorac Surg 2000;70:1986- 1990.
Davison R, Hartz R, Kaplan K, et al. Prophylaxis of supraventricular tachyarrhythmia after coronary bypass surgery with oral verapamil: a randomized, double-blind trial. Ann Thorac Surg 1985;39:336-339.
Doenst T, Wijeysundera D, Karkouti K, et al. Hyperglycemia during cardiopulmonary bypass is an independent risk factor for mortality in patients undergoing cardiac surgery. J Thorac Cardiovasc Surg 2005;130:1144-1150.
Dotani MI, Elnicki DM. Effect of preoperative statin therapy and cardiac outcomes after coronary artery bypass grafting. Am J Cardiol 2000;86:1128-1130.
Eagle KA, Guyton RA, Davidoff R, et al. ACC/AHA 2004 guideline update for coronary artery bypass graft surgery: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee to Update the 1999 Guidelines for Coronary Artery Bypass Graft Surgery). Circulation 2004;110:e340-437.
Eagle KA, Guyton RA, Davidoff R, et al. ACC/AHA 2004 guideline update for coronary artery bypass graft surgery: summary article. A report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee to Update the 1999 Guidelines for Coronary Artery Bypass Graft Surgery). J Am Coll Cardiol 2004;44:e213-310.
Edwards FH, Engelman RM, Houck P, et al. The Society of Thoracic Surgeons practice guideline series: antibiotic prophylaxis in cardiac surgery, part I: duration. Ann Thorac Surg 2006;81:397-404.
Fernández AP, Carreño R. Manejo del postoperatorio de cirugía cardiaca. Principios de urgencias, emergencias y cuidados críticos. 2005. Editorial Médica Panamericana. p.95-106
Filion K, Pilote L, Rahme E. Perioperative use of cardiac medical therapy among patients undergoing coronary artery bypass graft surgery: a systematic review. Am Heart J 2007;154:407.
Furnary A, Gao G, Grunkemeier G, et al. Continuous infusion reduces mortality in patients with diabetes undergoing coronary artery bypass grafting. J Thorac Cardiovasc Surg 2003;125:1007-1021.
Gandhi G, Nuttall G, Abel M, et al. Intensive intra-operative insulin therapy versus conventional glucose management during cardiac surgery. Ann Intern Med 2007;146:233-243.
Giri S, White CM, Dunn AB, et al. Oral amiodarone for prevention of atrial fibrillation after open heart surgery, the Atrial Fibrillation Suppression Trial (AFIST): a randomized placebo-controlled trial. Lancet 2001;357:830-836.
Goldman S, Copeland J, Moritz T, et al. Improvement in early saphenous-vein graft patency after coronary-artery bypass-surgery with antiplatelet therapy—results of a Veterans Administration Cooperative Study. Circulation 1988;77:1324-1332.
Guidelines Committee of the American College of Critical Care Medicine: Society of Critical Care Medicine and American Association of Critical Care Nurses Transfer Guidelines Task Force: Guidelines for the transfer of critically ill patients. Crit Care Med 1993;21:931-937.
Haupt M, Bekes C, Brilli R, et al. Guidelines on critical care services and personnel: recommendations based on system of categorization of three levels of care. Crit Care Med 2003;31:2677-2683.
Hindler K, Shaw AD, Samuels J, et al. Improved postoperative outcomes associated with preoperative statin therapy. Anesthesiology 2006;105:1079-1080.
Iglesias R. Cuidados perioperatorios en cirugía cardiovascular. Buenos Aires: Editorial Médica Panamericana 2000.
Insel J, Weissman C, Kemper M, et al. Cardiovascular changes during transport of critically ill and postoperative patients. Crit Care Med 1986;14:539-542.
Isakson P, Hubbard R. Chapter on nonsteroidal anti-inflammatory drugs. Anaesthetic pharmacology: physiologic principles and clinical practice. Oxford (UK): Churchill Livingstone;2004;447-448.
Jones RH, Hannan EL, Hammermeister KE, et al. Identification of preoperative variables needed for risk adjustment of short-term mortality after coronary artery bypass graft surgery. The Working Group Panel on the Cooperative CABG Database Project. J Am Coll Cardiol 1996;28:1478-1487.
Kehlet H. Acute pain control and accelerated postoperative surgical recovery. Surg Clin North Am 1999;79:431-443.
Kollef MH, Sharpless L, Vlasnik J, et al. The impact of nosocomial infections on patient outcomes following cardiac surgery. Chest 1997;112:666-675.
Konstantatos A, Silvers A, Myles P. Analgesia best practice after cardiac surgery. Anesthesiol Clin 2008;26:591-602.
Kowey PR, Taylor JE, Rials SJ, et al. Meta-analysis of the effectiveness of prophylactic drug therapy in preventing supraventricular arrhythmia early after coronary artery bypass grafting. Am J Cardiol 1992;69:963-965.
Lauer MS, Eagle KA, Buckley MJ, et al. Atrial fibrillation following coronary artery by-pass surgery. Prog Cardiovasc Dis 1989;31:367- 378.
Lecomte P, Foubert L, Nobels F, et al. Dynamic tight glycemic control during and after cardiac surgery is effective, feasible, and safe. Anesth Analg 2008;107:51-58.
Liakopoulos OJ, Choi J, Haldenwang PL, et al. Impact of preoperative statin therapy on adverse postoperative outcomes in patients undergoing cardiac surgery: a meta-analysis of over 30,000 patients. Eur Heart J 2008;29:1548-1559.
Lin P, Chang C,Ping-I Hsu S, et al. The efficacy and safety of proton pump inhibitors vs histamine-2 receptor antagonists for stress ulcer bleeding prophylaxis among critical care patients: a meta-analysis. Crit Care Med 2010; 38:1197-1205.
Magder S, Potter B, De Varennes B, et al . Fluids after cardiac surgery: a pilot study of the use of colloids versus crystalloids. Crit Care Med 2010;38:2117-2124.
Maisel WH, Rawn JD, Stevenson WG. Atrial fibrillation after cardiac surgery. Ann Intern Med 2001;135:1061-1073.
Mangano DT. Cardiovascular morbidity and CABG surgery- a perspective: epidemiology, costs, and potential therapeutic solutions. J Cardiovasc Surg 1995;10:366-368.
Mangano DT. Multicenter Study of Perioperative Ischemia Research Group. Aspirin and mortality from coronary bypass surgery. N Engl J Med 2002;347:1309 -1317.
Mannacio VA, Iorio D. Lipid-lowering effect of preoperative statin therapy on postoperative major adverse cardiac events after coronary artery bypass surgery. J Thorac Cardiovasc Surg 2007; 134:1143-1149.
Mathew JP, Parks R, Savino JS, et al. Atrial fibrillation following coronary artery bypass graft surgery: predictors, outcomes, and resource utilization: Multicenter Study of Perioperative Ischemia Research Group. JAMA 1996;276:300-306.
McIlroy Dr, Kharasch ED. Acute intravascular volume expansion with rapidly administered crystalloid or colloid in the setting of moderate hypovolemia. Anesth Analg 2003;96:1572-1577.
McQuay H, Moore A. Oral tramadol versus codeine and combination analgesics. In: McQuay H, Moore A, editors. An evidence based resource for pain relief; oral analgesic league table. Oxford (UK): Oxford University Press; 1999;140-145.
Mitchell LB, Exner DV, Wyse DG, et al. Prophylactic Oral Amiodarone for the Preventionof Arrhythmias that Begin Early After Revascularization, Valve Replacement, or Repair (PAPABEAR): A randomized controlled trial. JAMA 2005;294:3093-3100.
Myles PS, Daly D. A systematic review of the safety and effectiveness of fast-track cardiac anesthesia. Anesthesiology 2003;99:982- 987.
Nussmeier NA, Welton AA, Brown MT, et al. Complications of the cyclooxygenase-2 inhibitors parecoxib and valdecoxib after cardiac surgery. N Engl J Med 2005;352:1081-1091.
Ouattara A, Lecomte P, Le Manach Y, et al. Poor intra-operative blood glucose control is associated with a worsened hospital outcome after cardiac surgery in diabetic patients. Anesthesiology 2005;103:687-694.
Pan W, Pintar T, Anton J, et al. Statins are associated with a reduced incidence of perioperative mortality after coronary artery bypass graft surgery. Circulation 2004;110(11 Suppl 1):1145-1149.
Patel J, Stoner J, Owora A, et al. Evidence for using clopidogrel alone or in addition to aspirin in post coronary artery bypass surgery patients. Am J Cardiol 2009;103:1687-1693.
Pavri BB, O'Nunain SS, Newell JB, et al. Prevalence and prognostic significance of atrial arrhythmias after orthotopic cardiac transplantation. J Am Coll Cardiol 1995;25:1673-1680.
Perel P, Roberts I, Pearson M. Colloids versus crystalloids for fluid resuscitation in critically ill patients. Cochrane Database of Systematic Reviews 2007.
Reade MC. Temporary epicardial pacing after cardiac surgery: a practical review. Part 1: General considerations in the management of epicardial pacing. Anaesthesia 2007;62:264-271.
Remy C, Marret E, Bonnet F. Effects of paracetamol on morphine side-effects and consumption after surgery: meta-analysis of randomized controlled trials. Br J Anaesth 2004;94(4):505-513.
Roediger L, Larbuisson R, Lamy M. New approaches and old controversies to postoperative pain control following cardiac surgery. Eur J Anaesthesiol 2006;23:539-550.
Shiga T, Wajima Z, Inoue T, et al. Magnesium prophylaxis for arrhythmias after cardiac surgery: a meta-analysis of randomized controlled trials. Am J Med 2004;117:325-333.
Silverstein FE, Faich G, Goldstein JL, et al. Gastrointestinal toxicity with celecoxib vs nonsteroidal anti-inflammatory drugs for osteoarthritis and arthritis (CLASS). JAMA 2000;284:1247-1255.
Stein PD, Schunemann HJ, Dalen JE, et al. Antithrombotic therapy in patients with saphenous vein and internal mammary artery bypass grafts: the Seventh ACCP Conference on Antithombotic and Thombolytic Therapy. Chest 2004;126:600S- 608S.
Stein PD, Schunemann HJ, et al. Antithrombotic therapy in patients with saphenous vein and internal mammary artery grafts. The Seventh ACCP Conference on Antithombotic and Thombolytic Therapy. Chest 2004;126:600S-608S.
Subramaniam K, Koch CG, Bashour A, et al. Preoperative statin in-take and morbid events following isolated coronary artery bypass grafting. J Clin Anesth 2008;20:4-11.
Topol EJ, Lerman BB, Baughman KL, et al. De novo refractory ventricular tachyarrhythmias after coronary revascularization. Am J Cardiol 1986;57:57-59.
Tramer MR, Williams JE, Carroll D, et al. Comparing analgesic efficacy of nonsteroidal anti-inflammaroty drugs given by different routes in acute and chronic pain: a qualitative systematic review. Acta Anaesthesiol Scand 1998;42:71-79.
Tryba M. Sucralfate versus antacids or H2-antagonists for stress ulcer prophylaxis: a meta-analysis on efficacy and pneumonia rate. Crit Care Med 1991;19:942-949.
Van den Berghe G. Does tight blood glucose control during cardiac surgery improve patient outcome? Ann Intern Med 2007;146:307- 308.
Wake PJ, Cheng DC. Postoperative intensive care in cardiac surgery. Curr Opin Anaesthesiol 2001;14:41-45.
Wallace A, Cason B. Association of the pattern of use of perioperative ß- blockade and postoperative mortality. Anesthesiology 2010;113:794-805.
Warren J, Fromm R, Orr R, et al. Guidelines for the inter-and intrahospital transport of critically ill patients. Crit Care Med 2004;32:256-262.
Webb A, Leong S. The addition of tramadol infusion to patient controlled analgesia with morphine after abdominal surgery: a double-blinded, placebo-controlled randomized trial. Anesth Analg 2002;95:1713-1843.
Williams DB, Misbach GA, Kruse AP, et al. Oral verapamil for prophylaxis of supraventricular tachycardia after myocardial revascularization: a randomized trial. J Thorac Cardiovasc Surg 1985;90:592-596.
Yazigi A, Rahbani P, Zeid HA, et al. Postoperative oral amiodarone as prophylaxis against atrial fibrillation after coronary artery surgery. J Cardiothorac Vasc Anesth 2002;16:603-606.