Demostrar que la resección quirúrgica de la orejuela izquierda en los pacientes con enfermedad reumática mitral y fibrilación auricular persistente de larga evolución disminuye la posibilidad de embolia cerebral. Asimismo, esto también elimina la necesidad de anticoagulación oral a largo plazo.
MétodoSe estudiaron en forma observacional y prospectiva 27 pacientes adultos con enfermedad reumática mitral y fibrilación auricular persistente de larga evolución, sometidos a cirugía valvular mitral y resección quirúrgica de la orejuela izquierda. La anticoagulación oral con warfarina fue suspendida después del tercer mes postoperatorio, recibiendo solamente aspirina a largo plazo. El punto final fue la ausencia de embolia cerebral. Secundariamente, se evaluó la formación de trombos en la aurícula izquierda por ecocardiografía transtorácica postoperatoria.
ResultadosDespués del tercer mes, ningún paciente presentó embolia cerebral. Un paciente exhibió isquemia cerebral transitoria dentro de los primeros 3 meses en tratamiento con warfarina. Secundariamente, en la cirugía se encontró trombo en aurícula izquierda en 11 casos (40.7%). De estos 11, 6 (54.5%) habían tenido embolia cerebral previamente, sin encontrar significación estadística (p=0.703).
ConclusionesEste estudio muestra que pudiera haber indicios de que la orejuela izquierda pueda ser la principal fuente embolígena en la enfermedad reumática mitral, y que su resección pueda eliminar el riesgo de embolia cerebral en pacientes con enfermedad reumática mitral y fibrilación auricular persistente de larga evolución.
To demonstrate that surgical removal of the left atrial appendage in patients with rheumatic mitral valve disease and long standing persistent atrial fibrillation decreases the possibility of stroke. This also removes the need for long-term oral anticoagulation after surgery.
MethodA descriptive, prospective, observational study was conducted on 27 adult patients with rheumatic mitral valve disease and long standing persistent atrial fibrillation, who had undergone mitral valve surgery and surgical removal of the left atrial appendage. Oral anticoagulation was stopped in the third month after surgery. The end-point was the absence of embolic stroke. An assessment was also made of postoperative embolism formation in the left atrium using transthoracic echocardiography.
ResultsNone of the patients showed embolic stroke after the third post-operative month. Only one patient exhibited transient ischaemic attack on warfarin therapy within the three postoperative months. Left atrial thrombi were also found in 11 (40.7%) cases during surgery. Of these, 6 (54.5%) had had embolic stroke, with no statistical significance (P=.703).
ConclusionsThis study suggests there might be signs that the left atrial appendage may be the main source of emboli in rheumatic mitral valve disease, and its resection could eliminate the risk of stroke in patients with rheumatic mitral valve disease and long-standing persistent atrial fibrillation.
La enfermedad reumática (ER) es la forma más común de enfermedad cardiaca que afecta a la gente de estado socioeconómico bajo1. Se estima que 15.6 millones de personas en el mundo tienen ER, con aproximadamente 282,000 casos nuevos diagnosticados y 233,000 muertes por año2. Quince millones de personas sufren un accidente cerebrovascular embólico cada año3, siendo el 4.5-5.9% relacionados con ER4,5, lo cual representa cifras de 144,000-360,000 casos; y 108,000-269,000 muertes relacionadas, con 640,000 a 1.6 millones de sobrevivientes con algún déficit neurológico en grado variable2. La mortalidad por embolia cerebral (EC) debida a ER varía entre el 8.5% y el 47.4%6–7. Wang et al.8 encontraron en un revisión que la sola presencia de ER parece incrementar el riesgo de EC en pacientes con fibrilación auricular (FA). De hecho, la posibilidad de EC en pacientes con ER y FA aumenta hasta 17 veces, mientras que esta posibilidad disminuye hasta 5 veces en pacientes con FA solamente5. En un estudio realizado por Maru9, la ER se encontró en el 66.3% de los casos de EC y FA. Sin embargo, el riesgo de EC en pacientes con ER sin FA no ha sido bien estudiado. La presencia de ER aumenta la posibilidad de desarrollar FA hasta en 6 veces10. La ER mitral tiene un riesgo de tromboembolismo sistémico más elevado que cualquier forma de enfermedad valvular cardiaca adquirida. La incidencia de embolismo en la estenosis mitral reumática puede variar entre el 1.5% y el 14%. Con relación a los pacientes en FA, la presencia de embolia previa aumenta la posibilidad de un evento embólico nuevo en más de 3 veces11.
El procedimiento de Cox-Maze, diseñado para eliminar cualquier tipo de flutter y FA, incluye como parte de la técnica quirúrgica la resección de la orejuela izquierda (OI)12. Además de la restauración del ritmo sinusal y de la recuperación de la función de transporte de la AI13, gran parte del éxito de procedimiento de Maze estriba en que disminuye de forma importante las tasa de EC, hecho que pudiera estar ligado a la resección de la OI14,15. Sin embargo, dada la complejidad de esta técnica quirúrgica, existen casos de ER mitral con FA en los cuales no puede ser aplicado el procedimiento de Maze debido a factores preoperatorios que pueden aumentar la morbimortalidad operatoria (fracción de eyección del ventrículo izquierdo<0.30, enfermedad renal crónica, procedimiento quirúrgico múltiple, etc.) o a condiciones preoperatorias de la pared muscular de la AI (fibrosis, calcificación, tamaño excesivo) que la vuelven incapaz de recobrar funcionalidad de contracción adecuada.
Se sabe que el 91% de los trombos de la AI se forman dentro de la OI en la FA no-valvular. En principio, parecería no haber una diferencia significativa entre los pacientes con FA valvular y FA no-valvular con trombos en la AI y/u OI con extensión a AI (13 vs. 17%, respectivamente)16. Existe una falta de evidencia en cuanto a estudios aleatorizados para determinar si la tasa de trombogenicidad de la OI en la ER es superior, similar o inferior a la observada en la FA no-valvular. Tampoco se conoce el papel de la pared de la AI en la génesis de trombos, independientemente de la OI. En efecto, solo el 57% de los trombos en la ER se localizan en la OI, con o sin extensión a la AI16.
Este estudio analiza una serie de 27 pacientes operados por ER mitral y FA persistente de larga evolución mediante reparación valvular mitral o implante de prótesis biológica mitral asociados a la simple resección de la OI, haciendo énfasis en el manejo sin anticoagulantes orales con antivitamínicos K (AVK) (warfarina) a largo plazo. Según nuestro conocimiento, este es el primer estudio en la literatura con una cohorte de pacientes analizando estas variables en forma simultánea.
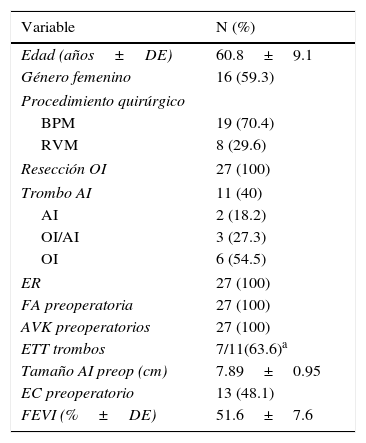
MétodosSe analizaron 27 casos operados con diagnóstico basal de ER mitral y FA persistente de larga evolución. A todos los casos, además de instalación de bioprótesis mitral o reparación mitral, se les realizó la resección quirúrgica de la OI. El estudio se realizó en forma observacional y prospectiva en nuestra institución, entre enero de 2014 y mayo de 2016. Todos los pacientes recibieron anticoagulación oral con AVK (warfarina) durante los primeros 3 meses postoperatorios (INR entre 2.5 y 3.5, nivel deseable 3), con monitoreo continuo del INR (primero semanalmente, hasta alcanzar nivel deseable por 3 tomas. Luego, cada mes. Si existió la necesidad de modificar la dosis, se realizó otro estudio de INR después de una semana ulterior al evento). Las características demográficas preoperatorias se muestran en la tabla 1.
Características preoperatorias y transoperatorias
| Variable | N (%) |
|---|---|
| Edad (años±DE) | 60.8±9.1 |
| Género femenino | 16 (59.3) |
| Procedimiento quirúrgico | |
| BPM | 19 (70.4) |
| RVM | 8 (29.6) |
| Resección OI | 27 (100) |
| Trombo AI | 11 (40) |
| AI | 2 (18.2) |
| OI/AI | 3 (27.3) |
| OI | 6 (54.5) |
| ER | 27 (100) |
| FA preoperatoria | 27 (100) |
| AVK preoperatorios | 27 (100) |
| ETT trombos | 7/11(63.6)a |
| Tamaño AI preop (cm) | 7.89±0.95 |
| EC preoperatorio | 13 (48.1) |
| FEVI (%±DE) | 51.6±7.6 |
AI: aurícula izquierda; AVK: antivitamínicos K; BPM: bioprótesis mitral; DE: desviación estándar; EC: embolia cerebral; ER: enfermedad reumática; ETT: ecocardiografía transtorácica; FA: fibrilación auricular; FEVI: fracción de expulsión del ventrículo izquierdo; OI: orejuela izquierda; RVM: reparación valvular mitral.
El seguimiento se llevó a cabo analizando a cada paciente en visita a consulta externa y mediante ecocardiografía transtorácica (ETT) en busca de trombos en AI a los 3, 6 y 12 meses postoperatorios. Un ECG de 12 derivaciones se obtuvo en cada visita postoperatoria. El punto final primario fue analizar la tasa de eventos de EC con este tipo de cirugía. Como punto final secundario, se observó la frecuencia de trombos en la AI mediante ETT.
Las variables cuantitativas se describen como medias y desviación estándar; las variables cualitativas como frecuencias y porcentajes. Para determinar la diferencia entre grupos se utilizó la t de Student en caso de resultados cuantitativos, y Chi cuadrada para los cualitativos. Se consideró un valor de p<0.05 como estadísticamente significativo. Todas las pruebas se calcularon utilizando Microsoft® Excel® 2011 para Mac, versión 14.6.2.
ResultadosNo hubo mortalidad operatoria. Se instaló una prótesis mitral biológica en 19 pacientes (70.4%), y se realizó reparación de la válvula mitral en 8 (29.6%). Todos los pacientes estaban en FA persistente de más de un año de evolución. Trece pacientes (48.1%) habían presentado EC previamente a la cirugía. El tamaño preoperatorio de la AI por ETT fue de 7.89±0.95cm. En la cirugía, se encontró trombo en AI en 11 casos (40.7%). De estos 11 casos, 6 (54.5%) habían tenido EC previamente y 5 (45.5%) no (p=0.703). El trombo estaba localizado exclusivamente en la pared posterior de la AI en 2 casos (18.2%), en la OI con extensión a la AI en 3 (27.3%), y en la OI exclusivamente en 6 (54.5%). Todos habían estado anticoagulados con warfarina previo a la cirugía. Todos los casos recibieron warfarina en los primeros 3 meses postoperatorios, con INR de 2.5-3.5 (nivel deseable, 3). En el seguimiento postoperatorio, 23 casos (85.2%) estaban en FA y 4 (14.8%) en ritmo sinusal después del tercer mes ulterior a la cirugía. Ningún caso ameritó colocación de marcapasos definitivo. Hubo solamente un caso de isquemia cerebral transitoria, dentro de los primeros 3 meses después de la cirugía, con recuperación ad integrum en las primeras 24h. La ETT no demostró trombosis en ningún caso a los 3, 6 y 12 meses. No se realizó ninguna ecocardiografía transesofágica, ya que ningún paciente presentaba OI después de la cirugía. No se llevó a cabo ningún otro estudio de gabinete neurológico, dado que solo un paciente presentó un evento transitorio, el cual fue evaluado clínicamente. En un seguimiento de 18 meses a 5 días, el 96.3% de los casos estaban libres de fenómenos tromboembólicos relacionados con la cirugía mitral. Dentro del grupo de pacientes después de los primeros 3 meses postoperatorios, sin AVK, y que están solo con un régimen de aspirina, ninguno mostró EC (tabla 2). Como datos adicionales, no se encontró relación directa entre el tamaño de la AI y la presencia de trombos al momento de la cirugía (7.29±0.8cm vs. 6.95±1.0cm, p=0.412), ni entre la presencia de EC preoperatoria y el tamaño de la AI (6.96±0.9cm vs. 7.20±0.9cm, p=0.533) (tabla 3). Tampoco se halló relación directa entre la presencia de trombo preoperatorio en la AI y EC preoperatoria (54.5 vs. 45.5%, p=0.703) (tabla 4).
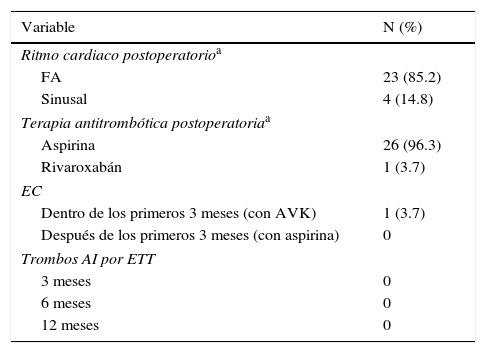
Resultados postoperatorios
| Variable | N (%) |
|---|---|
| Ritmo cardiaco postoperatorioa | |
| FA | 23 (85.2) |
| Sinusal | 4 (14.8) |
| Terapia antitrombótica postoperatoriaa | |
| Aspirina | 26 (96.3) |
| Rivaroxabán | 1 (3.7) |
| EC | |
| Dentro de los primeros 3 meses (con AVK) | 1 (3.7) |
| Después de los primeros 3 meses (con aspirina) | 0 |
| Trombos AI por ETT | |
| 3 meses | 0 |
| 6 meses | 0 |
| 12 meses | 0 |
AI: aurícula izquierda; AVK: antivitamínicos K; EC: embolia cerebral; ETT: ecocardiografía transtorácica; FA: fibrilación auricular.
Relación entre el tamaño preoperatorio de la aurícula izquierda, presencia de trombos en aurícula izquierda y embolia cerebral preoperatoria
| Variable | Tamaño preoperatorio de la AIa | Valor de p |
|---|---|---|
| Embolia cerebral | 6.96±0.9cm | 0.533 |
| Sin embolia cerebral | 7.20±0.9cm | |
| Trombos en AI | 7.29±0.8cm | 0.412 |
| Sin trombos en AI | 6.95±1.0cm |
AI: aurícula izquierda.
Relación entre embolia cerebral preoperatoria y la presencia de trombos en la aurícula izquierda
| Variable | Trombos en AI*, n (%) | Valor de p |
|---|---|---|
| EC preoperatoria | 6 (54.5) | 0.703 |
| Sin EC preoperatoria | 5 (45.5) |
AI: aurícula izquierda; EC: embolia cerebral.
Desde su aparición en los 60s las prótesis biológicas ofrecen el atractivo de no utilizar anticoagulación oral a largo plazo, en ausencia de alguna otra razón para el uso de AVK. Según las guías para la práctica clínica, la anticoagulación oral a base de AVK está indicada en los primeros 3 meses después de la cirugía en todo caso de implante de bioprótesis mitral17. La sola presencia de FA valvular, así como la ER con AI>55mm por ETT son indicaciones para anticoagulación oral con AVK a largo plazo17. Aun la FA no-valvular, con CHA2DS2VASc≥2 es una indicación para anticoagulación oral18. En nuestro estudio, todos los pacientes mostraban FA preoperatoria, y el 85.2% presentó FA después de la cirugía. Más aún, el tamaño preoperatorio de la AI fue de 7.89±0.95cm. Teóricamente, estos pacientes deberían de ser candidatos para anticoagulación oral a largo plazo. Sin embargo, debido a la eliminación de la OI, la anticoagulación oral después de los 3 meses postoperatorios fue solamente a base de aspirina (100/mg/día).
El principal argumento de este estudio surgió a partir de la observación directa de varios pacientes que, habiendo sido sometidos a un procedimiento de Cox-Maze III e implante de bioprótesis mitral por ER mitral, en un seguimiento a largo plazo mayor a un año, habían estado libres de anticoagulación oral, y exhibían nuevamente FA sin la formación de trombos ante el escrutinio de ecocardiografía transesofágica.
A pesar de que en pacientes con ER y FA la posibilidad de EC aumenta hasta 17 veces5, el papel de la eliminación de la OI como generadora de trombos no ha sido bien estudiado. Existen datos indirectos a partir de los estudios del procedimiento de Maze, el cual incluye la resección de la OI como parte de la técnica quirúrgica12. En efecto, la tasa de EC posterior al procedimiento de Maze es inferior al 0.7%13–15. Sin embargo, no ha sido bien dilucidado si este efecto es debido a la restauración del ritmo sinusal y función de transporte de las aurículas, o a la eliminación de la OI. El presente estudio ofrece indicios de que la simple eliminación de la OI en pacientes con ER mitral y FA persistente de larga evolución manejados sin anticoagulacio¿n oral a largo plazo pudiera disminuir la incidencia de EC. Hubo un caso de TIA dentro de los primeros 3 meses de la cirugía con recuperación neurológica total dentro de las primeras 24h. Se trató de un caso con reparación valvular mitral con AI de 82cm de diámetro. En un seguimiento después de los primeros 3 meses, solamente con tratamiento a base de 100mg/día de aspirina, ningún caso presentó fenómenos tromboembólicos, a pesar de observar el 87.2% de los casos en FA, y con un tamaño preoperatorio de la AI>55mm en el 88.9% de los casos.
Se ha demostrado que en pacientes sometidos a remplazo valvular mitral por ER la presencia de FA preoperatoria estuvo asociada a una reducción importante en la supervivencia (88.7%) comparada con aquellos en ritmo sinusal (96.6%, p=0.002) en un seguimiento medio a 8.6 años19. No obstante, el problema de la letalidad y efecto devastador de la FA radica en el gran número de embolias arteriales que produce. Es una enfermedad que mata en gran medida por EC. En más del 90% de los casos de FA no-valvular, la OI es el origen de los trombos resultantes en EC16. La OI ha sido llamada nuestro más letal apéndice humano20.
Sin embargo, sigue sin estudiarse la relación directa entre la FA valvular, la EC y la OI. Los estudios que han servido como piedra angular para el desarrollo de sistemas para la eliminación de la OI y disminución de EC por FA están enfocados exclusivamente en pacientes con FA no-valvular21.
Según un reporte de Blackshear et al.16, no parece haber una diferencia significativa entre los pacientes con FA valvular y FA no-valvular con trombos en la AI y/o OI con extensión a la AI (13 vs. 17%). En un estudio para determinar el grado de seguridad de la ecocardiografía en la detección de trombos, se determinó en forma intraoperatoria que en una serie de 474 pacientes con ER mitral el 22% presentaba trombos en AI. De estos, el 60.9% estaba localizado en la OI exclusivamente, el 24.7% en la OI con extensión a AI, y el 14.2% exclusivamente en AI22. De manera similar, en el presente estudio se encontraron trombos en la AI en el 40.7% de los casos, de los cuales el 54.5% estaba localizado exclusivamente en la OI, el 27.3% en la OI con extensión a AI, y el 18.2% estaba confinado a la pared posterior de la AI.
La ER mitral tiene el riesgo más elevado de tromboembolismo sistémico que cualquier forma de enfermedad valvular cardiaca adquirida. La incidencia de embolismo en la estenosis mitral reumática puede variar entre el 1.5% y el 14%11. Chiang et al.23 reportan un aumento de hasta 37.1 veces la posibilidad de EC cuando existe un trombo en AI, y de 22.4 veces con la presencia de regurgitación valvular aórtica severa. En nuestro estudio se encontró que el 48.1% de nuestros pacientes había tenido una historia previa de EC. Nosotros no hallamos ninguna relación directa entre la presencia de trombo preoperatorio en la AI y la EC preoperatoria (p=0.703), ni entre en tamaño de la AI y la presencia de trombos (p=0.412), ni tampoco entre el tamaño de la AI y la EC preoperatoria (p=0.533).
Colli et al.24 estudiaron una cohorte de 99 pacientes operados de implante de bioprótesis mitral, comparando el uso de warfarina, aspirina y sin tratamiento antitrombótico durante los primeros 90 días postoperatorios. Hubo 3 casos de EC (8.3%) en el grupo de warfarina, uno (2%) en el grupo de aspirina y uno (8.3%) en el grupo sin tratamiento. En nuestro estudio solamente tuvimos un caso de isquemia cerebral transitoria en los primeros 90 días después de la cirugía, aun con tratamiento a base de warfarina.
Durães et al.25 estudiaron una cohorte de 184 pacientes operados de implante de bioprótesis mitral o aórtica. Se analizaron 16 casos (27%) y 39 (31%) con aspirina y sin tratamiento antitrombótico, respectivamente. Solamente hubo 3 casos (5%) y 2 casos (1.3%) de EC en el grupo de mitrales con aspirina y sin tratamiento antitrombótico, respectivamente, en el primer mes postoperatorio sin diferencia estadísticamente significativa. Sin embargo, en ambos estudios, solamente se reclutaron pacientes en ritmo sinusal preoperatorio24,25.
No se encontró ningún estudio en la literatura que incluya a pacientes operados de implante de bioprótesis mitral o reparación valvular mitral por ER, en FA preoperatoria, con resección quirúrgica de la OI, sin tratamiento con AVK postoperatorio a largo plazo. Para nuestro conocimiento, este es el primer estudio que trata este rubro de pacientes con todas las variables antes mencionadas.
Una de las limitantes principales de este estudio es que no se puede considerar la comparación con otro grupo similar de pacientes dado que se tendrían que incluir pacientes con bioprótesis mitral o reparación mitral, en FA de larga evolución, con OI presente y sin tratamiento AVK después de los primeros 3 meses de la cirugía. La sola presencia de FA, con OI presente y permeable, es una indicación indiscutible para el uso de AVK a largo plazo18.
ConclusionesEste es el primer estudio que muestra que pudiera haber indicios de que la OI puede ser la principal fuente embolígena en la ER mitral, y que su resección puede eliminar el riesgo de EC en pacientes con ER mitral y FA persistente de larga evolución.
Aunque este estudio muestra indicios de que el tratamiento anticoagulante a base solamente de antiagregantes plaquetarios en este tipo de pacientes pudiera ser suficiente para evitar problemas tromboembólicos, no podemos concluir en forma contundente debido al bajo poder estadístico del mismo. Se necesita aumentar el número de pacientes y prolongar el tiempo de seguimiento de los mismos, incluso estudios multicéntricos, para poder obtener argumentos más sólidos que validen la variación en la modalidad de anticoagulación oral en estos pacientes.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónNinguna
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.