La hipertensión pulmonar tromboembólica crónica (HPTEC) se clasifica en el grupo iv del reciente Consenso de hipertensión pulmonar realizado en Niza, Francia1. Se caracteriza por trombos crónicos organizados adheridos a la capa media de la arteria pulmonar que obstruyen su luz2.
Para su diagnóstico se requiere obtener por cateterismo cardiaco derecho la presión en la arteria pulmonar (PAP) media≥25mmHg, presión capilar pulmonar≤15mmHg y la evidencia de al menos uno o más defectos de perfusión por métodos de imagen1,2.
La tromboendarterectomía pulmonar (TEnd) es el procedimiento quirúrgico de elección para resolver la HPTEC1,2, y requiere del uso de circulación extracorpórea, hipotermia y paro circulatorio3. La supervivencia a los 5 años es del 82% y a los 10 años del 75%4. La mortalidad postoperatoria se acepta que sea <5%1 para ser considerada centro de la referencia.
Las complicaciones asociadas a morbimortalidad son debidas a lesión por reperfusión, hemorragia pulmonar masiva, fallo del ventrículo derecho (VD) e hipertensión pulmonar persistente o residual3,5–9. En consecuencia, el retiro de la derivación cardiopulmonar (DCP) se torna difícil e incluso imposible, ya que lleva al fallecimiento del paciente. En estas condiciones el uso de oxigenador de membrana extracorpórea (ECMO, por sus siglas en inglés) puede utilizarse como un recurso más para el tratamiento de estos pacientes graves, ya que les proporciona soporte vital avanzado de tipo cardiopulmonar y tiempo para la recuperación del órgano6.
Actualmente hay reportes en la literatura que han sugerido el uso de ECMO venoarterial (ECMO-VA) como puente a la recuperación en aquellos pacientes que presentan estos tipos de complicaciones en el transoperatorio o posoperatorio inmediato5–9.
Presentamos en esta carta científica el primer caso exitoso informado en nuestro país con el uso de ECMO-VA para el tratamiento del fallo del VD posterior a TEnd. En la literatura internacional se ha informado su utilidad en el fallo del VD post-TEnd solo en 2 trabajos previos8,9.
Un hombre de 33 años de edad con antecedentes de sedentarismo, obesidad y tabaquismo, con cuadro clínico de 2 meses de evolución caracterizado por episodio de disnea súbita y síncope, fue referido a nuestra unidad por sospecha de tromboembolia pulmonar.
Al ingreso en urgencias se documentó saturación arterial de oxígeno (SaO2) del 85% al aire ambiente, presión arterial sistémica (PAS) (120/80mmHg) y el electrocardiograma con frecuencia cardiaca de 72 lat/min, desviación del eje a la derecha, bloqueo incompleto de rama derecha del haz de His, imagen S1 Q3 T3 y sobrecarga sistólica del ventrículo derecho.
En un ecocardiograma transtorácico se le encontró signo de McConell, dilatación de cavidades derechas, tronco y ambas ramas de la arteria pulmonar, la presión sistólica de la arteria pulmonar estimada en 61mmHg y excursión sistólica del plano del anillo tricuspídeo (TAPSE, por sus siglas en inglés) 16mm, índice de excentricidad del VD 1.9.
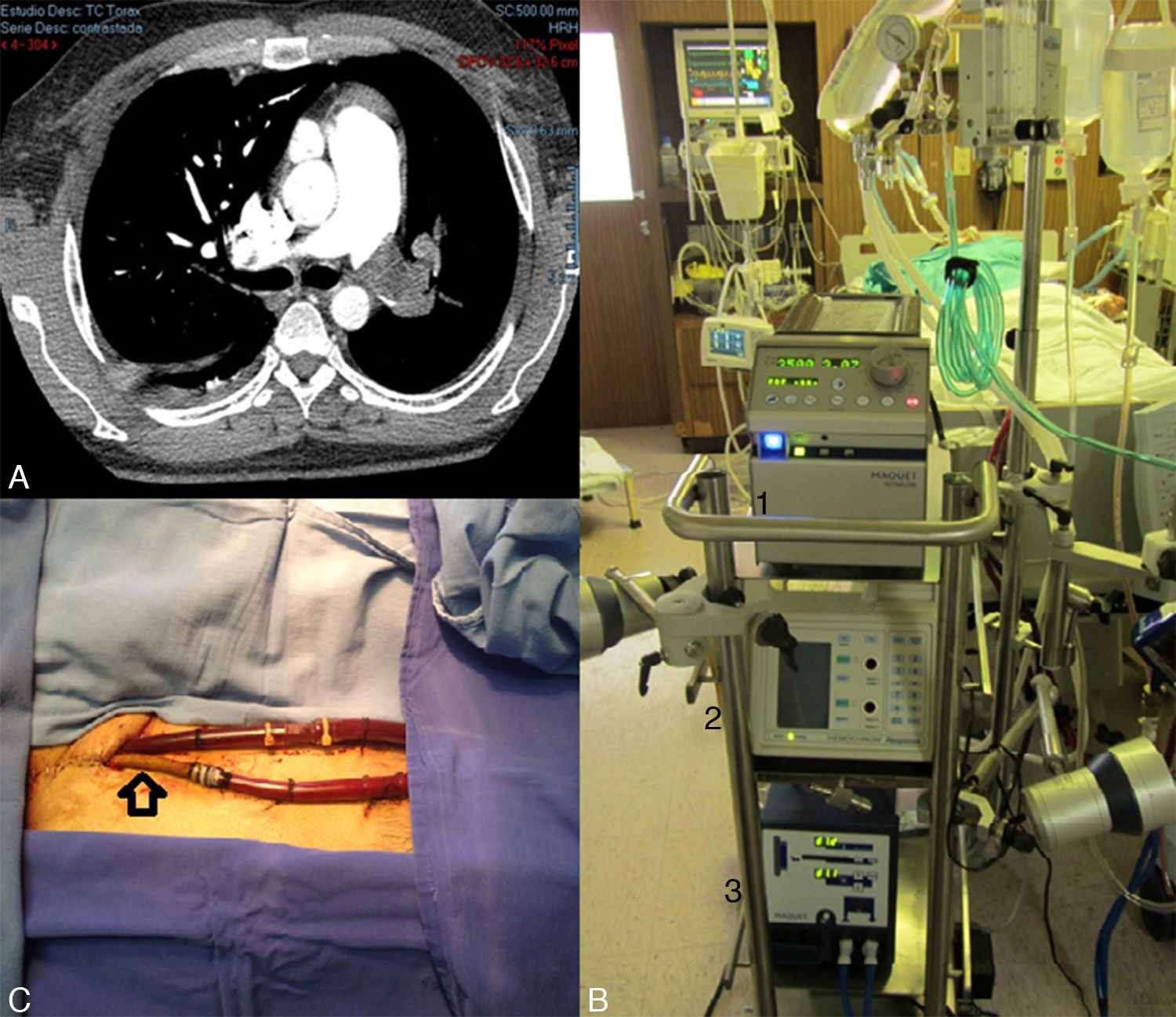
La angiotomografía de ingreso mostró datos en relación con trombosis de la rama arterial pulmonar izquierda y de ramos segmentarios superior e inferior de la arteria pulmonar derecha, derrame pleural derecho, nódulo pulmonar subpleural izquierdo en segmento posterobasal. Se decidió fibrinólisis con tenecteplase 50mg iv en dosis única. Se tuvo mejoría parcial del cuadro clínico y en la angiotomografía de control (fig. 1A) permaneció la imagen de oclusión vascular pulmonar bilateral. Por este motivo se consideró candidato a TEnd en sesión médico-quirúrgica.
A. Tomografía axial computarizada donde se aprecia obstrucción de ambas ramas de la arteria pulmonar posfibrinólisis. B. Componentes del oxigenador de membrana extracorpórea: 1. consola del oxigenador de membrana extracorpórea; 2. monitor de tiempo de coagulación; 3. intercambiador de temperatura. C. Cánulas arteriales con injerto de dacrón (flecha negra) y venosa.
En el transoperatorio se apreció cardiomegalia grado ii a expensas de cavidades derechas con dilatación del tronco y ambas ramas de la arteria pulmonar. Además se encontró un gran trombo organizado con extensión hacia las 2 ramas de la arteria pulmonar que en las arterias lobares izquierdas las obstruía en su totalidad. La red venosa colateral se estimó abundante.
El tiempo de derivación cardiopulmonar fue de 134min, pinzamiento aórtico de 76min, paro circulatorio con hipotermia profunda a 18°C de 25min y sangrado total de 625ml.
Posterior al retiro de la derivación cardiopulmonar presentó disminución de la SaO2 al 40%, aumento de la PAP a 88mmHg y dilatación del VD con disminución de la PAS a 46mmHg, por lo que se decidió en ese momento la colocación de ECMO-VA (fig. 1B) (sistema ECMO QUADROX PLS, Rotaflow —Maquet Cardiovascular, Hirrlingen, Alemania—), mediante disección de vena y arteria femorales. Se accedió a la vena mediante técnica de Seldinger y con anastomosis término-lateral e injerto de dacrón 8mm para la arteria, la cual se fijó directamente a una cánula aórtica arterial 22Fr y a la línea arterial del dispositivo (fig. 1C), con lo que mejoró su PAS media a 89mmHg, la SaO2 al 92% y la PAP media a 35mmHg posterior a la colocación del ECMO-VA.
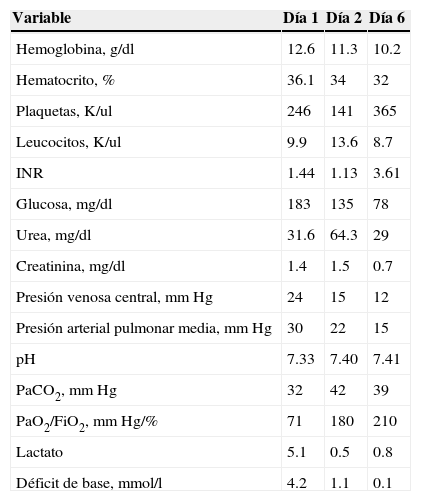
En la terapia intensiva el comportamiento fue hacia la mejoría en sus parámetros de laboratorio, hemodinámicos y del intercambio gaseoso, como se muestra en la tabla 1.
Comportamiento de los valores de laboratorio, hemodinámicos y de la gasometría arterial posteriores a la colocación del oxigenador de membrana extracorpórea
| Variable | Día 1 | Día 2 | Día 6 |
|---|---|---|---|
| Hemoglobina, g/dl | 12.6 | 11.3 | 10.2 |
| Hematocrito, % | 36.1 | 34 | 32 |
| Plaquetas, K/ul | 246 | 141 | 365 |
| Leucocitos, K/ul | 9.9 | 13.6 | 8.7 |
| INR | 1.44 | 1.13 | 3.61 |
| Glucosa, mg/dl | 183 | 135 | 78 |
| Urea, mg/dl | 31.6 | 64.3 | 29 |
| Creatinina, mg/dl | 1.4 | 1.5 | 0.7 |
| Presión venosa central, mmHg | 24 | 15 | 12 |
| Presión arterial pulmonar media, mmHg | 30 | 22 | 15 |
| pH | 7.33 | 7.40 | 7.41 |
| PaCO2, mmHg | 32 | 42 | 39 |
| PaO2/FiO2, mmHg/% | 71 | 180 | 210 |
| Lactato | 5.1 | 0.5 | 0.8 |
| Déficit de base, mmol/l | 4.2 | 1.1 | 0.1 |
INR: índice internacional ajustado; PaCO2: presión arterial de dióxido de carbono; PaO2/FiO2: relación presión arterial de oxígeno/fracción inspirada de oxígeno; pH: potencial hidrógeno.
El tratamiento con vasodilatadores pulmonares se realizó con óxido nítrico inhalado a razón de 20ppm, sildenafil 20mg vo cada 8h y milrinona iv a dosis variables.
Debido a evolución favorable se decidió el retiro del ECMO-VA 48h después de la cirugía. Así también se inició el retiro de la milrinona iv, del óxido nítrico y se sustituyó con iloprost inhalado a razón de 5mcg cada 4h.
Presentó neumonía asociada a la ventilación, la cual fue tratada con esquema a base de imipenem/amikacina. Al sexto día postoperatorio se extubó; fue egresado de la terapia intensiva y permaneció en hospitalización 15 días más.
La TEnd constituye el tratamiento de elección para la HPTEC de arterias proximales1–3. Los resultados obtenidos en este grupo de pacientes se consideran excelentes debido a mejoría en la técnica quirúrgica y cuidados postoperatorios. Debido a la supervivencia actual se considera un procedimiento curativo.
La mortalidad está relacionada con complicaciones perioperatorias como el sangrado pulmonar, la lesión pulmonar por reperfusión, la hipertensión pulmonar residual y el fallo del VD1,5–9. Su presencia puede hacer imposible el retiro de la derivación cardiopulmonar o complicar y prolongar el manejo de la ventilación mecánica.
En estas condiciones, en las que el tratamiento convencional no permite la supervivencia del paciente, el uso de ECMO es una alternativa que cada día es más aceptada1. La supervivencia al egreso hospitalario de estos pacientes, en los limitados estudios publicados con estas complicaciones, ha sido informado hasta del 57%8.
El paciente aquí presentado requirió apoyo mediante ECMO-VA secundario a fallo del VD posterior al retiro de la circulación extracorpórea. Su uso permitió la retirada de la derivación cardiopulmonar y estabilizar al paciente, como puede observarse en el comportamiento de las variables acotadas en la tabla 1.
El ECMO es una adaptación de la derivación cardiopulmonar en cirugía cardiaca y funciona como un corazón y pulmón artificial, ya que proporciona flujo sanguíneo a través de un circuito y una interface que sirve para el intercambio de dióxido de carbono y oxígeno10. El ECMO se ha categorizado por su uso como cardiaco, respiratorio o cardiorrespiratorio. De acuerdo al circuito puede ser venoarterial si el soporte es circulatorio y de intercambio gaseoso o venovenoso si solo es soporte del intercambio gaseoso el utilizado. En función del sitio de colocación puede ser central, conectado directamente al corazón o periférico a través de los vasos femorales1 (fig. 1C).
El utilizar un circuito venoarterial con respecto a uno venovenoso confiere las siguientes ventajas: 1) el circuito venoarterial permite «derivar» la circulación pulmonar, lo que reduce la presión pulmonar y evita el flujo sanguíneo a dicha zona; 2) mantiene una adecuada perfusión y oxigenación a los tejidos corporales, gracias al soporte cardiopulmonar que el dispositivo proporciona; 3) disminuye la sobrecarga al VD y la repercusión sobre la circulación sistémica por el fallo del VD; 4) debido al uso del oxigenador de membrana es posible también tratar la lesión por reperfusión pulmonar y la relacionada con la ventilación mecánica.
A manera de comentario final, en el fallo del VD visto en el postoperatorio de TEnd pulmonar el ECMO-VA puede ser utilizado para la retirada de la derivación cardiopulmonar.
FinanciaciónNo se recibió patrocinio de ningún tipo para llevar a cabo este artículo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.