Introducción
Los opiáceos representan la mejor arma terapéutica para el control del dolor oncológico crónico. Aproximadamente el 90% de los pacientes afectados con cáncer en fase terminal van a precisar de los opiáceos mayores para el alivio de su dolor. El arsenal analgésico opiáceo está constituido por los opiáceos efectivos para el control del dolor leve-moderado (denominados opiáceos débiles o menores), y los opiáceos efectivos para el control del dolor intenso (denominados opiáceos mayores).
En el presente artículo se describirá el uso de opiáceos menores y mayores en el control del dolor oncológico crónico.
Opiáceos menores1-7
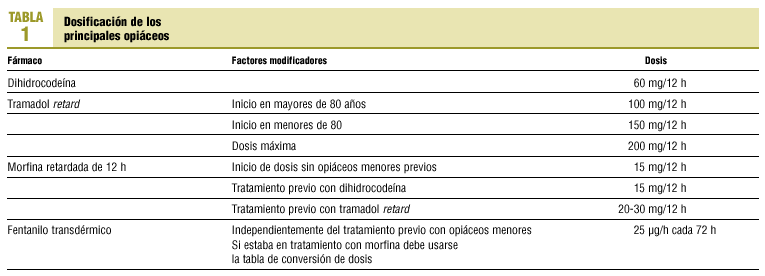
Los opiáceos menores u opioides eficaces en el control del dolor leve-moderado representan el segundo nivel de la escalera analgésica de la Organización Mundial de la Salud. Dentro de ellos destacan por su extendido uso la codeína, dihidrocodeína y el tramadol, cuyas dosis se describen en la tabla 1. El dextropropoxifeno presenta menor eficacia analgésica que los anteriores, por lo que no es de uso extendido en los cuidados paliativos. No existen diferencias de eficacia en el control del dolor entre la codeína y la dihidrocodeína. El tramadol es más eficaz como analgésico que los anteriores. La codeína y dihidrocodeína ocasionan mayor grado de estreñimiento que el tramadol, aunque éste también puede provocarlo.
Existen en el mercado asociaciones de aintiinflamatorios no esteroides (AINE) y codeína (especialmente paracetamol y codeína) a las que se puede recurrir cuando los
AINE por sí solos no son eficaces. Debe tenerse en cuenta, no obstante, que las dosis de cada fármaco en las asociaciones farmacéuticas disponibles son bajas (500 mg de paracetamol con 15 o 30 mg de codeína).
El tramadol es un opiáceo con características especiales que resulta eficaz para el control del dolor leve-moderado. Puede ser utilizado en formulaciones de liberación rápida o retardada a dosis de hasta 400 mg/día. Si no se obtiene respuesta, está indicado cambiar el fármaco por un opiáceo mayor. Al inicio del tratamiento, especialmente en personas mayores, puede provocar vómitos (evitables y tratables con antieméticos) o somnolencia transitoria.
Los incrementos paulatinos de dosis hasta el control del dolor se realizarán cada 48 h con dihidrocodeína, y tramadol retard, y cada 24 h con codeína y tramadol de liberación rápida. El control completo del dolor con la dihidrocodeína y el tramadol retard también se apoya en el uso de dosis adicionales de analgésicos (30-60 mg de codeína cuando se usa la dihidrocodeína o 50 mg de tramadol de liberación rápida) para el control del dolor irruptivo.
Cuando con los opiáceos menores no se consigue un control óptimo del dolor (ausencia completa del mismo), deberían utilizarse los opiáceos mayores. Para realizar el cambio de opiáceo han de tenerse presentes las dosis equianalgésicas existentes entre ellos (en la tabla 1 se describen los aspectos prácticos del cambio de opiáceo menor a mayor). El cambio se realiza suspendiendo el opiáceo previo e introduciendo el nuevo en la siguiente dosis. En el caso de iniciar un tratamiento con fentanilo transdérmico, dado el tiempo que tarda en actuar, éste se introducirá independientemente del momento en que el paciente haya ingerido el opiáceo menor previo.
Opiáceos mayores
Los opiáceos mayores comercializados en España son la morfina (para administración parenteral, oral de acción rápida [MAR] o de liberación sostenida de 12 h [MAS]), el fentanilo transdérmico (FTD) y la metadona (para administración oral y parenteral). Recientemente se ha comercializado una morfina de liberación sostenida cuyo efecto dura 24 h. Puede ser útil en el tratamiento de dolores adecuadamente controlados durante largo tiempo con dosis no muy altas de MAP. Está en proceso de comercialización una formulación transoral de fentanilo de actuación rápida, especialmente indicada para el tratamiento del dolor irruptivo o incidental.
El uso prolongado de la metadona puede favorecer su acumulación, con riesgo de toxicidad (en relación con una farmacocinética variable de sujeto a sujeto), por lo que no está recomendado su uso generalizado. De hecho, su empleo debería estar restringido a unidades especializadas con adecuada experiencia.
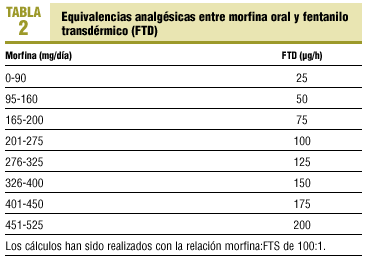
En general, la morfina oral y el fentanilo transdérmico son igual de eficaces en el control del dolor, por lo que la selección de uno u otro dependerá de otras razones como la dificultad para la ingesta oral o el coste del fármaco. En ocasiones el cambio de morfina oral a fentanilo transdérmico puede mejorar una situación de estreñimiento pertinaz que no responde adecuadamente a laxantes. Una contraindicación relativa para el uso del FTD es la presencia de un dolor intenso no controlado, ya que el inicio de acción del fentanilo transdérmico se presenta 12-18 h tras su administración, por lo que la consecución de la analgesia puede retrasarse más allá de lo deseado para un dolor intenso. La MAS puede permitir el conseguir de forma más rápida la analgesia deseada. La decisión posterior de cambiar o no de opiáceo depende de los deseos y situación del paciente. No debe olvidarse que durante el cambio de morfina a FTD puede producirse un descontrol pasajero del dolor hasta que el FTD sea efectivo, por lo que es preciso educar al paciente en el uso de dosis extras de morfina de liberación rápida para el control del dolor. En la tabla 2 se describen las dosis de conversión entre MAS y FTD. No obstante, como aproximación práctica, la cuantía del dispositivo de FTD (25, 50, 75 µg/h, etc.) se obtiene dividiendo por 2 la dosis total diaria de MAS.
Otros opiáceos mayores como la pentazocina o la buprenorfina no tienen un papel definido en el tratamiento del dolor oncológico. La presencia de techo analgésico para los dos fármacos y la elevada incidencia de efectos disfóricos con la pentazocina son circunstancias que limitan su eficacia como analgésicos de uso prolongado.
El problema del uso de la morfina:
mitos sobre sus efectos2-4,6-12
Los mitos erróneos sobre los efectos de la morfina (tabla 3) han sido reconocidos por la Organización Mundial de la Salud como uno de los principales problemas que presentan los profesionales a la hora de tratar adecuadamente el dolor oncológico. Derivado de ello se considera que el dolor oncológico está inadecuadamente tratado, por lo que muchos pacientes lo siguen padeciendo de forma injustificada.
El uso de la morfina, o del FTD, debe iniciarse cuando el dolor no sea controlable con los analgésicos de primera o segunda líneas. No existe el riesgo de desarrollo de tolerancia que haga que la morfina, o el fentanilo, lleguen a ser ineficaces por un uso prematuro. El hecho de que los opiáceos mayores no presenten techo analgésico hace que todo incremento de dosis comporte a su vez un incremento de la analgesia, por lo que retrasar su uso para evitar una situación de «acostumbramiento» o de «pérdida de efecto por su uso prolongado» no está justificado. La necesidad de incrementar las dosis de morfina o de fentanilo transdérmico obedece, principalmente, a un incremento de los estímulos dolorosos provocados por el crecimiento del tumor.
Los opiáceos, adecuadamente utilizados, no provocan depresión respiratoria, y no existe una mayor susceptibilidad en pacientes afectados por cáncer de pulmón o patología pulmonar crónica. La tolerancia a la depresión respiratoria se instaura rápidamente, por lo que no existe el riesgo de acortar la vida del paciente a causa de incrementar los trastornos respiratorios previos o del desarrollo de los mismos.
El efecto de la morfina y del FTD es analgésico. No cabe esperar efectos disfóricos durante su uso prolongado. La aparición de dichos efectos (como alucinaciones o alteraciones del comportamiento) debe inducir a la búsqueda de otras complicaciones como trastornos metabólicos o afectación tumoral del sistema nervioso central. Al inicio del tratamiento puede observarse cierto grado de somnolencia transitoria; si fuese intensa, deberían disminuirse las dosis con un incremento paulatino posterior. La persistencia de la somnolencia obliga a descartar las complicaciones previamente comentadas antes de considerar a los opiáceos como agentes causales.
El desarrollo de adicción no debería considerarse un problema en el uso de los opiáceos. La evolución continua del cáncer hace prácticamente imposible el poder prescindir de los opiáceos sin correr el riesgo de introducir al paciente en una situación de sufrimiento elevado secundario a su dolor o disnea, si ésta hubiese sido la indicación del opiáceo.
El uso de los opiáceos: aspectos prácticos1-7,13-15
Dosis iniciales e incrementos de dosis
Las dosis iniciales de los opiáceos mayores se describen en la tabla 1. Los incrementos paulatinos de dosis hasta el control del dolor se realizarán cada 48 h con morfina de liberación retardada. La dosis inicial de FTD será modificada a los 6 días de iniciado el tratamiento (después de haber ensayado dos cursos de tratamiento administración de dos dispositivos transdérmicos para permitir la estabilización del fármaco) y posteriormente cada 72 h si se precisa. Esta recomendación procede de lo observado en la práctica, sin que exista un consenso al respecto entre todos los autores.
Una vez que el paciente está en tratamiento prolongado con MAP, la dosis de ésta se incrementa en un 50% de la dosis total diaria si persiste la situación de dolor y el FTD en 25 µg/h.
Control de los efectos adversos
El inicio del tratamiento con tramadol, MAP o FTD puede provocar vómitos pasajeros. Éstos se evitan administrando metoclopramida oral (10-20 mg * 3) o 2,5 mg de haloperidol oral en dosis diaria durante las primeras 48-72 h de tratamiento. La profilaxis de los vómitos está especialmente recomendada en pacientes mayores de 75 años. El uso continuado de opiáceos mayores provoca estreñimiento, el cual debe ser controlado enérgicamente mediante el uso profiláctico de laxantes.
En el inicio del tratamiento puede aparecer una situación de somnolencia transitoria. Si ésta persiste deben reducirse las dosis durante unos días en un 30-50%, para incrementarlas posteriormente según la respuesta. Si la somnolencia persistiese, debería probarse un cambio de opiáceo (MAS a FTD, o viceversa). Si con la MAS y el FTD persistiese la somnolencia y ésta alterase la calidad de vida del paciente, habría que remitirlo a una unidad especializada para iniciar tratamiento con metadona, o en su defecto, instaurar tratamiento con dosis bajas de metilfenidato (5 mg en el desayuno y almuerzo).
En situaciones de fiebre alta y sostenida debe vigilarse la posibilidad de intoxicación por FTD, pues se incrementa la abosorción. Ante la duda, es aconsejable descender en 25 µg/h la dosis de FTD.
Uso de dosis extras de opiáceos
Su utilización persigue controlar episodios de dolor no aliviados con el tratamiento basal. Las dos situaciones posibles son:
1. Paciente tratado con morfina de liberación sostenida de 12 h. Se usarán comprimidos de morfina de liberación rápida en una dosis equivalente al 10% de la dosis total diaria de MAS.
2. Paciente tratado con fentanilo transdérmico: las dosis de rescate de MAR para pacientes con 25 µg/h de FTD será de 10-15 mg; con 50 µg/h de FTD, de 20-30 mg, y con 75 µg/h de FTD, de 40-50 mg.
La dosis de rescate puede repetirse a los 60-90 min si no se ha obtenido el alivio completo del episodio de dolor. La necesidad de 3-4 dosis de rescate/24 h debe inducir a incrementar la dosis basal de opiáceos. La educación del paciente en el uso correcto de las dosis extras antes de la
realización de las actividades causantes de dolor evita la aparición del dolor incidental.
Uso de los fármacos: información a los pacientes y familiares
Los comprimidos de MAS no pueden triturarse, deben ingerirse enteros para permitir que funcione el sistema de liberación sostenida. La zona de colocación cutánea de los dispositivos de FTD (parches) debe cambiarse junto con el cambio del parche. El parche no debe colocarse en zonas pilosas ni rasuradas recientemente. El parche de FTD debe eliminarse por un sistema adecuado, ya que en él persisten pequeñas dosis de opiáceos no liberados. Los comprimidos de MAR pueden ingerirse enteros o triturados; éstos son de 10 y 20 mg ranurados.
Criterios para la derivación de pacientes a unidades de cuidados paliativos
Los criterios están descritos en la tabla 4. En general corresponden a situaciones de dolor no controlado con dosis elevadas de opiáceos o persistencia de efectos secundarios presumiblemente derivadas del uso de opiáceos mayores.