Valorar la eficacia y la seguridad de la insulina de administración oral/bucal.
DiseñoRevisión sistemática.
Fuentes de datosBases de datos referenciales MEDLINE, EMBASE, Scopus, Current Contents, Web of Science, Cochrane Library, Agencia Europea del Medicamento, Food and Drug Administration, Red Internacional de Agencias de Evaluación de Tecnologías, Red Europea de Detección Precoz de Tecnologías (EuroScan) y varios registros de investigación.
Selección de los estudiosSe recuperaron 2 ensayos clínicos. Se excluyeron aquellos estudios que no comparaban la insulina oral/bucal con el tratamiento estándar con insulina inyectada en términos de parámetros clínicos en la población con diabetes.
Extracción de datosLectura crítica según la metodología propuesta por el programa CASPe y la escala de Jadad.
ResultadosLa insulina bucal produjo una reducción mayor y más temprana en la glucemia posprandial medida a los 30min en el grupo intervención frente al grupo control (reducción de 55mg/dl) y un pico de insulinemia mayor y más rápido (98 frente a 65μU/ml). Respecto a la insulina oral, los niveles de glucemia posprandial fueron equivalentes a los obtenidos con la insulina inyectada, y la concentración máxima de insulina fue superior (110±130 frente a 96,3±69,7μU/ml).
ConclusionesLa insulina oral/bucal presentó, al menos, resultados equivalentes al tratamiento estándar. No obstante, los estudios presentaron problemas metodológicos de validez interna y externa.
Se precisan estudios de mayor duración para evaluar la eficacia y la seguridad a largo plazo.
To evaluate the efficacy and safety of administering oral/buccal insulin.
DesignSystematic review.
Data sourcesReference databases, MEDLINE, EMBASE, Scopus, Current Contents, Web of Science, and Cochrane Library, European Drugs Agency, Food and Drug Administration, International Network of Technological Evaluation Agencies, European Network for New and Emerging Technologies (EuroScan), and gravel research registers.
Selection of the studiesTwo clinical trials were found. Those studies that did not compare oral/buccal insulin with the standard treatment with injected insulin in terms of clinical parameters in a population with diabetes were excluded.
Extraction of dataCritical reading according to the method proposed by the CASPe program and the Jadad scale.
ResultsBuccal insulin produced a greater and earlier reduction in post-prandial blood glucose at 30min in the intervention group compared to the control group (decrease of 55mg/dl) and a higher and more rapid peak blood insulin (98 compared to 65μU/mL). The postprandial levels with oral insulin were similar to those obtained with injected insulin, and had a higher maximum insulin concentration (110±130 vs. 96.3±69.7μU/mL).
ConclusionsOral/buccal insulin gives, at least, results similar to the standard treatment. However, the studies had methodological problems of internal and external validity. Studies of longer duration are required to evaluate the long-term efficacy and safety.
El uso de insulina inyectada constituye una necesidad para pacientes con diabetes tipo 1 (DM1) y con diabetes tipo 2 (DM2) mal controlada. Las inyecciones diarias de insulina pueden causar, además de malestar local en el sitio de inoculación, un riesgo potencial por el uso de agujas, así como un obstáculo social capaz de mermar la calidad de vida del paciente1. Una concentración de insulina periférica excesivamente elevada se asocia además con enfermedad coronaria, hipertensión, dislipidemia y ganancia de peso2,3.
Presentaciones no invasivas, como la insulina inhalada, no han cumplido hasta el momento los estándares mínimos de seguridad y de eficacia requeridos. Por esto, la búsqueda de formulaciones que reproduzcan al máximo el efecto de la insulina nativa y que puedan emplearse de forma no invasiva sigue siendo prioritaria.
La insulina bucal y la insulina oral presentan diferentes mecanismos de absorción. La primera pasa directamente al torrente circulatorio a través de la mucosa de las mejillas, mientras que la oral pasa a la circulación portal a través del aparato digestivo, por lo que se asemeja más al patrón fisiológico de la insulina nativa. El resto de las características farmacodinámicas de ambas presentaciones son similares4,5. Los beneficios de ambas vías de administración están aún por determinarse, aunque la insulina bucal ya se está comercializando en algunos países como India y Ecuador5. Por esto, se planteó la realización de una revisión sistemática con anterioridad a su posible aprobación por la Food and Drug Administration y la Agencia Europea del Medicamento, para evaluar la eficacia y la seguridad de la insulina de administración oral/bucal.
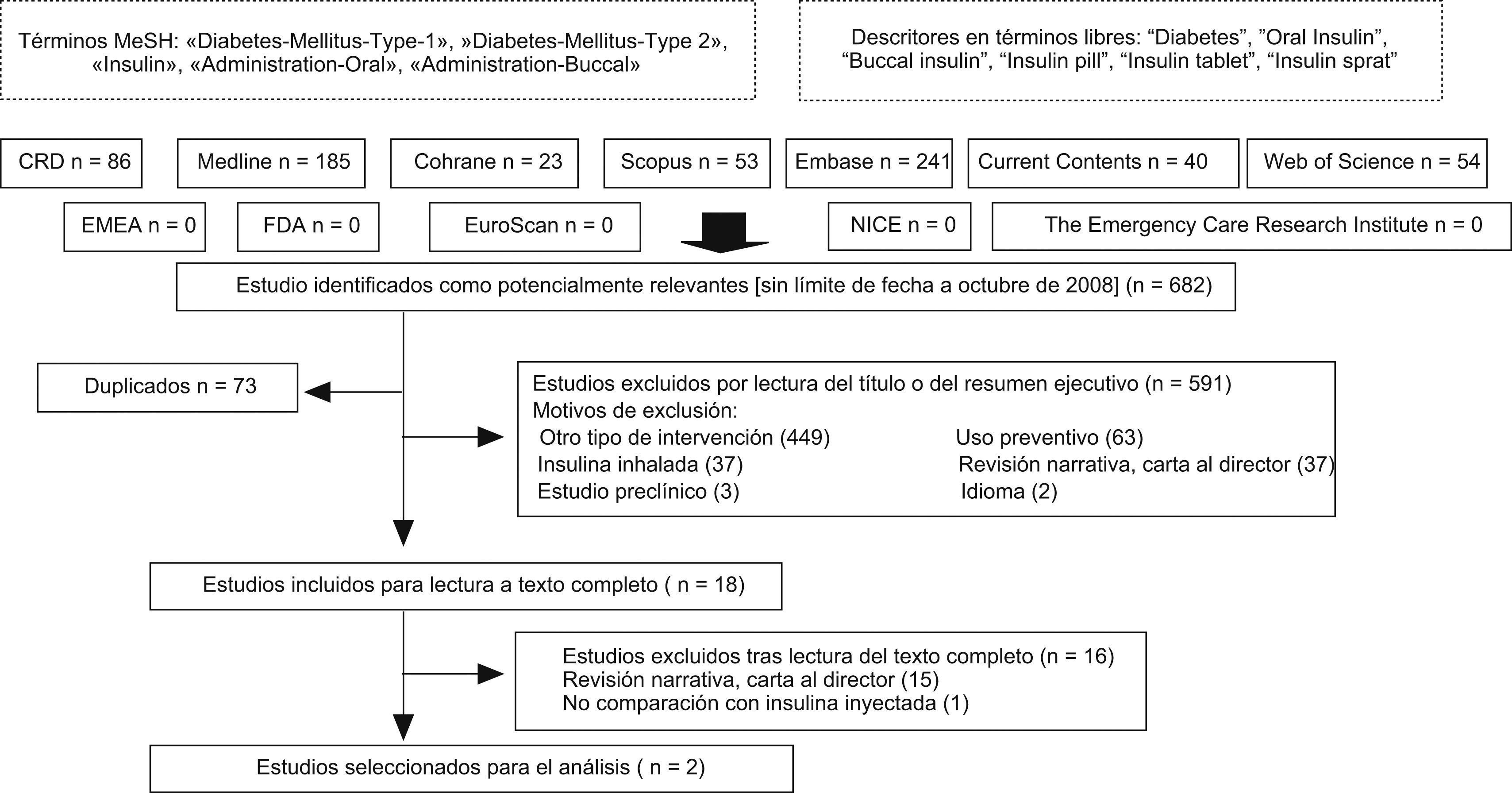
MetodologíaSe realizó una revisión sistemática de la literatura médica que incluyera ensayos clínicos en los que se comparara la insulina oral/bucal con el tratamiento estándar. La búsqueda se realizó en las bases de datos referenciales principales, en registros de ensayos clínicos y en otras fuentes bibliográficas (tabla 1). Además, se realizó una revisión manual en los sitios web de instituciones nacionales e internacionales, tanto generales (Ministerio de Sanidad y Consumo, la Organización Mundial de la Salud o los Centers for Disease Control) como específicas sobre diabetes, así como una revisión secundaria a partir de las referencias bibliográficas de los artículos recuperados.
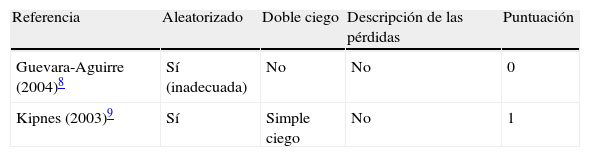
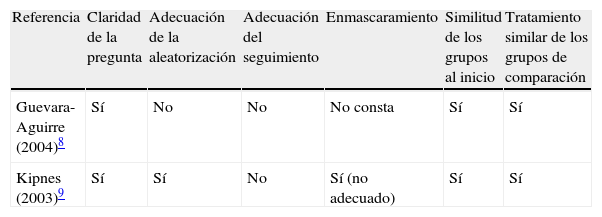
Calidad de los estudios incluidos en la revisión según la escala de Jadad*
| Referencia | Aleatorizado | Doble ciego | Descripción de las pérdidas | Puntuación |
| Guevara-Aguirre (2004)8 | Sí (inadecuada) | No | No | 0 |
| Kipnes (2003)9 | Sí | Simple ciego | No | 1 |
*Rango: 0–5; mala calidad: 0–2. Un punto por cada sí y 0 puntos por cada no. Con un punto adicional se describe el método de aleatorización y si éste es adecuado o se describe el método de enmascaramiento y si éste es adecuado.
Se seleccionaron aquellos ensayos clínicos aleatorizados en los que se comparara la eficacia de la insulina de administración oral/bucal para el tratamiento de la DM1 o de la DM2 frente al tratamiento con insulina inyectada mediante medidas relativas al control metabólico o a la satisfacción, adherencia al tratamiento y calidad de vida de los pacientes. Se contempló la calidad de vida como criterio de inclusión ya que, aun presentando resultados médicos semejantes, esta nueva aplicación podría resultar ventajosa a este respecto. Se excluyeron los estudios no originales, los resúmenes ejecutivos, los estudios sin grupo control, los trabajos que no aportaran resultados clínicos y los estudios preclínicos realizados sobre animales in vivo o ex vitro.
Dos investigadores (AL y ZH) realizaron la extracción de datos de forma independiente, y las discrepancias se solucionaron por consenso. Se realizó una lectura crítica según la metodología propuesta por el programa CASPe6 y la escala Jadad7 (tabla 2).
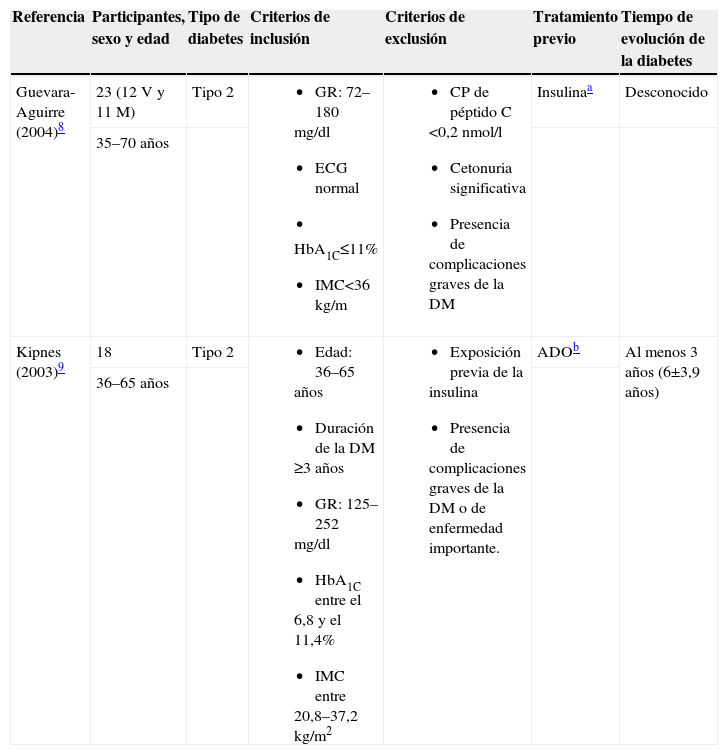
ResultadosSe recuperaron 2 ensayos clínicos de diseño cruzado en fase 8,9. Los 2 se realizaron con población diagnosticada de diabetes tipo 2, incluyendo entre 18 y 23 pacientes, tanto varones como mujeres caucasianos o hispanos, con edades comprendidas alrededor de 35–70 años8,9. Para una descripción más detallada de las poblaciones de estudio ver la tabla 3. Un estudio empleó la insulina bucal en spray (Oralin®) frente a la insulina ultra rápida inyectada8 más placebo, mientras que el segundo comparaba la insulina de administración oral HIM2® tanto con una insulina subcutánea rápida como con placebo9 en pacientes diabéticos sin exposición previa a insulina. En ambos ensayos se tomaron muestras sanguíneas previas al inicio del estudio para testar el control glucémico de los pacientes, y en el estudio de Guevara-Aguirre et al (2004)8 se realizó un entrenamiento previo de los pacientes en el uso del spray bucal. Ambos ensayos tenían diseño cruzado; en el primero se administró de manera aleatorizada a los pacientes en ayunas en 2 ocasiones (con un intervalo temporal de 3 a 7 días) insulina subcutánea más placebo en spray o insulina en spray bucal, y 10min más tarde tomaban un desayuno estándar. En el ensayo de Kipnes et al (2003)9, tras suspenderse el tratamiento con antidiabéticos orales (ADO) durante al menos 5 vidas medias, se administró a cada paciente en 3 días diferentes (y tras ayuno de al menos 8 h) insulina oral (dosis de 0,375, 0,5 o 1,0), insulina subcutánea o placebo oral, y se suministró a los pacientes una comida estándar 30 min más tarde.
Características de las poblaciones de estudio
| Referencia | Participantes, sexo y edad | Tipo de diabetes | Criterios de inclusión | Criterios de exclusión | Tratamiento previo | Tiempo de evolución de la diabetes |
| Guevara-Aguirre (2004)8 | 23 (12V y 11M) | Tipo 2 |
|
| Insulinaa | Desconocido |
| 35–70 años | ||||||
| Kipnes (2003)9 | 18 | Tipo 2 |
|
| ADOb | Al menos 3 años (6±3,9 años) |
| 36–65 años |
ADO: antidiabéticos orales; CP: concentración plasmática; DM: diabetes mellitus; ECG: electrocardiograma; GR: glucosa rápida; HbA1C: hemoglobina glucosilada; IMC: índice de masa corporal; M: mujeres; V: varones.
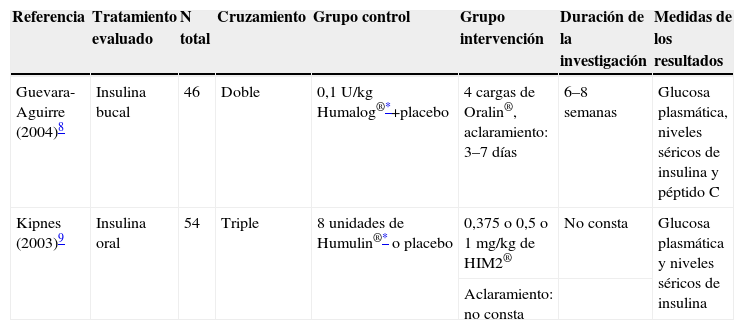
Las características de los estudios se resumen en la tabla 4.
Características de los estudios recuperados
| Referencia | Tratamiento evaluado | N total | Cruzamiento | Grupo control | Grupo intervención | Duración de la investigación | Medidas de los resultados |
| Guevara-Aguirre (2004)8 | Insulina bucal | 46 | Doble | 0,1U/kg Humalog®*+placebo | 4 cargas de Oralin®, aclaramiento: 3–7 días | 6–8 semanas | Glucosa plasmática, niveles séricos de insulina y péptido C |
| Kipnes (2003)9 | Insulina oral | 54 | Triple | 8 unidades de Humulin®* o placebo | 0,375 o 0,5 o 1mg/kg de HIM2® | No consta | Glucosa plasmática y niveles séricos de insulina |
| Aclaramiento: no consta |
ADO: metformina+gliburide.
H: hombres; M: mujeres; N: número de intervenciones.
La principal medida de resultado para el grupo intervención y control fue el control glucémico medido como glucemia posprandial, insulinemia y péptido C de manera inmediata tras la intervención y cada 10–30min, y hasta los 240min siguientes a la toma del medicamento o el placebo. Para la medición se emplearon distintas técnicas: Guevara-Aguirre et al (2004)8 determinaron los niveles de glucosa posprandial mediante el método de la hexocinasa, mientras que Kipnes et al (2003)9 emplearon el método de la glucosa oxidasa. Los niveles de insulina se determinan en los 3 estudios mediante radioinmunoanálisis (RIA). El RIA también se empleó para determinar los niveles de péptido C8.
Si se entiende por control glucémico todas aquellas medidas que facilitan mantener los valores de glucemia dentro de los límites de la normalidad, las medidas de resultado empleadas en los 2 ensayos seleccionados sólo permitieron valorar de manera limitada el control glucémico a muy corto plazo por limitarse el período de seguimiento al tiempo que dura la investigación, así como por tener diseños cruzados. A pesar de no recogerse todas las variables que a priori se consideraron óptimas y deseables, se seleccionaron los estudios por ser los únicos que, cumpliendo el resto de criterios de inclusión, aportaban información sobre el uso terapéutico de esta tecnología emergente.
Glucemia posprandialHubo mayor reducción de las concentraciones de glucosa posprandial con Oralin® frente a la insulina más placebo8 (diferencias que oscilaron entre −55 y −38mg/dl a los 30min de la ingesta). Se observaron cambios equivalentes entre ambos grupos cuando se comparaba la insulina oral con la insulina inyectada9.
Niveles de insulina y péptido CLa concentración sérica de insulina fue mayor y se alcanzó más rápidamente (perfil similar a la insulina nativa) con la insulina en spray que con el tratamiento con insulina más placebo (picos de concentración máxima entre 98±86μU/ml frente a 65μU/ml). La reducción del péptido C fue también significativamente mayor entre los pacientes del grupo intervención8.
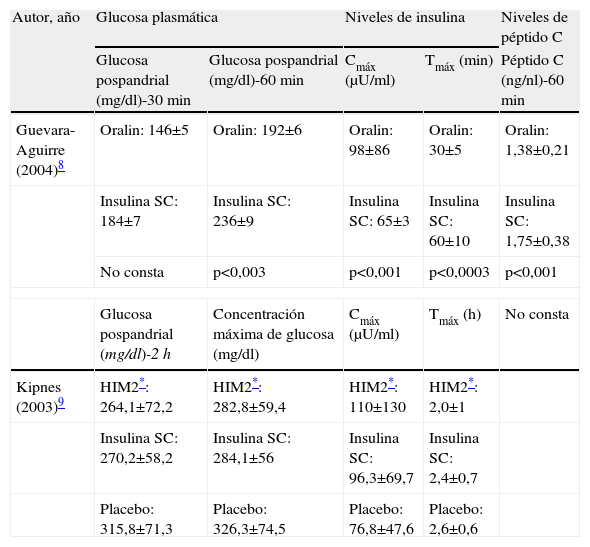
El HIM2® en dosis de 0,5 o 1 mg/kg produjo una concentración máxima de insulina (110±130μU/ml) superior a la generada con 8 unidades de insulina subcutánea (96,3±69,7μU/ml)9. Los resultados detallados se muestran en la tabla 5.
Resultados de los ensayos clínicos seleccionados
| Autor, año | Glucosa plasmática | Niveles de insulina | Niveles de péptido C | ||
| Glucosa pospandrial (mg/dl)-30min | Glucosa pospandrial (mg/dl)-60min | Cmáx (μU/ml) | Tmáx (min) | Péptido C (ng/nl)-60min | |
| Guevara-Aguirre (2004)8 | Oralin: 146±5 | Oralin: 192±6 | Oralin: 98±86 | Oralin: 30±5 | Oralin: 1,38±0,21 |
| Insulina SC: 184±7 | Insulina SC: 236±9 | Insulina SC: 65±3 | Insulina SC: 60±10 | Insulina SC: 1,75±0,38 | |
| No consta | p<0,003 | p<0,001 | p<0,0003 | p<0,001 | |
| Glucosa pospandrial (mg/dl)-2h | Concentración máxima de glucosa (mg/dl) | Cmáx (μU/ml) | Tmáx (h) | No consta | |
| Kipnes (2003)9 | HIM2*: 264,1±72,2 | HIM2*: 282,8±59,4 | HIM2*: 110±130 | HIM2*: 2,0±1 | |
| Insulina SC: 270,2±58,2 | Insulina SC: 284,1±56 | Insulina SC: 96,3±69,7 | Insulina SC: 2,4±0,7 | ||
| Placebo: 315,8±71,3 | Placebo: 326,3±74,5 | Placebo: 76,8±47,6 | Placebo: 2,6±0,6 | ||
ADO: metformina+gliburide.
Cmáx: concentración máxima de insulina circulante; SC: subcutánea; Tmáx: tiempo necesario para alcanzar la concentración máxima de insulina circulante.
Los efectos adversos se registraron en los 2 ensayos durante el tiempo de la intervención. La mayoría fueron leves o moderados, sin relación aparente con el medicamento en investigación, comparables en pacientes que tomaron insulina inyectada e insulina oral/bucal.
En el estudio de Kipnes et al (2003)9, el 72,2% de los pacientes experimentó algún efecto adverso leve, el dolor de cabeza (33,3%) y la anemia (16,7%) fueron los más comunes, sin relación aparente con el medicamento en investigación. Uno de los participantes presentó efectos adversos moderados (dolor de cabeza, nerviosismo y mareo), posiblemente relacionados con la administración de la insulina oral HIM2®.
DiscusiónSegún se deriva de los resultados expuestos, la reducción de la glucemia posprandial fue mayor y más rápida con la insulina bucal que con el tratamiento estándar o al menos equivalente en el caso de la insulina oral. No obstante, la lectura no sería completa sin el análisis de las limitaciones de los estudios incluidos en esta revisión. Los estudios fueron de baja calidad, según la escala de Jadad. Los principales problemas metodológicos afectaron tanto a la validez interna como a la externa. La comparabilidad de los grupos intervención y control no pudo garantizarse, ya que no se describió el método de asignación en ninguno de los estudios ni se registraron los abandonos. Además, sólo en uno de los trabajos se realizó enmascaramiento en la administración del fármaco, limitado al uso de insulina oral con el placebo y no mantenido para la insulina subcutánea9. Los estudios no ofrecieron información suficiente sobre el tiempo de aclaramiento necesario entre las intervenciones, por lo que no se pudo descartar el efecto remanente, básico para tener en cuenta cuando se realiza un estudio cruzado.
Con respecto a la aplicabilidad de los resultados, resaltamos el hecho de que los participantes no representaban la totalidad de la población diana debido a la formulación de criterios de exclusión muy estrictos, como la presencia de complicaciones mayores propias de la diabetes (neuropatías, retinopatías, etc.), un índice de masa corporal inferior a 20,8 o superior a 38, más de un episodio de hipoglucemia grave en el último año o duración de la enfermedad inferior a los 3 años. Además, los estudios se realizaron en condiciones estrictas de control dietético para asegurar que los niveles lipídicos y de glucosa basal estuvieran dentro del rango establecido por los autores. Otros aspectos que limitaron la validez externa fueron el reducido número de participantes, la falta de información sobre el cálculo del tamaño de la muestra y la escasa duración del seguimiento en vistas a identificar posibles efectos adversos. Además, en uno de los ensayos recuperados se empleó insulina inyectada en pacientes que previamente tomaban ADO y que antes no habían tenido ningún tipo de exposición previa a la insulina, lo que dificultó la atribución del efecto sólo y exclusivamente a la insulina oral, intervención asimismo nueva en estos pacientes.
Tanto el reducido número de trabajos recuperados, las limitaciones encontradas en la validez interna de los estudios originales como la heterogeneidad existente, fundamentalmente en las intervenciones realizadas y en el registro y medición de los resultados, hacen inviable la realización de una síntesis cuantitativa de los resultados.
Para la valoración completa de esta tecnología emergente serían convenientes un número suficiente de estudios de calidad y que éstos establecieran un mayor período de seguimiento para evaluar tanto el control metabólico a través de parámetros a largo plazo (hemoglobina glucosilada) como la seguridad del nuevo fármaco y su efecto sobre la satisfacción, aspecto esencial si tenemos en cuenta que actualmente su principal beneficio radicaría en la mejora de la calidad de vida de los pacientes con diabetes. Por último, estudios sobre costes son deseables para evaluar el impacto real que pudiera alcanzar esta nueva tecnología.
Lo conocido sobre el tema
La diabetes mellitus supone un importante problema de salud debido a su magnitud y a la morbimortalidad que ocasiona.
Aunque el tratamiento con insulina subcutánea ha cambiado el pronóstico de la enfermedad, disminuye la calidad de vida de los pacientes.
Presentaciones no invasivas no han cumplido, hasta el momento, los estándares mínimos de seguridad y de eficacia requeridos.
Qué aporta este estudio
Tanto la insulina oral como la bucal fueron equivalentes o superiores a la insulina inyectada en el control de la glucemia e insulinemia posprandial.
Los ensayos recuperados presentaron problemas de validez interna y externa.
Son necesarios estudios con mayor seguimiento para evaluar la situación metabólica y la seguridad a largo plazo.