Introducción
La diabetes mellitus constituye un importante factor de riesgo aterotrombótico. Entre el 60 y el 80% de las muertes en los pacientes diabéticos tipo 2 son secundarias a enfermedad cardiovascular (ECV). Haffner1 demostró, en su estudio finlandés, que el paciente diabético sin antecedentes de infarto agudo de miocardio (IAM) tiene un riesgo más elevado de presentar un episodio coronario que el paciente no diabético que hubiera sufrido un IAM previamente, por lo que, desde entonces, se considera al diabético como paciente con elevado riesgo cardiovascular (RCV) (> 20% a los 10 años)2.
Recientemente, Evans3 ha publicado un estudio en el que observa cómo el riesgo de presentar un episodio cardiovascular es inferior en el paciente diabético que en el que ya ha padecido un IAM, contradiciendo al estudio de Haffner1. Tal vez el hecho de que los diabéticos incluidos en este estudio no necesitan tratamiento farmacológico (son tratados exclusivamente con medidas higiénico-dietéticas) y que la evolución media de la diabetes en éstos es menor que en el grupo de Haffner nos lleva a establecer que ambos estudios no son comparables, por lo que creemos adecuado seguir considerando al diabético como un paciente de elevado RCV y tratarlo como tal.
En el laboratorio se ha comprobado que los diabéticos tienen plaquetas hipersensibles a la acción de agentes proagregantes y aumentada la síntesis de tromboxano plaquetario que se anula con dosis bajas de ácido acetilsalicílico (AAS)4.
En prevención secundaria de la ECV la eficacia del AAS está demostrada y su empleo claramente justificado5,6, y así figura en diversas guías de práctica clínica7-10; sin embargo, en prevención primaria existe una cierta controversia, ya que si bien el AAS podría reducir la incidencia de episodios cardiovasculares también aumentaría la de hemorragias digestivas y cerebrales, como se expone a continuación.
El US Physicians Health Study11 demostró una disminución de infartos de miocardio en el grupo tratado con AAS, pero carece de potencia estadística para precisar si incrementa el riesgo de hemorragias.
El metaanálisis APT-antiplatelet5 comparó distintas terapias y dosificaciones de antiagregantes (AAS, dipiridamol, ticlopidina) y determina una eficacia igual en los distintos grupos, por lo que finalmente recomienda 75-325 mg diarios de AAS.
Sanmuganathan12, en su metaanálisis, estudia los beneficios obtenidos con el empleo de AAS en el paciente diabético sin ECV previa respecto al riesgo de complicaciones, y concluye que a mayor RCV mayor es dicho beneficio, equilibrándose la relación beneficio/riesgo de hemorragias cuando el RCV es del 2,2% a los 10 años. Este autor justifica plenamente el uso de AAS en prevención primaria cardiovascular cuando el RCV es mayor del 15% a los 10 años, como ocurre en los diabéticos, de modo que el número necesario de tratamientos a realizar durante 5 años para evitar un episodio cardiovascular (casi siempre un IAM) se estima en 60 (IC del 95%, 44-77).
Otro metaanálisis, publicado hace unos meses por Hayden13, analiza la eficacia del AAS en prevención primaria cardiovascular en la población general, observándose una disminución de la incidencia de infartos de miocardio (mayor en el subgrupo de diabéticos), así como un incremento de las hemorragias gastrointestinales e intracraneales, por lo que aconseja el empleo de AAS cuando el RCV sea elevado, como sucede en la población diabética.
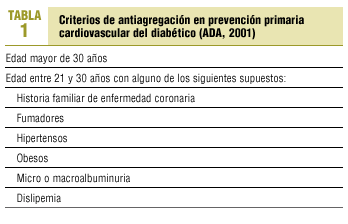
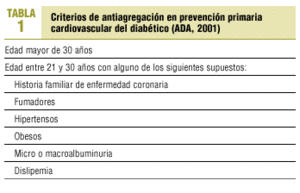
En función de todo lo expuesto, la American Diabetes Association (ADA)14,15 recomienda, desde 2001, el uso de antiagregantes (AAS a dosis de 81-325 mg/día) en prevención secundaria y en prevención primaria de los pacientes diabéticos (varones y mujeres) con alguno de los criterios expuestos en la tabla 1, siempre y cuando no exista contraindicación formal (alergia a AAS, tendencia a hemorragia, tratamiento con anticoagulantes, hemorragia gastrointestinal reciente, enfermedad hepática activa o edad menor de 21 años por el riesgo de síndrome de Reye).
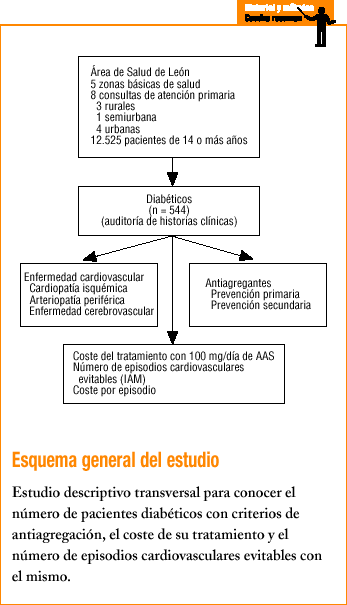
Basándonos en estas evidencias nos plantemos los siguientes objetivos: a) conocer cuántos diabéticos mayores de 21 años con algún criterio de antiagregación, de los que anteriormente hemos comentado, se beneficiarían en nuestro medio del tratamiento antiagregante; b) cuál sería el coste económico al tratar a nuestros pacientes diabéticos sin ECV previa (cardiopatía isquémica, arteriopatía periférica o enfermedad cerebrovascular) con 100 mg diarios de AAS, y c) cuántos episodios cardiovasculares evitaríamos con ello.
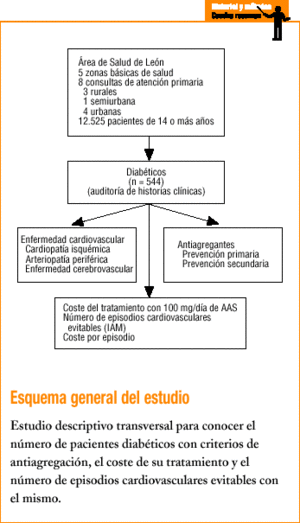
Material y métodos
Diseñamos un estudio multicéntrico descriptivo transversal, mediante una auditoría de las historias clínicas de 8 consultas de atención primaria (3 de ellas rurales, una semiurbana y 4 urbanas), pertenecientes a 5 zonas básicas del Área de Salud de León, que abarca una población de 12.525 personas. Los sujetos incluidos en el estudio fueron todos pacientes diabéticos de 14 o más años diagnosticados con criterios de la ADA (1997) a fecha 1 de enero de 2002.
Los médicos y enfermeras responsables de cada consulta recogieron durante el mes de enero de 2002 los siguientes datos de la historia clínica de los pacientes diagnosticados de diabetes: la edad y el sexo, la presencia de aquellos criterios a los que hace referencia la ADA para la antiagregación (antecedentes de cardiopatía isquémica en familiares de primer grado, varones menores de 45 años o mujeres menores de 55 años, fumador de más de un cigarrillo al día, presión arterial >= 140/90 mmHg, un índice de masa corporal > 30 kg/m2, una excreción urinaria de albúmina > 30 mg/día y un colesterol total > 200 mg/dl o un cLDL >= 100 mg/dl), la existencia de ECV establecida, así como el tratamiento antiagregante que reciben.
Para el cálculo de los costes económicos seleccionamos un envase de 30 comprimidos de 100 mg de AAS, con un coste (IVA incluido) de 1,82 e (303 ptas.).
Para analizar estadísticamente los datos hemos empleado el programa SPSS, v.10.1. Los resultados se expresan en forma de medias ± desviación estándar (DE) y porcentajes con sus respectivos IC del 95%.
Resultados
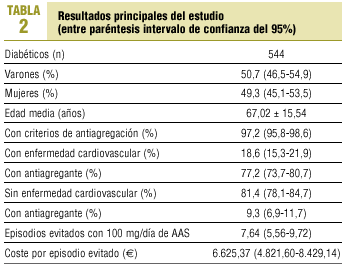
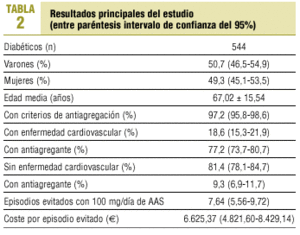
Con el diagnóstico de diabetes aparecen 544 sujetos, de los que 276 eran varones (50,7%; IC del 95%, 46,5-54,9) y 268 mujeres (49,3%; IC del 95%, 45,1-53,5). La edad media fue de 67,02 ± 15,54 años. Entre 14 y 20 años encontramos 8 diabéticos (1,5%; IC del 95%, 0,5-2,5), entre 21 y 30 años 18 (3,3%; IC del 95%, 1,8-4,8) y son mayores de 30 años 518 (95,2%; IC del 95%, 93,4-97) (tabla 2).
De los pacientes entre 21 y 30 años, 11 cuentan con algún criterio para antiagregar. Sumando estos 11 a la población diabética mayor de 30 años contamos con 529 diabéticos (97,2%; IC del 95%, 95,8-98,6) susceptibles de antiagregación.
Presentan algún tipo de ECV 101 pacientes (18,6%; IC del 95%, 15,3-21,9): 52 (9,6%; IC del 95%, 7,1-12,1) cardiopatía isquémica, 49 (9,0%; IC del 95%, 6,6-11,4) arteriopatía periférica y 19 (3,5%; IC del 95%, 2-5) enfermedad vascular cerebral; de ellos, reciben tratamiento antiagregante o anticoagulante 78 (77,2%; IC del 95%, 73,7-80,7).
No tienen ECV conocida 443 diabéticos (81,4%; IC del 95%, 78,1-84,7). Cumplen criterios de antiagregación 428 (78,7%; IC del 95%, 75,3-82,1) de los cuales 40 (9,3%; IC del 95%, 6,9-11,7) reciben tratamiento antiagregante.
En total, son 118 (21,7%; IC del 95%, 18,2-25,2) los diabéticos antiagregados o anticoagulados, 77 (14,2%; IC del 95%, 11,3-17,1) con AAS y 41 (7,5%; IC del 95%, 5,3-9,7) con otros antiagregantes o anticoagulantes: 19 son tratados con acenocumarol, 10 con trifusal, 7 con clopidogrel, 4 con ticlopidina y uno con dipiridamol.
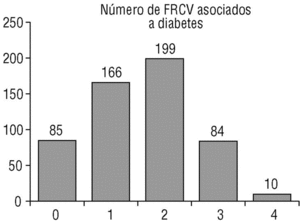
El número de factores de RCV añadidos a la diabetes en nuestros pacientes aparece representado en la figura 1. Se observa que el grupo modal es el que tiene 2 de estos factores.
Figura 1. Número de factores de riesgo cardiovascular (FRCV) asociados a diabetes en nuestros pacientes. Se han tenido en cuenta los siguientes FRCV: hipertensión arterial, dislipemia, obesidad y fumar.
Discusión
Entre las limitaciones de nuestro estudio se encuentra el que se trata de un estudio basado en historias clínicas y no en entrevistas clínicas protocolizadas a los pacientes objeto del estudio. Sin embargo, debido al importante número de casos de que disponemos y a que éstos responden a distintos ámbitos (rural y urbano) nos hace pensar que la situación global en nuestro medio no difiere demasiado de la encontrada.
En líneas generales, incumplimos las recomendaciones de la ADA en cuanto al empleo de antiagregantes en prevención primaria de la ECV del diabético, ya que sólo el 9,3% de nuestros diabéticos sin ECV establecida recibe terapia antiagregante.
No hemos encontrado ningún estudio español que evalúe la utilización de AAS como antiagregante en diabéticos para poder comparar nuestros resultados; sin embargo, un estudio americano, publicado por Rolka16, observa que el 20% de los diabéticos mayores de 21 años con ECV o con algún factor de riesgo recibe antiagregación con AAS; nuestras cifras no llegan al 15%, si bien al incluir a los pacientes que toman otros antiagregantes o anticoagulantes alcanzamos el 22,3%.
El 84,4% de nuestros diabéticos tiene, al menos, un factor de riesgo añadido a su diabetes. Hemos encontrado resultados similares en Aragón gracias a los datos publicados por Tamayo-Marco17 en 1997, coincidiendo en que el más prevalente es la dislipemia (66,5%), seguido de la hipertensión arterial (52%), la obesidad (40,1%) y el tabaquismo (14,9%).
Tratar a nuestros 428 diabéticos sin ECV y con criterios de antiagregación con 100 mg diarios de AAS ascendería a 9.373,20 e/año (1.559.569 ptas./año) con lo que evitaríamos 7,64 episodios cardiovasculares (IC del 95%, 5,56-9,72) en los próximos 5 años, lo que supondría un coste por episodio evitado de 6.625,37 e (IC del 95%, 4.821,60-8.429,14) o 1.102.369 ptas.
Nos llama poderosamente la atención el hecho de que sociedades científicas del prestigio de la ADA recomienden el empleo de AAS en prevención primaria cardiovascular del diabético, y que esto no se lleve a cabo por nuestra parte, con el agravante de que el coste económico para evitar un episodio cardiovascular (casi siempre un infarto) sea mucho menos de lo que supone la asistencia hospitalaria de un paciente que ha sufrido un IAM, a lo que hay que añadir gastos en concepto de incapacidades laborales, temporales o permanentes, pensiones de viudedad, etc.
Creemos, en definitiva, que nuestro estudio debe servir para replantearnos, siempre en función de la evidencia científica existente, si debemos antiagregar a nuestros diabéticos cuando haya indicación para ello, pues parece ser una intervención eficaz desde el punto de vista clínico y económico.
Se hace necesaria la difusión entre los profesionales médicos de medidas sanitarias como la tratada en este artículo a través de programas de formación continuada, promovida tanto por las distintas sociedades científicas (ADA, ESC, AHA, SEC, semFYC, etc.) como por las instituciones sanitarias, responsables de velar por la salud comunitaria y de administrar los presupuestos destinados a sanidad.
Nuestro artículo debe servir para reflexionar acerca de si las recomendaciones de las guías de práctica clínica son debidamente conocidas por parte de los médicos, lo que podría constituir la base de un estudio descriptivo, y si no nos interesaría a todos (pacientes, médicos y administración sanitaria) una mayor difusión de las mismas.
Agradecimientos
Los autores queremos agradecer a Joaquín Aira Neira, Julia Martín Macías, Federico Rodríguez Sánchez y Miguel Ángel Pérez Bernabéu la paciencia y el tiempo dedicado a la revisión de las historias clínicas de las consultas incluidas en nuestro estudio.
Correspondencia: Jaime López de la Iglesia. Cardenal Lorenzana, 3, 4.º A. 24001 León. España. Correo electrónico: saul-ea@mixmail.com
Premio Mejor Comunicación PAPPS-SCLMFyC. II Congreso de Atención Primaria de Castilla y León (Segovia, abril de 2002).
Manuscrito recibido el 26 de junio de 2002.
Manuscrito aceptado para su publicación el 18 de noviembre de 2002.