El objetivo de este estudio ha sido conocer las características de los pacientes EPOC por fenotipos y según la GOLD 2011-ABCD y el grado de concordancia de los tratamientos farmacológicos.
DiseñoEstudio transversal de observación y descriptivo.
EmplazamientoPacientes EPOC entre 40 y 85años pertenecientes al Área de León que figuran en la base de datos MEDORA de Atención Primaria.
ParticipantesDe los 5.522 pacientes recogidos en la base de datos de MEDORA con los criterios de selección descritos, se calculó un tamaño muestral de 734 sujetos, de los cuales se estudiaron finalmente 577 enfermos.
Mediciones principalesSe diseñó un cuestionario estructurado para recoger la información sociodemográfica, clínica, tratamientos y calidad de vida. Se incluía realización de espirometría y prueba broncodilatadora.
ResultadosDe los 734 enfermos muestreados se ha conseguido estudiar al 78,6% (577). En 166 pacientes (28,7%), el diagnóstico había sido realizado exclusivamente por la clínica, sin constancia de espirometría en el MEDORA. En 123 (21,3%) el índice FEV1/FVC fue superior a 0,7, por lo que se descartó el diagnóstico de EPOC. Con respecto a los tratamientos prescritos según fenotipos, observamos que en el fenotipo no agudizador existe una sobreprescripción de corticoides inhalados. Lo mismo sucede en los gruposA yB.
ConclusionesA pesar de las guías clínicas, el manejo de los pacientes con EPOC en la vida real sigue siendo mejorable, tanto en el aspecto diagnóstico como de medidas terapéuticas.
The purpose of this study was to evaluate different characteristics of COPD patients according to phenotypes and GOLD guidelines.according to GesEPOC phenotypes and GOLD 2011 ABCD guidelines and pharmacological treatment agreement.
DesignCross-sectional survey.
LocationCOPD patients aged 40-85 from León were randomly selected from Primary Care database, MEDORA.
Participants5222 eligible COPD patients were collected from MEDORA database. We calculated a sample size of 734 patients and finally studied 577 of them.
Main measurementsPatients¿ clinical, functional and health related quality of life information were collected. Spirometry and postbroncodilator test were performed.
ResultsA total of 577 patients were included in this study. 28.7% of them did not have a spirometry recorded in their files. 123 patients had a normal or non-obstructive spirometry pattern, so they were excluded from a COPD diagnostic. With regard to treatments, there was an overprescribing of inhaled steroids in patients from GOLD A and B groups, and also in patients with the called exacerbator phenotype (GesEPOC).
ConclusionAlthough there have been several published guidelines, management of COPD patients in real life should be improved.
La enfermedad pulmonar obstructiva crónica (EPOC) es una de las enfermedades crónicas más prevalentes. Afecta al 10,2% de la población española entre 40 y 80años, y actualmente es la cuarta causa de muerte en nuestro país1, suponiendo, por tanto, un importante impacto sociosanitario y económico2.
La publicación de guías de práctica clínica como la Global Initiative for Chronic Obstructive Lung Disease (GOLD)2 y la Guía Española de la EPOC (GesEPOC)3,4 aúna y facilita el manejo de estos pacientes. Sin embargo, existe un alto grado de infradiagnóstico, como se ha demostrado en estudios internacionales como el BOLD5, o nacionales, como el EPI-SCAN6 e IBERPOC7, en los que hasta el 70% de los pacientes con EPOC no estaban diagnosticados. Por otro lado, existe un importante diagnóstico inadecuado, demostrándose en varios estudios que tan solo en el 30-50% de los pacientes etiquetados como EPOC constaba la realización de una espirometría8. En otros trabajos se demuestra que en el 15-30% de los pacientes EPOC con espirometría, esta no era obstructiva9. Esto puede llevar a la prescripción inapropiada de fármacos y a un alto impacto económico.
En cuanto al tratamiento, la GesEPOC ha establecido unas recomendaciones según fenotipos. Por su parte, la GOLD, en su revisión del 2011, establece una clasificación en 4 grupos: A, B, C y D, en función de síntomas, exacerbaciones y limitación al flujo aéreo, así como recomendaciones terapéuticas para cada grupo10.
Una correcta implementación de estas guías puede ayudarnos a optimizar el manejo de estos pacientes11.
Teniendo en cuenta lo expuesto anteriormente, se diseñó este estudio (LEONPOC) con los objetivos de conocer las características epidemiológicas, clínicas, la adecuación diagnóstica por fenotipos y GOLD 2011-ABCD de los pacientes diagnosticados de EPOC en atención primaria (AP) en el Área de León, así como determinar el grado de concordancia en el tratamiento de acuerdo con las guías de práctica clínica (GesEPOC y GOLD).
MetodologíaSe realizó un estudio transversal, observacional y descriptivo cuya fuente de información fue el registro de la historia clínica electrónica de AP en Castilla y León (MEDORA®). Se elaboró un censo con todos los pacientes entre 40 y 85años con el diagnóstico de EPOC o códigos relacionados (CIES9, 491, 492, 496), pertenecientes al Área de Salud de León (348.000 habitantes). Este censo lo formaban 5.522 enfermos en enero de 2015. El trabajo de campo se realizó en el periodo de marzo a junio de 2015.
Se excluyeron aquellos pacientes que no firmasen el consentimiento informado. El estudio fue aprobado por el comité de ética e investigación del Complejo Asistencial Universitario de León.
Se diseñó un muestreo bietápico. En una primera etapa se seleccionaron unidades de AP con participación voluntaria. El marco muestral quedó conformado por todos los pacientes de los cupos de los médicos participantes en el estudio, que configuraron las unidades de segunda etapa. En cada estrato se realizó un muestreo aleatorio sistemático, proporcional al número de enfermos.
Variables estudiadasSe diseñó un cuestionario estructurado para recoger la información. Se midieron variables sociodemográficas: edad, sexo, peso, talla, medio rural o urbano, historia de tabaquismo; variables clínico-asistenciales: grado de disnea (mediante la escala modificada del Medical Research Council [mMRC]), y comorbilidades asociadas: índice de Charlson (ICh), número de agudizaciones en el último año (moderadas o graves) —según la GesEPOC, consideramos fenotipo agudizador al que presentó dos o más exacerbaciones moderadas o una grave en el último año—, fecha y edad al diagnóstico, y cómo se realizó el diagnóstico (clínica, espirometría basal, prueba broncodilatadora [PBD]).
Se identificaron los tratamientos pautados para la EPOC en el momento del estudio: beta-agonistas de acción corta (SABA), de acción larga (LABA), anticolinérgicos de acción corta (SAMA), de acción larga (LAMA), corticoides inhalados (CI), corticoides orales, oxigenoterapia domiciliaria, inhibidores de la fosfodiesterasa-4, mucolíticos y teofilinas. La calidad de vida relacionada con la salud se midió a través de los cuestionarios COPD Assesment Test (CAT) y el St George Respiratory Questionnaire (SGRQ).
Según protocolo, a todos los pacientes se les realizó una espirometría forzada basal y PBD. Se organizaron 4 cursos de formación en espirometría destinados a los profesionales de enfermería, empleando los espirómetros disponibles en cada centro de salud. La aceptabilidad de las pruebas fue analizada por 2 neumólogos mediante el visionado de las curvas de flujo-volumen, según la normativa American Thoracic Society/European Respiratory Society (ATS/ERS): comienzo adecuado; ausencia de artefactos y finalización correcta. Se consideró un diagnóstico incorrecto de EPOC cuando la espirometría realizada presentaba un índice FEV1/FVC>0,7 o 70%.
Análisis de datosSe realizó de manera centralizada. Los pacientes estudiados que no cumplían con la definición de EPOC fueron eliminados de los análisis posteriores. Los datos ausentes no se imputaron a ninguna categoría y se dejaron como perdidos.
Se realizó una descripción general de las variables incluidas, mediante las distribuciones de frecuencias absolutas y relativas de las variables cualitativas, así como las medidas de tendencia central y dispersión de las variables cuantitativas. Se calcularon los intervalos de confianza (IC) al 95%.
Los test de hipótesis realizados fueron en todos los casos bilaterales y con un nivel de significación de 0,05. Para las variables que no se ajustaban a una distribución normal se utilizaron los test de hipótesis de Mann Whitney.
Con el fin de identificar las características de los enfermos que son etiquetados erróneamente como enfermos de EPOC en la historia clínica de AP, se realizó un ajuste mediante regresión logística. La variable dependiente fue diagnóstico incorrecto con 2 categorías (sí/no).
El análisis de tablas de contingencia y la comparación de proporciones se realizó mediante el test de chi-cuadrado. Las diferencias entre grupos se evaluaron mediante la t de Student o ANOVA para comparar una variable cuantitativa con una cualitativa según tuvieran 2 o más categorías, respectivamente. Se utilizó el análisis de correlación y regresión lineal para analizar la relación entre 2 variables numéricas.
El programa estadístico utilizado fue el SPSSv14.0 para Windows.
ResultadosCon los criterios de selección descritos, existían 5.522 pacientes recogidos en la base de datos de MEDORA, lo que supone una prevalencia de la EPOC conocida del 3%. Se calculó un tamaño muestral de 734 sujetos, de los cuales se estudiaron finalmente 577 (cerca del 80% de la muestra inicial). Colaboraron 117 unidades de AP —el 40% de todos los profesionales del área—, con una distribución representativa de los pacientes por centros de salud.
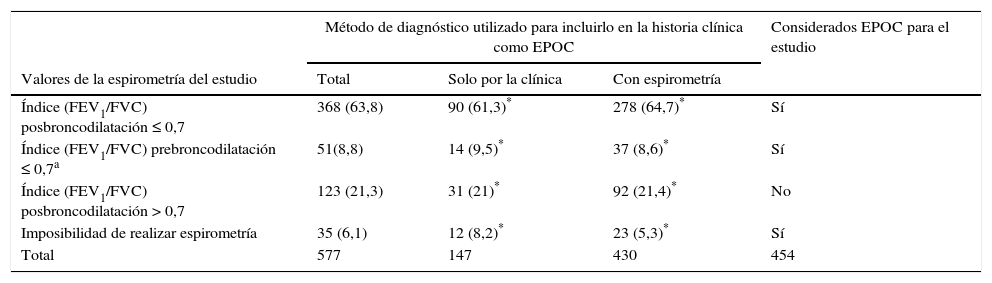
En la tabla 1 se observa la distribución de la muestra estudiada según el método diagnóstico que figura en la historia clínica del médico de AP y los resultados de la espirometría realizada en el estudio. Se consiguió hacer espirometría a 542 pacientes del estudio y PBD en 491 casos. En 35 (6,1%) no fue posible realizarla debido a una deficiente colaboración o por ser pacientes inmovilizados; estos últimos fueron considerados EPOC tras comprobar sus características clínicas, su hábito tabáquico y los valores de espirometrías previas. En 123 (21,3%) el índice FEV1/FVC fue superior al 0,7, por lo que se descartó el diagnóstico de EPOC. Finalmente fueron considerados como EPOC 454 enfermos.
Distribución de la muestra según el método de diagnóstico empleado para incluirlo como EPOC en la historia clínica de atención primaria y los resultado de la espirometría realizada en el estudio
| Método de diagnóstico utilizado para incluirlo en la historia clínica como EPOC | Considerados EPOC para el estudio | |||
|---|---|---|---|---|
| Valores de la espirometría del estudio | Total | Solo por la clínica | Con espirometría | |
| Índice (FEV1/FVC) posbroncodilatación ≤ 0,7 | 368 (63,8) | 90 (61,3)* | 278 (64,7)* | Sí |
| Índice (FEV1/FVC) prebroncodilatación ≤ 0,7a | 51(8,8) | 14 (9,5)* | 37 (8,6)* | Sí |
| Índice (FEV1/FVC) posbroncodilatación > 0,7 | 123 (21,3) | 31 (21)* | 92 (21,4)* | No |
| Imposibilidad de realizar espirometría | 35 (6,1) | 12 (8,2)* | 23 (5,3)* | Sí |
| Total | 577 | 147 | 430 | 454 |
FEV1: volumen máximo de aire espirado en el primer segundo; FVC: capacidad vital forzada.
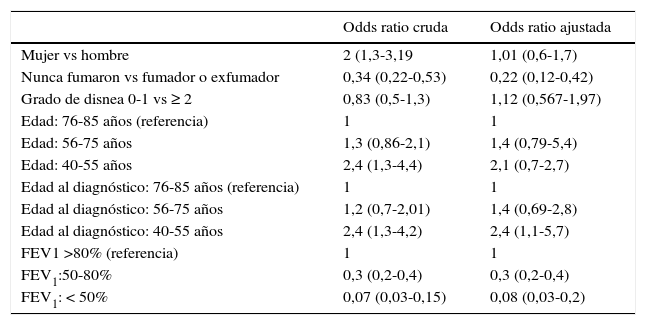
El ajuste mediante la regresión logística, como se expone en la tabla 2, identifica que una edad al diagnóstico menor de 55años se asocia significativamente (OR:2,4; IC del 95%:1,1-5,7), con una mayor frecuencia de ser clasificado erróneamente como EPOC.
Variables asociadas al diagnóstico erróneo de EPOC en MEDORA. Análisis de regresión logística
| Odds ratio cruda | Odds ratio ajustada | |
|---|---|---|
| Mujer vs hombre | 2 (1,3-3,19 | 1,01 (0,6-1,7) |
| Nunca fumaron vs fumador o exfumador | 0,34 (0,22-0,53) | 0,22 (0,12-0,42) |
| Grado de disnea 0-1 vs ≥ 2 | 0,83 (0,5-1,3) | 1,12 (0,567-1,97) |
| Edad: 76-85 años (referencia) | 1 | 1 |
| Edad: 56-75 años | 1,3 (0,86-2,1) | 1,4 (0,79-5,4) |
| Edad: 40-55 años | 2,4 (1,3-4,4) | 2,1 (0,7-2,7) |
| Edad al diagnóstico: 76-85 años (referencia) | 1 | 1 |
| Edad al diagnóstico: 56-75 años | 1,2 (0,7-2,01) | 1,4 (0,69-2,8) |
| Edad al diagnóstico: 40-55 años | 2,4 (1,3-4,2) | 2,4 (1,1-5,7) |
| FEV1 >80% (referencia) | 1 | 1 |
| FEV1:50-80% | 0,3 (0,2-0,4) | 0,3 (0,2-0,4) |
| FEV1: < 50% | 0,07 (0,03-0,15) | 0,08 (0,03-0,2) |
FEV1: volumen máximo de aire espirado en el primer segundo.
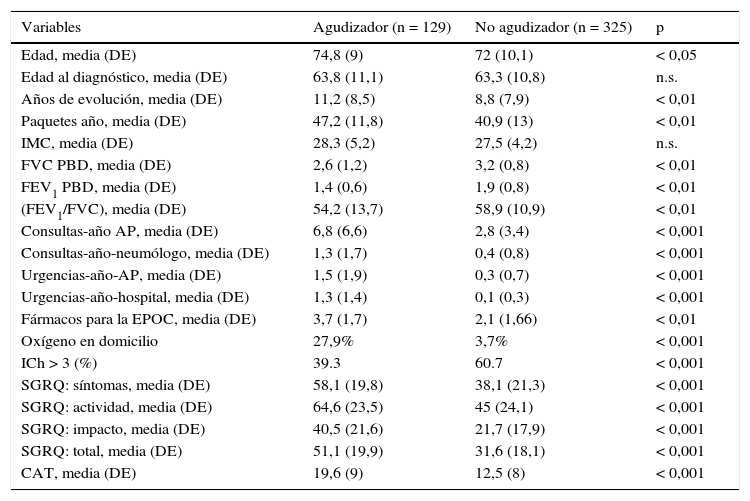
Destacamos la edad media elevada de los pacientes (72,8años; DE:10,6), así como la presencia de tabaquismo activo (20%). En cuanto a las características de los considerados agudizadores, se describen en la tabla 3. Suponen el 28% en nuestro estudio.
Características de los pacientes agudizadores y no agudizadores
| Variables | Agudizador (n = 129) | No agudizador (n = 325) | p |
|---|---|---|---|
| Edad, media (DE) | 74,8 (9) | 72 (10,1) | < 0,05 |
| Edad al diagnóstico, media (DE) | 63,8 (11,1) | 63,3 (10,8) | n.s. |
| Años de evolución, media (DE) | 11,2 (8,5) | 8,8 (7,9) | < 0,01 |
| Paquetes año, media (DE) | 47,2 (11,8) | 40,9 (13) | < 0,01 |
| IMC, media (DE) | 28,3 (5,2) | 27,5 (4,2) | n.s. |
| FVC PBD, media (DE) | 2,6 (1,2) | 3,2 (0,8) | < 0,01 |
| FEV1 PBD, media (DE) | 1,4 (0,6) | 1,9 (0,8) | < 0,01 |
| (FEV1/FVC), media (DE) | 54,2 (13,7) | 58,9 (10,9) | < 0,01 |
| Consultas-año AP, media (DE) | 6,8 (6,6) | 2,8 (3,4) | < 0,001 |
| Consultas-año-neumólogo, media (DE) | 1,3 (1,7) | 0,4 (0,8) | < 0,001 |
| Urgencias-año-AP, media (DE) | 1,5 (1,9) | 0,3 (0,7) | < 0,001 |
| Urgencias-año-hospital, media (DE) | 1,3 (1,4) | 0,1 (0,3) | < 0,001 |
| Fármacos para la EPOC, media (DE) | 3,7 (1,7) | 2,1 (1,66) | < 0,01 |
| Oxígeno en domicilio | 27,9% | 3,7% | < 0,001 |
| ICh > 3 (%) | 39.3 | 60.7 | < 0,001 |
| SGRQ: síntomas, media (DE) | 58,1 (19,8) | 38,1 (21,3) | < 0,001 |
| SGRQ: actividad, media (DE) | 64,6 (23,5) | 45 (24,1) | < 0,001 |
| SGRQ: impacto, media (DE) | 40,5 (21,6) | 21,7 (17,9) | < 0,001 |
| SGRQ: total, media (DE) | 51,1 (19,9) | 31,6 (18,1) | < 0,001 |
| CAT, media (DE) | 19,6 (9) | 12,5 (8) | < 0,001 |
AP: atención primaria; CAT: COPD Assesment Test; DE: desviación estándar; FEV1: volumen máximo de aire espirado en el primer segundo; FVC: capacidad vital forzada; ICh: índice de Charlson; IMC: índice de masa corporal; PBD: prueba broncodilatadora; SGRQ: St George Respiratory Questionnaire.
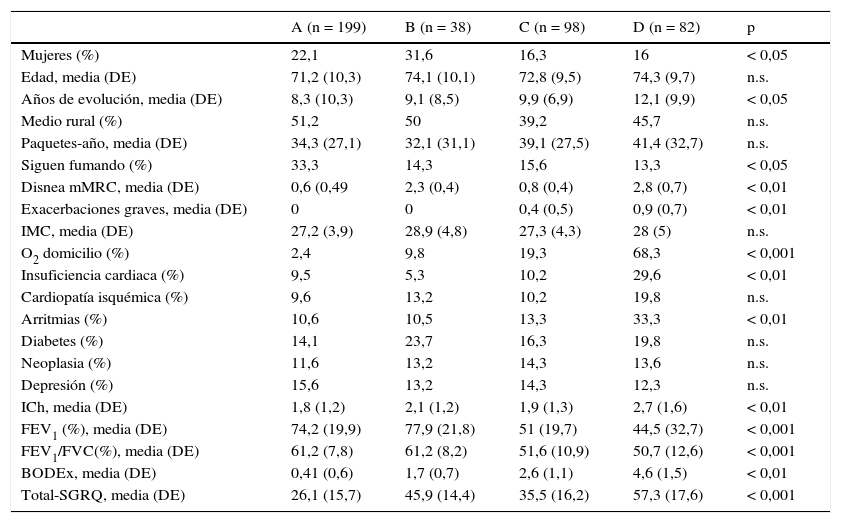
Según la clasificación GOLD 2011-ABCD, los pacientes se encuentran en su mayoría en el grupoA, con un 43,8%; presentan pocos síntomas y riesgo bajo. Le siguen los gruposC yD, con el 21,6 y el 20,5%, respectivamente, y el grupo con menos efectivos es el B, con solo el 8,4%; pacientes con bajo riesgo y muchos síntomas, como refleja la tabla 4.
Características de los pacientes clasificados según la GOLD 2011 (ABCD)
| A (n = 199) | B (n = 38) | C (n = 98) | D (n = 82) | p | |
|---|---|---|---|---|---|
| Mujeres (%) | 22,1 | 31,6 | 16,3 | 16 | < 0,05 |
| Edad, media (DE) | 71,2 (10,3) | 74,1 (10,1) | 72,8 (9,5) | 74,3 (9,7) | n.s. |
| Años de evolución, media (DE) | 8,3 (10,3) | 9,1 (8,5) | 9,9 (6,9) | 12,1 (9,9) | < 0,05 |
| Medio rural (%) | 51,2 | 50 | 39,2 | 45,7 | n.s. |
| Paquetes-año, media (DE) | 34,3 (27,1) | 32,1 (31,1) | 39,1 (27,5) | 41,4 (32,7) | n.s. |
| Siguen fumando (%) | 33,3 | 14,3 | 15,6 | 13,3 | < 0,05 |
| Disnea mMRC, media (DE) | 0,6 (0,49 | 2,3 (0,4) | 0,8 (0,4) | 2,8 (0,7) | < 0,01 |
| Exacerbaciones graves, media (DE) | 0 | 0 | 0,4 (0,5) | 0,9 (0,7) | < 0,01 |
| IMC, media (DE) | 27,2 (3,9) | 28,9 (4,8) | 27,3 (4,3) | 28 (5) | n.s. |
| O2 domicilio (%) | 2,4 | 9,8 | 19,3 | 68,3 | < 0,001 |
| Insuficiencia cardiaca (%) | 9,5 | 5,3 | 10,2 | 29,6 | < 0,01 |
| Cardiopatía isquémica (%) | 9,6 | 13,2 | 10,2 | 19,8 | n.s. |
| Arritmias (%) | 10,6 | 10,5 | 13,3 | 33,3 | < 0,01 |
| Diabetes (%) | 14,1 | 23,7 | 16,3 | 19,8 | n.s. |
| Neoplasia (%) | 11,6 | 13,2 | 14,3 | 13,6 | n.s. |
| Depresión (%) | 15,6 | 13,2 | 14,3 | 12,3 | n.s. |
| ICh, media (DE) | 1,8 (1,2) | 2,1 (1,2) | 1,9 (1,3) | 2,7 (1,6) | < 0,01 |
| FEV1 (%), media (DE) | 74,2 (19,9) | 77,9 (21,8) | 51 (19,7) | 44,5 (32,7) | < 0,001 |
| FEV1/FVC(%), media (DE) | 61,2 (7,8) | 61,2 (8,2) | 51,6 (10,9) | 50,7 (12,6) | < 0,001 |
| BODEx, media (DE) | 0,41 (0,6) | 1,7 (0,7) | 2,6 (1,1) | 4,6 (1,5) | < 0,01 |
| Total-SGRQ, media (DE) | 26,1 (15,7) | 45,9 (14,4) | 35,5 (16,2) | 57,3 (17,6) | < 0,001 |
DE: desviación estándar; FEV1: volumen máximo de aire espirado en el primer segundo; FVC: capacidad vital forzada; ICh: índice de Charlson; IMC: índice de masa corporal; mMRC: escala Medical Research Council modificada; PBD: prueba broncodilatadora; SGRQ: St George Respiratory Questionnaire.
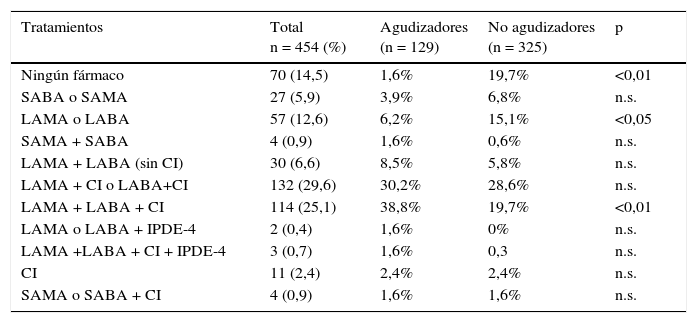
Con respecto a los tratamientos prescritos según fenotipos, observamos que en el no agudizador existe una sobreprescripción de corticoides inhalados. Lo mismo sucede en los gruposA yB, de bajo riesgo (tablas 5 y 6).
Pautas de tratamiento en agudizadores y no agudizadores
| Tratamientos | Total n = 454 (%) | Agudizadores (n = 129) | No agudizadores (n = 325) | p |
|---|---|---|---|---|
| Ningún fármaco | 70 (14,5) | 1,6% | 19,7% | <0,01 |
| SABA o SAMA | 27 (5,9) | 3,9% | 6,8% | n.s. |
| LAMA o LABA | 57 (12,6) | 6,2% | 15,1% | <0,05 |
| SAMA + SABA | 4 (0,9) | 1,6% | 0,6% | n.s. |
| LAMA + LABA (sin CI) | 30 (6,6) | 8,5% | 5,8% | n.s. |
| LAMA + CI o LABA+CI | 132 (29,6) | 30,2% | 28,6% | n.s. |
| LAMA + LABA + CI | 114 (25,1) | 38,8% | 19,7% | <0,01 |
| LAMA o LABA + IPDE-4 | 2 (0,4) | 1,6% | 0% | n.s. |
| LAMA +LABA + CI + IPDE-4 | 3 (0,7) | 1,6% | 0,3 | n.s. |
| CI | 11 (2,4) | 2,4% | 2,4% | n.s. |
| SAMA o SABA + CI | 4 (0,9) | 1,6% | 1,6% | n.s. |
CI: corticoides inhalados; IPDE-4: inhibidores de fosfodiesterasa 4; LABA: beta-agonistas de acción larga; LAMA: anticolinérgicos de acción larga; SABA: beta-agonistas de acción corta; SAMA: anticolinérgicos de acción corta.
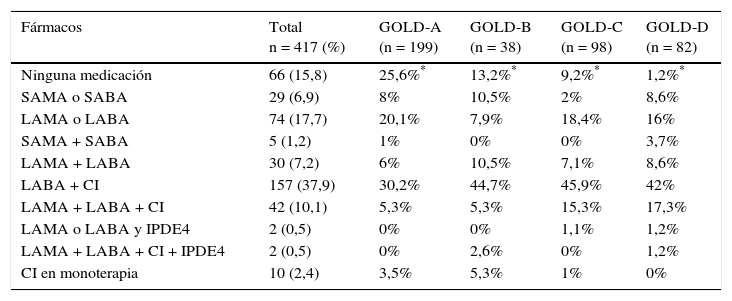
Enfermos con pautas terapéuticas según GOLD- 2011
| Fármacos | Total n = 417 (%) | GOLD-A (n = 199) | GOLD-B (n = 38) | GOLD-C (n = 98) | GOLD-D (n = 82) |
|---|---|---|---|---|---|
| Ninguna medicación | 66 (15,8) | 25,6%* | 13,2%* | 9,2%* | 1,2%* |
| SAMA o SABA | 29 (6,9) | 8% | 10,5% | 2% | 8,6% |
| LAMA o LABA | 74 (17,7) | 20,1% | 7,9% | 18,4% | 16% |
| SAMA + SABA | 5 (1,2) | 1% | 0% | 0% | 3,7% |
| LAMA + LABA | 30 (7,2) | 6% | 10,5% | 7,1% | 8,6% |
| LABA + CI | 157 (37,9) | 30,2% | 44,7% | 45,9% | 42% |
| LAMA + LABA + CI | 42 (10,1) | 5,3% | 5,3% | 15,3% | 17,3% |
| LAMA o LABA y IPDE4 | 2 (0,5) | 0% | 0% | 1,1% | 1,2% |
| LAMA + LABA + CI + IPDE4 | 2 (0,5) | 0% | 2,6% | 0% | 1,2% |
| CI en monoterapia | 10 (2,4) | 3,5% | 5,3% | 1% | 0% |
CI: corticoides inhalados; IPDE-4: inhibidores de fosfodiesterasa 4; LABA: beta-agonistas de acción larga; LAMA: anticolinérgicos de acción larga; SABA: beta-agonistas de acción corta; SAMA: anticolinérgicos de acción corta.
La selección de los participantes, realizada a partir del censo de pacientes con un diagnóstico de EPOC en la historia clínica de AP, puede limitar la generalización de nuestros resultados. No obstante, el método de muestreo permite inferir nuestros resultados a los pacientes que son atendidos cada día en las consultas. De igual forma, la participación voluntaria de los profesionales puede suponer un sesgo, aunque creemos que el hecho de que haya sido tan amplia reduce el mismo. Dada la naturaleza transversal del diseño, la interpretación de las asociaciones encontradas es de naturaleza estadística; no podemos establecer una relación causal.
Creemos necesario señalar ciertas fortalezas. La buena participación de los profesionales del área y la alta tasa de enfermos estudiados, casi el 80% del total de la muestra, confieren a este trabajo una buena validez interna. Las medidas de las variables, a pesar de ser realizadas por más de dos centenares de profesionales diferentes, fueron consensuadas mediante el protocolo de estudio; esto nos permite asegurar una buena homogeneidad y reproducibilidad de los resultados.
Comparación con otros estudiosEn cuanto al diagnóstico, el estudio pone de manifiesto que prácticamente uno de cada tres de los pacientes incluidos en MEDORA como EPOC fueron diagnosticados exclusivamente por criterios clínicos, sin la confirmación espirométrica. Por otro lado, hemos constatado un sobrediagnóstico de EPOC superior al 20%. En un estudio realizado por Miravitlles et al.12, el resultado más importante fue que más de la mitad de pacientes considerados como EPOC en AP no tenían una espirometría que confirmara su diagnóstico. Esta situación ha sido descrita en otras series: otros autores —Caramori13 en Italia y Buffels14 en Bélgica— también mostraron que solamente en un tercio de los pacientes el diagnóstico de EPOC estuvo confirmado mediante espirometría. Probablemente gran parte de los pacientes diagnosticados de EPOC lo fueron exclusivamente a partir de signos y síntomas clínicos cuya validez y fiabilidad son bajas15,16, por lo que insistimos en la necesidad de una espirometría para confirmar o descartar el diagnóstico17,18.
La edad media de los pacientes en nuestra serie es mayor a la práctica totalidad de las publicaciones. Al tratarse de enfermos más envejecidos, son también enfermos con más comorbilidad asociada, mayor demanda de cuidados y gran dependencia de los servicios sanitarios. El estudio COCOMICS19, en el que se analizan pacientes de 7 regiones españolas, las edades van desde una media de 62,9años de Tenerife a 72,2 de Terrassa; la media global de todas las cohortes era de 66,4años. El estudio On-Sint20 realizado en diferentes regiones de España obtiene una edad media de 66años. En el estudio ECLIPSE21 la edad media de los pacientes fue de 63,4años.
Un aspecto preocupante es que el 20% de los pacientes con EPOC siguen fumando. El estudio On-Sint obtiene un 26,5% de fumadores activos, cifra similar a la nuestra. Un 16% de nuestros pacientes nunca han fumado. En un estudio multicéntrico nacional, el EPI-SCAN, se objetivó un 26% de pacientes con EPOC que nunca fumaron. No hay que olvidar que existen otras fuentes de exposición que pueden dar lugar al desarrollo de EPOC: combustión de biomasa, contaminación atmosférica, tabaquismo pasivo o exposición laboral, todas ellas difíciles de cuantificar.
La comorbilidad en los enfermos de León es ligeramente superior a la publicada en otras series; así, en el estudio COCOMICS todas las cohortes arrojan un ICh inferior a 2. Un estudio europeo de EPOC en AP22 señala un promedio de 2 enfermedades por sujeto. Nuestros resultados se deben a que la edad de nuestros enfermos es superior.
El registro de las agudizaciones nos ha permitido establecer el fenotipo agudizador frente al no agudizador, observando características diferentes en ambos grupos. Queremos señalar que identificar el fenotipo agudizador permite adecuar el tratamiento y optimizar los recursos necesarios al tratarse de un grupo con alto consumo de fármacos y mayor frecuentación del sistema sanitario. Nuestros resultados son similares a los objetivados en el estudio CHAIN23.
De igual modo se ha podido calcular el índice BODEx, uno de los índices multicomponente validados. La utilización de este índice en la práctica diaria de AP es escasa. Sin embargo, es relativamente sencillo, permite valorar la actitud terapéutica y predecir la evolución de los pacientes a medio plazo24. El promedio del índice BODEx obtenido en nuestro estudio fue de 1,9, inferior al obtenido en las cohortes nacionales publicadas en el COCOMICS. La razón fundamental es que nuestra muestra procede de pacientes de AP evaluados en situaciones de estabilidad clínica. También la mayor proporción de mujeres de nuestro estudio (21,4%), en relación con la mayoría de los publicados, que se encuentran en estadios menos avanzados de EPOC, contribuye a un índice BODEx menor.
Siguiendo la GOLD-2011, nuestros pacientes se encuentran de forma mayoritaria en el grupoA. Recientemente varios estudios han empleado cohortes ya existentes de pacientes con EPOC para explorar diferentes aspectos de esta nueva clasificación, con resultados muy dispares, debido a diferentes motivos: diseño del estudio y criterios de inclusión, modo de selección de pacientes (de consultas de AP u hospitalizados o población general), y por último las características propias de cada población. Las comparaciones deben ser tomadas con cautela, puesto que los criterios de inclusión son diferentes.
Los pacientes del LEONPOC tienen similares características a los estudios que seleccionaron los pacientes del ámbito de la AP. Son los de mayor edad de todos los grupos de comparación. El porcentaje de mujeres (21,4%) es el mayor de todos, hecho que puede explicar el mayor porcentaje de enfermos que no han fumado nunca. Los valores espirométricos y la consiguiente clasificación de GOLD-2006 son diferentes a la mayoría de cohortes: la causa fundamental es que en una mayoría de cohortes fueron excluidos los que presentaban un FEV1 superior al 80% del valor de referencia25,26.
Se objetiva en nuestros pacientes un problema de sobreprescripción farmacológica, sobre todo en pacientes leves o de bajo riesgo, fundamentalmente a expensas de corticoides inhalados, al igual que lo publicado en la literatura27,28. Los broncodilatadores de larga duración en monoterapia o la doble broncodilatación LABA +LAMA está muy infrautilizada, incluso en el estadioB, con una tasa de concordancia menor del 30%. Al igual que en otros estudios, observamos una escasa implementación de las recomendaciones terapéuticas de las nuevas guías29,30. El estudio IDENTEPOC31 puso de manifiesto que existía una escasa adherencia, tanto en el ámbito de la AP como en el de la Neumología. En el estudio VICE32 también se concluye que el impacto de las guías en la práctica clínica es poco relevante. Se ha detectado una sobreprescripción farmacológica, sobre todo en los casos leves. En estudios más recientes33 se confirma esta tendencia.
Aplicabilidad práctica de los resultadosCon este estudio hemos querido tener una visión más exacta de los pacientes con EPOC en nuestra área, para poder identificar los puntos fuertes y las carencias en la atención de los mismos.
DirectricesEsta información nos permitirá diseñar acciones encaminadas a mejorar diferentes aspectos: incidir en un diagnóstico correcto de la EPOC mediante la utilización de la espirometría en AP; establecer un profesional de referencia en cada centro de salud para la realización de espirometrías; insistir en las medidas de deshabituación tabáquica en el ámbito de AP; detectar los pacientes agudizadores que consumen más recursos para prevenir las exacerbaciones, y optimizar el tratamiento de la enfermedad mediante cursos de formación.
- •
La publicación de guías de práctica clínica, como la Global Initiative for Chronic Obstructive Lung Disease (GOLD)2 y la Guía Española de la EPOC (GesEPOC)3,4, aúna y facilita el manejo de estos pacientes en atención primaria.
- •
A pesar de todo, existe un alto grado de infradiagnóstico de la EPOC, así como un importante diagnóstico inadecuado por la escasa utilización de la espirometría y su escasa calidad.
- •
Existe por otro lado escaso seguimiento de las guías en cuanto al tratamiento de estos pacientes.
- •
Hemos objetivado un gran interés de los profesionales de atención primaria en mejorar el manejo de los enfermos con EPOC.
- •
Nos permite conocer la situación de los pacientes en nuestro medio en la vida real y así poder detectar nuestros puntos débiles y aportar las medidas necesarias para mejorarlos.
- •
Los resultados pueden ser extrapolables a otras poblaciones con características similares y servir de referencia.
El estudio fue financiado parcialmente por la Gerencia Regional de Salud del SACYL (GRS 1113/B/15). Así mismo, ha sido avalado por la Sociedad Castellano-Leonesa y Cántabra de Patología Respiratoria (SOCALPAR) mediante la concesión de Premio de Investigación 2016.Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.