El adecuado tratamiento de la diabetes mellitus tipo2 (DM2) incluye la alimentación saludable y el ejercicio (150min/semana) como pilares básicos. Para el tratamiento farmacológico, la metformina es el fármaco de elección inicial, salvo contraindicación o intolerancia; en caso de mal control, se dispone de 8 familias terapéuticas (6 orales y 2 inyectables) como posibles combinaciones. Se presenta un algoritmo y unas recomendaciones para el tratamiento de la DM2. En prevención secundaria cardiovascular se recomienda asociar un inhibidor del cotransportador sodio-glucosa tipo2 (iSGLT2) o un agonista del receptor de glucagon-like peptide-1 (arGLP1) en pacientes con obesidad. En prevención primaria, si el paciente presenta obesidad o sobrepeso la metformina deberá combinarse con iSGLT2, arGLP1 o inhibidores de la dipeptidilpeptidasa tipo4 (iDPP4). Si el paciente no presenta obesidad, podrán emplearse los iDPP4, los iSGLT2 o la gliclazida, sulfonilurea recomendada por su menor tendencia a la hipoglucemia.
Treatment of diabetes mellitus type2 (DM2) includes healthy eating and exercise (150minutes/week) as basic pillars. For pharmacological treatment, metformin is the initial drug except contraindication or intolerance; in case of poor control, 8 therapeutic families are available (6 oral and 2 injectable) as possible combinations. An algorithm and some recommendations for the treatment of DM2 are presented. In secondary cardiovascular prevention, it is recommended to associate an inhibitor of the sodium-glucose cotransporter type 2 (iSGLT2) or a glucagon-like peptide-1 receptor agonist (arGLP1) in patients with obesity. In primary prevention if the patient is obese or overweight metformin should be combined with iSGLT2, arGLP1, or inhibitors of type4 dipeptidylpeptidase (iDPP4). If the patient does not present obesity, iDPP4, iSGLT2 or gliclazide, sulfonylurea, recommended due to its lower tendency to hypoglycaemia, may be used.
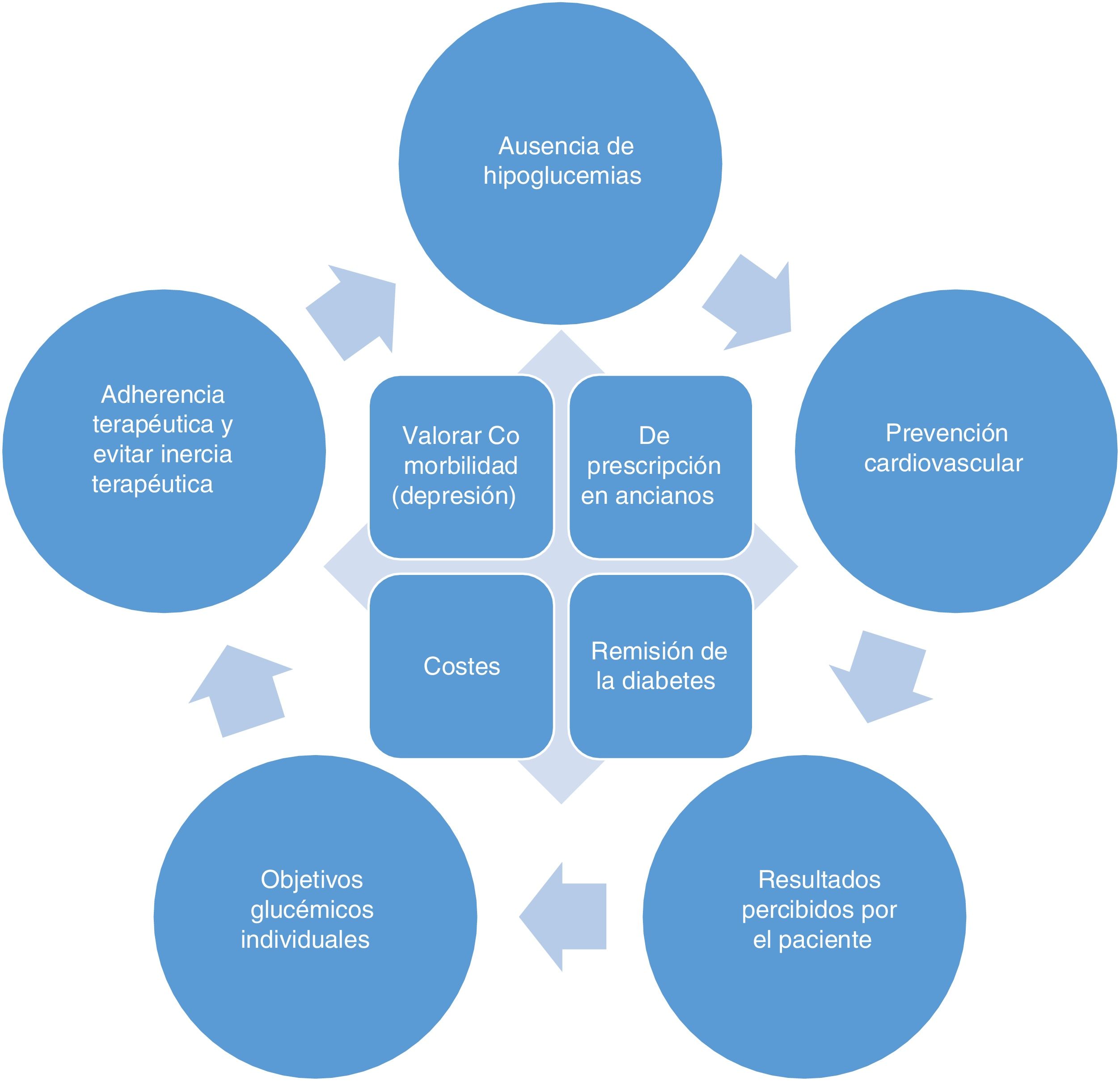
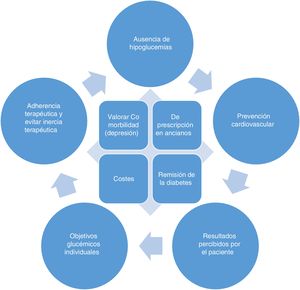
En la mayoría de las personas con diabetes tipo2 (DM2) el objetivo del tratamiento no es solo evitar síntomas, sino prevenir la aparición de complicaciones a medio/largo plazo, por lo que el paciente puede no percibir los beneficios del tratamiento, salvo la reducción de peso (en los fármacos que la producen) o la consecución de los objetivos de control. En la figura 1 se describen unos principios generales que deben tenerse en cuenta en el tratamiento de la diabetes. Aunque el presente documento se centra en el manejo de la hiperglucemia, se recomienda un abordaje integral de todos los factores de riesgo, centrado en las necesidades y preferencias del paciente mediante una toma de decisiones compartida, siguiendo las recomendaciones del Chronic Care Model1,2.
Los costes de la diabetes vienen condicionados en un 40-60% por los ingresos hospitalarios y en un 18% por los medicamentos3; en igualdad de beneficio y seguridad, debe emplearse el fármaco de menor coste.
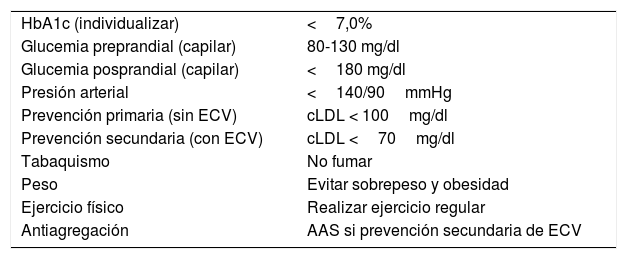
Objetivos de controlEn la tabla 1 se describen los objetivos de control glucémico en personas con diabetes4,5. Se deben tratar por objetivos, consensuados con el paciente, individualizándolos6 mediante el uso de herramientas prácticas como la aplicación A1c calculator (app A1CCalc), que puede ser utilizada desde dispositivos móviles. La falta de adherencia y la inercia terapéutica son las principales causas de falta de control7. Se recomienda valorar la adherencia8,9 de forma periódica y siempre antes de intensificar el tratamiento, y aplicar medidas para superar la falta de adherencia y la inercia.
Objetivos de control glucémico y de los factores de riesgo cardiovascular en pacientes con diabetes
| HbA1c (individualizar) | <7,0% |
| Glucemia preprandial (capilar) | 80-130 mg/dl |
| Glucemia posprandial (capilar) | <180 mg/dl |
| Presión arterial | <140/90mmHg |
| Prevención primaria (sin ECV) | cLDL < 100mg/dl |
| Prevención secundaria (con ECV) | cLDL <70mg/dl |
| Tabaquismo | No fumar |
| Peso | Evitar sobrepeso y obesidad |
| Ejercicio físico | Realizar ejercicio regular |
| Antiagregación | AAS si prevención secundaria de ECV |
AAS: ácido acetilsalicílico; ECV: enfermedad cardiovascular.
Adaptado de Guía de la Sociedad Americana de Diabetes 2019 y Recomendaciones del programa PAPPS de la Semfyc4,5.
La dieta y el ejercicio son pilares fundamentales del tratamiento en cualquier fase de la enfermedad. Estas medidas deberían iniciarse en pacientes con prediabetes, ya que pueden reducir la incidencia de diabetes en un 50%. La remisión de la diabetes, definida como una HbA1c<6,5% tras 2meses sin medicación antidiabética, es posible tras programas intensivos con dieta y ejercicio en pacientes con DM2 de pocos años de evolución, así como tras la cirugía metabólica10.
La tabla 2 recoge las principales recomendaciones sobre alimentación, ejercicio y hábitos tóxicos para priorizar en las personas con DM211,12.
Resumen de las principales recomendaciones sobre estilos de vida saludables a priorizar en las personas con diabetes tipo 2 (sistema GRADE)
| Recomendaciones | Calidad de la evidencia | Fuerza de la recomendación |
|---|---|---|
| La dieta es un componente esencial para el tratamiento de la DM2 y para su prevención | Alta | Fuerte a favor |
| La dieta mediterránea es la que más evidencias tiene en estos momentos en la prevención de eventos cardiovasculares en DM2 | Alta | Fuerte a favor |
| Las dietas bajas en hidratos de carbono, dietas con bajo índice glucémico, la dieta mediterránea y dietas con alto contenido en proteínas han demostrado mejoría en el control glucémico | Alta | Fuerte a favor |
| Se aconseja tener en cuenta las preferencias de las personas con DM2. Se pueden ofrecer como opción las dietas con bajo índice glucémico, bajo índice en hidratos de carbono y dietas altas en proteínas | Moderada | A favor |
| La reducción de la ingesta calórica y la pérdida de peso moderado (5-7%) mejoran la resistencia a la insulina y la glucemia a corto plazo | Alta | Fuerte a favor |
| Los adultos con DM2 deben realizar como mínimo 150min de actividad física aeróbica de moderada intensidad a la semana, en días alternos y en, por lo menos, 3 sesiones semanales | Alta | Fuerte a favor |
| En combinación con el ejercicio aeróbico, los pacientes con DM2 deberán realizar 2 o 3 entrenamientos semanales de fuerza muscular, a intensidad moderada o alta | Alta | Fuerte a favor |
| Debe recomendarse a todos los pacientes con DM2 el abandono del hábito tabáquico en cualquiera de sus formas | Alta | Fuerte a favor |
Modificado de las recomendaciones de la Fundación redGDPS12,13.
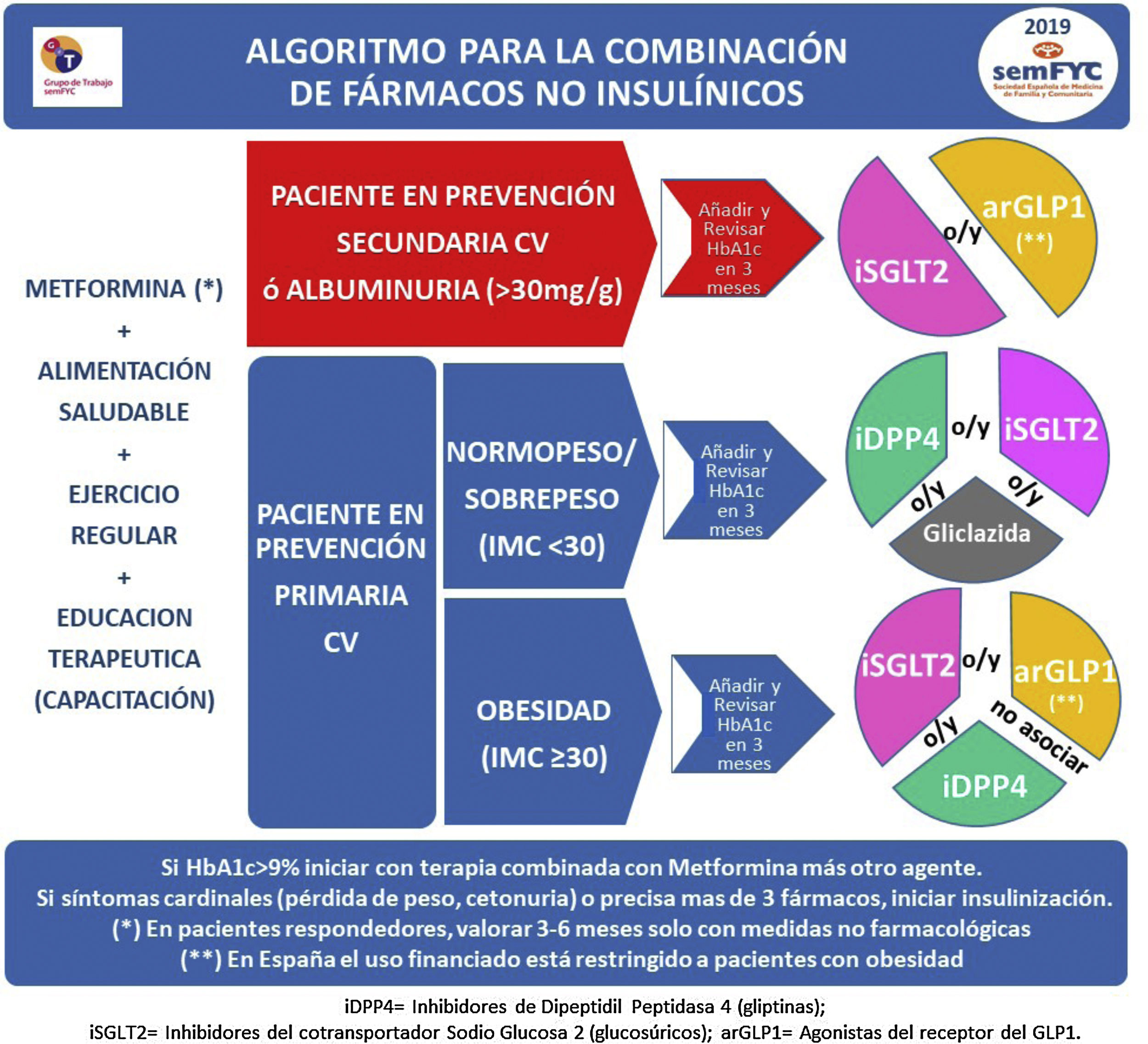
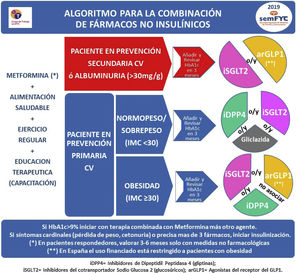
En la figura 2 se describe el algoritmo terapéutico de inicio y de combinación en doble y/o triple terapia de los diferentes fármacos no insulínicos.
MonoterapiaLa DM2 no tiene un inicio agudo, y los pacientes pueden estar sometidos a una situación hiperglucémica asintomática durante años antes de ser diagnosticados. Por ello, y por la dificultad del mantenimiento de cambios del estilo de vida, se recomienda en la mayoría de los pacientes prescribir conjuntamente, desde el momento del diagnóstico, un tratamiento farmacológico junto con los cambios en los estilos de vida. No obstante, si se considera que el paciente pueda ser muy adherente a las recomendaciones sobre dieta y ejercicio y los niveles de HbA1c no son muy elevados (<8%), se puede valorar la eficacia de una terapia de inicio exclusivamente no farmacológica durante 3-6meses (fig. 2).
El fármaco de inicio es la metformina, salvo contraindicación o intolerancia (fig. 2), por su seguridad, economía, efecto sobre el peso y eficacia hipoglucemiante13,14. La contraindicación más importante para su uso es un filtrado glomerular estimado (FGe)<30ml/min/1,73m215, debiéndose reducir la dosis a la mitad (850-1.000mg/día) cuando el FGe sea de 30-45ml/min/1,73m2. El efecto adverso más frecuente es gastrointestinal (dolor abdominal, diarrea y flatulencia), y puede minimizarse titulando la dosis. En pacientes en tratamiento crónico con metformina debe valorarse también si existe déficit de vitaminaB12 y suplementarse si estuviera disminuida16. Aunque la acidosis láctica es un efecto adverso muy poco frecuente, por su gravedad se aconseja suspender la toma de metformina 48h antes de una intervención quirúrgica17; en la administración de contraste yodado intravenoso, suspender la administración de metformina la mañana del procedimiento y no reiniciar hasta que se demuestre un FGe estable, generalmente 48h después del procedimiento18.
En caso de contraindicación o intolerancia a la metformina se empleará alguno de los fármacos de segunda línea en función de las características del paciente (fig. 2).
Si en el momento del diagnóstico la HbA1c es mayor del 9% o 1,5 puntos sobre el objetivo individualizado, se recomienda iniciar terapia combinada con metformina más otro fármaco1,19. La terapia combinada de inicio puede aportar una mayor durabilidad del control glucémico frente a la terapia escalonada20,21.
Si en el momento del diagnóstico el paciente presenta síntomas cardinales (polidipsia, polifagia, pérdida de peso, cetonuria), se recomienda iniciar el tratamiento con insulina, que puede ser transitorio o definitivo en función de la evolución.
Tras el inicio o cambios en el tratamiento, se debe solicitar una HbA1c a los 3meses para valorar la consecución de los objetivos individualizados; una vez alcanzados, se recomienda seguimiento mediante HbA1c cada 6meses.
Terapia combinada con dos fármacosSi con monoterapia no se alcanza el objetivo de control y la adherencia es buena, se debe añadir un segundo fármaco. Es preferible la asociación de dos fármacos que aumentar metformina por encima de 2.000mg, pues se incrementan los efectos adversos sin mejorar la eficacia.
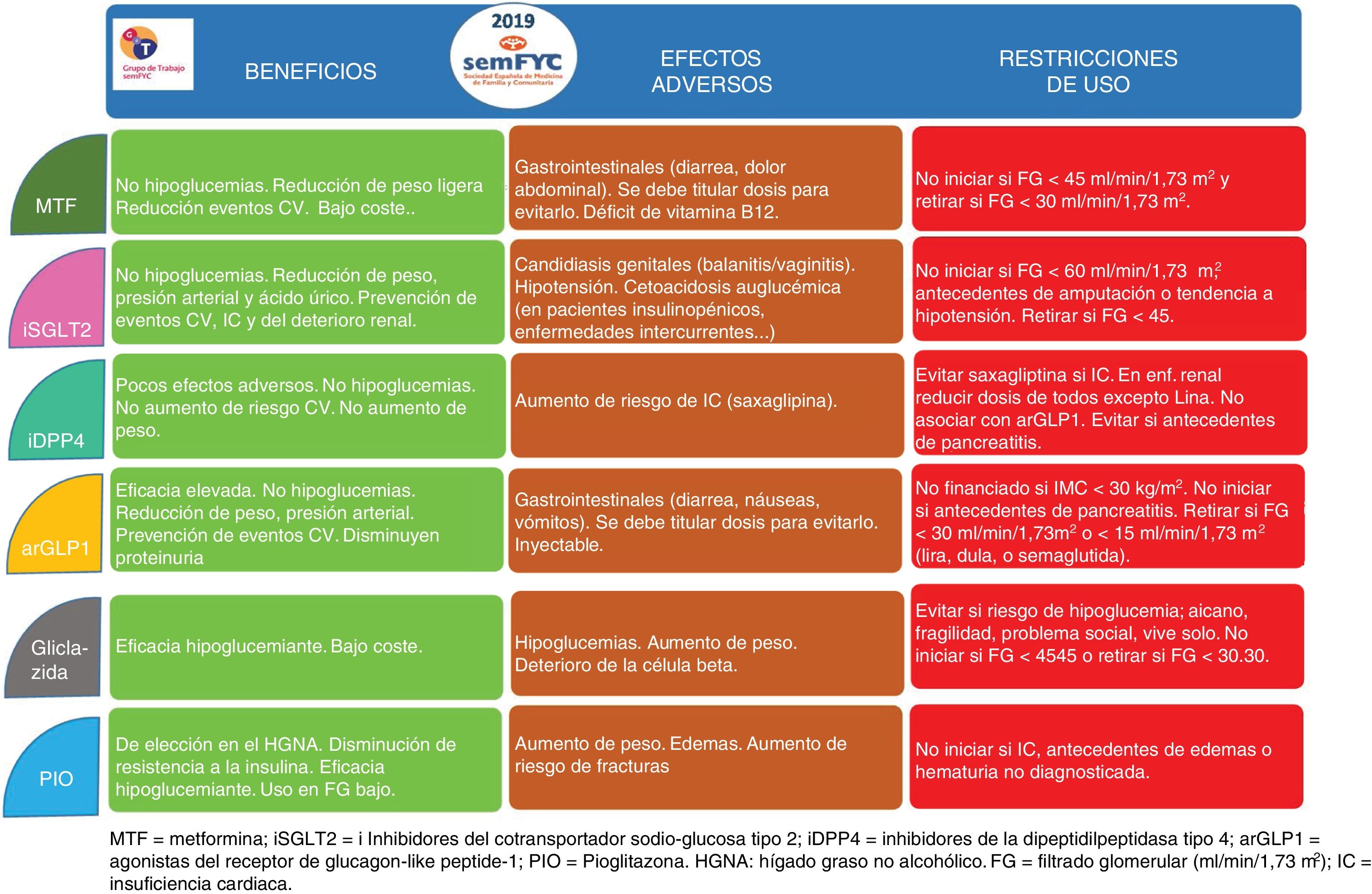
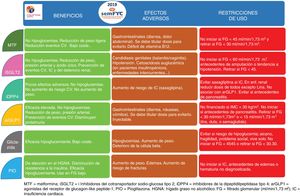
Existen 8 familias terapéuticas (6 orales y 2 inyectables) como posibles combinaciones, por lo que es aconsejable usar algoritmos que faciliten la toma de decisiones (fig. 2). En la figura 3 se describen las características de los principales fármacos no insulínicos. Los principales factores que condicionan la elección de la terapia que se añadirá a la metformina son la presencia de complicaciones cardiovasculares (prevención secundaria), la presencia de obesidad o sobrepeso, evitar la aparición de hipoglucemias y el estado de la función renal (figs. 1 y 2).
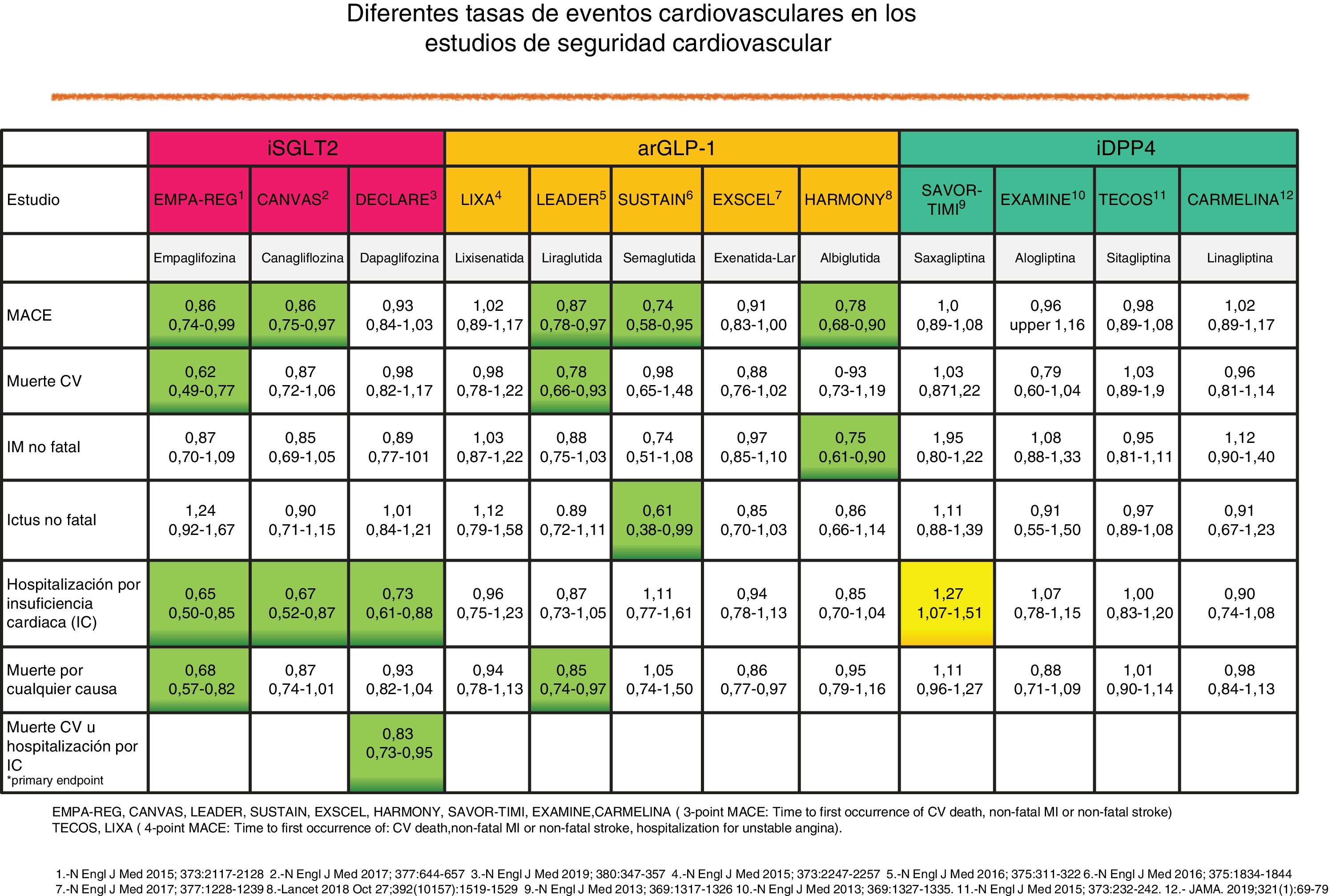
En pacientes en prevención secundaria cardiovascular (CV) debe asociarse preferentemente a fármacos con eficacia demostrada en prevención de eventos CV, bien los inhibidores del cotransportador sodio-glucosa tipo2 (iSGLT2) o los agonistas del receptor de glucagon-like peptide-1 (arGLP1) en pacientes con obesidad22. Estos fármacos reducen, además de la glucemia, la presión arterial y el peso, por lo que presentan un perfil de acción integral muy adecuado. En la figura 4 se describen los principales resultados de los estudios de prevención CV con fármacos antidiabéticos no insulínicos.
En prevención primaria CV, si el paciente presenta obesidad deberán priorizarse combinaciones con fármacos que reduzcan el peso, como los iSGLT2 o arGLP1, o al menos que no lo incrementen, como los inhibidores de la dipeptidilpeptidasa tipo4 (iDPP4). Si el paciente no presenta obesidad, podrán emplearse los iDPP4, los iSGLT2 o la gliclazida, sulfonilurea recomendada por su menor tendencia a la hipoglucemia23, respecto a otras sulfonilureas y glinidas.
Los iSGLT2 actúan inhibiendo la reabsorción de glucosa y sodio en el túbulo contorneado proximal del riñón ocasionando glucosuria y natriuresis. Reducen la HbA1c en torno al 1%. Además, inducen pérdida de peso y descenso de la presión arterial sistólica y diastólica. Empagiflozina13 y canagliflozina14 reducen el objetivo compuesto de muerte CV o ingreso hospitalario por cardiopatía isquémica o ictus. Empagiflozina13, canagliflozina14 y dapagliflozina24 reducen el riesgo de insuficiencia cardiaca y el de hospitalización por IC, así como el de progresión de enfermedad renal o incidencia de eventos renales. Debe tenerse en cuenta que en España los iSGLT2 no pueden iniciarse en pacientes con un filtrado glomerular (FG)<60ml/min/1,73m2 según ficha técnica25, no por seguridad sino por menor eficacia. No obstante, pueden ser útiles en pacientes con riesgo de progresión de enfermedad renal (p.ej., pacientes con albuminuria).
Su efecto adverso más frecuente son las infecciones micóticas (vaginitis, balanitis); en caso de aparecer, deben tratarse, y valorar de acuerdo con el paciente la sustitución del fármaco si son recidivantes. Su uso en pacientes frágiles y/o con riesgo de hipovolemia debe realizarse con precaución para evitar episodios de hipotensión (p.ej., ancianos). Cuando los iSGLT2 se usen en combinación con insulina o sulfonilurea se recomienda valorar la reducción de la dosis para disminuir el riesgo de hipoglucemia.
Los iSGLT2 están indicados en monoterapia en los pacientes con DM2 intolerantes a metformina o en los que esta esté contraindicada y presenten mal control con dieta y ejercicio. En terapia combinada pueden utilizarse junto a cualquier otro hipoglucemiante, incluyendo insulina. Como población de mayor interés para el uso de estos fármacos podrían destacarse los pacientes en prevención secundaria CV o con albuminuria o con insuficiencia cardiaca o en riesgo de padecerla, o en prevención primaria en pacientes con sobrepeso/obesidad que precisen un descenso conjunto de HbA1c, peso y presión arterial26.
Los arGLP1 son péptidos de acción similar al GLP1 endógeno producido a nivel intestinal y en otros órganos, que estimulan la producción de insulina por el páncreas, pero dependiente del nivel de glucemia, por lo que no producen hipoglucemias. También actúan inhibiendo la secreción de glucagón por la célula alfa e inhibiendo la gluconeogénesis. Aumentan la sensación de saciedad, por enlentecimiento del vaciado gástrico y acción sobre el sistema nervioso central. Se administran por vía subcutánea a dosis fija, previa titulación inicial, y a diferencia de la insulina, no precisan autoanálisis glucémico capilar ni ajuste de dosis. Los efectos adversos más frecuentes al inicio son gastrointestinales (náuseas, vómitos, diarreas), que suelen disminuir con el tiempo y pueden disminuirse titulando la dosis inicial. Reducen la HbA1c en torno al 1-2%. Inducen pérdida de peso y descenso de la presión arterial sistólica y diastólica. Son fármacos muy potentes en la reducción de HbA1c, incluso superando a la insulina, reduciendo peso y sin riesgo de hipoglucemia. En los pacientes que se precise terapia inyectable los arGLP1 serán de elección2. Hasta la fecha, solo liraglutida12 y semaglutida13 han demostrado en pacientes en prevención secundaria reducir el objetivo compuesto (MACE) de muerte CV o ingreso hospitalario por cardiopatía isquémica o ictus. Dulaglutida tiene previsto publicar resultados en breve (REWIND trial). Liraglutida se administra diariamente, mientras dulaglutida, exenatida-Lar y semaglutida son de administración semanal.
Exenatida y lixisenatida deberán suspenderse cuando el FGe se encuentre por debajo de 30ml/min/1,73m2; exenatida-Lar puede usarse hasta 50ml/min/1,73m2; dulaglutida, semaglutida y liraglutida, hasta 15ml/min/1,73m2.
En España su prescripción requiere la necesidad de visado, que autoriza su uso financiado solo en pacientes con obesidad (IMC>30kg/m2).
Liraglutida, dulaglutida y albiglutida están indicados en monoterapia en pacientes con DM2 intolerantes o con contraindicación a la metformina que presenten mal control con dieta y ejercicio. En terapia combinada, pueden utilizarse junto a cualquier otro hipoglucemiante oral, salvo los iDPP4, y pueden utilizarse con insulina basal.
Como población de mayor interés para el uso de estos fármacos podrían destacarse los pacientes con obesidad, bien en prevención secundaria CV o bien en prevención primaria que precisen un descenso conjunto de HbA1c, peso y presión arterial, así como en pacientes obesos con albuminuria.
Los iDPP4 inhiben la degradación de las incretinas intestinales (GLP1) por la enzima dipeptidil peptidasa4 (DPP4), favoreciendo la acción incretínica y estimulando la producción de insulina por el páncreas dependiente de la glucosa, por lo que no producen hipoglucemias. Su eficacia en la reducción de HbA1c es alrededor del 0,7% y son neutros en cuanto a modificación del peso o la presión arterial. Se administran por vía oral una vez al día (salvo vildagliptina, dos veces al día). Son fármacos bien tolerados y con pocos efectos adversos. Salvo linagliptina, precisan ajuste de dosis en caso de FGe por debajo de 45ml/min/1,73m2 (vildagliptina <50ml/min/1,73m2). Son fármacos seguros desde el punto de vista CV. El estudio TECOS27 con sitagliptina ha demostrado que no hay un aumento del riesgo CV, al igual que los estudios con alogliptina, linagliptina y saxagliptina28-30. Sin embargo, en el SAVOR-TIMI con saxagliptina se observó un incremento de riesgo de hospitalización por insuficiencia cardiaca30. Los iDPP4 están indicados en monoterapia en los pacientes con DM2 intolerantes a metformina o en los que esta esté contraindicada y presenten mal control con dieta y ejercicio. En terapia combinada pueden utilizarse junto a cualquier otro hipoglucemiante, incluyendo insulina, salvo con arGLP1, por compartir mecanismo de acción y no mejorar la eficacia. Como población de mayor interés para el uso de estos fármacos podrían destacarse los pacientes en prevención primaria CV, o con riesgo de hipoglucemia (personas mayores, insuficiencia renal, paciente frágil).
Las sulfonilureas y glinidas estimulan la secreción de insulina por el páncreas a través del cierre de los canales de potasio de forma independiente del nivel glucémico. Debe evitarse el uso de glibenclamida por el mayor riesgo de hipoglucemia y el de las glinidas por la peor adherencia terapéutica al tener que administrarse tres veces al día. Gliclazida es la sulfonilurea de elección en base a su perfil de seguridad y evidencias disponibles31,32.
El estudio ADVANCE23 demostró que el control glucémico intensivo con gliclazida redujo la incidencia de nefropatía (HR: 0,79; IC95%: 0,66-0,93), aunque no hubo beneficio en la reducción de eventos CV (HR: 0,94; IC95%: 0,84-1,06) o mortalidad CV o total (HR: 0,93; IC95%: 0,83-1,06).
Entre los efectos adversos más frecuentes destacan la hipoglucemia y el aumento de peso. Se ha descrito un posible incremento de riesgo CV probablemente más ligado a las sulfonilureas de primera generación33. No se recomienda su uso en pacientes con hipoglucemias previas, ancianos, pacientes que viven solos, pacientes en prevención secundaria CV, y debe tenerse precaución en pacientes tratados con insulina o pacientes que presentan insuficiencia renal. Pueden usarse en monoterapia en los pacientes con DM2 que presenten mal control con dieta y ejercicio. En terapia combinada pueden utilizarse junto a cualquier otro hipoglucemiante, incluyendo insulina, aunque debe tenerse en cuenta el incremento del riesgo de hipoglucemias. Como población de mayor interés para el uso de estos fármacos podrían destacarse los pacientes en prevención primaria CV, con normopeso, varones34, sin riesgo de hipoglucemias35, o diabetes con pocos años de evolución, donde son fármacos con una buena relación coste/eficacia.
Las glinidas no son un tratamiento para priorizar, pues comparten los inconvenientes de las sulfonilureas y la necesidad de tres tomas al día, lo que dificulta la adherencia terapéutica. En casos en que otras alternativas no sean útiles o posibles y predomine la hiperglucemia posprandial, la repaglinida puede ser de utilidad. En presencia de insuficiencia renal no precisan ajuste dosis, pero su vida media aumenta con FGe<30ml/min/1,73m2.
La pioglitazona es un fármaco excelente para reducir la resistencia a la insulina a nivel hepático y en tejido adiposo y muscular (pacientes con síndrome metabólico). Aunque se puede utilizar en monoterapia, su uso es preferible en asociación con insulina, para disminuir las dosis de esta, o con ISGLT2 o arGLP1. Se recomienda usar dosis no mayores de 15mg. Entre sus beneficios destaca la prevención CV (prevención del ictus y posiblemente en demencia) y su mayor durabilidad en el mantenimiento del control metabólico a largo plazo respecto a las sulfonilureas36-38. En prevención secundaria CV reduce la incidencia de eventos CV pero no el de mortalidad total, y aumenta el riesgo de insuficiencia cardiaca39. Entre sus inconvenientes estarían el aumento de peso y la contraindicación en pacientes con insuficiencia cardiaca. Está especialmente indicada en pacientes con esteatosis hepática no alcohólica. En pacientes con síndrome metabólico puede ser una opción eficaz ante el fracaso de otras opciones.
La acarbosa y el miglitol están en desuso debido a su menor eficacia, a la necesidad de tres tomas al día y a sus efectos adversos gastrointestinales.
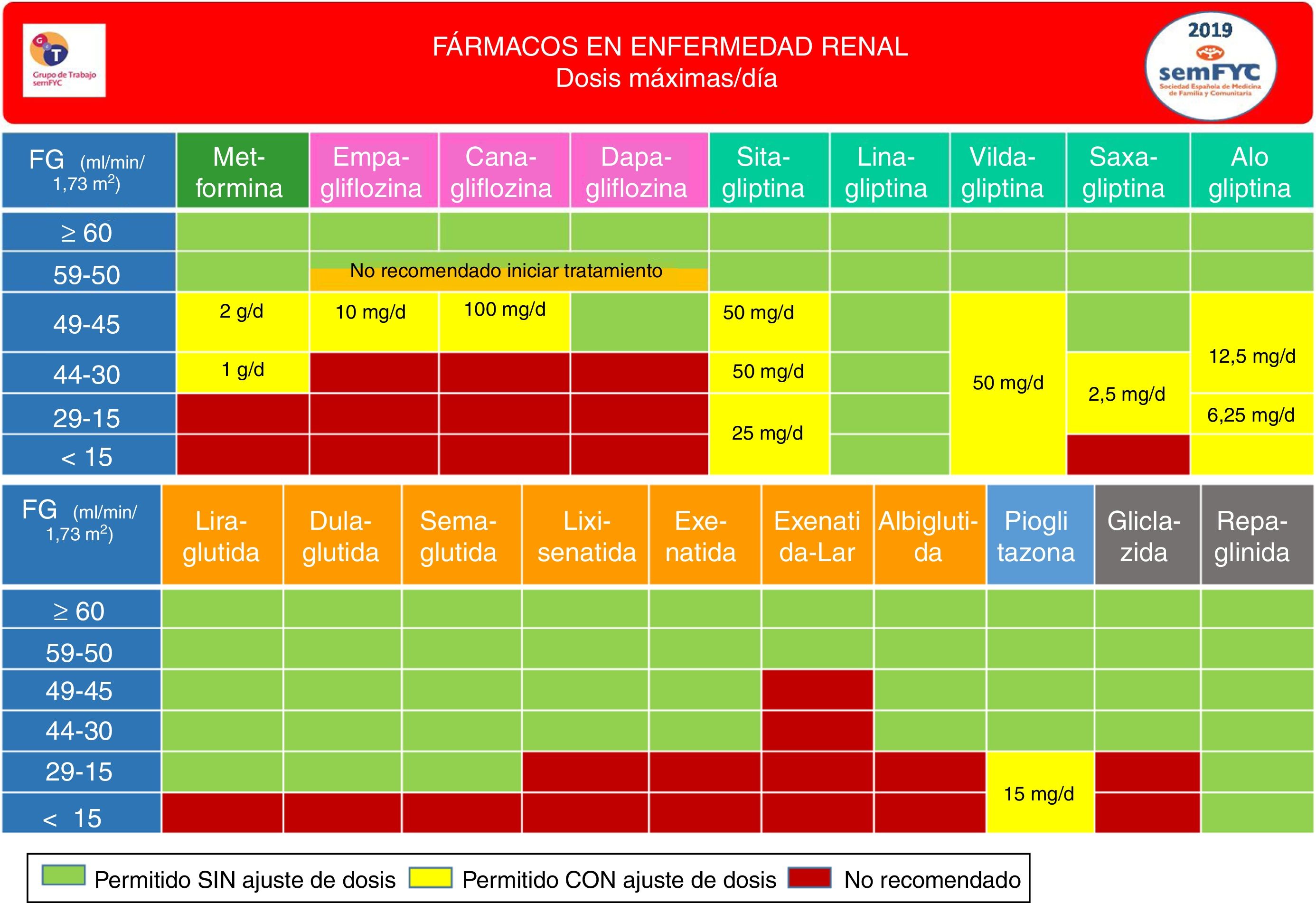
En la tabla 3 se presentan las evidencias para las recomendaciones de tratamiento de la DM2 (sistema GRADE). En la figura 5 se describe el uso de fármacos y el ajuste de dosis en pacientes con filtrado glomerular reducido.
Evidencias para las recomendaciones de tratamiento de la diabetes tipo 2 (sistema GRADE)
| Recomendaciones | Calidad de la evidencia | Fuerza de la recomendación |
|---|---|---|
| Metformina debe emplearse como el primer fármaco de elección en el tratamiento de la diabetes tipo 2 | Alta | Fuerte a favor |
| Metformina debe mantenerse en todas las combinaciones, incluyendo insulina, salvo contraindicación o intolerancia | Alta | Fuerte a favor |
| En prevención secundaria cardiovascular los fármacos de elección son los iSGLT2 (empaglifozina, canaglifozina) y los arGLP1 (liraglutida, semaglutida) | Alta | Fuerte a favor |
| Se recomienda priorizar el uso de fármacos de dosis única diaria, así como las terapias combinadas a dosis fijas, porque facilitan la adherencia terapéutica | Alta | Fuerte a favor |
La triple terapia seguiría las mismas recomendaciones realizadas anteriormente. Así, en pacientes en prevención secundaria CV se recomienda priorizar la triple asociación de metformina, iSGLT2 y arGLP1. En prevención primaria CV con obesidad se recomendaría priorizar metformina +iSGLT2 +iDPP4, o bien la misma asociación anteriormente comentada. En pacientes sin obesidad ni eventos CV metformina +gliclazida +iDPP4 puede ser una buena combinación si el paciente no presenta riesgo de hipoglucemia. La única asociación contraindicada es la de iDPP4 con arGLP1. No se recomienda asociar más de tres fármacos no insulínicos, dado que no existe evidencia actual que avale su beneficio.
InsulinizaciónSi no se consiguen lo objetivos de control glucémico con tres fármacos no insulínicos, debería considerarse iniciar la insulinización. No obstante, en pacientes con obesidad (IMC>30), si no se ha empleado un arGLP1, se recomienda su uso antes de iniciar la insulina40,41.
La insulinización requiere impartir medidas de educación terapéutica tanto al paciente como a sus familiares. Para ello, se trabajará juntamente con enfermería, principal responsable de la educación terapéutica, revisando la técnica de inyección, la monitorización de la glucemia, el ajuste de dosis, el almacenamiento de insulina, el reconocimiento y tratamiento de la hipoglucemia y las recomendaciones en caso de enfermedad intercurrente u otras situaciones especiales.
La insulina debe ser un fármaco de elección en los siguientes supuestos:
- •
De forma transitoria en el momento del diagnóstico, si el paciente presenta sintomatología cardinal y pérdida de peso, y/o cifras muy elevadas de glucemia (>300mg/dl; HbA1c>10%)4, reevaluando posteriormente la posibilidad del paso a medicación no insulínica si las necesidades de insulina basal son inferiores a 20U/día. También puede ser necesaria la insulinización transitoria en algunas circunstancias o episodios intercurrentes (enfermedad febril, tratamiento con corticoides, cirugía mayor, embarazo, hospitalizaciones…).
- •
De forma permanente cuando sea necesaria para alcanzar y mantener un adecuado control glucémico42. Se recomienda mantener el tratamiento con metformina, iDPP4, arGLP1 o con iSGLT2 si el paciente ya los estaba tomando, y vigilar la evolución de pacientes tratados con pioglitazona, por el mayor riesgo de edemas. Respecto a las sulfonilureas, si se retiran, es importante explicar al paciente que puede experimentar un empeoramiento del control glucémico hasta la titulación adecuada de la insulina basal; si se mantienen, se aconseja reducir su dosis por el riesgo de hipoglucemia. En cualquier caso, las sulfonilureas/secretagogos sí deben suspenderse cuando se utilice insulina rápida o mezclas43.
La presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de interesesLos autores declararan no tener conflictos de intereses en relación con la redacción de este documento. Las recomendaciones incluidas en el mismo se basan en la evidencia científica y en la experiencia y el consenso de los autores.