Las vacunas constituyen un instrumento esencial para la prevención de enfermedades infecciosas. Sin embargo, las falsas ideas y rumores sin fundamento científico sobre eventuales efectos negativos pueden disuadir de la vacunación, con los consiguientes riesgos para la protección de la población. El objetivo del artículo es evaluar el origen y los argumentos de algunos de los errores y rumores más frecuentes sobre eventuales efectos adversos de las vacunaciones. Se presentan algunos efectos adversos claramente establecidos, así como falsas creencias sobre diversas vacunas y potenciales daños para la salud. Las vacunas, como cualquier fármaco, pueden ocasionar efectos adversos, pero los eventuales efectos adversos de los programas de vacunación son claramente inferiores a sus beneficios individuales (a los vacunados) y colectivos (a los vacunados y a los que no pueden vacunarse por razones médicas). Cualquier efecto indeseable atribuible a las vacunas ha de poderse detectar mediante sistemas de farmacovigilancia potentes y bien estructurados.
Vaccines are an essential tool for the prevention of infectious diseases. However, false ideas and rumours with no scientific foundation about their possible negative effects may dissuade people from being vaccinated, with the consequent risks for the health of the population. The objective of this article is to evaluate the origin and the arguments of some of the most frequent mistaken ideas and rumours about the possible adverse effects of vaccines. Some clearly established adverse effects are presented, as well as false beliefs about various vaccines and potential harm to health. Vaccines, like any drug, can cause adverse effects, but the possible adverse effects of vaccination programs are clearly lower than their individual (vaccinated) and collective benefits (those vaccinated and those who cannot be vaccinated for medical reasons). The possible adverse effects attributable to vaccines should be detected by powerful and well-structured pharmacovigilance systems.
Las vacunas se encuentran entre los mayores logros de la salud pública a lo largo de la historia, previniendo miles de enfermedades y muertes cada año. Sin embargo, a medida que la enfermedad, la discapacidad y la muerte por enfermedades inmunoprevenibles han disminuido —gracias sobre todo al impacto de los programas de vacunación— ha aumentado, por el contrario, la preocupación sobre la seguridad de las vacunas. Aunque es mucho más probable que una persona se vea afectada por una enfermedad inmunoprevenible que por el efecto de una vacuna, algunas personas deciden no vacunarse o no vacunar a sus hijos con las vacunas recomendadas debido a percepciones inadecuadas sobre el riesgo de enfermar o la seguridad vacunal1,2.
Ciertamente la historia de las vacunas muestra acontecimientos adversos relacionados con la seguridad de las vacunas; algunos se han confirmado y la gran mayoría, a partir de las sospechas o asociaciones iniciales, han sido descartados tras las investigaciones realizadas.
Un primer ejemplo es el «incidente Cutter», ocurrido en 19553, meses después de que Jonas Salk descubriera la primera vacuna inactivada contra la polio y se iniciara en Estados Unidos el primer programa de vacunación masiva contra esta enfermedad. La poliomielitis era en aquel momento un grave problema de salud pública por las epidemias que producía, llegándose a considerar como la segunda preocupación para los americanos tras la bomba atómica. Algunos lotes de la vacuna fueron mal fabricados y contenían virus vivos en lugar de los virus inactivados descritos en el protocolo de Salk. A pesar de haber superado las pruebas de seguridad requeridas, se produjeron más de 40.000 casos de polio, 250 casos de polio paralítica y 10 fallecimientos atribuidos a vacunas producidas en una empresa familiar (Cutter Laboratories), mientras que las vacunas fabricadas por otros laboratorios no ocasionaron problemas. La vacuna fue retirada tras la detección de los primeros casos de polio. Este incidente fue decisivo en la historia de la fabricación de vacunas, ya que se establecieron modificaciones sustanciales en la supervisión gubernamental de las vacunas con reglas estrictas en los protocolos, mejora de los sistemas de seguridad en la fabricación y desarrollo de la vigilancia epidemiológica. Tras estas correcciones se reanudó la vacunación contra la polio.
En 1976, tras la administración en Estados Unidos de una vacuna contra la gripe estacional, se detectó un aumento del riesgo de síndrome de Guillain-Barré. El riesgo fue aproximadamente de un caso de síndrome de Guillain-Barré por cada 100.000 personas que habían recibido la vacuna. El Instituto de Medicina de los Estados Unidos llevó a cabo una exhaustiva revisión científica y concluyó que las personas que recibieron la vacuna contra la gripe tuvieron un mayor riesgo de desarrollar síndrome de Guillain-Barré. Existen múltiples teorías, pero la razón exacta de esta asociación sigue siendo desconocida4. En la actualidad se monitoriza continuamente la seguridad de las vacunas de gripe.
Más recientemente se ha asociado la vacuna pandémica antigripal (Pandemrix®) con narcolepsia. Estudios epidemiológicos de diferentes países (Finlandia, Suecia, Noruega, Inglaterra, Francia, Irlanda, Canadá) han mostrado un aumento en el riesgo de padecer narcolepsia en niños y adultos a los que se les había administrado la vacuna pandémica comparado con personas no vacunadas del mismo grupo de edad5,6. Se ha sugerido una asociación entre un determinado haplotipo y los componentes antigénicos de la vacuna, el adyuvante o ambos, si bien se requieren más estudios para verificar la hipótesis de la susceptibilidad genética.
En 1998, la agencia estadounidense Food and Drug Administration (FDA) aprobó la vacuna RotaShield®, la primera vacuna para prevenir la gastroenteritis por rotavirus. Poco después de su licencia, algunos bebés desarrollaron intususcepción intestinal después de la vacunación. Al principio no estaba claro si la vacuna o algún otro factor estaban causando las obstrucciones intestinales. Los Centers for Disease Control and Prevention (CDC) de los Estados Unidos rápidamente recomendaron suspender el uso de la vacuna e iniciar inmediatamente dos investigaciones de urgencia para averiguar si la vacuna estaba causando algunos de los casos de intususcepción. Las investigaciones mostraron que la vacuna había causado intususcepción en algunos bebés sanos menores de 12 meses de edad que normalmente tendrían un bajo riesgo de tener esta enfermedad. El Comité Asesor sobre Prácticas de Inmunización retiró su recomendación de vacunar a los lactantes con la vacuna RotaShield® y el fabricante la retiró voluntariamente del mercado en octubre de 19997.
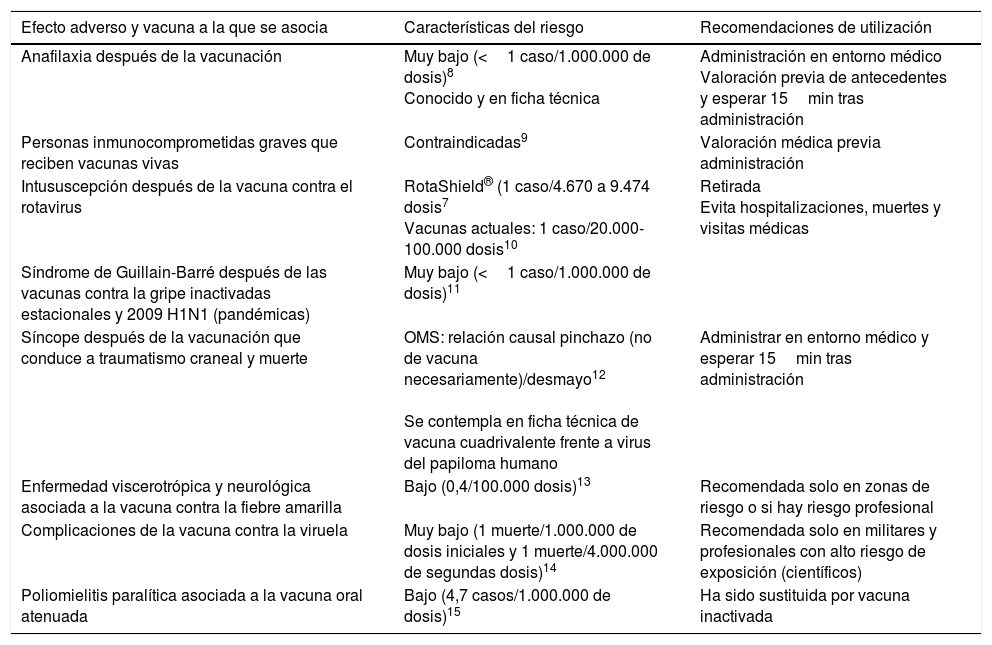
Algunos efectos adversos asociados a la vacunación para los que existe una evidencia científica están recogidos en la ficha técnica de la vacuna correspondiente: anafilaxia, intususcepción después de la vacuna contra el rotavirus, Síndrome de Guillain-Barré después de las vacunas contra la gripe inactivadas estacionales y pandémicas, síncope tras la vacunación en adolescentes, enfermedad viscerotrópica y neurológica tras la vacunación contra la fiebre amarilla o poliomielitis paralítica asociada a la vacuna oral contra la polio, entre otros8-16. En todos estos casos se ha estimado el riesgo y se han establecido unas recomendaciones de utilización dependientes de la situación epidemiológica de cada enfermedad y de la posibilidad o no de disponer de otra vacuna (tabla 1).
Efectos adversos asociados a determinadas vacunas y recomendaciones para su utilización
| Efecto adverso y vacuna a la que se asocia | Características del riesgo | Recomendaciones de utilización |
|---|---|---|
| Anafilaxia después de la vacunación | Muy bajo (<1 caso/1.000.000 de dosis)8 Conocido y en ficha técnica | Administración en entorno médico Valoración previa de antecedentes y esperar 15min tras administración |
| Personas inmunocomprometidas graves que reciben vacunas vivas | Contraindicadas9 | Valoración médica previa administración |
| Intususcepción después de la vacuna contra el rotavirus | RotaShield® (1 caso/4.670 a 9.474 dosis7 Vacunas actuales: 1 caso/20.000-100.000 dosis10 | Retirada Evita hospitalizaciones, muertes y visitas médicas |
| Síndrome de Guillain-Barré después de las vacunas contra la gripe inactivadas estacionales y 2009 H1N1 (pandémicas) | Muy bajo (<1 caso/1.000.000 de dosis)11 | |
| Síncope después de la vacunación que conduce a traumatismo craneal y muerte | OMS: relación causal pinchazo (no de vacuna necesariamente)/desmayo12 Se contempla en ficha técnica de vacuna cuadrivalente frente a virus del papiloma humano | Administrar en entorno médico y esperar 15min tras administración |
| Enfermedad viscerotrópica y neurológica asociada a la vacuna contra la fiebre amarilla | Bajo (0,4/100.000 dosis)13 | Recomendada solo en zonas de riesgo o si hay riesgo profesional |
| Complicaciones de la vacuna contra la viruela | Muy bajo (1 muerte/1.000.000 de dosis iniciales y 1 muerte/4.000.000 de segundas dosis)14 | Recomendada solo en militares y profesionales con alto riesgo de exposición (científicos) |
| Poliomielitis paralítica asociada a la vacuna oral atenuada | Bajo (4,7 casos/1.000.000 de dosis)15 | Ha sido sustituida por vacuna inactivada |
Fuente: modificado de Miller et al.16.
La posible asociación entre la vacunación y la muerte también ha sido objeto de evaluación. Los resultados han sido consistentemente tranquilizadores. Un estudio publicado en 2013 utilizando bases de datos electrónicas de más de 13 millones de personas vacunadas en que se comparó la mortalidad en estas personas con la de la población general de Estados Unidos proporcionó evidencia de que las vacunas no están asociadas con un mayor riesgo de muerte en la población16.
En la actualidad, las agencias regulatorias internacionales establecen procedimientos de seguridad en la fabricación, almacenamiento, manipulación, distribución y administración de las vacunas, así como sistemas de farmacovigilancia muy estrictos que tienen como función detectar posibles incidentes tras la administración de las vacunas. Sin embargo, la existencia de falsas creencias y rumores acerca de eventuales efectos negativos sin fundamento científico pueden disuadir de la vacunación, con los consiguientes riesgos para la protección inmunológica individual y colectiva de la población.
El objetivo del artículo es presentar y discutir, bajo la perspectiva del conocimiento científico disponible, el origen y los argumentos de algunos de los errores y rumores más frecuentes sobre eventuales efectos adversos de las vacunas.
¿Las vacunas contra la tos ferina de células enteras causan daño cerebral permanente?En la década de 1930 se realizó el primer ensayo clínico a gran escala para testar una vacuna inactivada de células enteras17. En 1948 la vacuna se combinó con los toxoides tetánico y diftérico dando lugar a la antidiftérica, antitetánica y antipertúsica de células enteras (DTPw), que consiguió reducir los casos de tos ferina en los países que la incluyeron en sus programas de vacunación. Las posteriores campañas de vacunación iniciadas a mediados de los años 60 despertaron dudas sobre su seguridad por la alta reactogenicidad que mostraba. A las reacciones locales y generales se añadió la especulación sobre una posible asociación con encefalopatías que ocasionaban daño cerebral permanente o con el síndrome de muerte súbita del lactante (SMSL). Ello condujo a la suspensión de la vacunación en países como Japón o Suecia durante los años 70 y 80, y a descensos de las coberturas vacunales en otros como Italia, Irlanda, Reino Unido o Australia. Estudios posteriores no han podido demostrar esta asociación18. Al disminuir la incidencia se había pasado del «miedo a la enfermedad» al «miedo a los efectos adversos de la vacuna».
¿Las vacunas causan síndrome de muerte súbita en el lactante (SMSL)?Durante los años 80, especialmente en Estados Unidos, tomó fuerza la alarma por la posible relación entre las vacunas y el SMSL, originando demandas contra los fabricantes de vacunas DTPw, que dejaron de producirla19. Al analizar la posible asociación entre SMSL y DTPw no se obtuvo evidencia20. La vacuna DTPw se ha ido sustituyendo por la antidiftérica, antitetánica y antipertúsica acelular (DTPa), constituida por diferentes componentes antigénicos (purificados o recombinantes) de Bordetella pertussis que atenúan los efectos indeseables de la vacuna de células enteras. El interés de los investigadores se centra actualmente en la duración de la protección.
¿Los recién nacidos son demasiado pequeños para desarrollar una respuesta inmunitaria adecuada a las vacunas?A las pocas horas de nacer, las células originales o adaptadas del sistema inmunitario ya participan activamente en los retos inmunitarios que comporta la exposición al medio ambiente, como la colonización por la flora bacteriana. El 95% de los niños vacunados en los primeros 6 meses de vida con múltiples vacunas contra difteria, tétanos, tos ferina, enfermedad por Haemophilus influenzae b, enfermedad neumocócica, hepatitis B y poliomielitis desarrollan respuestas inmunitarias específicas contra estas enfermedades18.
¿Las vacunas sobrecargan el sistema inmunitario de los niños?Uno de los argumentos que se utiliza en contra de la vacunación es que la aplicación simultánea de diversas vacunas comporta la exposición a múltiples antígenos vacunales y que dicha exposición alteraría el normal funcionamiento del sistema inmunitario en los niños.
Los recién nacidos son capaces de generar respuestas mediadas por linfocitos B (IgG, IgM e IgA) y linfocitos cooperadores (Th1 y Th2), que participan en la activación de los macrófagos y en la generación de linfocitos B.
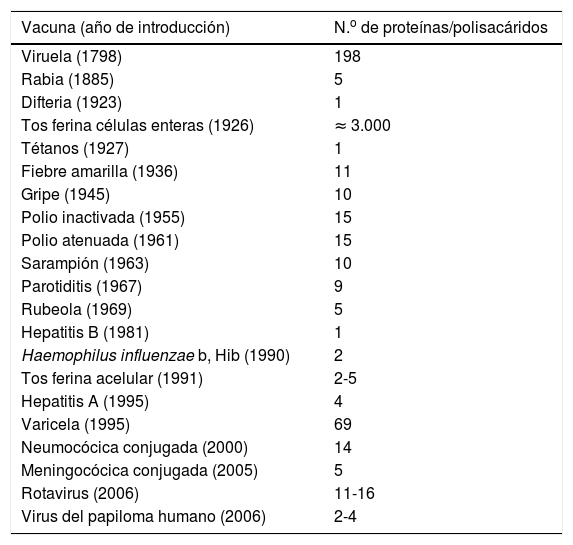
Asumiendo que una vacuna contiene como promedio 10 proteínas o polisacáridos inmunógenos, que cada proteína o polisacárido contiene 10 epítopos (porción de una macromolécula capaz de ser reconocida por el sistema inmunitario) y que circulan 107 linfocitos B por ml de sangre, cada niño podría responder a 105 vacunas, que resulta de dividir 107 por los 100 epítopos promedio de una vacuna (tabla 2)18.
Número de proteínas y de polisacáridos inmunógenos contenidos en diferentes vacunas
| Vacuna (año de introducción) | N.o de proteínas/polisacáridos |
|---|---|
| Viruela (1798) | 198 |
| Rabia (1885) | 5 |
| Difteria (1923) | 1 |
| Tos ferina células enteras (1926) | ≈ 3.000 |
| Tétanos (1927) | 1 |
| Fiebre amarilla (1936) | 11 |
| Gripe (1945) | 10 |
| Polio inactivada (1955) | 15 |
| Polio atenuada (1961) | 15 |
| Sarampión (1963) | 10 |
| Parotiditis (1967) | 9 |
| Rubeola (1969) | 5 |
| Hepatitis B (1981) | 1 |
| Haemophilus influenzae b, Hib (1990) | 2 |
| Tos ferina acelular (1991) | 2-5 |
| Hepatitis A (1995) | 4 |
| Varicela (1995) | 69 |
| Neumocócica conjugada (2000) | 14 |
| Meningocócica conjugada (2005) | 5 |
| Rotavirus (2006) | 11-16 |
| Virus del papiloma humano (2006) | 2-4 |
Fuente: DeStefano et al.18.
Estos datos no sustentan que la administración (simultánea o con intervalos de semanas a meses) de múltiples vacunas en la infancia pueda sobrecargar el sistema inmunitario. La respuesta del sistema inmunitario depende de la presencia de linfocitos B y de anticuerpos humorales y no del tamaño del organismo en que se produzca la interacción, por lo que un niño tiene una respuesta inmunitaria similar a la de un adulto frente a un determinado conjunto de epítopos21.
¿Las vacunas debilitan el sistema inmunitario?Se ha sugerido que los niños que han recibido vacunas combinadas tienen mayor riesgo de presentar infecciones por otros agentes. Sin embargo, en una cohorte de niños nacidos en Dinamarca no se observaron diferencias entre vacunados y no vacunados con vacunas combinadas en cuanto a incidencia de infecciones respiratorias, neumonía, septicemia, meningitis bacterianas o diarreas22
Con la disponibilidad de nuevas vacunas que contienen un solo antígeno o varios antígenos (vacunas combinadas) que han mostrado su eficacia y seguridad, los calendarios vacunales incrementan el número de vacunas incluidas. La opción de administrar vacunas combinadas ahorra pinchazos, actos sanitarios, almacenamientos y costes derivados, a la vez que mejora las coberturas de vacunación23. Por idénticos motivos se recomienda la administración simultánea de distintas vacunas si no existe incompatibilidad entre ellas.
¿Las vacunas causan enfermedades autoinmunes?Desde el momento del nacimiento, el timo y la médula ósea, mediante la detección y eliminación de los linfocitos dirigidos contra antígenos del propio cuerpo, evitan las reacciones de autoinmunidad (tolerancia central). Las células T y B responsables de autoinmunidad están presentes en todas las personas y mediante la tolerancia periférica se limita su activación. Las teorías que imputen un papel causal a las vacunas en las enfermedades autoinmunes deberían explicar cómo todos estos controles son eludidos.
La hipótesis de que la vacuna anti-hepatitis B causa esclerosis múltiple se generó por dos estudios de casos y controles que mostraron un aumento no significativo de la incidencia de esclerosis múltiple. Posteriormente, otros estudios no demostraron ninguna asociación ni tampoco que las vacunas antigripal o antitetánica agravasen los síntomas de la esclerosis múltiple24. Investigaciones sobre otras vacunas y el riesgo de diabetes tampoco muestran asociación.
¿Las vacunas causan alergias y asma?Las alergias están causadas por factores que desencadenan hipersensibilidad de tipo inmediato mediada por IgE. Se han apuntado dos teorías para explicar cómo las vacunas podrían aumentar la producción de IgE: desplazando la respuesta inmunitaria a los alérgenos desde células Th1 a Th2 y que al evitar infecciones frecuentes (hipótesis higienista) podrían inducir una respuesta más prolongada y frecuente de las células Th2. Ni las vacunas ni la inoculación de adyuvantes cambian la respuesta inmune de tipo Th1 a tipo Th2. La hipótesis higienista se descarta porque la mayoría de las infecciones que ocurren en los niños en los primeros 6 años de vida son causadas por virus para los que no existen vacunas. Además, en los países en desarrollo las tasas de alergia y asma son inferiores a pesar de las frecuentes infecciones por helmintos que inducen fuertes respuestas Th2. Algunos autores que realizaron estudios observacionales sugirieron asociación entre la vacuna contra tos ferina de células enteras y el desarrollo de asma, pero estudios más recientes han mostrado lo contrario25.
¿La vacuna contra el sarampión, la rubéola y la parotiditis (SRP) causa trastornos del espectro autista (TEA)?Los trastornos del espectro autista (TEA) son trastornos neuropsicológicos caracterizados por algún grado de alteración del comportamiento social, la comunicación y el lenguaje, y por un repertorio de intereses y actividades restringido, estereotipado y repetitivo. En la mayoría de los casos se manifiestan en los primeros 5 años de vida26.
En 1998 se publicó un estudio estableciendo una posible relación causal entre la vacuna SRP y el desarrollo de TEA27. Se basó en 12 niños con trastornos gastrointestinales y una regresión aguda de su desarrollo psicomotor; 8 fueron diagnosticados de autismo, en uno se asoció con el antecedente de sarampión y en los restantes con la vacuna SRP. No se ha podido demostrar el virus de la vacuna del sarampión en niños con autismo y 10 de 12 autores del artículo reconocieron que el estudio tenía errores metodológicos importantes y que no podía establecerse ningún tipo de relación causal entre la vacuna y el autismo. Finalmente, la revista se retractó de la publicación.
Las edades en las que se administran las vacunas en los niños normalmente preceden al diagnóstico de TEA, lo que en principio es solo una coincidencia temporal.
Las causas del autismo son poco conocidas, pero estudios de familias y gemelos sugieren factores genéticos. Además, la sobreexpresión de algunos neuropéptidos en niños que posteriormente presentaron autismo indica que factores pre o perinatales tienen más importancia que los posnatales. Otros factores de riesgo ambiental y alimentario están siendo estudiados.
¿El tiomersal causa autismo?El mercurio está presente en la naturaleza, y en forma de metilmercurio tiende a acumularse en el organismo causando efectos tóxicos. El tiomersal contiene etilmercurio, que se excreta más rápidamente y se acumula mucho menos18. Los datos científicos disponibles no muestran asociación entre TEA y el tiomersal de las vacunas. En Dinamarca, tras años de haber eliminado el tiomersal de las vacunas, la incidencia de autismo siguió aumentando22. A través de la lactancia materna un niño ingiere el doble de mercurio que todo el que ha podido recibir por las vacunas sin que le suponga ningún riesgo28.
A pesar de la ausencia de evidencia de que el tiomersal de las vacunas comporte riesgo, se ha ido eliminando de la mayoría de las vacunas que se administran en la infancia y en Europa y en Estados Unidos solo se utiliza en presentaciones multidosis.
¿El formaldehído es perjudicial?El formaldehído ha sido usado durante décadas en las vacunas como inactivador de toxinas bacterianas y virus en presentaciones multidosis. Aunque altas concentraciones pueden causar mutaciones en el ADN, el formaldehído es un producto del metabolismo del carbono que se detecta normalmente en el organismo humano. La cantidad de formaldehído presente en las vacunas es más de 600 veces menor que la necesaria para inducir toxicidad en animales de experimentación18. Todo ello va en contra de que el formaldehído presente en algunas vacunas tenga un efecto perjudicial sobre el organismo28.
¿El aluminio de las vacunas es perjudicial?Las sales de aluminio han sido usadas durante décadas para potenciar el efecto de las vacunas y conseguir el mismo efecto con menor dosis. Niveles altos de aluminio pueden causar reacciones inflamatorias locales, anemia o encefalopatía, pero estos niveles solamente se alcanzan en personas con reducción grave de la función renal cuando reciben altas dosis de aluminio, mientras que la cantidad de aluminio contenida en las vacunas es ínfima.
El aluminio es un elemento frecuente en plantas, aire y agua, y la lactancia materna aporta en promedio 7mg de aluminio durante los 6 primeros meses de vida, frente a los 4,4mg que contienen todas las vacunas recomendadas hasta esa edad. La administración de vacunas no modifica los niveles sanguíneos de aluminio en los niños18.
¿Las vacunas causan cáncer?Las vacunas contra la poliomielitis desarrolladas por Salk y Sabin a mediados del sigloXX se producían a partir de cultivos de células renales de macaco. En el año 1959 se descubrió que estas vacunas, especialmente las inactivadas, estaban contaminadas por el virus símico 40 (SV40). El virus SV40 está presente en algunos tumores humanos (mesotelioma, osteosarcoma y linfoma no Hodgkin), por lo que se formuló la hipótesis de que el virus vacunal podía producir leucemia infantil. Los estudios epidemiológicos realizados después de varios años de la administración de estas vacunas contaminadas (entre los años 1955 y 1963) no mostraron un incremento en el riesgo de padecer estos cánceres entre las personas que habían recibido la vacuna con SV40 respecto a las personas que no la habían recibido.
Diversos estudios han evaluado la posible asociación entre la leucemia infantil y la exposición a las vacunas triple vírica, antidiftérica, antitetánica, antipertúsica, antipoliomielítica, anti-Haemophilus influenzae b o anti-hepatitis B, sin que se haya evidenciado ninguna relación con la leucemia29,30.
ConclusiónLas vacunas, como cualquier fármaco, pueden ocasionar efectos adversos. Cualquier efecto indeseable atribuible a las vacunas ha de poder detectarse mediante sistemas de vigilancia potentes y bien estructurados. Las principales falsas creencias están relacionadas con efectos que se producen en las edades próximas a las de la administración de las vacunas, pero esta coincidencia no tiene por qué ser causal, como se ha demostrado en la mayoría de las ocasiones. Los eventuales efectos adversos son claramente inferiores a los beneficios individuales y colectivos que producen los programas de vacunaciones. La independencia, transparencia y visibilidad de los sistemas de control y vigilancia son necesarias para evitar los rumores y falsas creencias en este campo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses