Introducción: Desde el estudio DCCT, han sido muchas las investigaciones que han intentado evaluar las distintas propuestas de terapia intensiva. Pocos estudios a largo plazo incluyen variables psicosociales. Objetivos: Evaluar variables psicológicas y metabólicas en pacientes con diabetes tipo 1 tras 2 años de tratamiento con infusión subcutánea continua de insulina (ISCI). Materiales y métodos: Veintidós pacientes con diabetes tipo 1 en tratamiento con múltiples dosis de insulina recibieron tratamiento con ISCI. Se realizó una evaluación a los 6, 12 y 24 meses, utilizando diversos instrumentos como el BDI, el DQOL, la MHLC, el STAI y el cuestionari de miedo a las hipoglucemias. Se admitió un control glucémico adecuado con una HbA1c <7,5%. El análisis estadístico se realizó mediante pruebas no paramétricas y el coeficiente de correlación de Pearson. Resultados: Los pacientes partían de una puntuación media en depresión de 9,55 ± 9,12 (media ± DT). En calidad de vida, los datos iniciales fueron 92,95 ± 16,15, mientras que el nivel de HbA1c fue de 8,45 ± 1,59%. Al cabo de los 2 años de tratamiento, se aprecian mejoras significativas en las puntuaciones obtenidas en depresión (p= 0,018), calidad de vida (p= 0,005) y control glucémico (p= 0,003). La ansiedad rasgo y el locus de control externo correlacionaron significativamente, encontrándose una fuerte relación entre el miedo a las hipoglucemias y las variables psicológicas estudiadas. Los pacientes con mal control glucémico basal mejoraron al cabo de los 2 años de tratamiento. Conclusiones: Después de 2 años con ISCI, los pacientes con diabetes tipo 1 mejoran significativamente su calidad de vida, su control glucémico y su sintomatología depresiva.
Introduction: Since the DCCT study, many studies have tried to assess different intensive therapies. However, few long-term studies have included psychosocial variables. Objectives: To evaluate psychological and metabolic variables in patients with type 1 diabetes after 2 years of therapy with continuous subcutaneous insulin infusion (CSII). Materials and methods: Twenty-two type 1 diabetic patients treated with multiple daily injections were treated with CSII. An evaluation at 6, 12 and 24 months was performed, using several instruments as BDI, DQOL, MHLC and a questionnaire to evaluate fear of hypoglycaemia. Acceptable metabolic control was admitted with HbA1c <7.5%. Statistical analysis was realized using non parametric tests and Pearson's correlation coefficient. Results: Initially, patients had a mean score for depression of 9.55 ± 9.12 (mean ± SD). In quality of life, initial values were 92.95 ± 16.15, while the level of HbA1c was 8.45 ± 1.59%. After 2 years of treatment we found significant improvement in depression (p= 0.018) and quality of life (p= 0.005) scores and glycemic control (p= 0.003). Trait anxiety and external locus of control showed a significant correlation, with a strong correlation between fear of hypoglycemia and the analyzed psychosocial variables. Patients with bad basal glycemic control improved after 2 years of treatment. Conclusions: After two years with CSII, type 1 diabetic patients improve significantly their quality of life, glycemic control and depressive symptoms.
inventario de depresión de Beck
diabetes mellitus tipo 1
Diabetes Quality of Life (cuestionario de calidad de vida en la diabetes)
desviación típica
hemoglobina glucosilada
infusión subcutánea continua de insulina, infusor subcutáneo continuo de insulina
locus de control (interno/externo)
múltiples dosis de insulina
Escala de lugar de control
cuestionario de ansiedad estado-rasgo
terapia intensiva convencional
Desde que en 1993 el estudio DCCT1 (Diabetes Control and Complications Trial) informara de las mejoras asociadas al tratamiento intensivo insulínico con un infusor subcutáneo continuo de insulina (ISCI), han sido muchas las investigaciones que han perseguido evaluar las distintas propuestas de tratamiento insulínico intensivo. Específicamente, la terapia con ISCI ha producido abundante bibliografía científica sobre la eficacia de esta terapia intensiva tanto en adultos2, 3 como en población infantil4, 5. Estos resultados se han confirmado6 y ampliado7, encontrando bajos índices de hipoglucemia, menor variabilidad glucémica y mejor control de la diabetes, así como mayor satisfacción con el tratamiento ISCI que con múltiples dosis de insulina (MDI).
Hoy en día existe consenso sobre los beneficios de la terapia con ISCI8, 9. Pero no todos los pacientes pueden beneficiarse de este tratamiento. Pickup10 indica que los pacientes que más se benefician del cambio de tratamiento (MDI a ISCI) son aquellos que presentan hipoglucemias frecuentes e imprevisibles, altos niveles de glucosa en sangre y una HbA1c elevada y que no mejoran con el tratamiento MDI, consiguiendo una reducción mayor del riesgo de desarrollar complicaciones microvasculares. No obstante, algunos autores han advertido de sus riesgos11.
En la actualidad, la incorporación de las nuevas tecnologías supone un gran avance para el tratamiento de la diabetes mellitus tipo 1 (DM1) que ofrece resultados metabólicos claramente significativos. Sin embargo, debe tenerse en cuenta que una valoración más exhaustiva de estas técnicas arroja datos adicionales. Cuando se realizan estudios a largo plazo sobre la eficacia de la terapia con ISCI, algunos autores2, 3 refieren que las principales ganancias se obtienen en satisfacción y calidad de vida. En un reciente estudio12, a pesar de que no se encontraron diferencias significativas en el control metabólico entre ISCI y MDI tras 2 años de tratamiento, sí se obtuvieron diferencias en la satisfacción y la calidad de vida de los pacientes, un aspecto del que también informan otros autores2, 13. No obstante, las investigaciones sobre la eficacia de la terapia con ISCI a largo plazo no abundan7, 13-16 (tabla 1), y son escasas las que consideran variables psicológicas7, 17. Pero aún menor es el porcentaje de estos estudios en España7, 18, 19.
Estudios longitudinales sobre la eficacia de la terapia con infusión subcutánea continua de insulina (ISCI)
| Autores | Años | Tipo de muestra | País | Resultados |
| Bibergeil et al. (1987)29 | 3 | Adultos | Alemania | Efecto positivo de la ISCI en el metabolismo, así como en el curso de las fases tempranas de la microangiopatía y la neuropatíaLa mayoría de los pacientes que tuvieron una alta motivación antes de iniciar el tratamiento con ISCI mantuvieron una motivación positiva a lo largo de ésteNecesidad de evaluar un periodo más amplio |
| Bode et al. (1996)30 | 4 | Adultos | Estados Unidos | Reducción de las hipoglucemias severas |
| Linkeschova et al. (2002)31 | 2 | Adultos | Alemania | Disminución de la HbA1c y las hipoglucemiasEl aumento de la calidad de vida fue mayor en la ISCI que en la TIC |
| Hanas y Adolfsson (2006)32 | 5 | Infantil | Suecia | Descenso en la frecuencia de hipoglucemias severas y el nivel de HbA1c.Bajo riesgo de cetoacidosis |
| Ramchandani et al. (2006)33 | 3 | Adolescentes | Estados Unidos | Disminución de la HbA1c en los primeros 18 meses. La secreción exógena de insulina (péptido C) permanece estable durante los primeros 12 meses después del diagnóstico |
| Sulli y Shashaj (2006)34 | 4 | Infantil | Italia | Descenso de la HbA1c y del índice de masa corporalNo se encontraron diferencias en la cetoacidosis ni en las hipoglucemias severas |
| García-García (2007)35 | 2 | Infantil | España | Se evaluaron la HbA1c, el índice de masa corporal, el total de insulina diaria, las hipoglucemias severas y la cetoacidosis. No hubo diferencias significativas |
| Giménez et al. (2007)7 | 2 | Adultos | España | Reducción de la necesidad de insulina y las hipoglucemias leves y gravesIncremento del índice de masa corporal y de la calidad de vida |
| Schiaffini et al. (2007)15 | 2 | Infantil | Italia | Reducción de los valores de HbA1c |
| Scheidegger et al. (2007)13 | 1 | Adultos | Suiza | Aumento de la calidad de vida: los pacientes con DM1 se mostraron más satisfechos con el tratamiento recibido (ISCI) respecto a su control metabólico, así como en relación con factores psicosociales, el estado físico y la protección frente a las hipoglucemias y las complicaciones. Además, los pacientes refirieron que el tratamiento con ISCI les ofrecía mayor flexibilidad en las rutinas diarias, el tiempo libre y la dieta que el previo (MDI) |
| Scrimgeour et al. (2007)16 | 3,7 ± 1,9 | Infantil | Estados Unidos | Reducción de las hipoglucemias y la HbA1c |
| Aberle et al. (2008)14 | 5 | Adultos | Suiza | Disminución de HbA1c mayor en la ISCI que en la TIC. Estabilidad de los resultados |
El objetivo de este trabajo ha sido estudiar el impacto de la terapia intensiva con ISCI en algunas variables psicológicas, la calidad de vida y el control glucémico de pacientes adultos con diabetes mellitus tipo 1 durante 2 años de tratamiento, con lo que se pretende contribuir a aumentar los conocimientos sobre esta propuesta tecnológica, ya que la investigación en España de este tópico es escasa19.
Materiales y métodosDatos de los participantesEn este estudio se seleccionaron 22 pacientes (13 mujeres y 9 hombres) con DM1 que, en el momento de la evaluación basal, tenían prescrito tratamiento con MDI. La media de edad fue de 39,59 años (desviación típica [DT] 10,77), con una evolución de 19,05 ± 7,63 años. Los pacientes fueron reclutados de la Unidad de Diabetes del Servicio de Endocrinología del Hospital Carlos Haya de Málaga. Los criterios de inclusión fueron los siguientes: pacientes con diabetes tipo 1, en tratamiento con MDI, valorados positivamente en la Unidad de Diabetes para recibir tratamiento con ISCI (según indicaciones del BOJA.RSC 566/03), mayores de 14 años y con un péptido C menor de 0,5ng/mL. Como criterios de exclusión se consideraron tener diabetes tipo 2, o diabetes tipo 1 en tratamiento convencional (una o dos inyecciones/día) o en tratamiento con ISCI más sistema integrado infusor-sensor, estar embarazada o en periodo de preparación de la gestación, y presentar alteraciones psicológicas incapacitantes. El periodo de reclutamiento de pacientes duró 2 años (2004–2006). Se obtuvo el consentimiento informado de los 22 pacientes que formaron parte de este estudio. El proyecto obtuvo el informe positivo del comité de ética del hospital donde se realizó el estudio.
Variables e instrumentosCalidad de vidaDiabetes Quality of Life (DQOL) (Diabetes Control and Complications Trial Research Group, 1988): se utilizó una versión adaptada a la población española de este cuestionario20, que mide la calidad de vida de las personas con diabetes. Está compuesto por 43 ítems y evalúa cuatro dimensiones: «Insatisfacción con el tratamiento» (15 ítems), «Impacto del tratamiento» (17 ítems), «Preocupación por aspectos sociales/vocacionales» (7 ítems) y «Preocupación por los efectos futuros de la diabetes» (4 ítems). Cada ítem tiene cinco opciones de respuesta tipo Likert, que puntúan del 1 al 5 (1: «muy satisfecho» y 5: «nada satisfecho» en la subescala de satisfacción, y en el resto de subescalas 1: «nunca» y 5: «siempre»). Puede obtenerse una puntuación total y una puntuación por subescalas. Una menor puntuación indica una mejor calidad de vida. El cuestionario está diseñado para ser autoadministrado. Los datos de fiabilidad y validez del cuestionario referidos por sus autores son adecuados.
DepresiónInventario de depresión de Beck (BDI): se utilizó una versión adaptada a la población española de este cuestionario21. Está diseñado para evaluar la intensidad de la sintomatología depresiva que presenta un individuo. El instrumento es autoaplicable y consta de 21 preguntas, cada una de ellas con cuatro afirmaciones que describen el espectro de severidad de la categoría sintomática y conductual evaluada (0 indica la ausencia del síntoma y 3 la máxima severidad del síntoma). El instrumento original y sus adaptaciones al castellano han mostrado una validez y una fiabilidad adecuadas para su empleo en el ejercicio clínico y en la investigación.
AnsiedadCuestionario de ansiedad estado-rasgo (STAI): se utilizó la adaptación al castellano realizada por Seisdedos22. Este cuestionario de 40 ítems mide la ansiedad como estado y como rasgo. Los primeros 20 ítems evalúan la sintomatología ansiosa como reacción transitoria (subescala de ansiedad estado, STAI-E) y los 20 siguientes evalúan la presencia de sintomatología ansiosa como rasgo persistente de ansiedad (subescala de ansiedad rasgo, STAI-R). Las preguntas del STAI se contestan en una escala tipo Likert que puntúa de 0 a 3 (en el STAI-E, 0: «nada» y 3: «mucho»; en el STAI-R, 0: «casi nunca» y 3: «casi siempre»). El STAI posee validez discriminatoria y una buena consistencia interna.
«Locus» de controlEscala de lugar de control (MHLC): se utilizó la versión adaptada a la población española23. Esta escala evalúa dónde sitúa la persona el lugar de control o locus de control (LOC) de su salud, es decir, si la persona piensa que por sí misma puede vencer el obstáculo de salud o al menos controlarlo (LOC interno), o piensa que no puede controlar las variables de la salud y que su evolución o afrontamiento de un hecho negativo depende de variables externas como la suerte, el personal sanitario, la medicación, etc. (LOC externo). Este autoinforme está compuesto de 18 ítems, de los cuales 6 valoran un LOC interno y 12 evalúan un LOC externo. Sus preguntas se contestan en una escala tipo Likert de rango 1 («completamente en desacuerdo») a 6 («completamente de acuerdo»). Los autores del instrumento informan de una fiabilidad y una validez adecuadas para su empleo en el ejercicio clínico y en la investigación.
Control glucémicoLa evaluación objetiva del control glucémico se realizó mediante la hemoglobina glucosilada (HbA1c), que se midió a través de una cromatografía líquida de alta presión (HPLC) con un aparato modelo Kyoto Daiichi Kageki. La HbA1c es un indicador de la media de glucemia del paciente en los últimos 3 meses aproximadamente. Basándonos en criterios clínicos y en las características de la muestra, se estableció una HbA1c inferior al 7,5% como punto de corte de un buen control glucémico.
Miedo a las hipoglucemiasCuestionario de miedo a las hipoglucemias, elaborado y validado (aunque pendiente de publicación en Psychological Assessment) por el grupo de investigación SEJ2007-63786 (MICINN). El cuestionario consta de 21 ítems (19 negativos y 2 positivos) evaluados mediante una escala tipo Likert cuyos valores oscilan entre 1 («nunca») y 5 («todos los días»).
ProcedimientoEl estudio se llevó a cabo íntegramente en una consulta perteneciente a la Unidad de Diabetes del Servicio de Endocrinología del Hospital Regional Universitario Carlos Haya de Málaga. Tras aplicar los criterios de inclusión y exclusión indicados en el apartado «Datos de los participantes», se recogió información de los pacientes seleccionados sobre las variables sociodemográficas (edad, estudios, ocupación, etc.) y clínicas (control glucémico valorado mediante la HbA1c, número de hipoglucemias graves, complicaciones, etc.). En segundo lugar, se registraron las medidas antropométricas de los pacientes (peso, talla, cintura/cadera) y se realizaron extracciones de sangre para, posteriormente, analizar las muestras. A continuación, se llevó a cabo una evaluación psicológica mediante la administración de una batería de test en formato de entrevista (estructurada) con el fin de recoger datos sobre variables psicológicas (depresión, ansiedad y locus de control) y de calidad de vida de los pacientes. Tras la primera evaluación, los 22 pacientes con DM1 iniciaron tratamiento con ISCI, volviendo a ser evaluados a los 6, 12 y 24 meses. No se produjeron abandonos durante el estudio; sin embargo, hubo algún valor perdido en las evaluaciones de los 6 o 12 meses, generalmente porque el paciente no pudo asistir a consulta.
Para contrastar las hipótesis planteadas se utilizaron test no paramétricos (la prueba U de Mann–Whitney y la prueba de rangos con signo de Wilcoxon) y el coeficiente de correlación de Pearson, este último para medir las posibles relaciones entre las distintas variables objeto de estudio. El nivel de confianza para realizar estos contrastes fue del 95%. Se empleó la versión 16.0 del SPSS (Statistical Package for the Social Sciences) para llevar a cabo los análisis de este estudio.
También se evaluó la fiabilidad de los instrumentos utilizados en este estudio. La fiabilidad hace referencia a la precisión, la consistencia y la constancia en la medida. Se dice que un test es fiable si, aplicado varias veces a una misma muestra, en las mismas condiciones, los resultados son idénticos en todas ellas. Por ello, el test utilizado debe evaluar con precisión, es decir, los resultados obtenidos con él deben ser consistentes. Existen varios métodos para estudiar la fiabilidad. En esta investigación se utilizó el método de consistencia interna, que evalúa en qué medida los elementos de una prueba son homogéneos o consistentes entre sí. Para ello, se aplicó el coeficiente alfa de Cronbach, que es uno de los coeficientes de fiabilidad de consistencia interna más conocidos. El rango de valores de este coeficiente oscila entre 0 y 1. Cuanto más se acerque el valor a 1 mayor es la fiabilidad, entendida como consistencia interna, del instrumento.
ResultadosLos test de evaluación utilizados en este estudio mostraron una alta consistencia interna. Así, en el caso del DQOL, el valor del a de Cronbach indicó una buena consistencia interna (a= 0,855). Las subescalas de dicho cuestionario también presentaron una consistencia interna adecuada (DQOL-Insatisfacción con el tratamiento, a= 0,602; DQOL-Impacto del tratamiento, a= 0,818; DQOL-Preocupación por aspectos sociales/vocacionales, a= 0,672; DQOL-Preocupación por los efectos futuros de la diabetes, a= 0,695). Los instrumentos con los que se evaluaron las variables depresión y ansiedad (tanto el estado como el rasgo) mostraron una buena consistencia interna en este estudio (BDI-II, a= 0,919; STAI-E, a= 0,944; STAI-R, a= 0,845). La versión española de la escala de lugar de control presentó una consistencia mediana (LOC interno, a= 0,632; LOC externo, a= 0,568). También resultó adecuada la consistencia interna del cuestionario de miedo a las hipoglucemias (a= 0,810), previamente validado en nuestro equipo de investigación y pendiente de publicación.
Al cabo de los 2 años de tratamiento, mejoraron significativamente las puntuaciones en depresión (p= 0,018), calidad de vida (p= 0,005) y control glucémico (p= 0,003) de los pacientes (tabla 2), así como en las subescalas de calidad de vida «Insatisfacción con el tratamiento» (p= 0,029) e «Impacto del tratamiento» (p= 0,001). Debe tenerse en cuenta que una mayor puntuación en cualquiera de los instrumentos de evaluación psicológica utilizados (excepto en el caso del locus de control interno) implica una peor situación en la variable medida.
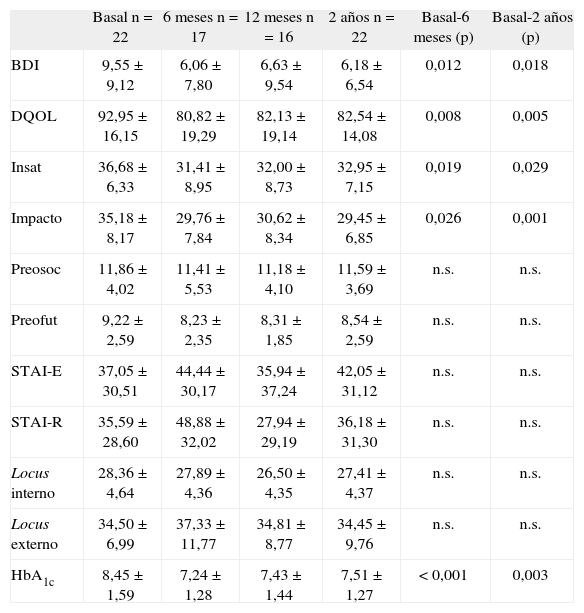
Estadísticos descriptivos de las variables psicológicas y el control glucémico
| Basal n= 22 | 6 meses n= 17 | 12 meses n= 16 | 2 años n= 22 | Basal-6 meses (p) | Basal-2 años (p) | |
| BDI | 9,55 ± 9,12 | 6,06 ± 7,80 | 6,63 ± 9,54 | 6,18 ± 6,54 | 0,012 | 0,018 |
| DQOL | 92,95 ± 16,15 | 80,82 ± 19,29 | 82,13 ± 19,14 | 82,54 ± 14,08 | 0,008 | 0,005 |
| Insat | 36,68 ± 6,33 | 31,41 ± 8,95 | 32,00 ± 8,73 | 32,95 ± 7,15 | 0,019 | 0,029 |
| Impacto | 35,18 ± 8,17 | 29,76 ± 7,84 | 30,62 ± 8,34 | 29,45 ± 6,85 | 0,026 | 0,001 |
| Preosoc | 11,86 ± 4,02 | 11,41 ± 5,53 | 11,18 ± 4,10 | 11,59 ± 3,69 | n.s. | n.s. |
| Preofut | 9,22 ± 2,59 | 8,23 ± 2,35 | 8,31 ± 1,85 | 8,54 ± 2,59 | n.s. | n.s. |
| STAI-E | 37,05 ± 30,51 | 44,44 ± 30,17 | 35,94 ± 37,24 | 42,05 ± 31,12 | n.s. | n.s. |
| STAI-R | 35,59 ± 28,60 | 48,88 ± 32,02 | 27,94 ± 29,19 | 36,18 ± 31,30 | n.s. | n.s. |
| Locus interno | 28,36 ± 4,64 | 27,89 ± 4,36 | 26,50 ± 4,35 | 27,41 ± 4,37 | n.s. | n.s. |
| Locus externo | 34,50 ± 6,99 | 37,33 ± 11,77 | 34,81 ± 8,77 | 34,45 ± 9,76 | n.s. | n.s. |
| HbA1c | 8,45 ± 1,59 | 7,24 ± 1,28 | 7,43 ± 1,44 | 7,51 ± 1,27 | <0,001 | 0,003 |
Datos expresados como media ± desviación típica. n.s.: no significativo. BDI: inventario de depresión de Beck; DQOL: Diabetes Quality of Life; HbA1c: hemoglobina glucosilada; Impacto: impacto del tratamiento; Insat: insatisfacción con el tratamiento; Locus externo: locus de control externo; Locus interno: locus de control interno; Preofut: preocupación por los efectos futuros de la diabetes; Preosoc: preocupación por aspectos sociales/vocacionales; STAI-E: cuestionario de ansiedad-estado; STAI-R: cuestionario de ansiedad-rasgo.
El mayor descenso en las puntuaciones de los pacientes se produjo a los 6 meses de iniciar el tratamiento, en las variables depresión (p= 0,012), calidad de vida (p= 0,008) y nivel de hemoglobina glucosilada (p <0,001), así como en las subescalas del cuestionario de calidad de vida (DQOL) «Insatisfacción con el tratamiento» (p= 0,019) e «Impacto del tratamiento» (p= 0,026).
Se produjo un aumento de las puntuaciones en las variables ansiedad y locus de control externo a los 6 meses de tratamiento, aunque no alcanzaron significación estadística, observándose posteriormente un descenso y una estabilización en dichas puntuaciones. De hecho, tras 2 años de tratamiento no se encontraron diferencias significativas.
El punto de corte para un buen control glucémico se estableció en el 7,5%. La media basal de los pacientes en esta variable fue 8,45% (DT= 1,59). Atendiendo a este punto de corte, se establecieron dos grupos: mal control inicial (14 pacientes) y buen control inicial (8 pacientes). En los pacientes del grupo con mal control glucémico se observó una mejoría clara y significativa, al cabo de los 2 años de tratamiento (tabla 3), en las variables calidad de vida (p= 0,016) y depresión (p= 0,013), así como en las subescalas «Insatisfacción con el tratamiento» (p= 0,015) e «Impacto del tratamiento» (p= 0,009). El mayor descenso en las puntuaciones también se produjo en los primeros 6 meses de tratamiento, tanto en la variable calidad de vida (p= 0,019) como en la variable depresión (p= 0,003), del mismo modo que en las subescalas «Insatisfacción con el tratamiento» (p= 0,025) e «Impacto del tratamiento» (p= 0,037). En el grupo de pacientes con buen control glucémico no se encontraron diferencias significativas, quizá por la falta de potencia estadística debida al pequeño tamaño de ese grupo (8 pacientes). Sí se encontraron diferencias basales entre ambos grupos (buen y mal control glucémico) en las variables locus de control interno (p= 0,034) y ansiedad rasgo (p= 0,024). La variable depresión estuvo cerca de alcanzar la significación (p= 0,055). Dichas diferencias fueron favorables al grupo de pacientes que partía de un buen control glucémico. Al cabo de los 2 años de tratamiento, no se apreciaron diferencias significativas entre ambos grupos (mal/buen control basal).
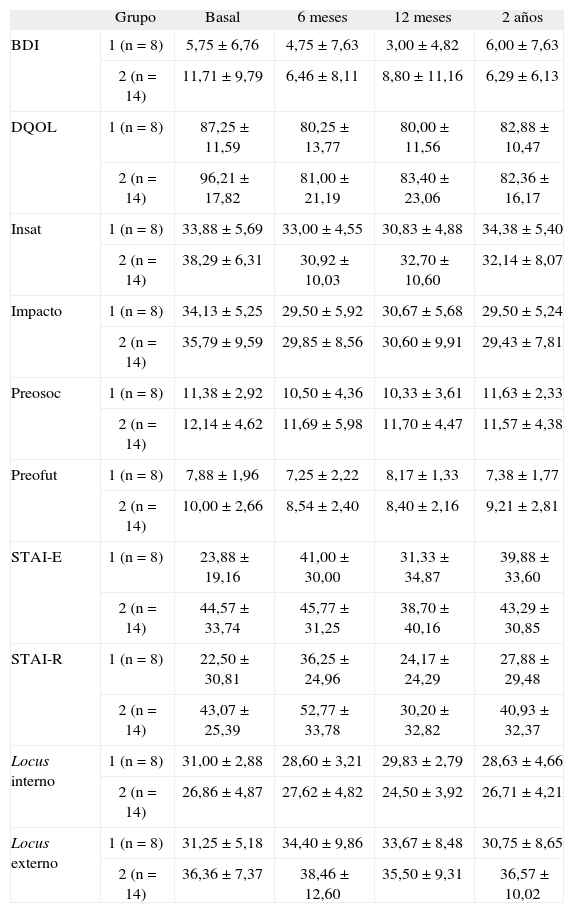
Estadísticos descriptivos de las variables psicológicas en función del tipo de control glucémico (buen o mal control glucémico)
| Grupo | Basal | 6 meses | 12 meses | 2 años | |
| BDI | 1 (n= 8) | 5,75 ± 6,76 | 4,75 ± 7,63 | 3,00 ± 4,82 | 6,00 ± 7,63 |
| 2 (n= 14) | 11,71 ± 9,79 | 6,46 ± 8,11 | 8,80 ± 11,16 | 6,29 ± 6,13 | |
| DQOL | 1 (n= 8) | 87,25 ± 11,59 | 80,25 ± 13,77 | 80,00 ± 11,56 | 82,88 ± 10,47 |
| 2 (n= 14) | 96,21 ± 17,82 | 81,00 ± 21,19 | 83,40 ± 23,06 | 82,36 ± 16,17 | |
| Insat | 1 (n= 8) | 33,88 ± 5,69 | 33,00 ± 4,55 | 30,83 ± 4,88 | 34,38 ± 5,40 |
| 2 (n= 14) | 38,29 ± 6,31 | 30,92 ± 10,03 | 32,70 ± 10,60 | 32,14 ± 8,07 | |
| Impacto | 1 (n= 8) | 34,13 ± 5,25 | 29,50 ± 5,92 | 30,67 ± 5,68 | 29,50 ± 5,24 |
| 2 (n= 14) | 35,79 ± 9,59 | 29,85 ± 8,56 | 30,60 ± 9,91 | 29,43 ± 7,81 | |
| Preosoc | 1 (n= 8) | 11,38 ± 2,92 | 10,50 ± 4,36 | 10,33 ± 3,61 | 11,63 ± 2,33 |
| 2 (n= 14) | 12,14 ± 4,62 | 11,69 ± 5,98 | 11,70 ± 4,47 | 11,57 ± 4,38 | |
| Preofut | 1 (n= 8) | 7,88 ± 1,96 | 7,25 ± 2,22 | 8,17 ± 1,33 | 7,38 ± 1,77 |
| 2 (n= 14) | 10,00 ± 2,66 | 8,54 ± 2,40 | 8,40 ± 2,16 | 9,21 ± 2,81 | |
| STAI-E | 1 (n= 8) | 23,88 ± 19,16 | 41,00 ± 30,00 | 31,33 ± 34,87 | 39,88 ± 33,60 |
| 2 (n= 14) | 44,57 ± 33,74 | 45,77 ± 31,25 | 38,70 ± 40,16 | 43,29 ± 30,85 | |
| STAI-R | 1 (n= 8) | 22,50 ± 30,81 | 36,25 ± 24,96 | 24,17 ± 24,29 | 27,88 ± 29,48 |
| 2 (n= 14) | 43,07 ± 25,39 | 52,77 ± 33,78 | 30,20 ± 32,82 | 40,93 ± 32,37 | |
| Locus interno | 1 (n= 8) | 31,00 ± 2,88 | 28,60 ± 3,21 | 29,83 ± 2,79 | 28,63 ± 4,66 |
| 2 (n= 14) | 26,86 ± 4,87 | 27,62 ± 4,82 | 24,50 ± 3,92 | 26,71 ± 4,21 | |
| Locus externo | 1 (n= 8) | 31,25 ± 5,18 | 34,40 ± 9,86 | 33,67 ± 8,48 | 30,75 ± 8,65 |
| 2 (n= 14) | 36,36 ± 7,37 | 38,46 ± 12,60 | 35,50 ± 9,31 | 36,57 ± 10,02 |
Datos expresados como media ± desviación típica. Grupo 1: buen control; grupo 2: mal control. BDI: Inventario de depresión de Beck; DQOL: Diabetes Quality of Life; Impacto: Impacto del tratamiento; Insat: insatisfacción con el tratamiento; Locus externo: locus de control externo; Locus interno: locus de control interno; Preofut: preocupación por los efectos futuros de la diabetes; Preosoc: preocupación por aspectos sociales/vocacionales; STAI-E: cuestionario de ansiedad-estado; STAI-R: cuestionario de ansiedad-rasgo.
Se constató asimismo, al cabo de los 2 años de tratamiento con ISCI, una fuerte correlación entre las puntuaciones de ansiedad rasgo y las de locus de control externo (r= 0,585; p= 0,004), así como entre las puntuaciones del cuestionario de miedo a las hipoglucemias y las variables psicológicas estudiadas (tabla 4).
Correlaciones significativas entre las variables psicológicas estudiadas
| Correlaciones significativas al cabo de 2 años de tratamiento | Coeficiente de correlación de Pearson |
| STAI-R - Locus externo | r= 0,585 (p= 0,040) |
| BDI - Miedo a las hipoglucemias | r= 0,531 (p= 0,013) |
| DQOL - Miedo a las hipoglucemias | r= 0,593 (p= 0,005) |
| STAI-E - Miedo a las hipoglucemias | r= 0,459 (p= 0,036) |
| STAI-R - Miedo a las hipoglucemias | r= 0,633 (p= 0,002) |
| Locus externo - Miedo a las hipoglucemias | r= 0,648 (p= 0,001) |
BDI: inventario de depresión de Beck; DQOL: Diabetes Quality of Life; STAI-E: cuestionario de ansiedad-estado; STAI-R: cuestionario de ansiedad-rasgo.
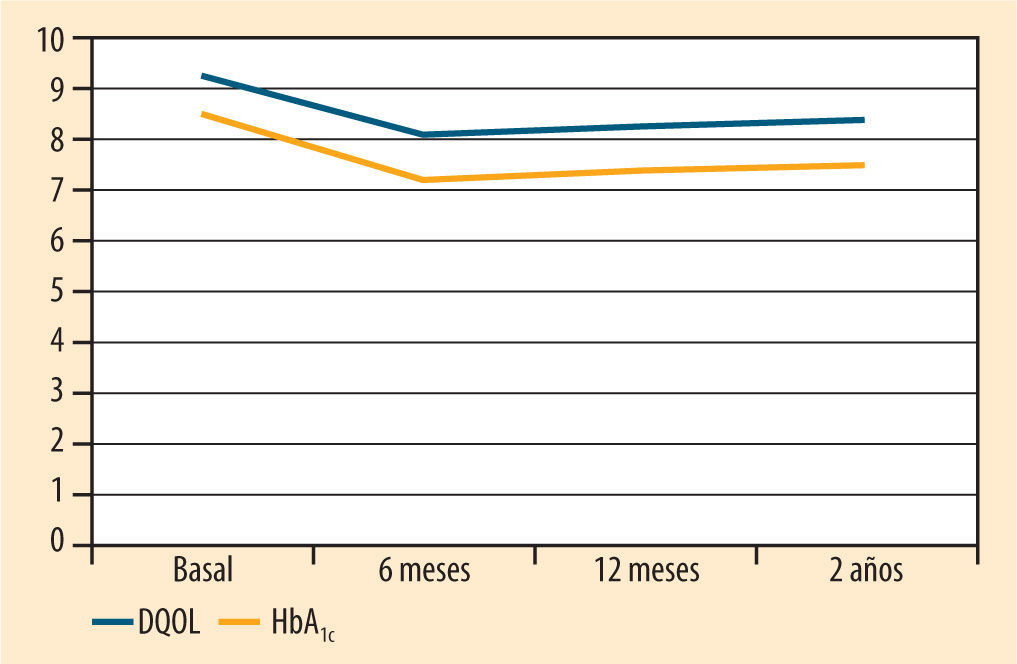
El objetivo de este trabajo ha sido estudiar el impacto de la terapia intensiva con ISCI en una serie de variables psicológicas, la calidad de vida y el control glucémico de pacientes adultos con DM1 tras 2 años de tratamiento. Aunque se ha constatado una mejora significativa en el control glucémico (medido por la HbA1c) de estos pacientes, las principales ganancias se han obtenido en la satisfacción con el tratamiento y en la calidad de vida (figura 1), resultados que se sitúan en la línea de otras investigaciones12. Este estudio aporta también evidencia empírica sobre el estado emocional de los pacientes, observándose una mejoría significativa de la sintomatología depresiva. Los pacientes que más se han beneficiado de estas ganancias han sido aquellos con peor control glucémico. Es decir, el mal control glucémico inicial no ha impedido que el tratamiento surta efectos positivos en estos pacientes, pues han conseguido optimizar su control glucémico, su calidad de vida y su sintomatología depresiva.
Evolución de las puntuaciones medias en el Diabetes Quality of Life (DQOL) y la HbA1c. Dado que la media de las puntuaciones en la HbA1c y el DQOL fue de 8,45 y 92,95, respectivamente, se han divido entre 10 las puntuaciones del DQOL para poder comparar las dos variables, pues en la escala original la distancia entre las puntuaciones es muy grande y no se observa tan claramente el efecto producido
El aumento en los niveles de ansiedad (rasgo) y el locus de control externo al comenzar el tratamiento podría indicar que, a pesar de sus bondades, este tipo de tratamiento hace que el paciente se sienta más nervioso y tenga la percepción de que ha perdido el control de su enfermedad, ya que la atención constante que debe mantener sobre un aparato desconocido supone una situación de tensión continua e incontrolada. No obstante, a partir de los 6 meses -esto es, cuando el paciente se ha familiarizado con el sistema de ISCI-, estos niveles descienden y tienden a estabilizarse. De hecho, la mejoría comienza a observarse a los 6 meses de tratamiento, estabilizándose a partir de los 12 meses. Por tanto, una intervención psicológica en este primer periodo de implantación del sistema de ISCI podría optimizar este tipo de tratamiento y, posiblemente, podría disminuir el número de abandonos que pudieran producirse en dicho periodo, aunque en este estudio no tuvieron lugar.
Los resultados de esta investigación también sugieren que debería prestarse una especial atención al miedo a las hipoglucemias, ya que se relaciona significativamente con el descenso en la calidad de vida y el aumento de los niveles de ansiedad, los síntomas depresivos y el locus de control externo. Es decir, el miedo a las hipoglucemias tiene un efecto negativo en las variables psicológicas analizadas en este estudio, disminuyendo el bienestar y la satisfacción del paciente. Parece, pues, necesario y conveniente profundizar en el estudio de esta variable y su relación con la calidad de vida del paciente, por lo que se plantea como una futura línea de investigación.
El análisis de la evolución de los pacientes tratados con ISCI ha resultado clarificador. Se constata que la evaluación a largo plazo permite obtener datos adicionales que complementan la información aportada por los estudios transversales y con los que se pueden alcanzar conclusiones más válidas. De este modo, en la literatura científica numerosos estudios informan de la eficacia de esta terapia intensiva2-4 para el control metabólico del paciente. Sin embargo, cuando se consideran las escasas investigaciones que evalúan los efectos a largo plazo (entre 1 y 5 años) de este tipo de tratamiento intensivo, los resultados muestran que los mayores beneficios se observan en la calidad de vida percibida por el paciente, así como en algunas variables psicológicas (fundamentalmente, ansiedad y depresión). En nuestro estudio se han confirmado estos hallazgos en una muestra española.
Aunque las iniciativas todavía son exiguas, cada vez se observa una mayor sensibilización sobre los aspectos psicosociales en la DM1, ya que el tratamiento de esta enfermedad requiere un abordaje integral. Para ello, son necesarios equipos multidisciplinares en los que se incluyan psicólogos clínicos especializados en diabetes, a fin de atender las demandas que este tipo de pacientes requiere, lo que hoy constituye un reto importante que superar. Así lo sugieren diversas investigaciones24, dado que el tratamiento con ISCI y con otras alternativas tecnológicas requiere un mayor grado de participación y autocuidado, así como una actitud más activa del paciente. Por ello, es necesario que el paciente adquiera tanto el conocimiento sobre manejo de los sistemas de infusión de insulina como entrenamiento en la toma de decisiones, en el uso de estrategias de afrontamiento y solución de problemas así como de modificación de actitudes. La carencia de estas habilidades y actitudes puede ser la causa de muchos de los fracasos de pacientes en tratamiento con ISCI y otras tecnologías aplicadas a la diabetes.
A la luz de estos resultados, el seguimiento a largo plazo de los pacientes con DM1 tratados con ISCI parece conveniente. Para dicho seguimiento ya empiezan a incorporarse los avances de la tecnología25. El futuro vendrá marcado por el uso de las nuevas tecnologías en el seguimiento de los pacientes con ISCI, mediante aplicaciones virtuales o de telefonía móvil26, lo que no implica la exclusión de la evaluación continua del paciente por el especialista. Se trata más bien de un servicio que las nuevas tecnologías aportan tanto al paciente como a los profesionales que los atienden, y que permite mejorar la relación con el enfermo, facilitando la comunicación médico-paciente.
En suma, como señalan Jeandidier et al.27, para verificar la eficacia y seguridad de los infusores de insulina es necesaria una evaluación a largo plazo (al menos anual), que debería incluir la evaluación de aspectos psicosociales24. Sin duda se precisan más investigaciones, sobre todo de este último aspecto, que permitan extraer conclusiones fiables, válidas y útiles.
La principal limitación de este estudio ha sido el tamaño muestral. No obstante, se trata de una limitación propia de los estudios clínicos, en los que resulta difícil obtener muestras con un tamaño elevado. Por otro lado, es posible que la adherencia al tratamiento haya estado modulada por factores personales28 no considerados en este estudio; sin embargo, su evaluación requería la utilización de múltiples instrumentos que hacían inviable la investigación.
Conclusiones- •
Los pacientes con DM1 tratados con ISCI mejoran significativamente su calidad de vida y estado emocional (depresión) tras 2 años de tratamiento.
- •
La mejoría comienza a observarse a los 6 meses de tratamiento y se estabiliza a partir de los 12 meses.
- •
Aunque inicialmente se aprecia un aumento (no significativo) en la ansiedad (rasgo) y el locus de control externo, tras la familiarización con el sistema ISCI, a los 6 meses, estos niveles descienden y tienden a estabilizarse.
- •
El miedo a las hipoglucemias se relaciona significativamente con el descenso de la calidad de vida y el aumento de las puntuaciones en el BDI, el STAI y el locus de control externo. Se sugiere una especial atención a esta variable, que será objeto de futuras investigaciones.
Declaración de potenciales conflictos de intereses
Los autores declaran que no existen conflictos de intereses en relación con el contenido del presente artículo.
Esta investigación se ha realizado con la financiación recibida del Ministerio de Ciencia e Innovación para el proyecto SEJ2007-63786/PSIC, el Servicio Andaluz de Salud (240/2006) y el Instituto de Salud Carlos III (P107 90330). ¿






 DQOL) y la
DQOL) y la 