diabetes mellitus tipo 2;
hemoglobina glucosilada;
cotransportador de sodio-glucosa 2 (sodium-glucose co-transporter-2).
Muchos pacientes con diabetes mellitus tipo 2 (DM2) no cumplen los objetivos de control glucémico1. Las principales barreras para ello son los efectos secundarios asociados a los fármacos actualmente disponibles, sobre todo la hipoglucemia y el aumento de peso. Por ello son necesarios nuevos tratamientos, con formas de actuación diferentes, que sean eficaces y carezcan de estas limitaciones.
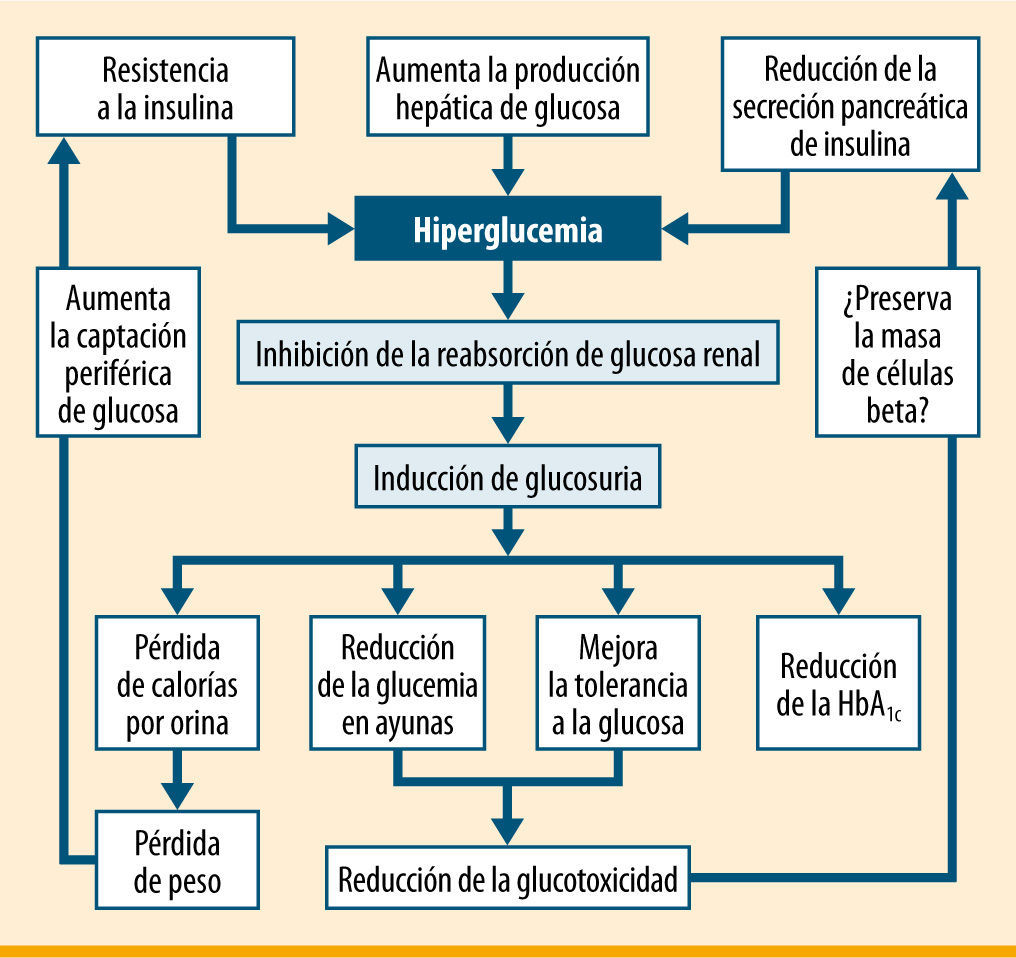
El riñón desempeña un papel clave en el manejo de la glucemia. En personas sanas, los riñones filtran una gran cantidad de glucosa a través del glomérulo (aproximadamente 180g/día) y reabsorben activamente casi toda la glucosa filtrada, debido fundamentalmente a la proteína cotransportadora de sodio-glucosa tipo 2 (SGLT2, sodiumglucose co-transporter-2). En los pacientes con DM2, la expresión de SGLT2 está aumentada en las células epiteliales del túbulo contorneado proximal2, lo que conlleva una mayor reabsorción renal de glucosa, con efectos adversos, dado que contribuye a mantener la hiperglucemia. La supresión de la actividad de SGLT2 inhibe la reabsorción renal de glucosa, aumenta su excreción renal y ayuda a la reducción de la hiperglucemia. A diferencia de otros fármacos orales, los inhibidores de SGLT2 no estimulan la secreción de insulina y, por tanto, es de esperar que prevengan el riesgo de hipoglucemia. Además, existe la posibilidad de que favorezcan la pérdida de peso debido a la glucosuria concomitante3, y es de esperar que la pérdida de peso contribuya a disminuir la producción hepática de glucosa y a reducir la glucotoxicidad, lo que resultará en una mejoría del nivel glucémico (figura 1).
Efectos clínicos de la inhibición de SGLT2. La inhibición de la reabsorción tubular renal de glucosa da lugar a glucosuria y a un descenso en los niveles plasmáticos de glucosa. La pérdida de calorías inducida por la glucosuria ocasiona pérdida de peso y reducción de la resistencia a la insulina, mientras que el descenso de la glucemia reduce la glucotoxicidad sobre la célula beta pancreática, y por tanto preserva potencialmente la función de la célula beta. Modificada de Idris et al.5
Aunque la inducción de glucosuria preocupa por sus posibles efectos a largo plazo, este aspecto ha sido evaluado en un modelo genético de inhibición de SGLT2 derivado de una mutación finalizadora (non-sense mutations) en pacientes con glucosuria renal4. Estos pacientes no padecen anomalías en la función renal ni alteraciones histológicas, lo que sugiere que los inhibidores de SGLT2 pueden tener un buen perfil de seguridad.
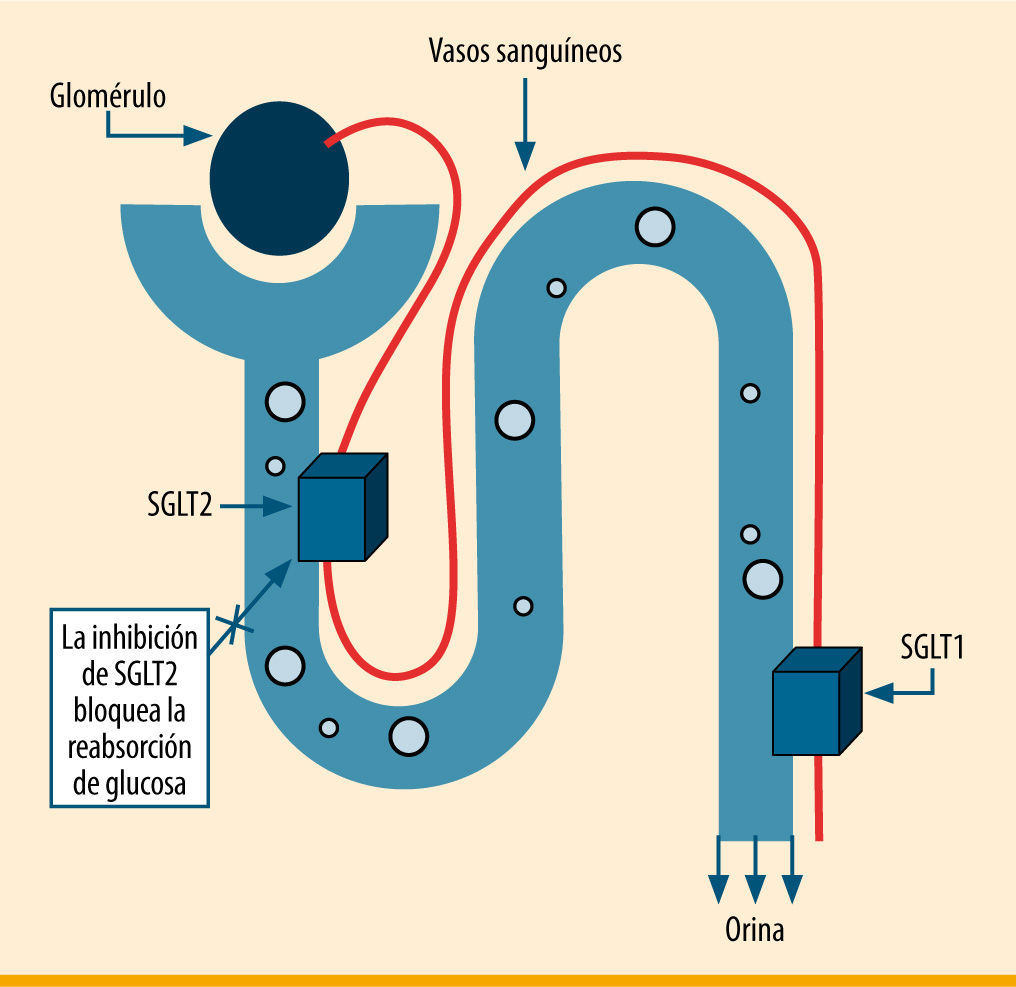
Desarrollo de los inhibidores de SGLT2Las SGLT son una gran familia de proteínas de membrana implicadas en el transporte de glucosa, aminoácidos, vitaminas, y algunos iones a través del borde en cepillo del epitelio intestinal y del túbulo renal proximal5. El transportador SGLT1, de baja capacidad y alta afinidad, se expresa fundamentalmente en el tracto gastrointestinal, donde tiene un importante papel en la absorción de glucosa6, aunque sólo es responsable de la reabsorción renal del 10% de la glucosa filtrada. El SGLT2, en cambio, de alta capacidad y baja afinidad, se expresa principalmente en el riñón5, donde es responsable del 90% de la reabsorción de la glucosa filtrada en la porción inicial S1 del túbulo contorneado proximal renal (figura 2). Existen otros miembros de la familia SGLT, como SGLT3, 4, 5 y 6, pero sin efectos conocidos sobre la reabsorción renal de glucosa6. En consecuencia, el objetivo ha sido diseñar fármacos inhibidores de SGLT2, más determinante en la reabsorción renal de glucosa.
Mecanismo de acción de los inhibidores de SGLT2. El cotransportador sodio-glucosa tipo 2 (SGLT2) se expresa en el primer segmento del túbulo contorneado proximal y es responsable de la mayor parte de la reabsorción renal de glucosa. Modificada de Idris et al.5
La florizina es un inhibidor clásico del transporte de glucosa dependiente de sodio. Sin embargo, tiene importantes limitaciones: en primer lugar, es un potente inhibidor tanto de SGLT1 como de SGLT2, por lo que no permite distinguir la actividad SGLT1 de la de SGLT27; en segundo lugar, la administración oral de florizina causa malabsorción intestinal de glucosa y produce diarrea.
Inhibición selectiva de SGLT2Los inhibidores selectivos de SGLT2 actúan exclusivamente sobre el riñón. Este efecto se traduce en una mayor excreción renal de glucosa, lo que produce un balance energético negativo y sin efectos secundarios gastrointestinales. Actualmente, dapagliflozina es el que se encuentra en una fase más avanzada de investigación8. También han sido estudiados otros inhibidores selectivos de SGLT29 (tabla 1), pero en muchos de ellos se ha suspendido la investigación10 y de otros no se dispone aún de datos clínicos11. Por ello, los datos que se comentan a continuación se referirán exclusivamente a estudios realizados con dapagliflozina.
Inhibidores selectivos de SGLT2 que han sido investigados clínicamente
| Compuesto | Compañía | Fase* | Resultado |
| Dapagliflozina | Bristol-Myers Squibb/Astrazeneca | III | Compuesto en fase de investigación más avanzada No comercializado todavía para uso clínico (véase texto) |
| Canagliflozina | Mitusbishi Tanabe Pharma y Johnson & Johnson | III | No hay datos clínicos disponibles |
| Sergliflozina | Kissei/Glaxo Smith Kline | II | Bien tolerado↑ excreción de glucosa al administrar 3 veces/día Investigación suspendida |
| Remogliflozina | Kissei/Glaxo Smith Kline | II | Bien tolerado↓ glucemia↓ presión arterial↑ excreción de glucosa Sin interacciones con metformina Investigación suspendida |
| AVE 2268 | Sanofi-Aventis | II | Bien toleradaExcreción de glucosa con dosis de 600 y 1.200mg Investigación suspendida |
| TS-033 | Taisho | II | Suspendido por un compuesto de reserva |
| BI 10773 | Boehringer-Ingelheim | III | No hay datos clínicos disponibles |
| LX4211 | Lexicon | II | Bien tolerado↑ excreción de glucosa dosisdependiente |
| ASP-1941 | Astellas Pharma Inc. y Kotobuki | III | No hay datos clínicos disponibles |
Dapagliflozina tiene una selectividad 1.200 veces mayor sobre SGLT2 que sobre SGLT1, lo que contrasta con los resultados ofrecidos por florizina, que tiene una selectividad sólo 10 veces mayor8. En el ser humano, dapagliflozina ha demostrado eficacia, sola o en combinación con metformina, en la reducción de la hiperglucemia en pacientes con DM212.
En un estudio en el que se evaluaron cinco dosis diferentes (de 2,5 a 50mg/día) durante 12 semanas, dapagliflozina indujo glucosuria moderada (52–85g/día) y demostró mejorías significativas de la glucemia comparada con placebo, con descensos de HbA1c del 0,55 al 0,90% y de glucemia en ayunas de 16 a 31mg/dL. Además, se produjo una reducción del peso de 1,3 a 2,0kg3.
También ha mostrado su eficacia en pacientes en tratamiento con insulina y otros agentes orales. Wilding et al. evaluaron los efectos de 10 o 20mg de dapagliflozina añadidos a fármacos orales como metformina y/o pioglitazona o rosiglitazona, concomitantemente con una reducción del 50% de la dosis de insulina que utilizaban los pacientes. Este estudio fue de 12 semanas de duración, aleatorizado, doble ciego y controlado con placebo13. Se produjeron descensos de HbA1c del 0,70 y el 0,78% tras 12 semanas de tratamiento con dapagliflozina 10 y 20mg, respectivamente, en comparación con placebo. Los cambios en los niveles plasmáticos de la glucemia en ayunas fueron de +17,8, +2,4 y −9,6mg/dL con placebo, 10 y 20mg de dapagliflozina. La evolución del peso fue de −1,9, -4,5 y −4,3kg en los grupos de placebo, 10mg de dapagliflozina y 20mg de dapagliflozina, respectivamente. Aunque la reducción de la dosis de insulina en un 50% dio lugar a una pérdida de peso de 1,9kg en el brazo de placebo, el tratamiento con dapagliflozina ocasionó una mayor reducción ponderal al cabo de las 12 semanas de tratamiento (−4,5 y −4,3kg en los grupos de 10 y 20mg, respectivamente).
Finalmente, un reciente estudio de Zhang et al. (2010)14ha demostrado que este inhibidor selectivo de SGLT2 es útil tanto en fases precoces como en fases avanzadas de la diabetes4. Un total de 151 pacientes con DM2 en fase precoz, la mayoría diagnosticados hacía menos de 1 año, y 58 pacientes con DM2 en fase tardía, diagnosticados en su mayor parte hacía más de 10 años, fueron tratados de forma aleatorizada con 10 o 20mg/día de dapagliflozina o placebo durante 12 semanas. En los pacientes con DM2 en fase precoz, el cambio de HbA1c fue de −0,2, -0,7 y −0,5% con placebo, 10mg y 20mg de dapagliflozina, respectivamente. En los de fase tardía la disminución de la HbA1c fue de 0, -0,6 y −0,8% con placebo, 10 y 20mg/día de dapagliflozina, respectivamente14. Todos los pacientes tratados con dapagliflozina redujeron peso, y la disminución fue estadísticamente mayor en los pacientes con DM2 en fase tardía, con una pérdida de 0,6, 2,3 y 2,5kg más que los pacientes con DM2 en fase precoz tratados con placebo, 10 y 20mg de dapagliflozina, respectivamente14.
Datos de seguridad de dapagliflozinaA pesar de la falta de datos a largo plazo, los estudios coinciden en la buena tolerancia y el buen perfil de seguridad de dapagliflozina. La inhibición de SGLT2 se acompaña de una incidencia de hipoglucemia (6-10%) similar a la del placebo (4%) o a la de metformina (9%)3, excepto cuando se añade a insulina más antidiabéticos orales (placebo más insulina: 13%; dapagliflozina 10mg más insulina: 29,2%; dapagliflozina 20mg más insulina: 25%; entre éstos, un caso de hipoglucemia severa en el grupo de placebo)13. Tampoco se han identificado alteraciones de la función renal ni electrolíticas3,12, salvo elevaciones del magnesio y descensos del ácido úrico de significado incierto3. El efecto diurético de este fármaco se ha asociado a descensos de la presión arterial sistólica de 2,6-6,4mmHg, con hipotensión en el 0-2% de los pacientes, pero estos resultados fueron similares a los de los grupos de placebo (2%) y metformina (4%)3. Finalmente, el porcentaje de infecciones del tracto urinario parece ser similar al del grupo placebo, pero no ocurrió lo mismo con las infecciones genitales secundarias a la glucosuria, que parecen estar aumentadas, aunque sin significación estadística, en los pacientes tratados con dapagliflozina: el 2-7%, frente al 0% en el grupo placebo y al 2% en el grupo de metformina3.
ConclusionesLos SGLT2 desempeñan un papel importante en la reabsorción de glucosa en el túbulo contorneado proximal renal. La inhibición selectiva de SGLT2 reduce la glucemia sin inducir secreción de insulina, hipoglucemia ni aumento de peso, y por su mecanismo de acción podría ser útil tanto en DM2 como en diabéticos tipo 1. Actualmente, el inhibidor de SGLT2 en fase más avanzada de investigación es dapagliflozina, con datos prometedores tanto en estudios con animales como en el ser humano. Sin embargo, es preciso constatar qué efectos tiene la glucosuria inducida a largo plazo. Además, estos compuestos son liposolubles y atraviesan la barrera hematoencefálica, por lo que es posible que tengan efectos a nivel central15.
Declaración de potenciales conflictos de interesesLos autores declaran no tener conflictos de intereses en relación con el tema de este artículo.
En el numero de septiembre-octubre de 2010 de Avances en Diabetología se publico una version erronea de este manuscrito. Este documento sustituye al anterior y es el que debe citarse en caso de ser referenciado.





 SGLT2. La inhibición de la reabsorción tubular renal de glucosa da lugar a glucosuria y a un descenso en los niveles plasmáticos de glucosa. La pérdida de calorías inducida por la glucosuria ocasiona pérdida de peso y reducción de la resistencia a la insulina, mientras que el descenso de la glucemia reduce la glucotoxicidad sobre la célula beta pancreática, y por tanto preserva potencialmente la función de la célula beta. Modificada de Idris et al.5' title='Efectos clínicos de la inhibición de
SGLT2. La inhibición de la reabsorción tubular renal de glucosa da lugar a glucosuria y a un descenso en los niveles plasmáticos de glucosa. La pérdida de calorías inducida por la glucosuria ocasiona pérdida de peso y reducción de la resistencia a la insulina, mientras que el descenso de la glucemia reduce la glucotoxicidad sobre la célula beta pancreática, y por tanto preserva potencialmente la función de la célula beta. Modificada de Idris et al.5' title='Efectos clínicos de la inhibición de  SGLT2. El cotransportador sodio-glucosa tipo 2 (
SGLT2. El cotransportador sodio-glucosa tipo 2 (