Las guías terapéuticas actuales difieren en las recomendaciones para la triple terapia cuando no se consiguen los objetivos con el tratamiento combinado de dos agentes orales. También difieren en el tipo de asociación y en la denominación de triple terapia. En el presente trabajo se realiza una revisión de la evidencia científica existente para determinar si la triple terapia es eficaz y segura, así como la asociación más favorable en el paciente con diabetes tipo 2. Revisando los estudios disponibles, se observa que la triple terapia mejora el control glucémico. Sin embargo, los ensayos clínicos aleatorizados disponibles en general no exceden el año de seguimiento, y no ofrecen datos sobre variables finales como morbilidad y mortalidad. En consecuencia, hasta el momento el beneficio a largo plazo y la seguridad de una triple terapia no están demostrados. En conclusión, con los datos disponibles actualmente no hay razón para retrasar la introducción de la insulina en el tratamiento de los pacientes con diabetes tipo 2 tras el fracaso de una terapia combinada doble, excepto en los casos de resistencia de los pacientes al inicio de la insulinización.
Current guidelines differ in their recommendations for triple therapy when targets are not achieved with a combined treatment of two oral agents. In addition, they diverge also in the type of association and the name given for the triple therapy. In the present manuscript we review the available scientific evidence to determine whether triple therapy is effective and safe, as well as the more favorable association in patients with type 2 diabetes. Reviewing available literature, we have noticed that triple therapy improves glycemic control. However, available randomized control trials do not extend more than one year of follow-up and they don't have data over endpoint variables as morbidity and mortality. Therefore, the long-term safety of triple therapy has not been demonstrated until now. In conclusion, with the currently available data there is no reason to delay introduction of insulin in the treatment of patients with type 2 diabetes after failure of dual combination therapy, except in cases of patients' resistance to initiate insulin therapy.
American Association of Clinical Endocrinology
American College of Clinical Endocrinology
American Diabetes Association
antidiabético oral
Australian Public Affairs Information Service-Health
Cumulative Index to Nursing and Allied Health Literature
diabetes mellitus tipo 2
dipeptidilpeptidasa 4
European Association for the Study of Diabetes
Embase Biomedical Database
Grupo de Estudio de la Diabetes en Atención Primaria de la Salud
glinidas
péptido similar al glucagón tipo 1
glitazonas
hemoglobina glucosilada
Institute for Clinical Systems Improvement
base de datos de la US National Library of Medicine
metformina
National Institute for Clinical Excellence
sulfonilureas
triple terapia
triple terapia con insulina
triple terapia sin insulina
No hay un acuerdo en la utilización del término «triple terapia» (TT). Por un lado, se emplea para describir la triple terapia oral y, por otro, también se utiliza en los regímenes con insulina en la terapia combinada oral de dos fármacos. Así pues, en las asociaciones de más de dos fármacos orales, distinguiremos las siguientes:
- •
Triple terapia sin insulina (TTO).
- •
Triple terapia con insulina (TTI).
Es sabido que la diabetes mellitus tipo 2 (DM2) tiene un mecanismo fisiopatológico complejo y progresivo, con un incremento de la producción hepática de glucosa, una reducción en la captación de glucosa por el músculo esquelético, un defecto de secreción de insulina pancreática, una respuesta anómala del glucagón tras la ingesta y un defecto en la secreción de péptido similar al glucagón tipo 1 (GLP-1) y de péptido inhibidor gástrico. Cada una de estas alteraciones puede ser revertida de forma parcial –al menos temporalmente– y de forma específica por los diversos fármacos de los que disponemos hasta el momento. Por lo tanto, tiene plausibilidad biológica que en algún momento determinado pudieran abordarse terapéuticamente todos los caminos fisiopatológicos de una manera simultánea para alcanzar los objetivos, pudiéndose por tanto hablar de triple terapia, e incluso de cuádruple terapia, situándose en el paso anterior a la plena insulinización.
La guía canadiense1 de 2008 recomienda añadir a la terapia combinada otro fármaco oral de distinta clase, o insulina, sin especificar las asociaciones más recomendables. Por el contrario, la guía 2008 del National Institute for Clinical Excellence (NICE)2 recomienda la asociación de metformina con sulfonilurea e insulina basal, y en caso de que esta última fuera inaceptable o ineficaz, asociar una glitazona. En este punto considera también exenatida, siempre y cuando el paciente presente una obesidad manifiesta (IMC >35 kg/m2) que afecte a su calidad de vida. La guía NICE constata también la limitación que existe a la hora de comparar estudios, por el gran número de combinaciones de fármacos diferentes, con distintas dosificaciones y regímenes. En mayo de 2009, una actualización del NICE consideraba añadir sitagliptina a la asociación de metformina más sulfonilurea, siempre y cuando fuera inaceptable o inapropiada la introducción de insulina.
En cuanto a la guía de consenso de la Asociación Americana de Diabetes y la Asociación Europea para el Estudio de Diabetes (ADA-EASD)3 de 2009, recomienda metformina más insulina y, dentro del apartado de tratamientos menos validados, considera como triple terapia oral la combinación de metformina, pioglitazona y sulfonilurea.
En la guía 2009 del Institute for Clinical Systems Improvement (ICSI)4 no existe una mención expresa a la triple terapia.
El consenso entre la Asociación Americana de Endocrinología Clínica y el Colegio Americano de Endocrinología (AACE/ACE) establece claramente la utilización en triple terapia de los nuevos fármacos moduladores del sistema de las incretinas (GPL-1 miméticos e inhibidores de la dipeptidilpeptidasa 4 [DPP-4]) con metformina, añadiendo sulfonilureas (SU), glitazonas (GLT) o glinidas (GLN), diferenciando también los valores de hemoglobina glucosilada (HbA1c)5.
En nuestro entorno, la guía de 2008 del Ministerio de Sanidad6 recomienda que, tras el fracaso de la terapia combinada oral, se ofrezca el tratamiento con insulina. Posteriormente indica que la triple terapia oral con metformina, sulfonilureas y glitazonas (MET + SU + GLT) puede recomendarse, después de una valoración de sus posibles riesgos cardiovasculares, en pacientes seleccionados en los que existan problemas para la insulinización. En 2009, el Grupo de Estudio de la Diabetes en Atención Primaria de la Salud (GEDAPS) modificaba su algoritmo del año anterior, incluyendo la posibilidad de añadir un análogo GLP-1 a la terapia combinada de dos antidiabéticos orales.
Ante esta discrepancia de criterios, y teniendo en cuenta que en la práctica clínica no debemos conformarnos sólo con lo plausible biológicamente, es nuestra intención buscar evidencias que nos permitan decidir entre las distintas posibles asociaciones y/o la insulinización de los pacientes.
ObjetivosEl objetivo principal fue determinar la eficacia y seguridad de la triple terapia en el tratamiento de los pacientes con diabetes tipo 2.
Los objetivos secundarios fueron:
- •
Determinar si la triple terapia con antidiabéticos orales (ADO) es mejor que la triple terapia con insulina en cuanto al control glucémico y a la disminución de la morbimortalidad de los pacientes.
- •
Determinar si existe una asociación mejor que otras en el control glucémico.
Se hicieron búsquedas en múltiples bases de datos bibliográficas electrónicas, incluyendo The Cochrane Library, MEDLINE, EMBASE, CINAHL, APAIS-Health, Australian Medical Index, Web of Science, Dissertation Abstracts y BioMed Central.
Las palabras clave utilizadas fueron «triple therapy», «combined therapy» y «diabetes», y se seleccionaron todos los artículos obtenidos.
Resultados y discusiónComo era de esperar, la bibliografía encontrada es reciente y relativamente escasa.
Triple terapia sin insulina (TTO)A la hora de ir haciendo la selección de fármacos, lo primero que nos preguntamos es si hay más de una asociación posible. Basándonos en los diferentes mecanismos de acción de los distintos fármacos, como mencionamos anteriormente, contestaríamos que sí y en la figura 1 vemos la mayoría de posibilidades.
La triple terapia oral (figura 1) con una sulfonilurea, metformina y una glitazona presenta un mayor descenso de la HbA1c en comparación con una sulfonilurea y metformina7-15 o con metformina y una glitazona (al añadir la SU)16. Se observa una mayor incidencia de hipoglucemia y mayores aumentos de peso, excepto en uno de los estudios, en el que no se observa variación del peso si MET está presente en el paso previo de terapia combinada con insulina17.
En el estudio de Charpentier y Halimi8, esta triple terapia es más eficaz cuando el nivel basal de HbA1c es menor del 8,5%, pues por encima de este valor sólo alcanzaron cifras objetivo el 13% de los pacientes. Confirma estos datos el estudio de Rosenstock et al.18
No se pueden extraer conclusiones sobre el seguimiento de la eficacia o efectividad de esta triple asociación en estos estudios, ya que la mayoría no llegaron a los 6-12 meses, excepto el de Bell, en el que se evaluó, a los 3 años, a 35 pacientes (74% en objetivos de HbA1c)12 y a los 6 años a la misma cohorte (51% en objetivos de HbA1c)19.
Tampoco se pueden realizar estudios que, estadísticamente, en cierta forma homogeneicen todos los datos de estos trabajos, ya que, por un lado, se consideraron diferentes niveles de HbA1c como cifras objetivo y, en segundo lugar, se desconoce el método de estandarización de dichas HbA1c.
La triple terapia oral con sulfonilurea, metformina y un inhibidor de la alfaglucosidasa presenta un mayor descenso de la HbA1c en comparación con la combinación sulfonilurea y metformina (−0,5 ± 0,2%, frente a placebo 0,1 ± 0,2%)20. El efecto secundario más destacable es la flatulencia (62%). En el trabajo de Standl et al. (miglitol), se constató una reducción de la HbA1c (0,55%, p= 0,04), siendo la flatulencia y la diarrea los efectos secundarios más frecuentes21. Ambos fueron estudios a 24 semanas.
Puede llamar la atención que en casi la totalidad de los estudios de TTO haya estado presente una glitazona en detrimento de otros fármacos (p. ej., acarbosa, miglitol). Pensamos que esto es debido a que, prácticamente, la triple terapia oral nace con la aparición en el mercado de las glitazonas, ya que de la combinación de sulfonilurea más metformina se pasaba ya al uso de insulina, y ello ha condicionado que en prácticamente la mayoría de los estudios sobre este aspecto haya estado presente una glitazona.
La TTO con metformina, sulfonilurea y sitagliptina ha sido estudiada en un brazo del estudio de Hermansen et al. (116 pacientes) durante 24 semanas, en el que se consiguió un descenso de HbA1c del 0,89%. Hubo un modesto aumento de las hipoglucemias y el peso22. Del mismo modo, en dos revisiones recientes23,24, los autores concluyen que la asociación de metformina, glitazona e incretina (IDPP-4 y análogos del GLP-1) tiene ventajas teóricas frente a otras, pero que es necesario una mayor investigación para tenerlas en cuenta en la elaboración de nuevas guías clínicas25.
En cuanto a la comparación entre las distintas asociaciones, sólo hemos encontrado un estudio retrospectivo en el que se compara la adición a la terapia combinada (sulfonilurea más metformina) de rosiglitazona o pioglitazona, que dio como resultado un similar control glucémico26.
La triple terapia oral de metformina más sulfonilurea a las que se añade una glitazona consigue un control glucémico –medido como una disminución de la HbA1c (partiendo de cifras moderadamente altas)– similar al obtenido si añadimos insulina18,27, aunque con un mayor coste, según los autores. En el estudio de Rosenstock et al., las cifras de HbA1c se redujeron más en el grupo insulina cuando se partía de cifras basales de HbA1c >9,5%. En el grupo insulina se registraron más hipoglucemias pero menos ganancia de peso y edemas18.
En pacientes naїve con inicio reciente de la DM2, la TTO (añadiendo pioglitazona a una sulfonilurea y metformina) tuvo similar eficacia que la combinación de insulina basal más metformina a 36 meses, sin llegar a presentar diferencias en hipoglucemias28. En el estudio de Aljabri et al., también mostró igual eficacia en los mismo términos de HbA1c, añadiendo pioglitazona o insulina, con menos hipoglucemias en la primera29.
Triple terapia con insulina (TTI)El añadir insulina a un régimen de terapia combinada de dos fármacos mejora el control metabólico independientemente del tipo de régimen de insulina (basal, bifásica o preprandial). En el trabajo de Holman et al. con diferentes análogos añadidos a la asociación MET + SU, el control glucémico fue similar30. Ese beneficio continuó a los 3 años, aunque los mejores resultados se consiguieron cuando se sustituyó la SU por un segundo tipo de insulina31. La eficacia era similar si a la combinación MET + SU se añadía insulina basal (glargina) o rosiglitazona a 6 meses32.
La triple terapia con insulina (metformina + glitazona + insulina basal) frente a la doble terapia combinada (insulina + metformina o insulina + glitazona) obtuvo más bajos niveles de HbA1c y una menor dosis de insulina17. Del mismo modo, metformina + glitazona + insulina rápida (aspart) mejora el control glucémico de pacientes obesos tipo 2 frente a la utilización de insulina NPH y/o mezcla33. También el mantenimiento de la combinación MET + GLT (rosiglitazona) al añadir insulina mejora el control glucémico sin aumentar la incidencia de hipoglucemias, aunque aumenta el peso y la frecuencia de edemas34. Por otro lado, la adición de una GLN (nateglinida) a la asociación MET + INS mejora el control de las hiperglucemias posprandiales, pero aumenta la incidencia de hipoglucemias35.
En resumen, la asociación de la triple terapia sin insulina no parece demostrar una relación beneficio/riesgo mayor que el inicio de la triple terapia con insulina, y en cambio «parece» ser más costosa según algunos autores18,27; y decimos «parece», porque en este caso de similar eficacia tendríamos que plantearnos cuál es la coste-eficacia incremental, pues revela la verdadera carga económica más que una simple comparación de costes, y de momento esto lo desconocemos (la coste-eficacia incremental se calcula a partir del NNT, valorando el coste incremental de un tratamiento completo × el número de pacientes necesario para producir una unidad de eficacia).
Hasta aquí hemos visto que todos los estudios (figura 1) utilizan como puntos finales variables subrogadas, fundamentalmente los cambios en la HbA1c, en lugar de resultados clínicos; por otro lado, la duración de los estudios no sobrepasa, en general, los 6 meses, y, por último, nos encontramos con un escaso número de pacientes estudiados. Sólo existe un estudio en investigación básica en el que se observa una reducción de los factores implicados en patologías cardiacas en ratas con resistencia a la insulina36.
Cuádruple terapiaEn cuanto a la posibilidad de una cuádruple terapia, y aunque farmacológicamente es posible abordar los diferentes caminos fisiopatológicos, creemos que si ya la triple terapia presenta muchos condicionantes para su manejo con cierta seguridad, puesto que para su prescripción individualizada se deben valorar la edad, el peso del paciente, la disfunción renal y hepática y las comorbilidades cardiopulmonares, y se requiere un seguimiento más estrecho del paciente, mucho más complejo resultaría aún el manejo de cuatro fármacos antidiabéticos orales en un paciente que posiblemente esté tomando, para otras morbilidades, otros tantos fármacos orales.
Siguiendo el principio bioético de la no maleficencia, y teniendo otras alternativas conocidas y seguras (insulina), creemos que en el momento actual esta posibilidad entra más en el campo de la investigación que en el de la práctica clínica.
ConclusionesLa TT es eficaz para mejorar el control glucémico de los pacientes diabéticos tipo 2. No obstante, el beneficio a medio y largo plazo y la seguridad de una TTO frente a la introducción de la insulina son inciertos. Por ello, con los datos actuales, de momento no encontramos «ventajas» para retrasar la introducción de la insulina en el régimen terapéutico tras el fracaso de una terapia combinada doble, haciendo la salvedad de los casos de resistencia de los pacientes a la insulinización.
Declaración de potenciales conflictos de interesesEdelmiro Menéndez Torre ha recibido honorarios por actividades docentes por invitación de sanofi-aventis, Novo Nordisk, MSD, Novartis, GSK y Lilly, y ha participado en ensayos clínicos financiados total o parcialmente por Novo Nordisk, sanofi-aventis y Lilly.




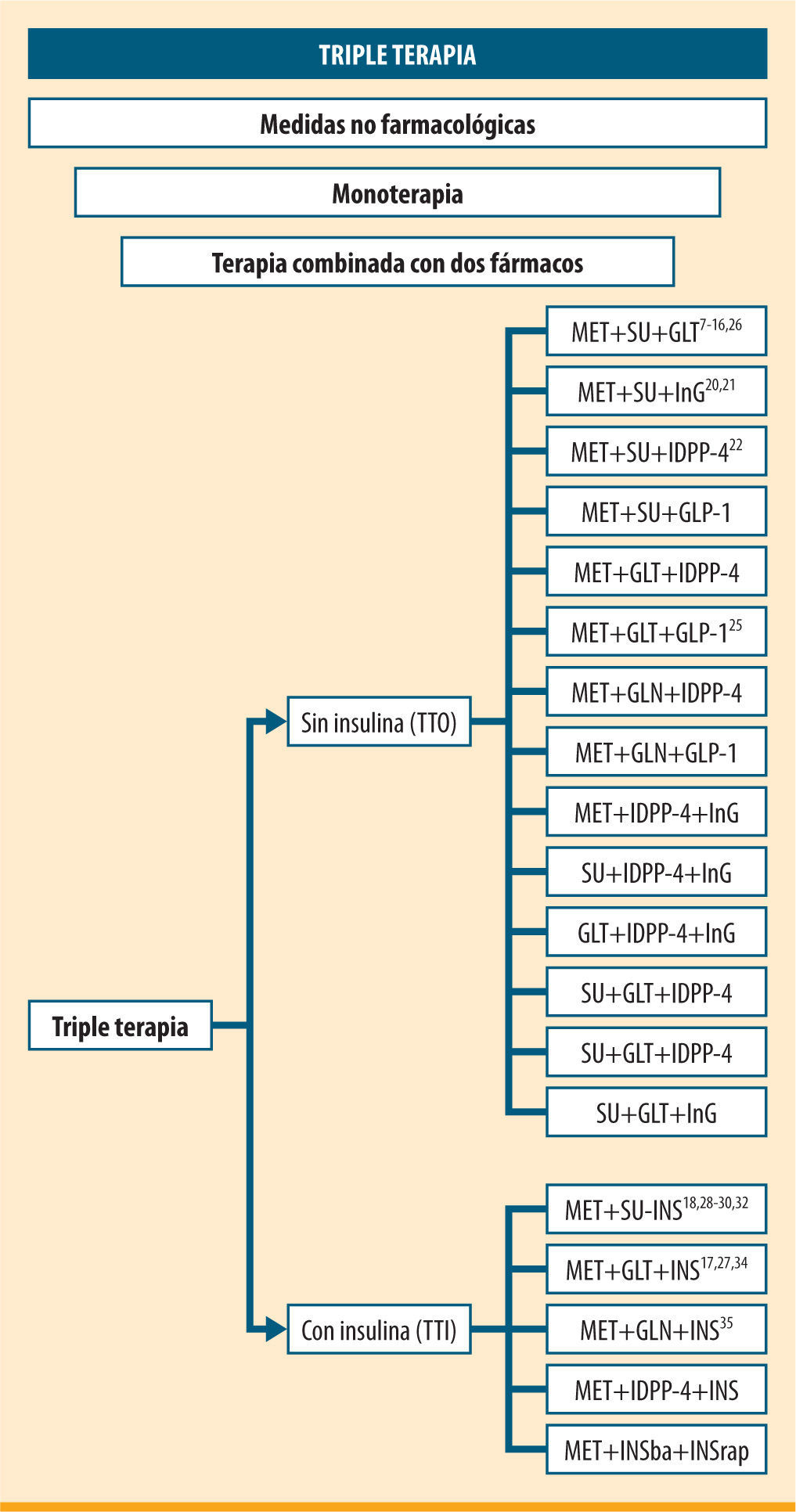
 MET: metformina;
MET: metformina; 