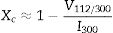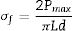Compactados de hidroxiapatita estequiométrica (HAp) y solución sólida de magnesio hidroxiapatita (Mg-HAp) fueron preparados mediante la técnica de compactación hidrotérmica en caliente (CHC), a diferentes temperaturas (150, 175 y 200°C), utilizando una presión de carga uniaxial de 60MPa durante 6h, con la adición del 10% en peso de agua desionizada. El material de partida fue obtenido mediante síntesis hidrotérmica a 150°C durante 10h. Los productos compactados fueron caracterizados química, física y mecánicamente. De acuerdo con el análisis de resultados, se determinó que un incremento en la temperatura de CHC favoreció la reacción entre las partículas de HAp o Mg-HAp y el agua promoviendo fases con mayor grado de cristalinidad, sin generar subproductos o alteraciones estructurales. Este resultado es particularmente relevante, ya que durante la CHC se produce un empaquetamiento efectivo de las partículas, activado por el mecanismo de disolución-recristalización en presencia del agua, con lo cual se logró una densificación del orden del 70%. Los compactados de HAp y Mg-HAp obtenidos a 200°C, con porosidad abierta del orden del 30-36%, mostraron valores de máxima densidad aparente de 3,085±0,138g/cm3 y 2,792±0,021g/cm3, respectivamente, con una máxima resistencia a la tensión de 7,10±0,20 y 5,89±0,06MPa. De acuerdo a estos resultados, el material obtenido podría ser utilizado en aplicaciones ortopédicas y/u odontológicas.
Preparation of hydrothermal hot-pressed (HHP) compacts of the stoichiometric hydroxyapatite and solid-solution of magnesium hydroxyapatite powders (HAp and Mg-HAp) was carry out at different temperatures 150, 175 and 200°C, using uniaxial pressure load of 60MPa for 6h, with the addition of 10% wt. of deionized water as a solvent. The starting powders were obtained by hydrothermal synthesis at 150°C for 10h. The HHP compacts were chemical, physical and mechanically characterized. According to the results, it has been determined that an increase of the HHP temperature stimulate the reaction between the added water and the particles of HAp or Mg-HAp, which results on an increase of crystallinity degree without the formation of any addition products or alteration of the HAp structure. This result is particularly relevant, due to during HHP process, the production of effective packing of the particles which is activate by the dissolution-recrystallization mechanism in presence of added water which allow a densification near of 70%. For the HHP compacts of the HAp and Mg-HAp prepared at 200°C, with porosity near to 30-36% of open pores, achieve the maximum apparent density value of 3.085±0.138g/cm3 and 2.792±0.021g/cm3, respectively, with the maximum tensile strength of 7.10±0.20 and 5.89±0.06MPa. From these results, the obtained HHP compacts might be useful for orthopedics and/or dentist applications.
Los fosfatos de calcio como la hidroxiapatita (HAp, Ca10(PO4)6(OH)2) son utilizados ampliamente como materiales de partida en la fabricación de implantes de hueso y dientes, debido a la similitud química y cristalográfica que comparten con la parte mineral del tejido óseo [1,2]. En la estructura de la HAp es posible la sustitución de los cationes y aniones, lo que permite aproximar la composición de este material a la parte inorgánica del tejido óseo natural. El reemplazo de iones magnesio por iones calcio dentro de la estructura de la HAp ha sido estudiado desde hace más de dos décadas, encontrando que la incorporación del magnesio inhibe la cristalización de la hidroxiapatita reduciendo la relación molar Ca/P, además de disminuir el tamaño del cristal [3]. El contenido de magnesio en el tejido duro está distribuido en el esmalte, dentina y hueso, que contienen 0,44, 1,23 y 0,72% en peso de magnesio, respectivamente [4]. Algunos estudios sugieren que el contenido máximo de magnesio que se puede incorporar en la hidroxiapatita sintética es del 0,4% en peso, debido a que altas concentraciones de magnesio forman diferentes fases cristalinas. Sin embargo, ese comportamiento está en función del método de síntesis y de la presencia de otros iones en la estructura, tales como el carbonato o fluoruro, que se incorporan de forma simultánea con el magnesio [3,5].
Teniendo en cuenta que las rutas de procesamiento de polvos de HAp incluyen la posibilidad de intercambiar iones, el método propuesto para obtener cuerpos sólidos de alta densidad es un aspecto importante para mejorar las propiedades mecánicas que amplían el uso de este material [6]. En este sentido, muchas investigaciones relacionadas con la consolidación de polvos de HAp incluyen una amplia gama de técnicas de procesamiento [7,8].
Es conocido que el tratamiento térmico de la HAp está relacionado con el incremento en el tamaño de las partículas y con la estabilidad termoquímica que presenta al ser calcinada por encima de los 700°C, ya que se induce la liberación de iones hidroxilo, provocando la descomposición de la HAp en fosfato tricálcico (β-TCP) [9,10].
Recientemente se realizaron investigaciones enfocadas a estudiar el comportamiento de la densificación de partículas de HAp preparadas mediante el método químico de precipitación y mecanoquímico. Los métodos de síntesis empleados permitieron la cristalización de partículas de HAp con diferentes tamaños [11]. Mediante el método de precipitación fue posible la obtención de partículas aglomeradas del orden de 108nm, mientras que por la vía de síntesis mecanoquímica los productos de reacción presentaron un tamaño de partícula de 1μm. Los cuerpos porosos de estos polvos fueron preparados mediante prensado uniaxial, con cargas de 1,3 y 2,5MPa, seguido de una etapa de prensado isostático en frío, que se efectuó a 200MPa. Posteriormente, a estas muestras se les realizaron tratamientos de sinterización, en el rango de temperaturas de 1.000-1.400°C por un periodo de 2h. Ramesh et al. [11] determinaron que los cuerpos de HAp preparados mediante la ruta de síntesis por precipitación mostraron un mejor comportamiento de densificación que los cuerpos sintetizados mediante la ruta mecanoquímica. Esta diferencia fue atribuida principalmente a que las partículas de tamaño más fino, durante el tratamiento térmico, disminuyeron el área superficial de transferencia de calor, promoviendo un aumento en la densidad durante la sinterización, mientras que las partículas de mayor tamaño, constituidas por grandes aglomerados duros, no mostraron un buen empaquetamiento en verde, dando como resultado una pobre densificación.
Por otra parte, la técnica de compactación hidrotérmica en caliente (CHC) fue desarrollada durante la década de 1980 por varios investigadores, con el propósito de densificar diversos materiales a bajas temperaturas y bajas presiones de compactación en condiciones hidrotérmicas, inhibiendo así el crecimiento de partículas y manteniendo su morfología inicial [12,13]. El mecanismo de reacción durante la CHC de partículas involucra calentamiento a temperaturas relativamente bajas y la aplicación de compresión simultáneamente, lo que acelera la densificación de los polvos, al producirse la unión de las partículas por la reacción hidrotérmica, que sucede debido a que el agua actúa como un agente de unión. El resultado de la reacción hidrotérmica une las partículas e incrementa la resistencia mecánica del compactado [14]. Este método ha sido utilizado para consolidar materiales que convencionalmente no son fáciles de sinterizar, y también se ha utilizado para el reciclaje de numerosos tipos de materiales inorgánicos que, mezclados con agua o una solución alcalina o ácida, han servido para preparar diversos tipos de materiales compactados tales como vidrios de borosilicato [13–15], ceniza de carbón [16], hidroxiapatita deficiente en calcio [14] y hidroxiapatita comercial HAP-300 [17], entre otros.
En el presente trabajo de investigación se muestran los resultados más significativos de la consolidación de polvos de hidroxiapatita estequiométrica (HAp) y polvos de soluciones sólidas de magnesio hidroxiapatita (Mg-HAp) sintetizados en condiciones hidrotérmicas y posteriormente sometidos al proceso de CHC, evaluando particularmente la influencia de la temperatura.
Parte experimentalInicialmente en este trabajo se sintetizaron los polvos de HAp y de Mg-HAp, con un contenido del 4% molar de Mg, mediante la ruta de síntesis hidrotérmica empleando una temperatura de 150°C durante un periodo de 10h. Posteriormente los polvos sintetizados fueron utilizados en la preparación de compactados de 20±0,1mm de diámetro y 5±0,1mm de espesor mediante el proceso de CHC, en una autoclave de cuerpo cilíndrico y dos pistones de acero inoxidable [12]. Los parámetros de CHC utilizados fueron 10% en peso de agua como solvente, un período de tiempo de 6h, carga de presión uniaxial de 60MPa y utilización de tres diferentes temperaturas: 150, 175 y 200°C.
Cabe resaltar que se realizaron 3 compactados bajo las mismas condiciones de compactación con el propósito de tener muestras por triplicado. Para obtener cada pastilla compactada se tomaron 5g de polvo de HAp o Mg-HAp, subsecuentemente el polvo de la hidroxiapatita fue mezclado homogéneamente con el agua desionizada y fue colocado en la cámara de la autoclave. Una vez ajustada la presión de carga se inició el calentamiento hasta la temperatura deseada, utilizando una velocidad de calentamiento de 5°C/min. Terminada la reacción de compactación, la autoclave se dejó enfriar hasta temperatura ambiente, y la pastilla compactada fue removida para llevarla a caracterización. Con el propósito de mantener la pastilla libre de humedad, se sometió a calentamiento en un horno a 80°C durante 24h.
Los productos de la compactación fueron caracterizados mediante análisis cuantitativo vía húmeda por espectroscopia de emisión atómica con acoplamiento de plasma inducido (AES-ICP, Shimadzu ICPE-9000 Multi-type ICP Emission Spectrometer) con una precisión de 1ppb para Ca, Mg, H y O, y 1-10ppb para el P, tomando para este análisis 20±0,1mg; la muestra fue disuelta en 100±0,15ml de solución de HNO31M. La presencia de los grupos PO34− y OH− fue determinada mediante análisis por espectroscopia infrarroja acoplado con transformada de Fourier, el cual se realizó utilizando un equipo FT/IR-400, JASCO. Una fracción de la pastilla compactada fue molida en mortero de ágata y mezclada con KBr en una proporción 1:200 para formar pastillas de 5mm de diámetro; estas mezclas fueron mantenidas a 100°C durante 24h para eliminar toda la humedad previo al análisis. El rango de la longitud de onda utilizado fue entre 400 y 4.000cm−1. Las fases cristalinas fueron determinadas mediante difracción de rayosX, utilizando como equipo un difractómetro de rayosX Ultima IV, Rigaku, y las indexaciones se realizaron con la carta JCPDS 09-0432. De acuerdo con Landi y colaboradores [18], el grado de cristalinidad de las muestras (Xc) corresponde a la fracción de la fase cristalina en el volumen examinado, y fue determinado mediante la relación:
Donde I300 es la intensidad de la reflexión (300) de la HAp y V112/300 se refiere a la diferencia que existe entre las intensdades de las reflexiones (112) y (300), que desaparecen completamente en muestras no cristalinas.
La densidad aparente de los compactados se llevó acabo para un total de 3 pastillas compactadas a las mismas condiciones, contenido de agua del 10% en peso y presión de carga de 60MPa para las tres temperaturas (150, 175 y 200°C). Esta determinación de la densidad aparente fue obtenida mediante el método de Arquímedes, utilizando un picnómetro de helio (Multipycnometer Quantachrome PY3000) a una presión de gas de 0,117MPa. Cabe mencionar que para esta determinación se realizaron compactados por triplicado a las diferentes temperaturas de CHC (150-200°C); subsecuentemente todos los compactados fueron secados a 80°C durante 24h para asegurar que estuvieran totalmente secos. Por cada muestra analizada, el picnómetro de He realizó un total de 5 mediciones, a una temperatura constante de 25°C; la desviación estándar del equipo fue mantenida en 0,008% en todas las determinaciones, y la desviación estándar promedio de la densidades obtenidas fue del orden de ±0,026.
Para la determinación de la resistencia a la tensión (ensayo de compresión diametral conocido como ensayo Brazilian, método estandarizado por la Sociedad Internacional de Mecánica de Rocas [19,20]) se consideró el promedio de 2 muestras compactadas por experimento. En esta prueba se colocó el disco de los compactados con el eje horizontal entre las platinas de la máquina de compresión (Shimadzu, Autograph® AG-IS 50kN) y se sometió a una carga uniaxial con una velocidad de cabezal de 0,5mm/min, hasta que se presentó la falla por separación a lo largo del diámetro vertical, obteniendo así la carga máxima soportada. La resistencia a la tensión se calculó con la carga de ruptura de la probeta de acuerdo a la ecuación:
Donde σf es la resistencia a la tensión, Pmax es la carga de ruptura, y L y d son el diámetro y el espesor de la muestra, respectivamente.
Las observaciones de morfología y tamaño de las partículas en la superficie de fractura de los compactados como en los polvos de partida se realizaron mediante microscopia electrónica de barrido de alta resolución (MEB) con el microscopio JEOL JSM-6610LV, utilizando 15Mv y un recubrimiento de oro sobre las muestras observadas. Las imágenes obtenidas fueron en un rango de magnificación entre 20.000 a 80.000X. Se utilizó el analizador de imágenes (Image-Pro® Plus) para la determinación del tamaño promedio de partícula, empleando las imágenes obtenidas por microscopia. Se realizaron conteos entre 400 y 500 por campo.
Resultados y discusiónCaracterización de los polvos del material de partidaCon la finalidad de determinar la composición química del material de partida utilizado en la CHC, los polvos de HAp y Mg-HAp, respectivamente, fueron analizados mediante análisis cuantitativo vía húmeda (ICP), lo cual se reporta en la tabla 1. Se determinó que la composición química de los polvos de HAp producidos corresponde a la Ca9,99(PO4)6,00(OH)2, y asimismo los polvos de Mg-HAp producidos mediante síntesis hidrotérmica presentaron la composición química Ca9,63Mg0,37(PO4)6(OH)2. Por otra parte, mediante el análisis de difracción de rayosX se determinó que tanto los polvos de HAp como los de Mg-HAp producidos para este estudio presentaron las reflexiones características correspondientes con la HAp de estructura hexagonal de acuerdo con la carta patrón JCPDS 09-0432. Asimismo, se evidenció el corrimiento hacia ángulos 2θ mayores de todas las reflexiones del polvo de soluciones sólidas de magnesio hidroxiapatita (Mg-HAp), debidas a la incorporación de los iones magnesio en la estructura y trayendo consigo modificaciones en la red cristalina de la HAp, fenómeno que ha sido reportado por diversos autores que han sintetizado Mg-HAp [3,21,22]. Mediante el análisis de imágenes realizado a las micrografías de estos polvos se determinó que en el caso del polvo de HAp se obtuvo un tamaño promedio de partícula de 47,54±1,58nm y la morfología exhibida fue del tipo esfenoide, con una relación axial (factor de forma [largo/diámetro] [23]) igual a 1,65, mientras que en caso de los polvos de Mg-HAp el tamaño promedio fue de 42,50±2,89nm, igualmente con una morfología del tipo esfenoide con una relación axial 2,48.
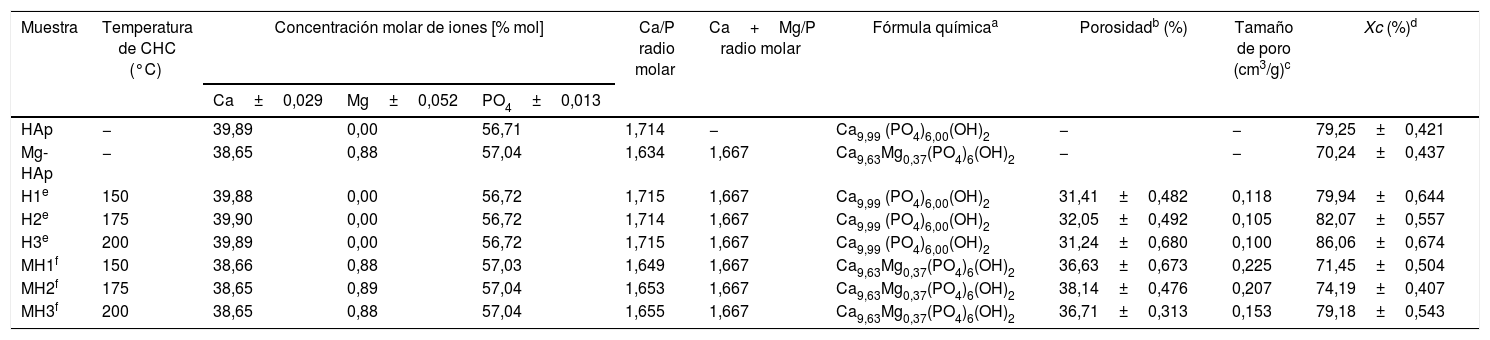
Resumen de las condiciones iniciales de los polvos y resultado de los análisis químicos de las muestras compactadas hidrotérmicamente
| Muestra | Temperatura de CHC (°C) | Concentración molar de iones [% mol] | Ca/P radio molar | Ca+Mg/P radio molar | Fórmula químicaa | Porosidadb (%) | Tamaño de poro (cm3/g)c | Xc (%)d | ||
|---|---|---|---|---|---|---|---|---|---|---|
| Ca±0,029 | Mg±0,052 | PO4±0,013 | ||||||||
| HAp | − | 39,89 | 0,00 | 56,71 | 1,714 | − | Ca9,99 (PO4)6,00(OH)2 | − | − | 79,25±0,421 |
| Mg-HAp | − | 38,65 | 0,88 | 57,04 | 1,634 | 1,667 | Ca9,63Mg0,37(PO4)6(OH)2 | − | − | 70,24±0,437 |
| H1e | 150 | 39,88 | 0,00 | 56,72 | 1,715 | 1,667 | Ca9,99 (PO4)6,00(OH)2 | 31,41±0,482 | 0,118 | 79,94±0,644 |
| H2e | 175 | 39,90 | 0,00 | 56,72 | 1,714 | 1,667 | Ca9,99 (PO4)6,00(OH)2 | 32,05±0,492 | 0,105 | 82,07±0,557 |
| H3e | 200 | 39,89 | 0,00 | 56,72 | 1,715 | 1,667 | Ca9,99 (PO4)6,00(OH)2 | 31,24±0,680 | 0,100 | 86,06±0,674 |
| MH1f | 150 | 38,66 | 0,88 | 57,03 | 1,649 | 1,667 | Ca9,63Mg0,37(PO4)6(OH)2 | 36,63±0,673 | 0,225 | 71,45±0,504 |
| MH2f | 175 | 38,65 | 0,89 | 57,04 | 1,653 | 1,667 | Ca9,63Mg0,37(PO4)6(OH)2 | 38,14±0,476 | 0,207 | 74,19±0,407 |
| MH3f | 200 | 38,65 | 0,88 | 57,04 | 1,655 | 1,667 | Ca9,63Mg0,37(PO4)6(OH)2 | 36,71±0,313 | 0,153 | 79,18±0,543 |
El resultado de los análisis cuantitativos por vía húmeda de los compactados hidrotérmicos, preparados a diferentes temperaturas de compactación, se muestra en la tabla 1. Se determinó que en la composición nominal de los compactados se presenta una estabilidad del contenido de magnesio con respecto al incremento de la temperatura de compactación. Asimismo, se comprobó que existe un ligero aumento en la relación Ca/P, como resultado de la reacción hidrotérmica que ocurre durante la CHC; este resultado es consistente con lo reportado por K. Yanagisawa y colaboradores [14] en su investigación sobre la compactación de hidroxiapatita deficiente en calcio.
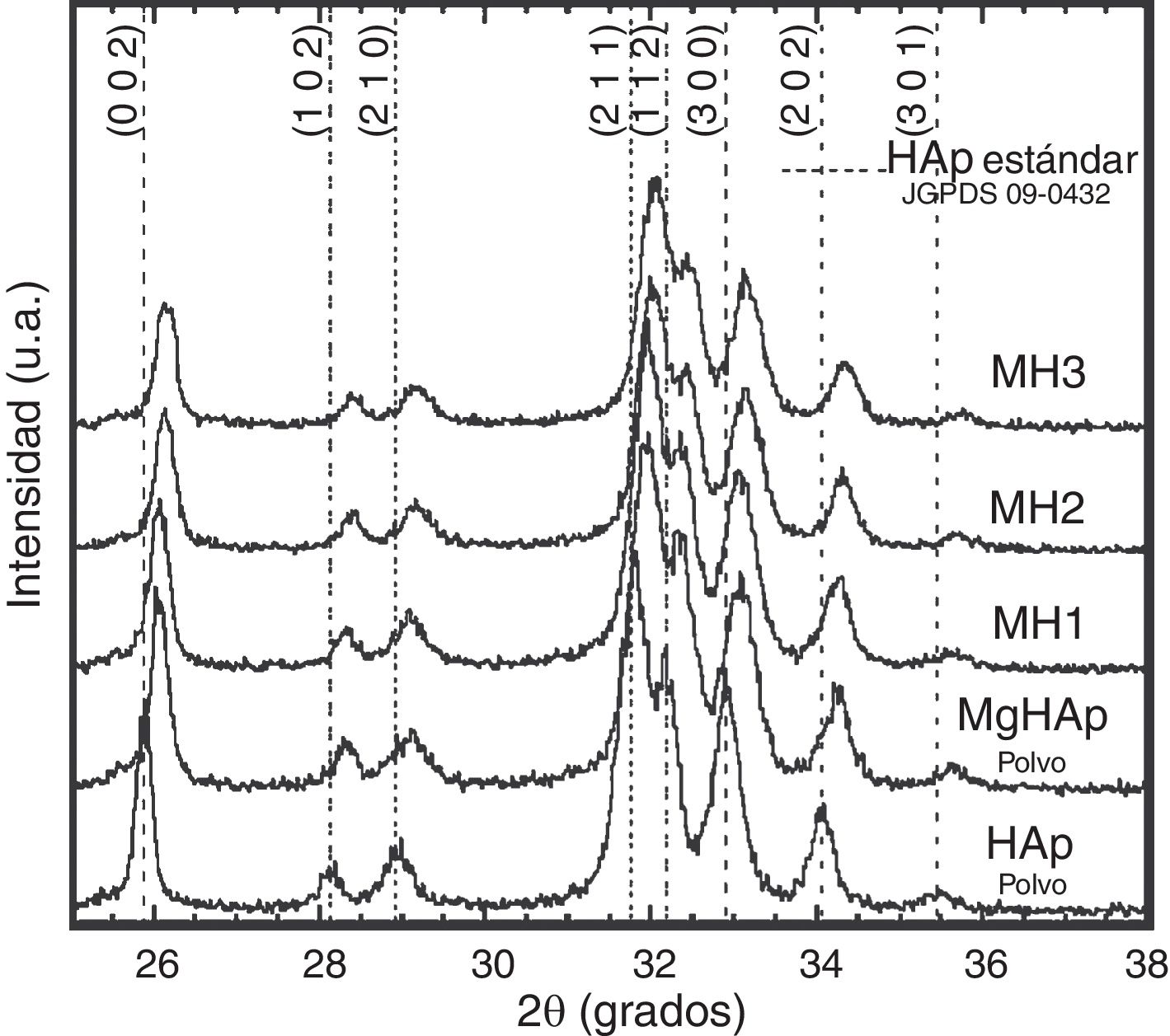
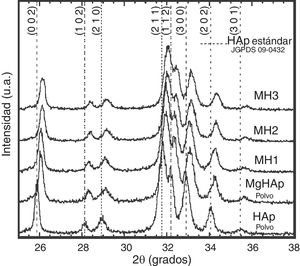
Los patrones de difracción de rayosX correspondientes a las muestras antes y después de ser sometidas a CHC variando la temperatura de compactación desde 150 hasta 200°C se muestran en la figura 1. Se evidenció la presencia de las reflexiones características de la estructura hexagonal de la hidroxiapatita correspondientes con la carta patrón JCPDS 09-0432, donde la reflexión principal y de mayor intensidad pertenece al plano (211), ubicado en el ángulo 2θ=31,7°, el cual se complementa con la presencia de tres reflexiones de menor intensidad: una en el plano (112), localizado en el ángulo 2θ=32,2°; la segunda en el plano (300), situado en el ángulo 2θ=32,9°, y la tercera, de menor intensidad, en el plano (202), encontrado a un ángulo 2θ=34,22°. Se corroboró también que para el caso de los compactados de Mg-HAp todas las reflexiones de la difracción que fueron presentadas en el material de partida mantuvieron el corrimiento hacia ángulos 2θ mayores, comportamiento debido a la incorporación del magnesio en la estructura cristalina. Asimismo, se puede decir que durante el proceso de CHC ocurrió una recristalización en el material empleado, promovido por el mecanismo de disolución-recristalización que rige este tipo de reacciones de compactación hidrotérmica, lo cual favoreció un ligero incremento del grado de cristalinidad (Xc). Este comportamiento se hizo evidente en ambos tipos de polvos compactados (HAp y Mg-HAp). En el caso de los polvos de la solución sólida de Mg-HAp, inicialmente se presentó un grado de cristalinidad de 70,24%, y tras la CHC a 150°C ascendió a 71,45%. No obstante, el cambio más evidente se dio con el tratamiento de CHC a la mayor temperatura (200°C), donde se alcanzó un valor de Xc de 79,18%, el equivalente a un incremento del 8,9%.
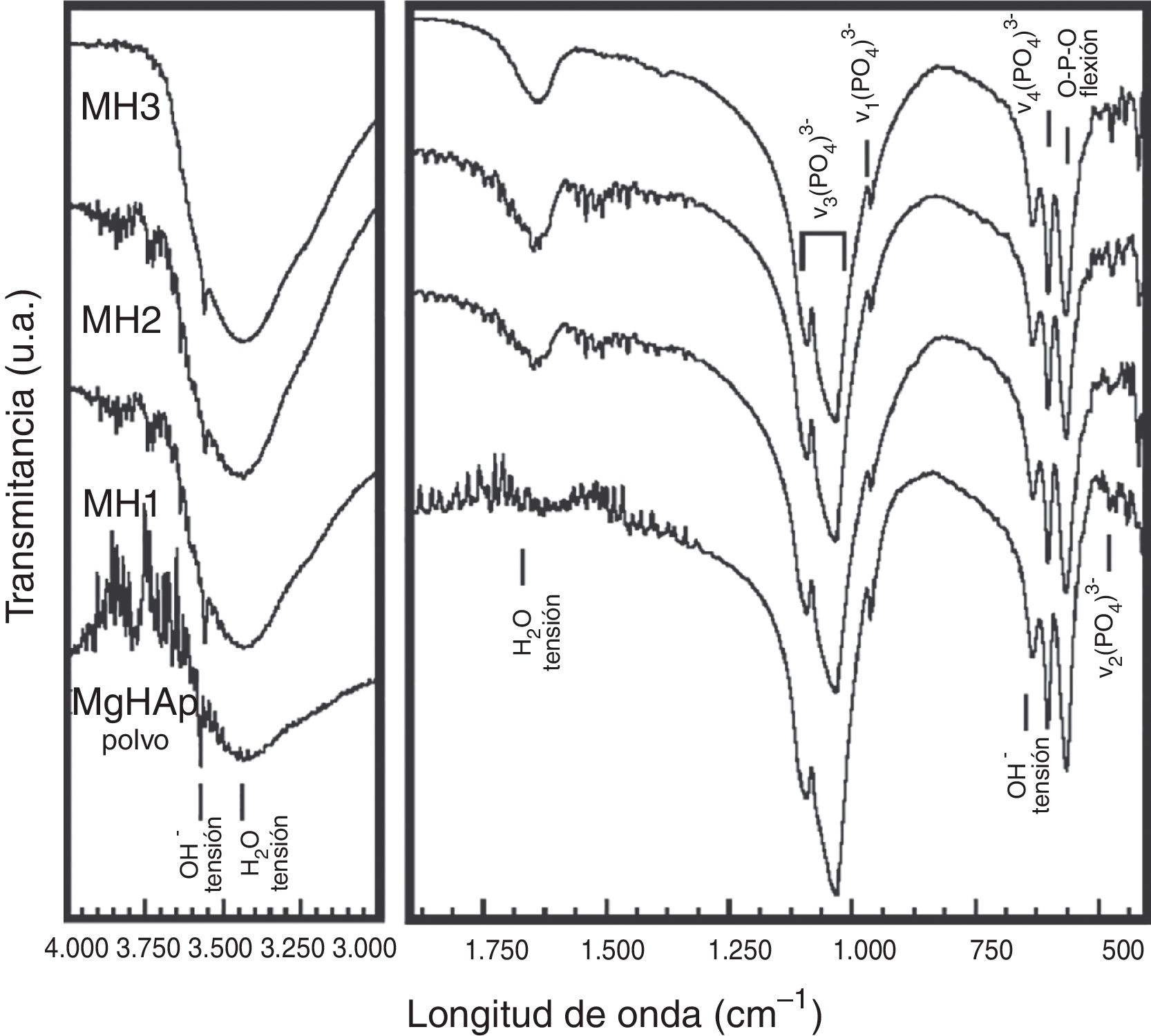
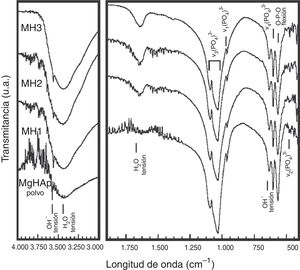
Por otra parte, los análisis por espectroscopia infrarroja de la figura 2 corresponden a las muestras de Mg-HAp antes y después de ser compactadas hidrotérmicamente a diferentes temperaturas (150-200°C). Se lograron identificar claramente las señales características de la hidroxiapatita, en la cual las vibraciones procedentes de los grupos PO4−3 fueron registradas en las longitudes de onda 1.093, 1.033, 961, 605 y 463cm−1, las bandas de flexión del grupo O–P–O fueron detectadas en 563cm−1 y las bandas de tensión del enlace O–H del grupo hidroxilo se localizaron en las longitudes de onda 3.561 y 634cm−1. Así mismo, se corroboró la presencia de bandas características de tensión de la molécula de agua en la longitud de onda 3.438cm−1, procedentes del agua utilizada como medio disolvente en el proceso de CHC.
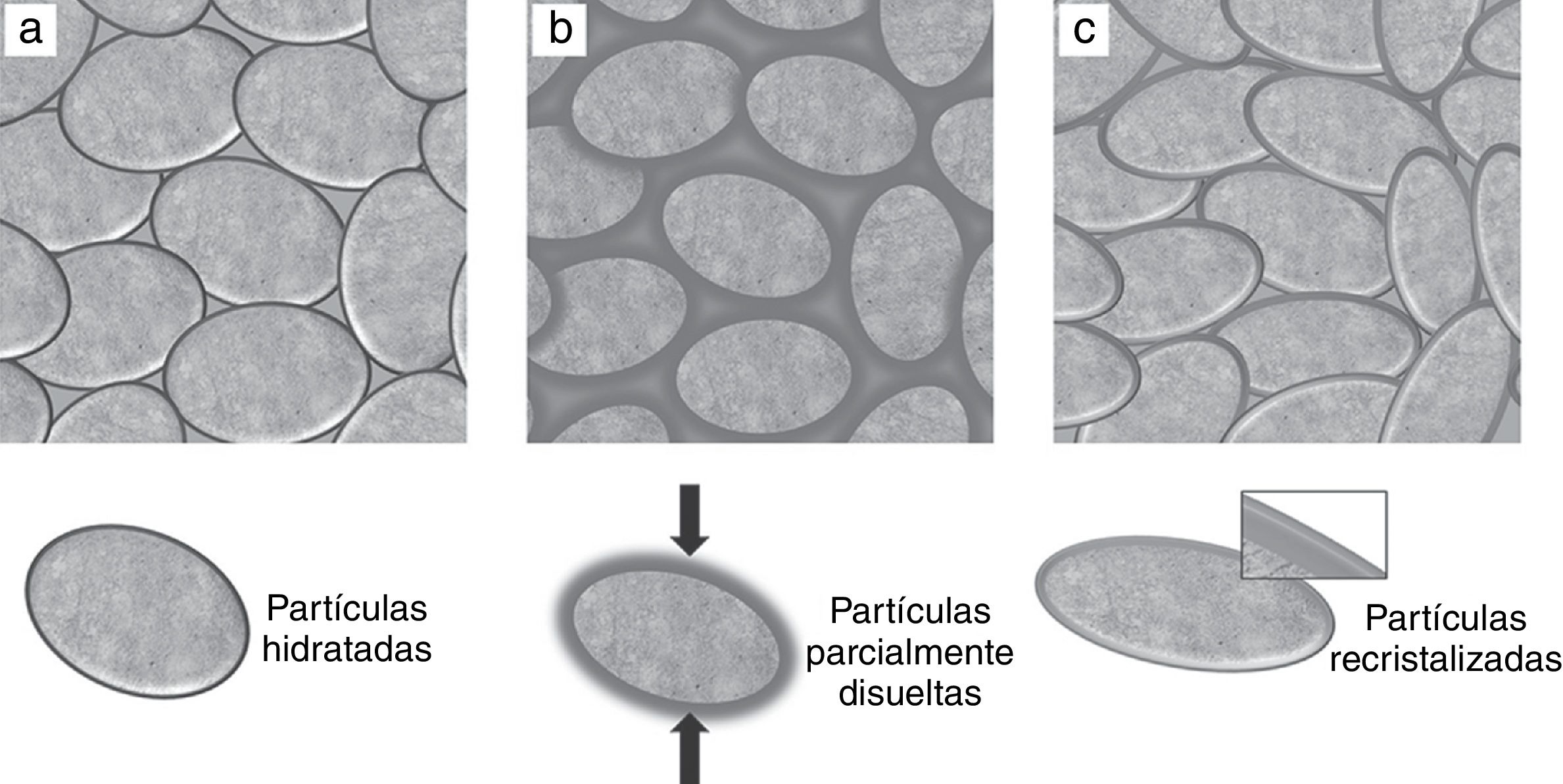
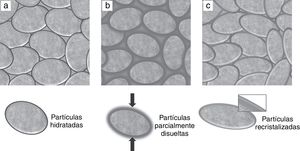
Las imágenes de la superficie de fractura de las muestras compactadas hidrotérmicamente a 150 y 200°C, respectivamente, se muestran en la figura 3. En el análisis de las imágenes, para el caso de los compactados de HAp (fig. 3a,b), se observó un ligero aumento en la longitud de las partículas, de cerca del 8% con el incremento de la temperatura de CHC. Asimismo, para los compactados obtenidos en condiciones hidrotérmicas a baja temperatura (150°C) con los polvos de Mg-HAp (fig. 3c) se observaron aglomeraciones de las partículas esfenoides, las cuales presentaron un tamaño promedio de 42,67±4,64nm y relación axial de 2,68. De manera similar a lo observado en los compactados de HAp, con el incremento de la temperatura de compactación hidrotérmica hasta 200°C (fig. 3d) se promovió el crecimiento longitudinal en las partículas de Mg-HAp, obteniéndose un valor promedio de 44,89±4,72nm y una relación axial de 3,84, lo que representa un incremento en la longitud de las partículas de aproximadamente un 5%. Por otra parte, cabe mencionar que la morfología de las partículas, a pesar de que permaneció de tipo esfenoidal en todos los casos, presentó un incremento significativo en cuanto a la relación axial, obteniéndose una modificación del 25% después de la CHC en los compactados de HAp a 200°C, mientras que en los compactados de Mg-HAp a las mismas condiciones se presentó un 35% de modificación. Estos ligeros incrementos en la longitud, así como los más evidentes cambios en los diámetros de las partículas de HAp y Mg-HAp, se asocian con las reacciones hidrotérmicas que ocurren durante el proceso de compactación, por el mecanismo de disolución-recristalización [14], permitiendo que en las partículas, especialmente en la parte central, se concentre el esfuerzo de compresión y, por lo tanto, se presente el alargamiento de la partícula con dirección hacia los extremos de la misma, tal como se ilustra en la figura 4. Esta ligera modificación en la morfología de las partículas posiblemente se debe a la reacción de las partículas con el agua presente durante la CHC, permitiendo que existiera una continua disolución-recristalización de las partículas, que a su vez depende de la presencia de magnesio en la estructura de la hidroxiapatita y de la temperatura. De esta manera se puede decir que la compactación en condiciones hidrotérmicas de los polvos de HAp y Mg-HAp fue lograda con éxito.
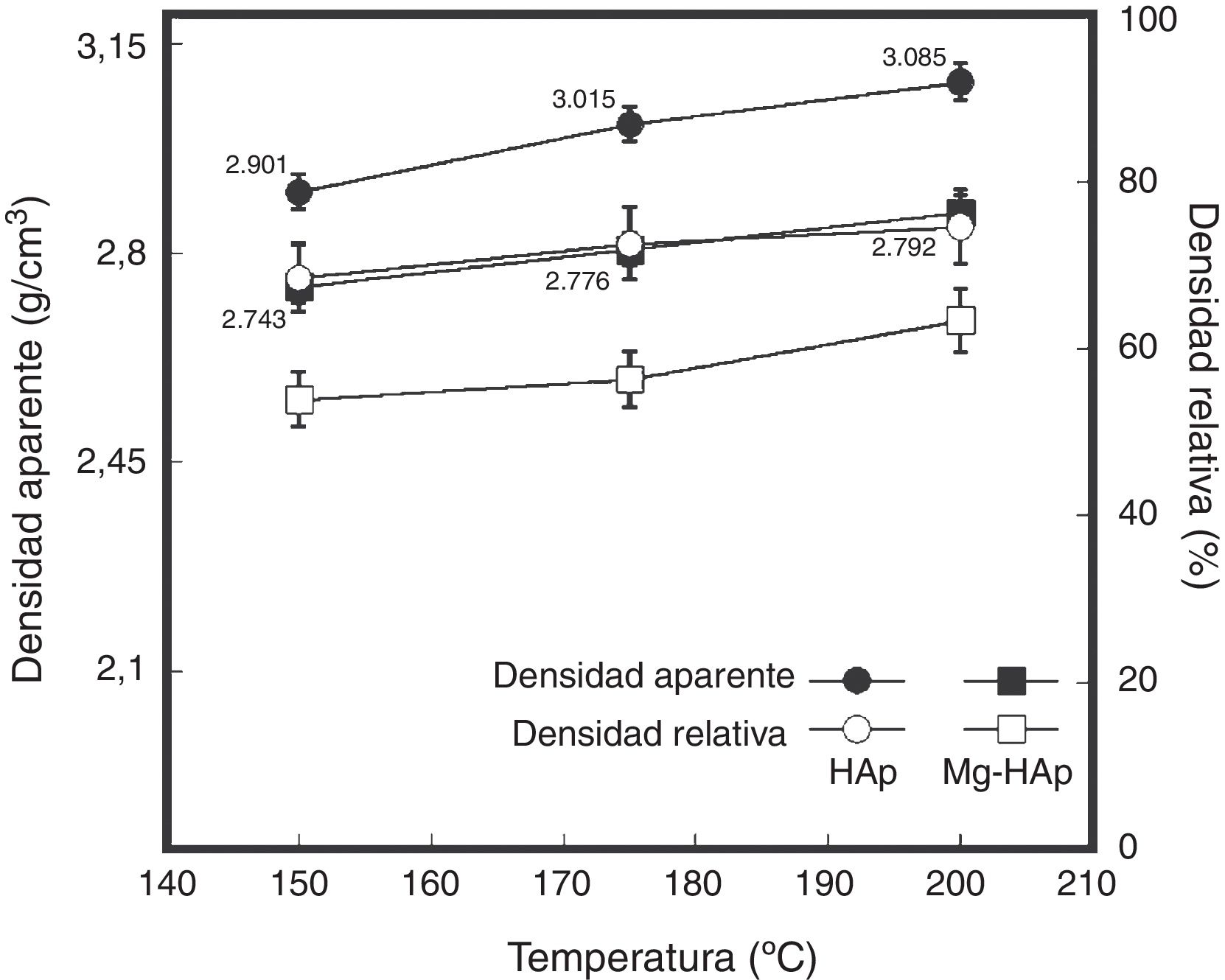
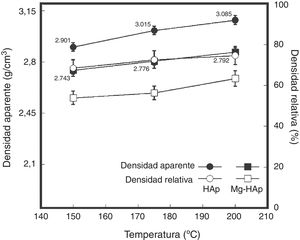
El comportamiento típico de la densidad aparente y relativa de los compactados de los polvos de HAp y Mg-HAp estudiados fue graficado en función de la temperatura, como se muestra en la figura 5. En general, cuando los polvos de Mg-HAp fueron compactados a diferentes temperaturas durante 6h con un contenido del 10% en peso de H2O, el análisis de los resultados evidencia que todos los polvos de HAp y Mg-HAp fueron densificados exitosamente en las condiciones de CHC investigadas. Se determinó que el valor máximo de la densidad aparente alcanzada para los compactados de HAp y Mg-HAp fue de 2,901±0,013 y de 2,743±0,013g/cm3, respectivamente, obtenidos a 150°C, mientras que para los compactados preparados a mayor temperatura (200°C) el valor de densidad aparente máxima fue de 3,085±0,138 y de 2,792±0,021g/cm3, para los compactados de HAp y Mg-HAp, respectivamente. De esta manera se puede decir que con el incremento de la temperatura de CHC se promueve la obtención de compactados con mayores valores de densidad aparente.
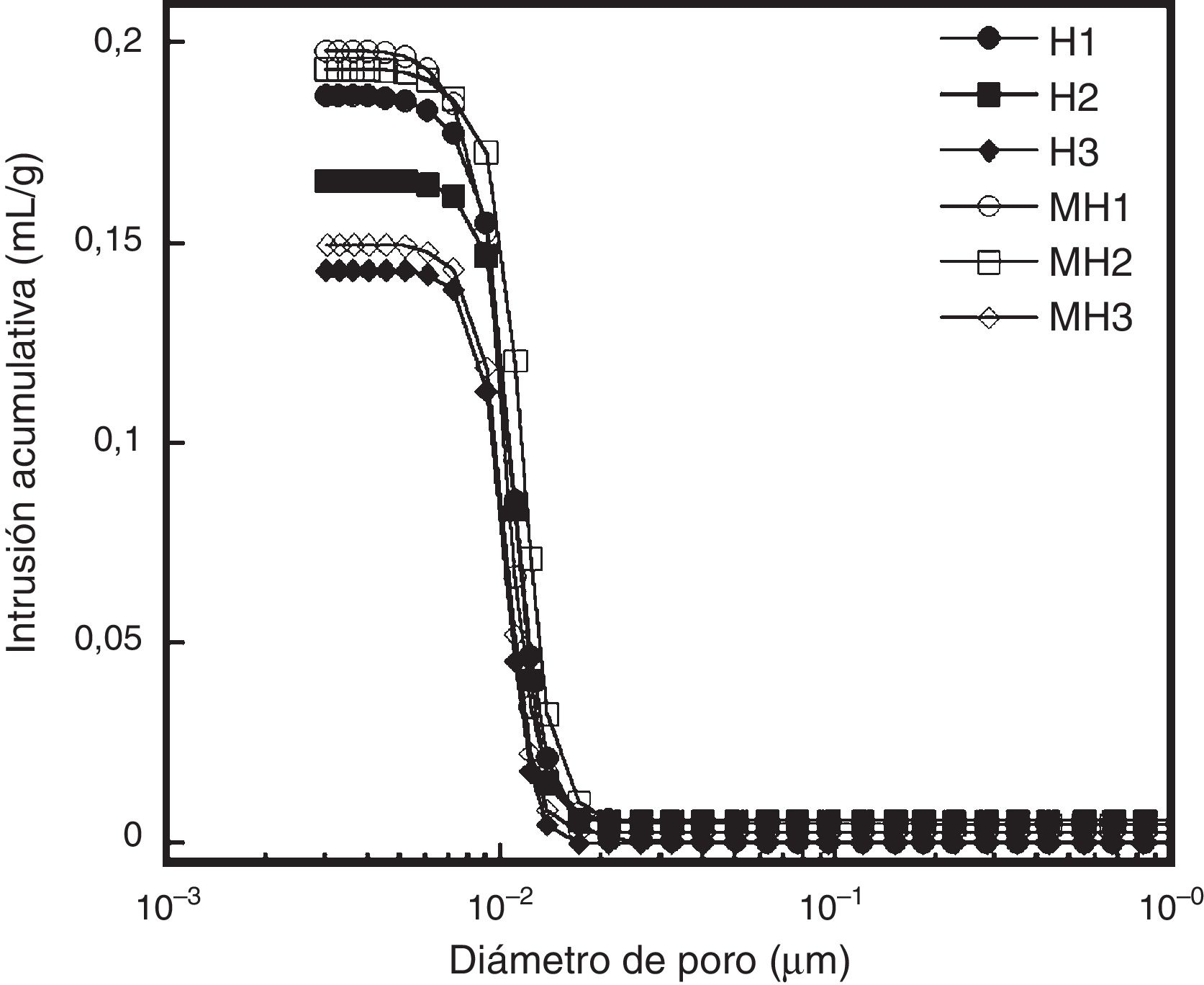
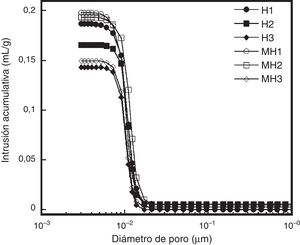
Sin embargo, con base en los resultados obtenidos para todos los compactados preparados a partir de los polvos de HAp, se determinó que los valores de densidad aparente son ligeramente mayores en comparación con los valores alcanzados en los compactados preparados a partir de los polvos de Mg-HAp. Este comportamiento sugiere que la solución sólida de los polvos de HAp con magnesio puede tener un efecto directo sobre la densidad debido a que la morfología de las partículas de Mg-HAp se ve modificada, ya que se presentan los polvos con una forma esfenoide más definida, así como partículas más finas que tienden a aglomerarse, lo que puede conducir a una dificultad para un buen empaquetamiento en la compactación, contribuyendo así a la obtención de valores de densidad ligeramente menores en los compactados de Mg-HAp, en contraste con el comportamiento de densificación que se logró con los polvos de HAp, cuya morfología es más equiaxial y promueve un mejor mecanismo de disolución-recristalización, por lo cual se atribuye una mayor densificación. Estos resultados tienen congruencia con lo reportado por otros autores [24], que mencionan que para la obtención de altos valores de densidad, además de tamaños de partícula pequeños, existe una dependencia directa con la morfología de las partículas; así mismo mencionan que partículas más alargadas tienden a presentar aglomerados que disminuyen la densificación de la HAp. Por otra parte, cabe hacer mención que se llevó a cabo un análisis de porosimetría de intrusión de mercurio para estos compactados hidrotérmicos, y el comportamiento de las curvas de esta determinación se muestra en la figura 6, donde se exhibe el volumen de intrusión acumulado en función del diámetro de poro de las muestras mencionadas. Se puede observar que los compactados de HAp presentaron valores ligeramente inferiores del volumen de intrusión total con respecto a los presentados por los compactados de Mg-HAp, lo que sugiere que la porosidad presentada por los compactados de Mg-HAp puede ser abierta, lo cual sustenta el resultado de densidad aparente para este tipo de compactados con una ligera disminución de los valores de densidad.
Gráficas de intrusión acumulativa respecto al diámetro de poro de los compactados preparados hidrotérmicamente con polvos de hidroxiapatita (H) y polvos de solución sólida de magnesio hidroxiapatita 4% mol (MH) y a diferentes temperaturas: 150°C (H1 y MH1), 175°C (H2, MH2) y 200°C (H3, MH3), respectivamente.
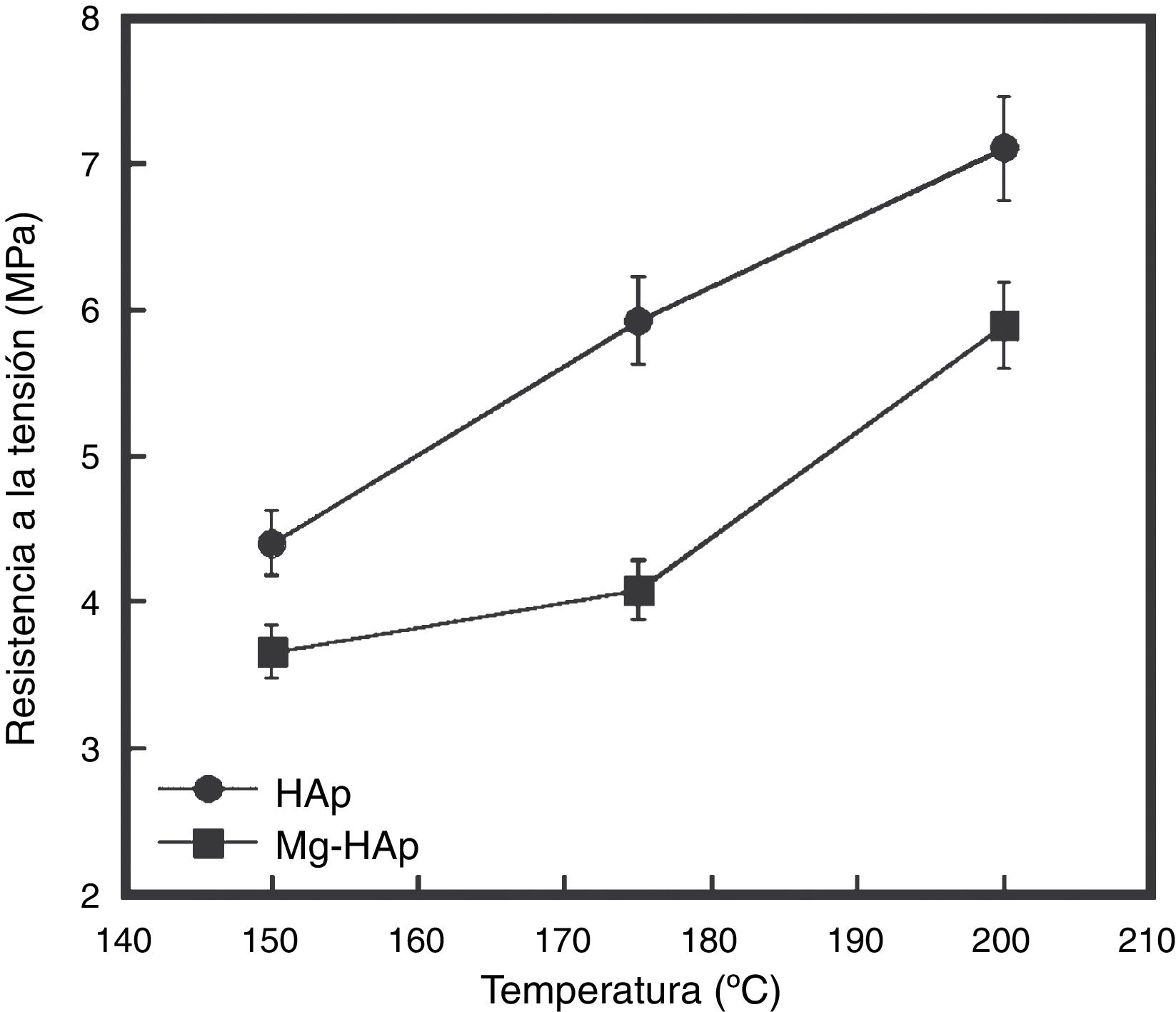
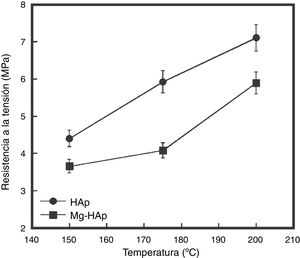
Como se mencionó anteriormente, la resistencia de los cuerpos compactados de los polvos de HAp y Mg-HAp fue determinada por el ensayo Brazilian. Los valores promedio de los resultados de esta prueba están representados en la figura 7, donde se muestra una dependencia importante con el parámetro de la temperatura de compactación. Se logró alcanzar un aumento significativo en la resistencia a la tensión en todas las muestras estudiadas a la mayor temperatura de CHC (200°C). En general este incremento en la resistencia a la tensión es más acentuado para los compactados de HAp, de los cuales se obtuvo un valor mínimo de 4,40MPa para los especímenes compactados a 150°C; en contraste con la mayor temperatura de CHC (200°C), la resistencia a la tensión mostró un incremento máximo hasta un valor de 7,10MPa. Por otra parte, para los compactados de Mg-HAp en condiciones hidrotérmicas similares el valor de la resistencia a la tensión máxima logrado a 200°C fue de 5,89MPa. Los valores máximos de resistencia a la tensión de estos compactados son comparables con los valores reportados para las propiedades del hueso trabecular [25] y con los reportados por K. Hosoi y colaboradores [26] en su investigación sobre compactación de HAp, en la cual reportaron hasta 8MPa de resistencia en compactados preparados a 150°C y 40MPa a 6h.
ConclusionesDe acuerdo al análisis de los resultados obtenidos, se encontró que la temperatura de CHC presenta una influencia significativa en el resultado de las evaluaciones de los compactados de los polvos de HAp pura en comparación con los polvos de solución sólida de Mg-HAp (4% molar).
- a)
En condiciones de CHC, 6h y 10% en peso de agua a diferentes temperaturas (150-200°C), se lograron conservar las características de composición química de los polvos de HAp y polvos de solución sólida de Mg-HAp.
- b)
El grado de cristalinidad (Xc) incrementó hasta un 8,9% cuando la temperatura de compactación en condiciones hidrotérmicas fue de 200°C y la compactación se llevó a cabo durante 6h, lo cual se relacionó con un proceso de recristalización durante la CHC.
- c)
El incremento en la temperatura de compactación hidrotérmica promovió una mayor eficiencia del proceso de disolución-recristalización de las partículas, además de que se presentó una ligera modificación en la morfología de las partículas, posiblemente debido a la reacción de las partículas con el agua presente durante el CHC, permitiendo que existiera una continua disolución-recristalización de las partículas, y a su vez depende de la presencia de magnesio en la estructura de la hidroxiapatita y de la temperatura. De esta manera se puede decir que la compactación de los polvos de HAp y Mg-HAp fue lograda con éxito.
- d)
Baja temperatura de compactación (150°C) en condiciones hidrotérmicas permite arreglos microestructurales de las partículas, favoreciendo la obtención de compactados con densidades del orden de 2,901±0,013 y 2,743±0,017g/cm3 para los polvos de HAp pura y de la solución sólida de Mg-HAp. A la temperatura de 200°C se alcanzó una densidad de hasta 3,085±0,138 y 2,792±0,021g/cm3 para los compactados de HAp y Mg-HAp, respectivamente, comportamiento que se atribuye a una ligera modificación en la morfología de las partículas, permitiendo que existiera una cohesión entre los polvos, lo cual incrementó la densidad de estos compactados.
- e)
La máxima resistencia a la tensión diametral para los polvos compactados de HAp pura y Mg-HAp obtenidos a 200°C fue de 7,10±0,199 y 5,89±0,06MPa, respectivamente; este resultado corresponde a un incremento de más de un 61% respecto a los materiales compactados a 150°C.
Los autores quieren agradecer al CONACYT, por el soporte para la realización de esta investigación a través del proyecto CB-2008-01-0107052. Z.M.V y J.C.R.A. están en deuda con SNI-CONACYT. ZMV agradece al proyecto DGEST 5610.15P. E.E.M.M agradece al CONACYT por el soporte otorgado para realizar estudios de doctorado a través de la beca 388871. Muchas gracias al Profesor T. Yamamoto y al Dr. T. Matsusaki por el apoyo incondicional y la asistencia en el microscopio electrónico de barrido FE-SEM del Marine Core Research, Kochi University, Japan. Al Dr. T. Kono, del Centro Tecnológico Industrial de la prefectura de Kochi-Japón, por su invaluable asistencia en las mediciones de caracterización mecánica de todos los especímenes compactados.