La fibrilación auricular (FA) es la arritmia sostenida más frecuente, con una prevalencia del 1% en la población general y del 6 y el 9% en los mayores de 65 y 80 años, respectivamente. Esta prevalencia es mucho mayor entre los pacientes afectos de una cardiopatía estructural. En España, la prevalencia de esta arritmia entre los pacientes intervenidos de cirugía cardiaca ronda el 16%. Es especialmente frecuente entre aquellos con valvulopatía mitral donde está presente en alrededor de un 60%1.
La FA está asociada con un incremento significativo de la morbimortalidad. Es un factor de riesgo independiente de mortalidad con un riesgo relativo de 1,5 en hombres y 1,9 en mujeres1. Este aumento de morbimortalidad está relacionado con los clásicos tres efectos deletéreos ocasionados por esta arritmia: la existencia de un ritmo cardiaco irregular que puede provocar una importante sintomatología de malestar y ansiedad, sobre todo en los pacientes con FA paroxística; la pérdida de sincronía auriculoventricular que compromete la hemodinámica cardiaca y puede provocar la aparición de síntomas de insuficiencia cardiaca, y el estasis sanguíneo intraauricular por la pérdida de la función de transporte asociado a la ausencia de latido efectivo de las aurículas y que incrementa el riesgo de tromboembolismos. El riesgo de sufrir un ACV mayor en pacientes con FA es cinco veces superior al del resto de la población1,2.
El tratamiento de las consecuencias, tanto directas como indirectas, de la FA ocasiona un enorme gasto sanitario. Dicho gasto ha sido calculado en Estados Unidos con una cuantía superior a los 6,6 billones de dólares anuales.
Un tratamiento adecuado de dicha arritmia debe solventar las tres consecuencias deletéreas expuestas anteriormente. Por esta razón son más adecuados aquellos tratamientos encaminados hacia un control del ritmo cardiaco que buscan reestablecer el ritmo sinusal y la función contráctil de ambas aurículas. El tratamiento médico es altamente ineficaz en este sentido con un índice de fracaso del 50% al año y del 84% a los dos años. Pero, además, dicho tratamiento lleva asociada una elevada tasa de efectos adversos de gravedad que incrementan de forma no despreciable la morbimortalidad en los pacientes tratados. La ineficacia del tratamiento farmacológico para la FA en el control del ritmo cardiaco ha tenido dos consecuencias. En primer lugar, desde el punto de vista farmacológico se opta en la mayoría de los casos por desviar el objetivo del tratamiento hacia un control paliativo de la frecuencia ventricular más la anticoagulación de los pacientes para atenuar el riesgo de tromboembolismos. En segundo lugar, en las últimas décadas ha tenido lugar un importante trabajo de investigación de otros métodos alternativos de tratamiento de la FA encaminados hacia la resolución de esta y el restablecimiento del ritmo sinusal. Cox et al desarrollaron a lo largo de la década de 1980 el que hasta ahora ha sido el método más efectivo de tratamiento de la FA: la técnica quirúrgica del Maze o laberinto. Fruto de un profundo estudio y conocimiento de la electrofisiología de esta arritmia, el Maze ha conseguido «curar» al 90–99% de los pacientes tratados, siendo en la actualidad el «gold standard» en el tratamiento de la FA. Dicha técnica quirúrgica consigue eliminar la arritmia y solventar todos los efectos deletéreos asociados a esta, recuperando no solo el ritmo sinusal, sino la contracción auricular en la mayoría de los casos, y con ello la función de transporte de las aurículas. No obstante, debido a su complejidad asociada a un incremento no despreciable del riesgo quirúrgico, dicha técnica no ha logrado tener una amplia difusión ni incorporarse a la práctica quirúrgica rutinaria. La industria ha desempeñado un importante esfuerzo en un intento de permitir efectuar un procedimiento análogo a la cirugía de Maze basado en los mismos principios, de forma rápida, segura y fácil para hacerlo asequible a cualquier cirujano. Para ello se han desarrollado diversos dispositivos que permiten realizar líneas de ablación mediante la lesión transmural de la pared auricular aplicando distintos tipos de energía1–5.
Toda vez que la tecnología actual permite llevar a cabo el Maze de forma rápida, fácil y prácticamente sin incrementar el riesgo de la cirugía, esto abre la puerta a la posibilidad de generalizar su práctica y plantea la duda sobre qué tipo de paciente podría o debería beneficiarse de este tratamiento.
IndicacionesDado que aún no existen indicaciones absolutas (clase I), las recomendaciones están basadas en resultados de estudios de menor potencia estadística y en opiniones de expertos3–5.
Se recomienda que todos los pacientes que vayan a ser sometidos a una cirugía cardiaca como tratamiento de una cardiopatía estructural y que se encuentren en FA, tanto paroxística como permanente, sean sometidos a tratamiento quirúrgico de su FA. Se trata de una indicación con un nivel de evidencia clase IIa (tabla 1).
Indicaciones de cirugía de la fibrilación auricular
| Clase I |
| Ninguna |
| Clase IIa |
|
| Clase IIb |
|
| Clase III |
|
ECG: electrocardiograma; FA: fibrilación auricular.
(Ann Thorac Cardiovasc Surg. 2005;11:154–8).
No obstante, otros muchos ejemplos en la Medicina nos han enseñado que indicaciones tan genéricas suelen llevar asociados resultados subóptimos, haciéndose necesario seleccionar determinados subgrupos de pacientes en los que tal indicación se asocie con mayor tasa de éxito y menos complicaciones y excluir aquellos en los que el tratamiento se haya mostrado más ineficaz o menos seguro. En este sentido se ha podido determinar una serie de características en los pacientes con FA y que son sometidos a cirugía cardiaca, que pueden hacer desaconsejable e incluso contraindicar el tratamiento quirúrgico de la FA en estos. En la tabla 2 quedan reflejadas cuáles son tales características. Básicamente se desaconseja la cirugía de la FA en aquellos pacientes en los que el tratamiento quirúrgico de esta se asocia a una menor tasa de éxito y aquellos en los cuales existe un riesgo quirúrgico elevado, bien por la naturaleza de la propia cirugía de base o por la comorbididad asociada en dicho paciente o por el mayor riesgo que pueda ser ocasionado por la propia cirugía de Maze.
Criterios de pacientes no adecuados para cirugía de la fibrilación auricular
| Mayores |
|
| Menores |
|
FA: fibrilación auricular.
Los criterios expuestos en la tabla 2 no son criterios absolutos. Es necesario evaluar cada caso de manera particular, y aunque en alguna ocasión un solo criterio mayor podría antojarse suficiente para desaconsejar el tratamiento de la FA, como norma general es necesaria la presencia de al menos dos criterios mayores o uno mayor y dos o más criterios menores para desaconsejar dicho tratamiento.
En el caso de FA con aurículas severamente dilatadas, algunos grupos proponen la cirugía de Maze añadiendo una reducción del tamaño de estas, pero se trata de un procedimiento con elevado consumo de tiempo quirúrgico en circulación extracorpórea y no exento de riesgos, fundamentalmente hemorrágicos, y con aún dudosa efectividad. En el caso de pacientes reintervenidos es posible completar la cirugía de Maze en la aurícula izquierda mediante ablación endocárdica empleando alguno de los diferentes dispositivos y fuentes de energía disponibles en el mercado. En este caso, la efectividad es también cuestionable, principalmente por el hecho de no poder asegurar la transmuralidad de todas las lesiones5.
Algunos proponen llevar a cabo la ablación de las venas pulmonares como procedimiento aislado en pacientes con FA paroxística. En la FA paroxística, el «trigger» que desencadena la arritmia se encuentra en las venas pulmonares en un 90% de los casos. Podría considerarse adecuada esta actitud en pacientes con contraindicaciones para la cirugía de Maze, pero se antoja poco justificable efectuar un procedimiento con una tasa esperada de fracaso del 10% en sujetos en los que por otra parte la cirugía de Maze no supone un incremento del riesgo. Un planteamiento similar ocurre con el resto de los protocolos quirúrgicos que restan líneas de ablación a la cirugía de Maze y que de forma constante se han asociado a resultados inferiores a los del Maze completo. Si bien podrían tener cabida en pacientes seleccionados es difícil justificarlos en aquellos con ausencia de contraindicaciones.
Técnica quirúrgicaDe las distintas fuentes de energía empleadas, entre las que se encuentran los ultrasonidos, la radiofrecuencia, las microondas, la crioablación y el láser, y los diversos diseños de los dispositivos hemos seleccionado la radiofrecuencia bipolar irrigada. La radiofrecuencia es la forma de energía que cuenta con mayor experiencia de uso en las técnicas de ablación y que, por tanto, tiene un perfil de seguridad mejor definido. El uso de la sonda bipolar aporta importantes ventajas: 1) asegura la transmuralidad de las lesiones; 2) define bien la franja del tejido sobre la que se aplica la energía disminuyendo el riesgo de dañar estructuras adyacentes, y 3) permite realizar el procedimiento completo en un corto período de tiempo.
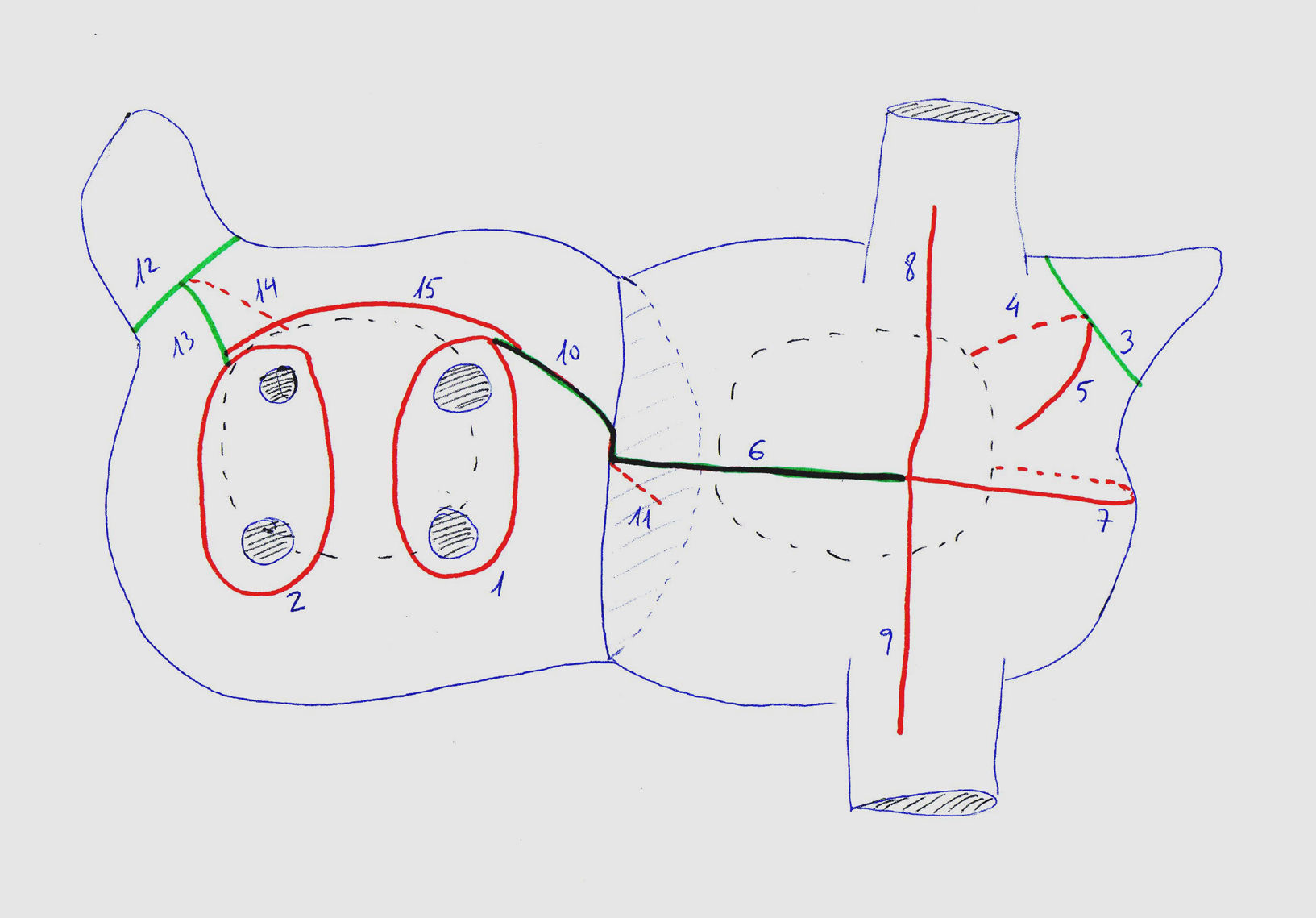
Todas las líneas de ablación pueden ser llevadas a cabo con la sonda bipolar, con la sola excepción de tres de ellas realizadas mediante incisiones en las aurículas (fig. 1).
Con el paciente en circulación extracorpórea mediante canulación venosa independiente de ambas cavas y con el corazón latiendo realizamos una disección roma de las venas pulmonares. Seguidamente pinzamos con la sonda ambas venas pulmonares del mismo lado y realizamos la ablación de estas. El mismo procedimiento se lleva a cabo en el lado contralateral (líneas 1 y 2). Para disminuir el riesgo de estenosis cicatricial de la vena pulmonar es recomendable desplazar la pinza medialmente para realizar la línea de ablación sobre el tejido auricular más que sobre la propia pared de la vena.
A continuación cerramos los torniquetes sobre las venas cavas. Todas las líneas de ablación en la aurícula derecha pueden ser llevadas a cabo sin necesidad de clampaje aórtico, salvo en aquellos pacientes que presentan un defecto septal auricular. Amputamos la orejuela derecha (línea 3). A través del orificio resultante introducimos la pinza dirigiéndola hacia el anillo tricúspide, cuidando de no avanzar en exceso para no dañar la coronaria derecha, y hacemos la línea 4. A continuación cambiamos la orientación de la pinza hacia la pared libre de la aurícula y hacemos la línea 5, cuidando de no extenderla demasiado porque tendrá que quedar una banda del tejido separando el extremo de esta línea con la línea 6–7.
Hacemos una incisión en la zona media de la pared libre de la aurícula derecha, perpendicular al surco interauricular y en dirección a este, dirigiéndolo hacia la desembocadura de la vena pulmonar superior derecha sin entrar aún en la aurícula izquierda (línea 6). Empleando la sonda bipolar desde el extremo superior de esta incisión en sentido opuesto con dirección al anillo de la tricúspide, hacemos la línea 7, de nuevo cuidando de no dañar la coronaria derecha. Desde ese mismo extremo de la incisión 6, pero esta vez en una dirección perpendicular a esta, realizamos con la sonda las líneas 8 y 9 hacia cada una de las cavas, cuidando de penetrar dentro de estas.
Concluido el procedimiento en el lado derecho, es necesario el pinzamiento de la aorta y la parada cardiaca antes de proseguir con la aurícula izquierda. Prolongamos la línea 6 hacia el septo interauricular y abrimos la aurícula izquierda. Continuamos dicha incisión hacia el borde superior de la línea de ablación de las venas pulmonares derechas (línea 10). Realizamos un corte en el septo interauricular en dirección a la fosa oval sin sobrepasarla. Esta es la línea 11. Si el paciente tiene una comunicación interauricular tipo ostium primum, es imprescindible no realizar esta línea para evitar un bloqueo auriculoventricular.
Amputamos la orejuela izquierda (línea 12) continuando la incisión en su parte posterior hacia el borde superior de la línea de ablación de las venas pulmonares izquierdas (línea 13). Introducimos la pinza de radiofrecuencia por el orificio de la orejuela amputada, en su parte anterior, dirigiéndola hacia el anillo mitral con cuidado de no avanzar demasiado para no dañar la arteria circunfleja y creamos la línea 14. Para realizar la línea 15 debemos introducir la pinza, de derecha a izquierda o al revés, yendo el brazo interno de esta por dentro de la aurícula izquierda (desde el extremo medial de las incisiones 10–13 o al contrario) y el externo por el seno transverso y por detrás de la cava superior, para lo que es necesario previamente disecar el espacio entre la vena cava superior y la vena pulmonar superior derecha. Con esta disposición de la línea 15 evitamos disecar la pared posterior de la aurícula izquierda y el riesgo de dañar el esófago.
ResumenLa cirugía de la FA puede ser llevada a cabo actualmente de forma rápida, sencilla y segura gracias al uso de dispositivos que emplean diferentes tipos de energía para crear líneas de ablación en las aurículas según los principios del Maze. Su práctica está recomendada en todos los pacientes con FA que tienen que ser sometidos a cirugía cardiaca. No obstante, deberían excluirse de esta recomendación los pacientes en los que las posibilidades de éxito de la técnica sean más reducidas y sean considerados de alto riesgo, siempre que no existan circunstancias particulares derivadas de las complicaciones causadas por la arritmia que justifiquen asumir dicho riesgo.