La inflamación tiene un papel establecido, tanto en la génesis y progresión del proceso aterosclerótico como en el desarrollo del síndrome coronario agudo. Diferentes células inflamatorias (monocitos y células T), citocinas y otras biomoléculas están implicadas en estos procesos y han sido, por tanto, investigadas como potenciales marcadores de progresión de la placa aterosclerótica y de riesgo cardiovascular. En el ámbito de la enfermedad coronaria, la proteína C reactiva es el biomarcador inflamatorio más ampliamente estudiado y validado. Sin embargo, nuevos biomarcadores, como la molécula de adhesión intracelular-1, la interleucina-6 o el factor de necrosis tumoral-α, podrían añadir información adicional para la estratificación del riesgo cardiovascular. Diferentes marcadores inmunológicos también han sido implicados en el proceso aterosclerótico: un subgrupo de linfocitos T, denominados CD4+CD28‐, se encuentran implicados en la inestabilización de la placa aterosclerótica y la recurrencia de eventos coronarios agudos; el sistema CD40/CD40 ligando así como la forma soluble del CD40 ligando pertenecen a la superfamilia del factor de necrosis tumoral y son moléculas con actividad protrombótica y proinflamatoria cuyo papel en el proceso aterosclerótico es actualmente foco de una intensa investigación.
Esta revisión analiza la evidencia actual que soporta el papel de biomarcadores inflamatorios e inmunológicos en el proceso aterosclerótico y su papel pronóstico, tanto en los síndromes coronarios agudos como en la enfermedad coronaria estable.
It is now generally recognized that chronic inflammation plays a key role in atherogenesis, atherosclerotic plaque progression and acute coronary syndrome. Inflammatory cells (monocytes and T-cells), cytokines and other biomolecules are implicated in these processes and have, therefore, been investigated as potential markers of atherosclerotic plaque progression and cardiovascular disease risk. C-reactive protein is currently the best validated inflammatory biomarker; in addition new biomarkers such as soluble intercellular adhesion molecule-1, interleukin 6, and tumor necrosis factor-α, may provide additional information for cardiovascular risk stratification and prediction. Different immunological markers have also been implicated in the atherogenic process; CD4+CD28 null T cells are an unusual subset of helper cells which expand and have deleterious effects in coronary artery disease. CD40/CD40 ligand system and soluble form of CD40 ligand belong to the tumor necrosis factor superfamily, and they are molecules with a dual prothrombotic and proinflammatory role and their role in atherothrombosis is widely accepted. However, the exact mechanisms linking the CD40/CD40L system and the soluble form of CD40 ligand with atherothrombosis are currently a topic of intensive research.
This review retraces the evidence supporting the role of inflammatory and immunological biomarkers in the biology of the atherogenic process.
La aterosclerosis es el proceso subyacente que desencadena la formación de placas de ateroma en la pared arterial y la aparición de las diferentes manifestaciones de la enfermedad cardiovascular. La aterosclerosis es actualmente reconocida como un proceso predominantemente inflamatorio con producción de citocinas e incremento de reactantes de fase aguda, en el que está especialmente involucrado el sistema inmunológico. Como consecuencia, un gran número de marcadores inflamatorios e inmunológicos han sido propuestos como marcadores pronósticos, tanto en los síndromes coronarios agudos (SCA) como en la enfermedad coronaria estable. En los últimos años se han realizado importantes avances en el conocimiento de los mecanismos inflamatorios implicados en el desarrollo de la aterosclerosis, aunque muchos aspectos permanecen todavía sin aclarar.
Marcadores inflamatoriosLa proteína C reactiva (PCR) es el marcador inflamatorio más conocido y sobre el que existe una mayor evidencia de su relación con las enfermedades cardiovasculares. Los niveles de PCR se han asociado con el pronóstico a corto y a largo plazo en los SCA y también en la angina estable. Además, en los pacientes con infarto agudo de miocardio las concentraciones de PCR se correlacionan con la extensión de la necrosis, y es también un predictor de riesgo de reestenosis y eventos cardiovasculares tras la revascularización1. Con respecto a su posible aplicación clínica es interesante señalar que las estatinas son capaces de disminuir las concentraciones de PCR de forma independiente a su efecto hipolipidemiante. En el estudio JUPITER se estudió el efecto del tratamiento con estatinas en una población aparentemente sana que no presentaba hiperlipidemia, pero sí elevación de los niveles de PCR, obteniendo una reducción significativa en la incidencia de eventos cardiovasculares mayores en el grupo tratado con rosuvastatina.
A pesar de la amplia evidencia existente sobre la PCR, todavía existen dudas sobre si debería ser utilizada rutinariamente en la práctica clínica, habiéndose publicado varias revisiones donde se pone en duda su relevancia clínica. Como marcador inespecífico de inflamación, la PCR puede estar elevada por múltiples causas, la mayoría reflejando injuria tisular, habiéndose encontrado incluso variaciones de los niveles de PCR en función del origen étnico.
Otros marcadores inflamatorios, como la molécula de adhesión intracelular-1 (ICAM-1), la interleucina (IL) 6 o el factor de necrosis tumoral α (TNF-α) también han sido estudiados. Se ha observado que las concentraciones de la ICAM-1 predicen la aparición de eventos coronarios y el desarrollo de ateromatosis carotídea en pacientes con factores de riesgo, mientras que en pacientes con enfermedad coronaria las ICAM-1 no fueron predictoras de eventos cardiovasculares futuros. En sujetos sin enfermedad vascular, los valores de IL-6 son predictores de enfermedad coronaria, insuficiencia cardíaca e ictus, mientras que los niveles de IL-6 en pacientes hospitalizados por un SCA resultaron predictores de mortalidad cardiovascular2.
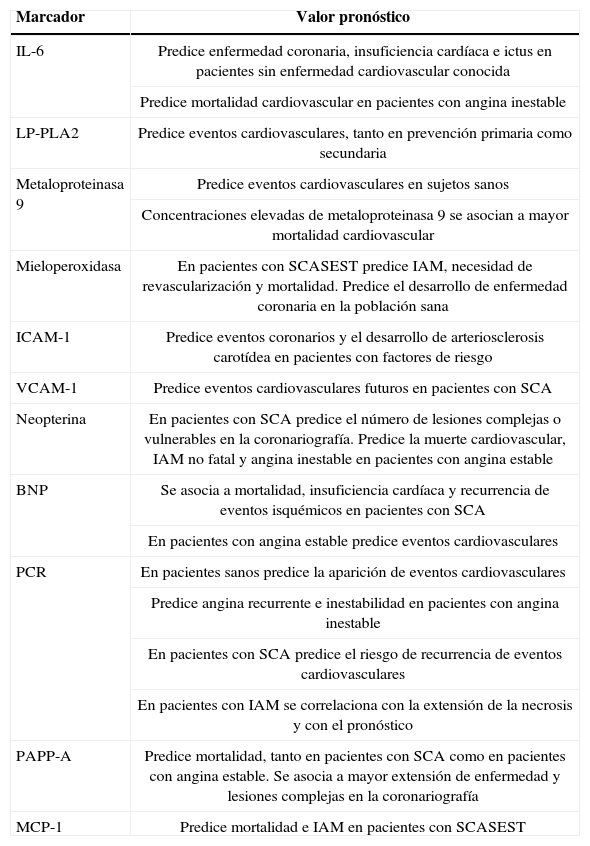
En la tabla 1 se resume el valor pronóstico de los principales marcadores inflamatorios. Es importante señalar que incluso utilizando conjuntamente varios de los marcadores inflamatorios, éstos sólo aumentan de forma moderada la información aportada por los marcadores de riesgo clásicos en la valoración del riesgo individual de desarrollar enfermedad coronaria.
Valor pronóstico de los marcadores inflamatorios
| Marcador | Valor pronóstico |
| IL-6 | Predice enfermedad coronaria, insuficiencia cardíaca e ictus en pacientes sin enfermedad cardiovascular conocida |
| Predice mortalidad cardiovascular en pacientes con angina inestable | |
| LP-PLA2 | Predice eventos cardiovasculares, tanto en prevención primaria como secundaria |
| Metaloproteinasa 9 | Predice eventos cardiovasculares en sujetos sanos |
| Concentraciones elevadas de metaloproteinasa 9 se asocian a mayor mortalidad cardiovascular | |
| Mieloperoxidasa | En pacientes con SCASEST predice IAM, necesidad de revascularización y mortalidad. Predice el desarrollo de enfermedad coronaria en la población sana |
| ICAM-1 | Predice eventos coronarios y el desarrollo de arteriosclerosis carotídea en pacientes con factores de riesgo |
| VCAM-1 | Predice eventos cardiovasculares futuros en pacientes con SCA |
| Neopterina | En pacientes con SCA predice el número de lesiones complejas o vulnerables en la coronariografía. Predice la muerte cardiovascular, IAM no fatal y angina inestable en pacientes con angina estable |
| BNP | Se asocia a mortalidad, insuficiencia cardíaca y recurrencia de eventos isquémicos en pacientes con SCA |
| En pacientes con angina estable predice eventos cardiovasculares | |
| PCR | En pacientes sanos predice la aparición de eventos cardiovasculares |
| Predice angina recurrente e inestabilidad en pacientes con angina inestable | |
| En pacientes con SCA predice el riesgo de recurrencia de eventos cardiovasculares | |
| En pacientes con IAM se correlaciona con la extensión de la necrosis y con el pronóstico | |
| PAPP-A | Predice mortalidad, tanto en pacientes con SCA como en pacientes con angina estable. Se asocia a mayor extensión de enfermedad y lesiones complejas en la coronariografía |
| MCP-1 | Predice mortalidad e IAM en pacientes con SCASEST |
BNP: péptido natriurético cerebral; IAM: infarto agudo de miocardio; ICAM-1: molécula de adhesión intercelular-1; IL: interleucina; LP-PLA2: lipoproteína asociada a fosfolipasa A2; MCP-1: proteína quimiotáctica 1; PAPP-A: proteína plasmática A asociada al embarazo; PCR: proteína C reactiva; SCA: síndrome coronario agudo; SCASEST: síndrome coronario agudo sin elevación del ST; VCAM-1: molécula de adhesión vascular celular-1.
Los linfocitos T han sido sistemáticamente encontrados en las placas ateroscleróticas, estando implicados tanto en el inicio como en la progresión de la enfermedad, además de contribuir a la desestabilización de la lesión aterosclerótica que da lugar a los SCA. Recientes estudios han identificado un subgrupo de linfocitos T, denominados CD4+CD28−, que se encuentra implicado en la inestabilización de la placa aterosclerótica y la recurrencia de eventos coronarios agudos.
El CD28 es un receptor de membrana presente en los linfocitos T que transduce las señales recibidas por moléculas coestimuladoras de la familia B7, necesarias para la correcta activación de los linfocitos T. Este subgrupo de linfocitos se caracteriza por la producción de mayores niveles de interferón-γ (IFN-γ), TNF-α e IL-2, además de presentar capacidad citotóxica mediada por enzimas citolíticas, como las perforinas, granzima A y granzima B, que normalmente están presentes en los linfocitos T CD8+, pero no en los linfocitos T CD4+. Además, estas células han demostrado ser resistentes a los mecanismos de apoptosis celular, debido a una mayor actividad de la proteína antiapoptótica Bcl-2, y no son sensibles a la regulación por los linfocitos T reguladores, lo que lleva a su anormal expansión y acumulación. Por último, este subgrupo de linfocitos no expresa en su membrana el ligando para CD40 lo que las inhabilita para producir las señales necesarias para la producción de anticuerpos por los linfocitos B3.
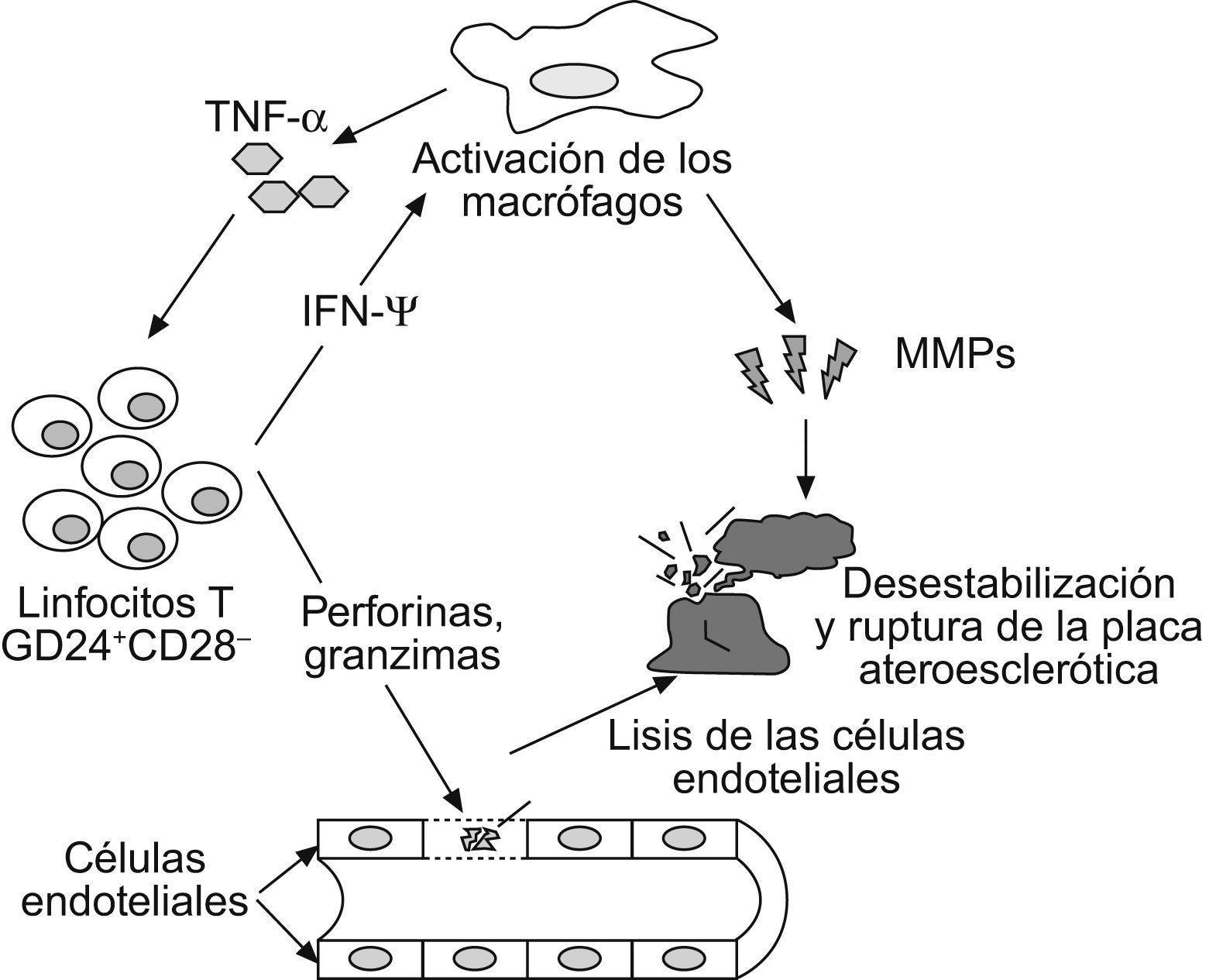
Las manifestaciones más severas de la enfermedad arterial coronaria, como son el infarto agudo de miocardio y la muerte súbita, son el resultado de la ruptura de la placa aterosclerótica que lleva a la formación de un trombo y la oclusión de la arteria. Se han observado altos niveles de IFN-γ así como un incremento de CD4+CD28− en pacientes con angina inestable en relación con los pacientes con angina estable. Además, los niveles de IFN-γ se correlacionan directamente con los niveles de CD4+CD28−, lo que sugiere que este grupo de linfocitos son la principal fuente de IFN-γ. Además, se ha observado una preferencia en la acumulación de linfocitos T CD4+CD28− en placas ateroscleróticas inestables con respecto a las lesiones estables. De hecho, se ha sugerido un papel directo en la desestabilización de la placa, dada su potencial capacidad de lisis sobre las células endoteliales (CE), que es un conocido desencadenante de inestabilización y ruptura de la placa aterosclerótica3. Por último, recientes estudios han mostrado que niveles elevados de este subgrupo de linfocitos son un predictor independiente de eventos cardiovasculares futuros en pacientes con angina inestable. Los principales efectos patogénicos de los linfocitos T CD4+CD28− aparecen recogidos en la figura 1.
Efectos patogénicos de los linfocitos T CD4+CD28− en la enfermedad arterial coronaria. Modificado de Dumitriu et al3.
El sistema CD40/CD40 ligando (CD40L) es otro de los mecanismos implicados en la relación entre inflamación y aterotrombosis. El CD40 es un receptor de membrana expresado principalmente por los linfocitos B, aunque también puede estar presente en la superficie de otras células, como las CE, las células musculares lisas o las plaquetas, la mayoría de las cuales también expresan el CD40L. La expresión de CD40 y de CD40L es inducida por estímulos inflamatorios, como las IL-1, IL-3 e IL-4, el TNF-α y el IFN-γ. La activación de CD40 desencadena una serie de procesos intracelulares que llevan a la sobreexpresión de los genes proinflamatorios y proaterogénicos. Este sistema es regulado a través de la vía del óxido nítrico, de forma que la inhibición del óxido nítrico sintasa induce la activación y la consiguiente sobreexpresión de CD404.
La expresión del complejo CD40/CD40L interviene en el desarrollo de la aterosclerosis, aunque los mecanismos implicados están aún por esclarecerse. En estudios in vitro, la interacción entre CD40/CD40L en la superficie de las CE lleva a la activación del endotelio y a la expresión de moléculas de adhesión, lo que sería un paso inicial en el desarrollo de la placa aterosclerótica. También se ha observado que esta interacción induce la maduración y la activación de las células dendríticas, que regulan la infiltración de los linfocitos T, que se encuentra típicamente en las placas ateroscleróticas inestables. Por último, también induce la expresión de metaloproteasas que degradan el colágeno intersticial y la capa fibrosa de las placas de ateroma, llevando a la inestabilidad de la placa y su ruptura.
Tras la activación celular, la parte extracelular del CD40L es liberada a la circulación en forma de CD40L soluble (sCD40L). Las plaquetas liberan más del 95% del sCD40L circulante. Esta forma soluble interacciona con la integrina Mac-1, presente en las células del sistema monocito-macrófago, induciendo la migración y la adhesión de células inflamatorias. Además, el sCD40L también se une a los receptores de la GP IIb/IIIa, induciendo su activación. En estudios in vitro se ha observado que los antagonistas de la GP IIb/IIIa reducen la liberación de sCD40L por las plaquetas activadas. Pacientes, tanto con angina estable como con SCA, presentan niveles elevados de sCD40L y se ha sugerido como posible marcador pronóstico. De hecho, la evidencia sugiere que reducir los niveles de sCD40L mediante el uso de fármacos habituales, como los antiplaquetarios, podría mejorar el pronóstico. Sin embargo, su papel en la aterosclerosis debe ser esclarecido, ya que, dado que su principal fuente son las plaquetas, el sCD40L puede ser más una señal de la activación plaquetaria que presentar un efecto directo en el desarrollo de la placa ateromatosa.
Sistema Fas/Fas ligandoEl sistema Fas/Fas ligando (FasL) interviene en los procesos de apoptosis celular, de tal forma que la unión de FasL a su receptor desencadena la apoptosis o muerte celular programada de la célula que expresa el receptor. La presencia de estímulos inflamatorios es capaz de disminuir la expresión de FasL en las CE, facilitando de este modo la acumulación de células inflamatorias en las etapas iniciales de la formación de la placa aterosclerótica. Se ha observado una relación lineal entre las concentraciones de la forma soluble de FasL (sFasL) y la respuesta vasodilatadora a la hiperemia reactiva en pacientes con CAD, sugiriendo que la sFasL puede ser un marcador de disfunción endotelial5. En consistencia con estos hallazgos, se han encontrado niveles disminuidos de sFasL en pacientes con alto riesgo cardiovascular, aunque se necesitan nuevos estudios para determinar su valor pronóstico.
Heat shock proteinsLas heat shock proteins (HSP) son una familia de proteínas cuya función es facilitar el ensamblaje correcto de las proteínas, así como también favorecer la eliminación de las proteínas que están dañadas de forma permanente. Las HSP70 se encuentran disminuidas en pacientes con aterosclerosis y se ha observado una correlación inversa entre los niveles de HSP70 y el grosor íntima-media carotídeo en pacientes hipertensos. Además, la presencia de niveles elevados de HSP70 se relaciona con menor riesgo de enfermedad coronaria y un menor número de vasos afectados en la coronariografía2.
ConclusionesLos marcadores inflamatorios tienen valor en la investigación, pero en la práctica clínica su uso aún no se ha definido claramente, ya que su contribución en la valoración del riesgo individual no parece ser superior en relación con la información aportada por los factores de riesgo clásicos.
Recientemente, el foco de la investigación se ha dirigido a marcadores inmunológicos que pueden aportar información adicional sobre el pronóstico y ayudar a predecir el riesgo cardiovascular. Entender sus mecanismos es fundamental para determinar cuál es su papel en el desarrollo de la aterosclerosis y cómo pueden ser incorporados a la práctica clínica. Los avances tecnológicos emergentes en la genómica, proteonómica y metabolómica pueden permitir la identificación de nuevos genes, proteínas y metabolitos implicados en el desarrollo de la enfermedad coronaria, no relacionados con los factores de riesgo conocidos y que serían susceptibles de convertirse en el futuro en nuevos marcadores de screening, diagnóstico o pronóstico en la enfermedad coronaria.