La regeneración de los tejidos animales es un fenómeno muy corriente en la naturaleza, que ocurre en numerosos organismos inferiores. No es de extrañar que cuando cortamos un miembro a una estrella de mar o a ciertos anfibios, éstos son capaces de regenerar el miembro amputado. En nuestra especie se suceden procesos regenerativos a una menor escala, como es el caso de la regeneración del tejido endometrial tras cada ciclo menstrual, la regeneración de las células sanguíneas de la línea roja (las cuales tienen una vida media de ciento veinte días) y la regeneración cotidiana de la piel (cuya duración es de siete días) o la regeneración de ésta tras una herida. Estos fenómenos naturales invitan a pensar que debe existir un tipo de célula especial que tenga la capacidad de convertirse en «aquello que se necesite en cada momento» o, en otras palabras, de diferenciarse en respuesta a un estímulo. En esta idea se enmarca el concepto de célula madre, como aquella célula que no se encuentra «diferenciada ni especializada», pero que puede llegar a diferenciarse o especializarse en un tejido u otro, a través de su potencialidad, dependiendo de las señales que la estimulen.
Las células madre y la cardiología: «la terapia reparativa cardiovascular»Hasta ahora, la mayoría de los tratamientos utilizados en cardiología se han basado en terapias farmacológicas y quirúrgicas, que han contribuido a una mejoría de los síntomas y de la supervivencia de los pacientes. Estas terapias han sido dirigidas a prevenir la progresión y revertir las consecuencias de la enfermedad cardiovascular. El único tratamiento que remplazaría completamente el tejido dañado, recobrando así la función del miocardio, sería un transplante de corazón, pero debido entre otras causas a la baja disposición de donantes e inmunorrechazos, se considera un tratamiento limitado1. La búsqueda de nuevas alternativas para la regeneración del miocardio ha llevado a la necesidad de impulsar la investigación básica, basándose en las múltiples evidencias de que células madres procedentes de orígenes dispares podrían diferenciarse hacia cardiomiocitos, vasos sanguíneos o tejido conectivo, potenciado la capacidad regenerativa del tejido cardiaco, con el fin de algún día solventar dicho problema. Para ello es necesario conocer algunas nociones básicas sobre las propiedades y características que les confiere el significado de célula madre o stem cell.
Las características propias que definen a una célula madre son:
- I.
Capacidad de autorrenovación, definida como la capacidad que tiene la célula de dividirse, dando lugar a dos células completamente iguales, sin modificarse durante largos períodos de tiempo, es decir, divisiones celulares sucesivas manteniéndose de manera indiferenciada.
- II.
Capacidad de diferenciación hacia células especializadas en respuesta a un estímulo.
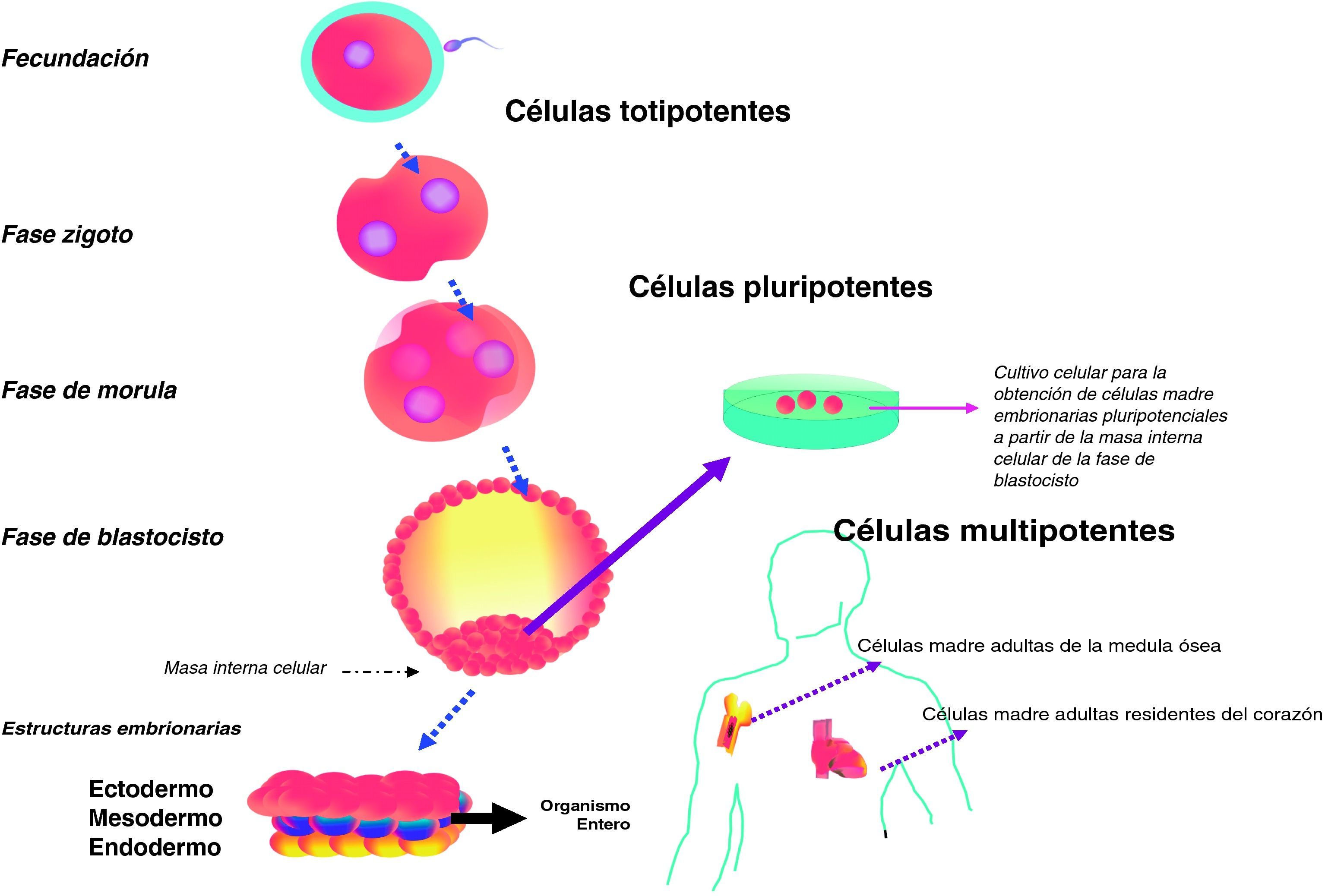
Las células madre se clasifican atendiendo a su potencial de transformación. Esto se refiere a su capacidad de originar pocos o muchos tipos celulares funcionales, clasificándolas en células totipotentes, pluripotentes y multipotentes2 (fig. 1).
- 1.
Las células madre totipotentes son las células que participan inicialmente en el desarrollo embrionario, incluyendo el cigoto y las células resultantes de las sucesivas divisiones celulares (fase de mórula); son células madre con capacidad de generar un organismo entero originando tanto las células somáticas (células que no transmiten la herencia génica) como las células germinales (células que transmiten la herencia génica), así como todas las membranas necesarias para el desarrollo (placenta, saco vitelino). La totipotencialidad es una característica que se pierde gradualmente mediante las sucesivas divisiones mitóticas3.
- 2.
Las células madre pluripotentes son células con capacidad de diferenciarse en cualquier tipo de célula, de cualquier línea germinal. En la fase de blastocisto se desarrolla la masa interna celular, formada por unas doscientas células. De estas doscientas células derivan las tres capas germinales, denominadas endodermo (p. ej., células del páncreas, tiroides y células alveolares del pulmón), mesodermo (p. ej., células del músculo cardiaco, esquelético y sanguíneas) y ectodermo (p. ej., células neuronales y epidermis). A partir de estas tres capas germinales se originarán todas las demás células, órganos y tejidos del cuerpo, creando un organismo completo3.
- 3.
Las células madre multipotentes son las que sólo pueden diferenciarse en células especializadas de la misma línea germinal; por ejemplo, las células madre mesenquimales sólo se pueden especializar en células propias del mesénquima: células del hueso, corazón o grasa. A este grupo pertenecen la gran mayoría de tipos de células madre posnatales2.
Otra clasificación utilizada se basa en el origen o procedencia de las células madre, refiriéndose al estadio embrionario o post-natal:
- 1.
Las células madre embrionarias son las que derivan de la masa interna del blastocisto (etapa del desarrollo del embrión), y de ellas se obtienen todos los tipos celulares del cuerpo.
- 2.
Las células madre no embrionarias o adultas (posnatales) se han identificado en ciertos órganos y tejidos como en el cerebro, la medula ósea, la sangre periférica, los vasos sanguíneos, la piel, los dientes, el músculo esquelético y el corazón. Se piensa que residen en áreas especificas de cada tejido conocidas como «nichos» y que se mantienen de forma quiescente (sin división celular) durante largos periodos de tiempo, hasta que son activadas para participar en la renovación y regeneración de tejidos tanto para su mantenimiento como para la reparación de los tejidos lesionados. Dentro de los diferentes tipos de células madre adultas se engloban las células madre hematopoyéticas, que darán lugar a todas las células sanguíneas; las células madre mesenquimales, que se pueden diferenciar hacia células de hueso, cartílago, adipocitos o corazón; las células madre neurales y las células madre de la piel. Éstas podrían ser consideradas como unidades de generación de tejidos4.
La característica fisiopatológica de la isquemia cardiaca es la pérdida de cardiomiocitos debida a la necrosis celular, que da lugar a un deterioro de la capacidad de la función del miocardio y que afecta a la función del ventrículo izquierdo. Hasta ahora se pensaba que el corazón era un órgano con una naturaleza terminalmente diferenciada (posmitótico), es decir, una vez que los cardiomiocitos mueren el corazón es incapaz de remplazarlos. Sin embargo, actualmente se ha observado que en el corazón pueden existir células cardiacas formadas de novo, como se muestra en el estudio realizado por el grupo de Hocht-Zeisberg5. Estos investigadores observaron, que cuando se trasplantaban corazones procedentes de donantes femeninos a receptores masculinos, existían células en el corazón cuya procedencia no era del donante sino del huésped, hallándose células miocárdicas generadas de novo. Estos hallazgos abrieron una brecha en la investigación de las células madre y en la búsqueda del tipo de célula «ideal», que potencialmente pudiese reparar el tejido cardiaco.
Para el uso de una terapia con células madre, la pregunta más trascendente sería: ¿cuál es el tipo de célula madre capaz de dar a lugar una mayor variedad de tejidos; dónde se podrían aplicar y de qué forma? La utilización de las células madres embrionarias humanas tiene como ventaja principal su capacidad de diferenciación en cualquier tipo de tejido, aunque poseen la capacidad de formación de teratomas. Los teratomas son tumores sólidos que contienen una mezcla de tejidos diferenciados como neuronas, músculo cardiaco y epitelio secretor. Un problema añadido de la utilización de las células madre embrionarias en la terapia reparativa son los inmunorrechazos, debido a que las células que se trasplantan proceden de un donante diferente al receptor. Otro inconveniente que limita su utilización es el debido a cuestiones ético-morales y legales. Las células madre adultas humanas no presentan problemas ético-morales ni legales, ya que se obtienen de tejido adulto. Este tipo de células tienen una baja producción de teratomas debido a su baja capacidad de proliferación. Sin embargo, poseen limitaciones tanto en la multiplicación celular como en su capacidad de diferenciación hacia una amplia variedad de tejidos. Se sabe que las células de médula ósea adulta tienen una remarcada plasticidad y pluripotencialidad, señalándolas como células madre adultas universales. Se conoce también la existencia de células madre residentes en tejidos adultos similares a las células madre de medula ósea, que pueden proporcionar una fuente de células autólogas sanas evitando los procesos de inmunorrechazo4.
Se han citado al menos 2 posibles fuentes de células madre o progenitoras que podrían dar a lugar nuevos cardiomiocitos en la vida posnatal. Se clasifican como fuentes endógenas, que incluirían a los cardiomiocitos con capacidad replicativa limitada, las células progenitoras cardiacas y las células derivadas del epicardio que dan a lugar a cardiomiocitos en roedores, y las fuentes exógenas, que incluirían las células madre embrionarias, las células pluripotentes inducidas (iPS) y las células madre mesenquimales6.
El proceso biológico por el cual las células madre adultas acuden al tejido infartado tras una isquemia se denomina homing. Lo realizan las células procedentes de médula ósea desde sus nichos biológicos hacia los tejidos dianas lesionados. Este proceso se encuentra dirigido por una serie de moléculas implicadas en la atracción y en la migración de ciertos tipos de células hacia tejidos isquémicos. Algunas de las moléculas implicadas en este proceso son el factor derivado del estroma 1 (SDF-1), el factor de crecimiento del endotelio vascular (VEGF) y el factor de crecimiento de hepatocitos (HGF). Sin embargo, a pesar de conocer algunas de las moléculas implicadas en estos procesos, se piensa que este mecanismo es aún más complejo de lo hasta ahora descritoy que en este proceso probablemente participan un gran abanico de moléculas implicadas en la quimioatracción y en los mecanismos de interacción entre las células, todavía sin esclarecer.
Aplicaciones de la terapia reparativa en enfermedades cardiovascularesCiertos autores clasifican las diferentes células con potencial regenerativo para el corazón en dos grupos: las células residentes en el tejido cardiaco y las no residentes7.
- 1.
Las células no residentes del tejido cardiaco incluyen las células madre derivadas de medula ósea, siendo las células madre hematopoyéticas una de las poblaciones mejor definidas, ya que partir de ellas se origina el linaje sanguíneo. Éstas fueron las primeras donde quedó demostrado in vitro la capacidad de diferenciación hacia cardiomiocitos. Otro tipo son las células progenitoras endoteliales, caracterizadas por un aumento de su número en sangre periférica tras un infarto de miocardio, pudiendo contribuir a la revascularización8. Las células madre mesenquimales, procedentes tanto de médula ósea como de tejido adiposo, pueden diferenciarse a cardiomiocitos y son uno de los mejores candidatos para terapias celulares, ya que no producen inmunorrechazos. Las células pluripotentes inducidas (iPS) son células procedentes de células somáticas de fibroblastos embriogénicos de ratón, que se trasforman en células madre pluripotenciales mediante técnicas de ingeniería genética. Estas células poseen la capacidad de diferenciarse hacia cardiomiocitos y desarrollar autolatencia. Los mioblastos esqueléticos fueron elegidos como candidatos para la regeneración de tejido cardiaco por su similitud estructural con los cardiomiocitos. Sin embargo, se observó que tras el implante de los mioblastos se producían arritmias cardiacas malignas2,3 (tabla 1).
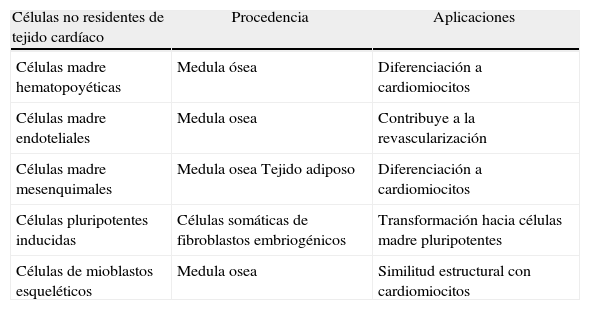
Tabla 1.Tipos de células madre no residentes y residentes de tejido cardiaco, con potencial regenerativo.
Células no residentes de tejido cardíaco Procedencia Aplicaciones Células madre hematopoyéticas Medula ósea Diferenciación a cardiomiocitos Células madre endoteliales Medula osea Contribuye a la revascularización Células madre mesenquimales Medula osea Tejido adiposo Diferenciación a cardiomiocitos Células pluripotentes inducidas Células somáticas de fibroblastos embriogénicos Transformación hacia células madre pluripotentes Células de mioblastos esqueléticos Medula osea Similitud estructural con cardiomiocitos Células residentes de tejido cardíaco Procedencia Aplicaciones Células progenitoras vasculares Corazón Formadoras de vasos coronarios Diferenciación a células endoteliales Diferenciación a músculo liso Células progenitoras de miocitos Corazón Diferenciación a cardiomiocitos Células progenitoras cardíacas o cardioesferas Corazón Diferenciación a cardiomiocitos - 2.
En cuanto a las células madre residentes en el tejido cardiaco, se ha sugerido que hay dos tipos de células progenitoras en el corazón9: las células progenitoras vasculares, que formarán los vasos coronarios, y las células progenitoras de miocitos, que se diferenciarán hacia cardiomiocitos. Se ha comprobado que las células progenitoras vasculares son capaces de migrar dentro del miocardio y diferenciarse a células endoteliales y músculo liso y de organizarse en vasos coronarios. Las células progenitoras cardiacas, también denominadas cardioesferas, se aíslan directamente de tejido cardiaco adulto y se caracterizan porque al co-cultivarlas con cardiomiocitos pueden desarrollar un potencial de acción y contraerse10 (tabla 1).
Este manuscrito se ha realizado con la ayuda de una Beca de Investigación de la Sociedad Andaluza de Cardiología, Beca 2009, y de la Red Cardiovascular RECAVA-ISCIII.
Al Dr. Eduardo de Teresa Galván, Jefe del Servicio de Cardiología del Hospital Clínico Virgen de la Victoria, y al Dr. Borja Fernández Corujo, Profesor del Departamento de Biología Animal de la Facultad de Ciencias de la Universidad de Málaga, por la discusión y revisión científica del manuscrito, y a Beatriz Segura, Técnico de Laboratorio, por su esfuerzo constante y ayuda a este manuscrito.