La fibrilación auricular (FA) es el trastorno del ritmo más frecuente1, con una prevalencia en la población general del 1% y de hasta el 8% en mayores de 80 años, y se asocia con un incremento de 2 veces el riesgo de mortalidad y de 2–6 veces el riesgo de presentar un ictus.
Cuando atendemos a un paciente con FA, una vez tratados los factores desencadenantes, tendremos que valorar el tipo de FA (paroxística, persistente o permanente), la edad y las comorbilidades, los síntomas asociados, la presencia de cardiopatía así como el perfil de riesgo tanto embólico como hemorrágico para poder decidir qué estrategia seguir en cuanto al control de ritmo o frecuencia y la necesidad o no de anticoagulación o antiagregación.
Control de ritmo o control de frecuenciaIndudablemente los mecanismos desencadenantes de la FA se ponen en marcha muchos años antes de su aparición y, en este sentido, la prevención primaria es crucial para evitar la pérdida del ritmo actuando precozmente sobre todos los factores de riesgo modificables: hipertensión, diabetes, obesidad, alteraciones tiroideas, insuficiencia cardíaca (IC), apnea obstructiva, etc.
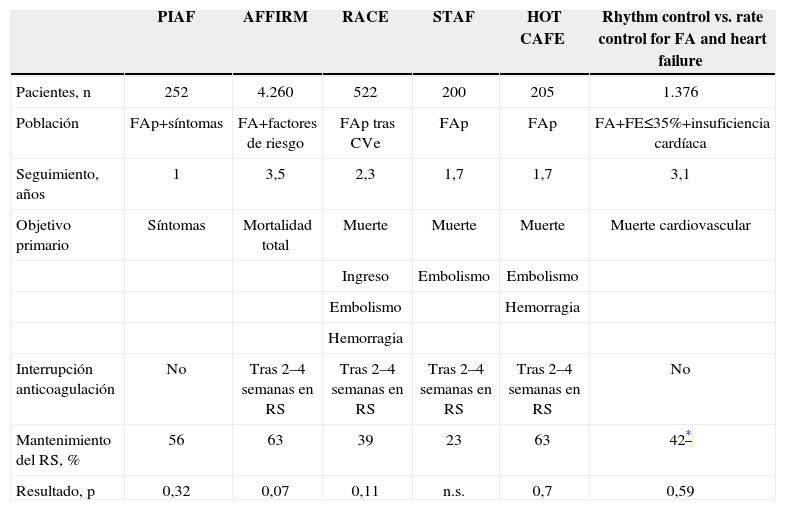
En prevención secundaria de FA, varios ensayos aleatorizados (tabla 1) han comparado ambas estrategias farmacológicas (control de ritmo vs. frecuencia) sin encontrar diferencias significativas en cuanto a mortalidad, calidad de vida, complicaciones tromboembólicas o aparición de IC, siendo incluso las hospitalizaciones y las reacciones adversas más frecuentes en el grupo de control del ritmo. No obstante, hay que tener en cuenta que en estos trabajos se incluyó a pacientes de edad avanzada (edad media de 70 años) con cardiopatía y seleccionando aquellos que podían tolerar la persistencia en FA. El grupo de control del ritmo se vio lastrado por la ineficacia de los antiarrítmicos para mantener el ritmo sinusal (RS), con tasas de eficacia de entre el 23% del STAF y el 63% del AFFIRM, y la interrupción del tratamiento anticoagulante tras el aparente control del ritmo, salvo en el rhythm or rate control in atrial fibrillation – pharmacologic intervention in atrial fibrillation a randomized trial (PIAF), un hecho que pudo condicionar una mayor incidencia de complicaciones embólicas. Cuando se ha analizado específicamente la mejor estrategia farmacológica en pacientes con IC y disfunción ventricular2 tampoco se han encontrado diferencias entre ambas opciones.
Estudios que comparan estrategia de control de ritmo frente a control de frecuencia
| PIAF | AFFIRM | RACE | STAF | HOT CAFE | Rhythm control vs. rate control for FA and heart failure | |
| Pacientes, n | 252 | 4.260 | 522 | 200 | 205 | 1.376 |
| Población | FAp+síntomas | FA+factores de riesgo | FAp tras CVe | FAp | FAp | FA+FE≤35%+insuficiencia cardíaca |
| Seguimiento, años | 1 | 3,5 | 2,3 | 1,7 | 1,7 | 3,1 |
| Objetivo primario | Síntomas | Mortalidad total | Muerte | Muerte | Muerte | Muerte cardiovascular |
| Ingreso | Embolismo | Embolismo | ||||
| Embolismo | Hemorragia | |||||
| Hemorragia | ||||||
| Interrupción anticoagulación | No | Tras 2–4 semanas en RS | Tras 2–4 semanas en RS | Tras 2–4 semanas en RS | Tras 2–4 semanas en RS | No |
| Mantenimiento del RS, % | 56 | 63 | 39 | 23 | 63 | 42* |
| Resultado, p | 0,32 | 0,07 | 0,11 | n.s. | 0,7 | 0,59 |
CVe: cardioversión; FA: fibrilación auricular; FAp: fibrilación auricular paroxística; FE: fracción de eyección; n.s.: no significativo; RS: ritmo sinusal.
Hemos aprendido que un control aparente del ritmo no elimina el riesgo tromboembólico, y que con los fármacos antiarrítmicos clásicos, por un lado, es difícil mantener el RS y, por otro lado, no disminuyen la morbilidad asociada a la FA. Además, en estos ensayos no están representados los pacientes más jóvenes sin comorbilidades ni los muy sintomáticos.
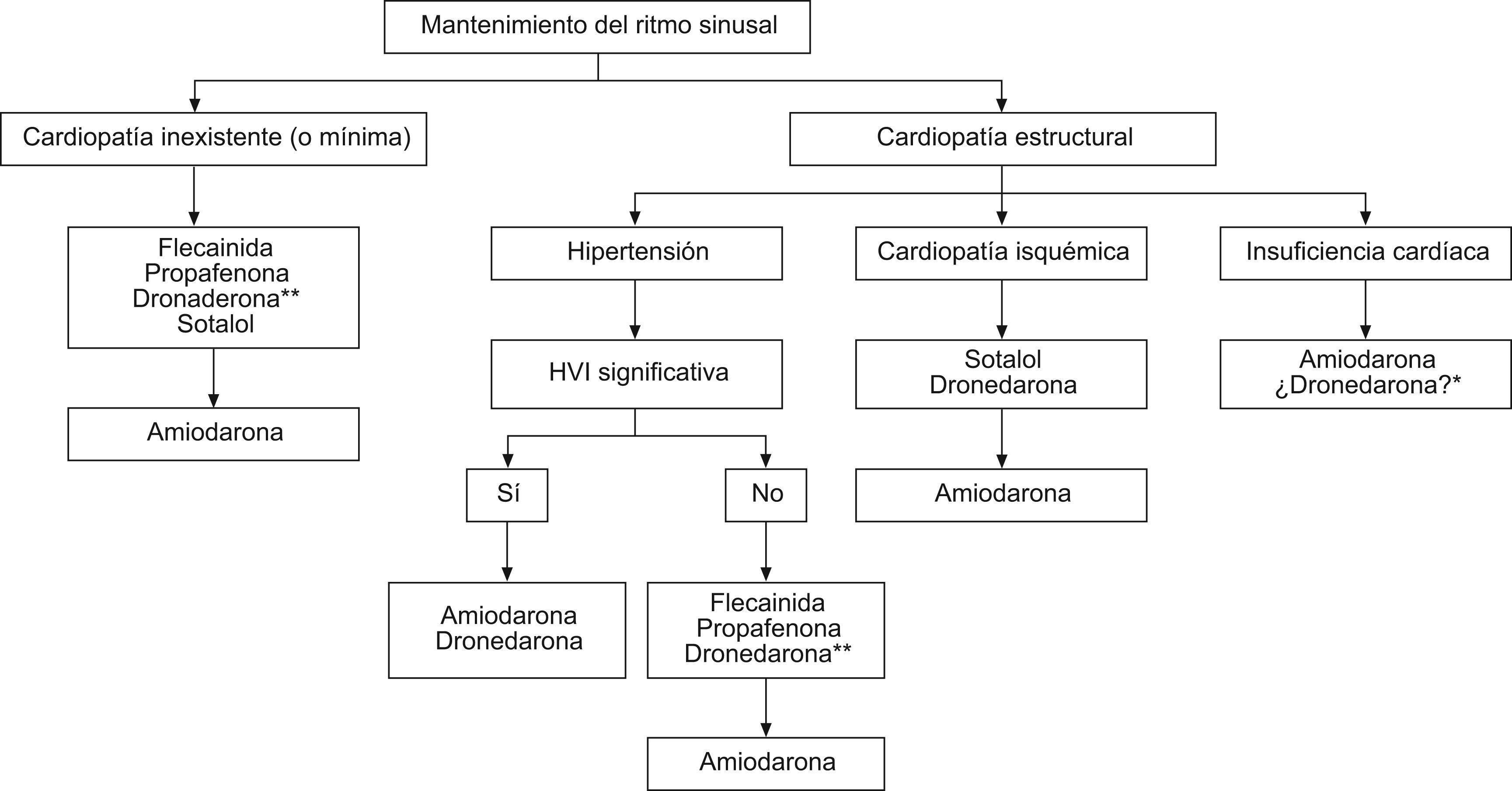
Fármacos para el control del ritmoLas indicaciones para seleccionar el fármaco antiarrítmico vienen condicionadas más por las contraindicaciones que por la eficacia (fig. 1):
- •
En pacientes sin cardiopatía, antiarrítmicos 1C según la clasificación de Vaughan Williams, como la flecainida y la propafenona. En la FA de inducción vagal, la disopiramida por su acción anticolinérgica podría ser la primera opción.
- •
En el caso de presentar IC o hipertensión arterial con hipertrofia ventricular se recomendaría el uso de amiodarona y cuando se asocia a cardiopatía isquémica se recomienda el sotalol.
- •
Los betabloqueantes tienen una eficacia moderada para mantener el RS y pueden ser la primera opción, especialmente si hay otras indicaciones para tomarlos (hipertensión, IC, hipertiroidismo).
Elección del fármaco antiarrítmico para el mantenimiento del ritmo sinusal en pacientes con fibrilación auricular1. Se ha excluido el dofetilide no disponible en España. *La dronedarona no se podría administrar en pacientes con disfunción ventricular (FEVI≤35%) y descompensación (grado iii–iv de la NYHA) en el último mes. **No hay estudios que comparen la dronedarona con antiarrítmicos 1C.
Con el uso de los fármacos 1C existe el riesgo de desarrollar un flúter 1C con conducción auriculoventricular 1:1, por lo que es aconsejable añadir fármacos con acción sobre el nodo aurículo-ventricular (NAV).
La amiodarona, siendo el fármaco más eficaz para el mantenimiento del RS, es también el que se asocia a una mayor toxicidad, principalmente tiroidea y pulmonar, lo que limita su uso a largo plazo en muchas ocasiones. Como alternativa se presenta la dronedarona, molécula derivada de la amiodarona que carece de yodo en su composición y que ha demostrado ser eficaz en disminuir la recurrencia de FA en dos estudios, EURIDIS y ADONIS, y de disminuir la FC en el estudio ERATO. Cuando se ha comparado con amiodarona3 resulta menos eficaz que esta para mantener el RS, pero a cambio de menos efectos adversos. En el estudio ATHENA, la dronedarona además demostró disminuir la mortalidad y la necesidad de hospitalización. Únicamente estaría contraindicado su uso en pacientes con disfunción ventricular severa y descompensación reciente de IC a la vista de los resultados del estudio ANDROMEDA.
El ensayo ATHENA nos enseña que al evaluar un antiarrítmico importa el ECG, pero todavía más los síntomas, la calidad de vida y la morbilidad de quien los toma.
En la figura 1 podemos observar un algoritmo de elección del fármaco antiarrítmico para el mantenimiento del RS.
Otras opciones para minimizar los riesgos son el uso de los fármacos 1C solo para acortar las crisis cuando estas son esporádicas y toleradas, en la opción conocida como «píldora en el bolsillo», y el empleo de dosis bajas de amiodarona oral (3–5 comprimidos en la semana).
Indicaciones del control del ritmo- •
Primer episodio de FA persistente. Siempre debería intentarse al menos una cardioversión con o sin fármacos antiarrítmicos a continuación, salvo si hay pocos síntomas y baja probabilidad de mantener el ritmo por cardiopatía con dilatación severa auricular.
- •
FA paroxística sintomática.
- •
FA persistente sintomática y probabilidad de mantener el RS.
- •
FA persistente y taquimiopatía.
El objetivo establecido empíricamente en las guías de alcanzar una frecuencia cardíaca (FC) en reposo de entre 60 y 80 latidos por minuto y de entre 90 y 115 latidos por minuto durante el ejercicio se ha visto cuestionado recientemente tras la publicación del ensayo RACE II4, en el que un control menos estricto de la FC, siendo el objetivo una FC en reposo por debajo de 110 latidos por minuto, no era inferior a un control estricto de la FC en cuanto al objetivo primario compuesto de muerte de causa cardiovascular, hospitalización por IC, ictus, embolismos, sangrado y eventos arrítmicos graves.
Los fármacos indicados son aquellos que actúan sobre la conducción del NAV: betabloqueantes, digoxina, amiodarona, diltiazem y verapamilo. Los betabloqueantes son los fármacos más eficaces para controlar la FC alcanzando el objetivo especificado en el AFFIRM en un 70 frente a un 54% del verapamilo o el diltiazem. La digoxina es eficaz en reposo, pero no durante el ejercicio y estaría indicada a dosis bajas diarias en pacientes con vida sedentaria, además de ser de elección para controlar la frecuencia en pacientes con IC o disfunción ventricular.
Prevención tromboembólicaLa FA de origen no reumático es responsable del 15–20% de los accidentes cerebrovasculares de origen isquémico, aumentando el riesgo de ictus la FA valvular hasta en 18 veces. Las guías de FA contemplan una serie de factores de riesgo para presentar eventos cardioembólicos sobre la base de los que indican la necesidad de anticoagulación o antiagregación. De los sistemas de puntuación para valorar el riesgo embólico, el más validado es el CHADS2, que recomienda anticoagular a pacientes con una puntuación superior o igual a 2. Ni el tipo de FA paroxística o persistente ni la presencia o no de síntomas asociados modifican el riesgo y, por tanto, las indicaciones de anticoagulación.
Cuando se compara la eficacia de la prevención tromboembólica de la antiagregación y la anticoagulación en pacientes con FA, la antiagregación con aspirina es claramente inferior quedando indicada para pacientes con un menor riesgo embólico (CHADS<2). El ensayo ACTIVE observó que en caso de contraindicación para el uso de antagonistas de la vitamina K, la asociación de aspirina y clopidogrel frente a la aspirina sola reducía el riesgo de eventos vasculares mayores incrementando, sin embargo, el número de hemorragias mayores.
En la FA, el INR objetivo estaría entre 2,0 y 3,0, salvo si el riesgo es alto por embolismo previo bajo anticoagulación, donde estaría entre 2,5 y 3,5. En pacientes con alto riesgo de sangrado hay que individualizar la indicación de anticoagulación y en todo caso monitorizar estrechamente el INR y optar por un rango menor entre 1,6 y 2,5. La dosis recomendada de aspirina para la antiagregación sería de entre 81 y 325mg/día.
Ha supuesto un enorme paso en la búsqueda de alternativas a la anticoagulación con antagonistas de la vitamina K el estudio RELY5, donde el dabigatran, un inhibidor directo de la trombina de administración oral y que no precisa monitorización del efecto anticoagulante, ha demostrado a dosis de 110mg/día ser equivalente en la protección de eventos isquémicos reduciendo el riesgo de sangrado con respecto a la warfarina y a dosis de 150mg/día ser superior en la protección de eventos isquémicos, aunque aumentando el riesgo de hemorragias.
Una alternativa en fase de investigación clínica en pacientes de alto riesgo con FA no valvular con contraindicación para la anticoagulación oral es la oclusión de la orejuela izquierda con dispositivos de cierre percutáneo a la vista de los resultados de estudios, como el PROTECT AF, donde se demostró la ausencia de inferioridad respecto al tratamiento con warfarina en cuanto al objetivo primario compuesto de ictus, muerte cardiovascular y embolismo sistémico, aunque con una tasa de efectos adversos mayor.
ConclusionesEl paradigma del tratamiento del paciente con FA está cambiando en varios sentidos. Cabe resaltar la importancia en la prevención de su desarrollo tratando los factores de riesgo. Una vez que ha aparecido la FA sigue siendo crucial tratar los posibles factores desencadenantes y a continuación centrarnos en las características del paciente para poder decidir la mejor estrategia a seguir. Ahora sabemos que siendo importante el mantenimiento del RS para evitar el remodelado adverso asociado a la FA lo es más el control de los síntomas, la calidad de vida y la reducción de complicaciones asociadas a la arritmia. En este sentido, la llegada de un antiarrítmico como la dronedarona, con mejor perfil de seguridad, va a permitir, junto con el uso juicioso de los antiarrítmicos clásicos y la ablación con catéter, una mayor difusión de la estrategia de control del ritmo con la que aminorar las complicaciones derivadas de la FA. No menos importante va a ser la mayor adherencia a las indicaciones de prevención tromboembólica que seguro va a traer asociado el disponer de alternativas más seguras y cómodas que los antagonistas de la vitamina K.