La gran evolución en el conocimiento y el manejo de las arritmias en adultos en los últimos 20 años se ha visto reflejada en la población pediátrica, para la que actualmente se dispone de un armamentario similar. No obstante, es común el temor a posibles complicaciones de los procedimientos de ablación relacionadas con el tamaño del paciente, con los efectos de la radiación a largo plazo o con la presencia de cardiopatías congénitas, entre otros.
Por otro lado, el uso de dispositivos implantables se ha extendido gracias a la mayor esperanza de vida de los pacientes con cardiopatías congénitas y a los avances técnicos, fundamentalmente los relacionados con la miniaturización de generadores y electrodos.
¿Presentan aspectos diferenciales los procedimientos de ablación por catéter y sus indicaciones en la población pediátrica?La idea de que los niños son simplemente adultos pequeños no es totalmente inexacta en el caso de los procedimientos de ablación por catéter, sobre todo a partir de los 11 o 12 años de edad. No obstante, lo que parece ser simplemente una diferencia de escala puede tener importantes implicaciones en las indicaciones, el diagnóstico y las posibles complicaciones del procedimiento.
Al margen de los aspectos relacionados con el tamaño, como las menores dimensiones de las cámaras cardiacas, el escaso grosor parietal y la menor distancia entre las distintas estructuras, hemos de considerar otros aspectos diferenciales, tales como la potencial curación espontánea de la arritmia con el desarrollo del miocardio o la posibilidad de crecimiento de la lesión por radiofrecuencia con el tiempo. Del mismo modo, se deben optimizar las medidas de protección radiológica, ya que el riesgo de presentar efectos adversos tardíos es inversamente proporcional a la edad en que se produce la exposición.
Otro aspecto que se debe destacar es la menor colaboración del paciente, lo que hace que cobre un papel fundamental la sedación. En nuestro caso, el programa de ablación pediátrica se sustenta en la estrecha colaboración entre la Unidad de Arritmias y los Servicios de Cardiología Pediátrica y Anestesia, realizándose la mayoría de los procedimientos bajo anestesia general, con objeto de evitar, además de la vivencia del procedimiento, el desplazamiento indeseado de los catéteres en momentos críticos del mismo.
En cuanto a las indicaciones, es fundamental enfatizar en la seguridad sobre la eficacia. El curso relativamente benigno de la mayoría de las arritmias en la infancia y el temor a complicaciones como el bloqueo auriculoventricular (AV), conducen a un diferente algoritmo de decisión para niños y adultos. Por ejemplo, en pacientes menores de 5 años con síndrome de Wolff-Parkinson-White se individualiza la indicación, incluso en pacientes sintomáticos, en función de la localización de la vía, el peso o la frecuencia y tolerancia de las taquicardias, debido al mayor riesgo de complicaciones y al cese espontáneo de la conducción por la vía accesoria hasta en el 40% los casos. A partir de los 5 años de edad, en el caso de arritmias sintomáticas, el balance entre riesgos y beneficios se inclina a favor de la ablación, pero únicamente si esta puede realizarse con seguridad; a partir de los 10 años, incluso en pacientes asintomáticos, estaría justificado un manejo más agresivo que en los adultos, ya que este grupo etario tiene más riesgo de presentar una muerte súbita como primera manifestación clínica en el caso de vías accesorias de alto riesgo.
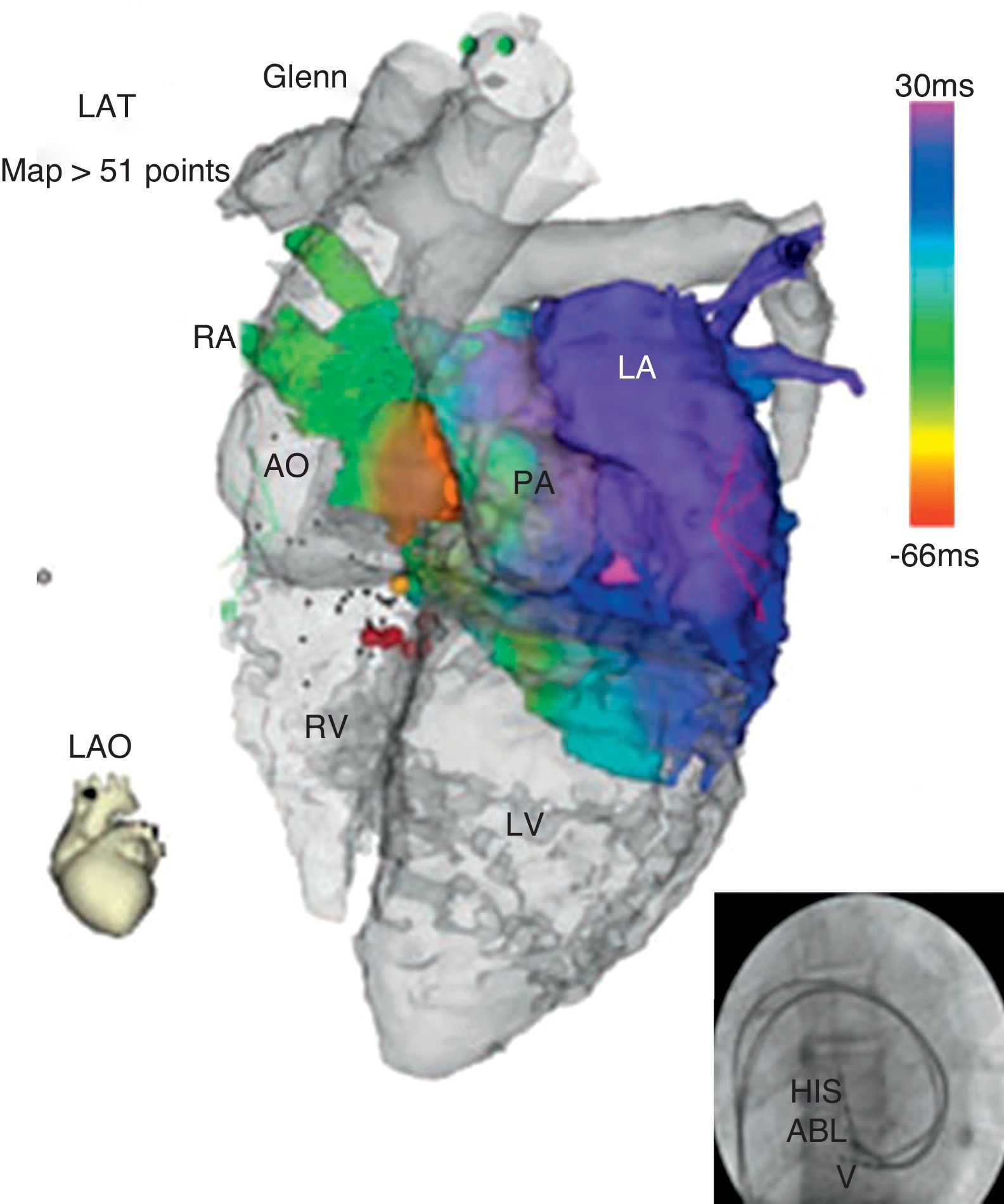
Mención especial merece el uso de la crioablación como fuente de energía, que ha surgido en los últimos años como alternativa a la radiofrecuencia, y que presenta una serie de ventajas que incluyen la reversibilidad de sus efectos durante la fase de criomapeo antes de provocar una lesión definitiva, la adhesión del catéter al endocardio, el bajo riesgo de lesión de las arterias coronarias cercanas y la baja incidencia de formación de trombos. Estas características la convierten en una fuente de energía atractiva en la ablación pediátrica, sobre todo para sustratos septales1 (por el menor riesgo de bloqueo AV), niños pequeños y pacientes con una anatomía anormal en los que no conozcamos la localización precisa del sistema específico de conducción. En este último grupo de pacientes con anatomía anormal desempeñan un importante papel los mapas electroanatómicos creados mediante sistemas de navegación, habitualmente integrados en imágenes de tomografía computarizada o resonancia magnética (fig. 1), que permiten adaptar el procedimiento a la anatomía del paciente2.
¿Qué sustratos son los más frecuentemente abordados y qué resultados podemos esperar?La distribución de frecuencias de las arritmias en niños varía sustancialmente con respecto a los adultos. La taquicardia ventricular es infrecuente, ya que supone el 5% de las taquicardias en niños y el 20% de las taquicardias de QRS ancho.
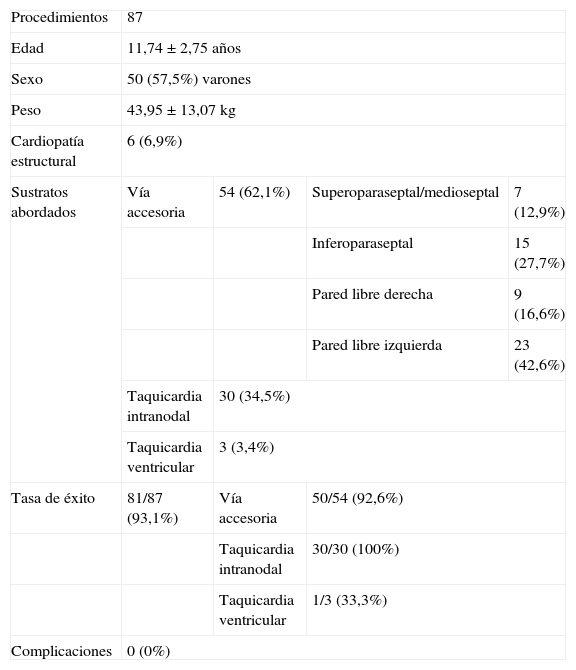
Las mediadas por vías accesorias suponen alrededor del 70% de las taquicardias supraventriculares en niños, mientras que en adultos son responsables del 30-40%. La tasa de éxito de los procedimientos de ablación para este sustrato se sitúa por encima del 90% en la mayoría de las series3 (tabla 1) y es superior en las vías accesorias de pared libre izquierda. Entre las potenciales complicaciones del procedimiento se encuentran la lesión coronaria y el bloqueo AV, casi exclusivo de las vías de localización superoparaseptal y medioseptal, con una incidencia del 3%.
Características basales y resultados obtenidos según los distintos sustratos en pacientes menores de 15 años sometidos a ablación en la Unidad de Arritmias del Hospital Universitario Virgen del Rocío
| Procedimientos | 87 | |||
| Edad | 11,74±2,75 años | |||
| Sexo | 50 (57,5%) varones | |||
| Peso | 43,95±13,07kg | |||
| Cardiopatía estructural | 6 (6,9%) | |||
| Sustratos abordados | Vía accesoria | 54 (62,1%) | Superoparaseptal/medioseptal | 7 (12,9%) |
| Inferoparaseptal | 15 (27,7%) | |||
| Pared libre derecha | 9 (16,6%) | |||
| Pared libre izquierda | 23 (42,6%) | |||
| Taquicardia intranodal | 30 (34,5%) | |||
| Taquicardia ventricular | 3 (3,4%) | |||
| Tasa de éxito | 81/87 (93,1%) | Vía accesoria | 50/54 (92,6%) | |
| Taquicardia intranodal | 30/30 (100%) | |||
| Taquicardia ventricular | 1/3 (33,3%) | |||
| Complicaciones | 0 (0%) | |||
Al igual que en nuestra experiencia (tabla 1), el segundo sustrato en frecuencia es la taquicardia por reentrada intranodal. El procedimiento y sus resultados no difieren de los de la población adulta, con una tasa de éxito de alrededor del 95%. No obstante, hemos de tener en cuenta que existe un teórico mayor riesgo de bloqueo AV debido a la menor distancia entre la región de la vía lenta (objeto de la ablación) y el nodo AV compacto, por lo que en niños menores de 20kg es preferible la crioablación, que ha demostrado similares tasas de éxito y de recidiva que la radiofrecuencia1, sin que se haya descrito ningún caso de bloqueo AV permanente hasta el momento.
La taquicardia auricular es responsable del 5 al 20% de las taquicardias supraventriculares en niños, mientras que en adultos únicamente supone el 2%. Con frecuencia, tiene un carácter incesante, pudiendo dar lugar a una taquimiocardiopatía. La reversibilidad de la disfunción ventricular tras cesar la arritmia y la escasa eficacia de los fármacos antiarrítmicos dan un papel preponderante a la ablación con catéter, con una tasa de éxito del 90 al 100% según las distintas series. Al margen de las complicaciones comunes a todos los procedimientos de ablación, como las relativas a la zona de punción o el taponamiento cardiaco, en el caso de las taquicardias auriculares es posible la estenosis de venas pulmonares cuando el foco se localiza en las mismas, el daño al nervio frénico en las taquicardias cristales o el bloqueo AV en las del vértice del triángulo de Koch.
La taquicardia juncional ectópica es una entidad rara y difícil de manejar con fármacos, habitualmente incesante, aunque en ocasiones se puede resolver espontáneamente. Debido al posible riesgo elevado de bloqueo AV se debe optar inicialmente por un tratamiento conservador. En cualquier caso, el porcentaje de éxito descrito tanto con radiofrecuencia como con crioablación se sitúa alrededor del 85%, con una aceptable tasa de complicaciones.
¿Qué peculiaridades presenta el implante de dispositivos en niños y pacientes con cardiopatías congénitas?Los problemas técnicos inherentes al implante de un dispositivo en la población pediátrica se deben a la complejidad anatómica en el caso de las cardiopatías congénitas, a la desproporción entre el tamaño del generador y el tejido subcutáneo, y al crecimiento del paciente. Por ello, la planificación del acceso y el abordaje previo al procedimiento son de vital importancia. Determinadas situaciones obligan a un implante epicárdico, como en los casos con una anatomía anormal en los que no es posible acceder a las cavidades derechas de forma endovenosa o niños pequeños en los que los vasos no tienen el diámetro suficiente. Por otro lado, algunos autores aconsejan un abordaje epicárdico en el caso de cortocircuitos intracardiacos, debido al riesgo de embolia paradójica. Desconocemos qué papel desempeñarán en el futuro en las técnicas de implante los electrodos de desfibrilación subcutáneos.
Los trastornos de la conducción se pueden dar en pacientes con un corazón estructuralmente normal, como la mayoría de los bloqueos AV congénitos, o acompañando a una cardiopatía, bien de forma primaria o secundaria a los procedimientos quirúrgicos habituales, como en los casos en que se actúa sobre las aurículas (Senning, Glenn, Fontan), que pueden ocasionar disfunción sinusal. Por su parte, el bloqueo AV puede ser primario (defecto septal AV, transposición congénitamente corregida de las grandes arterias) o secundario a cirugía o intervencionismo. Las indicaciones para el implante de marcapasos en niños y pacientes con cardiopatías congénitas quedan recogidas en la tabla 24.
Indicaciones para el implante de marcapasos en niños, adolescentes y cardiopatías congénitas
| Indicaciones clase i |
| 1. Bloqueo AV de segundo grado avanzado o de tercer grado asociado a bradicardia sintomática, disfunción ventricular o bajo gasto cardiaco |
| 2. Disfunción del nodo sinusal sintomática cuando se ha demostrado la correlación de los síntomas con la bradicardia |
| 3. Bloqueo AV de segundo grado avanzado o de tercer grado postoperatorio cuya resolución no es esperable o si han pasado al menos 7 días desde la cirugía |
| 4. Bloqueo AV de tercer grado congénito con ritmo de escape de QRS ancho, ectopia ventricular compleja o disfunción ventricular |
| 5. Bloqueo AV de tercer grado congénito durante el primer año de vida con frecuencia cardiaca menor a 55 spm o cardiopatía congénita y frecuencia cardiaca menor a 70 spm |
| Indicaciones clase iia |
| 1. Bradicardia sinusal (intrínseca o secundaria a fármacos) y cardiopatía congénita, para la prevención de taquiarritmias auriculares |
| 2. Bloqueo AV de tercer grado congénito después del primer año de vida con frecuencia cardiaca media menor a 50 spm, pausas ventriculares 2 o 3 veces superiores a la longitud de ciclo basal, o asociado a síntomas debidos a incompetencia cronotropa |
| 3. Bradicardia sinusal asociada a cardiopatía congénita compleja con frecuencia cardiaca en reposo menor a 40 spm o pausas mayores a 3 s |
| 4. Cardiopatía congénita y bajo gasto debido a bradicardia sinusal o a pérdida de la sincronía AV |
| 5. Síncope de causa no aclarada en paciente con cirugía cardiaca previa complicada con bloqueo AV paroxístico y bloqueo fascicular |
| Indicaciones clase iib |
| 1. Bloqueo AV de tercer grado postoperatorio transitorio con bloqueo bifascicular al retornar a ritmo sinusal |
| 2. Bloqueo AV de tercer grado congénito en niños o adolescentes asintomáticos, con frecuencia cardiaca aceptable, QRS estrecho y función ventricular normal |
| 3. Bradicardia sinusal asintomática tras reparación de cardiopatía congénita compleja con frecuencia cardiaca en reposo menor a 40 spm y pausas mayores a 3 s |
Por lo que se refiere al desfibrilador automático implantable (DAI), su uso está bien establecido en el caso de la prevención secundaria, es decir, tras una muerte súbita recuperada o un episodio de taquiarritmia ventricular con compromiso hemodinámico4, pudiendo considerarse también en pacientes con disfunción ventricular y síncope de causa no aclarada. Más compleja es la decisión con respecto al implante de un DAI en prevención primaria, ya que no existen ensayos clínicos que respalden su uso sistemático y son más frecuentes las complicaciones asociadas al dispositivo, fundamentalmente la disfunción del electrodo, así como el riesgo de descargas inapropiadas, que es significantemente superior al de los adultos5. Por tanto, hemos de realizar una estratificación individualizada del riesgo arrítmico, considerando asimismo la probabilidad de potenciales complicaciones asociadas al dispositivo.
La terapia de resincronización (TRC) se ha empleado tanto de forma permanente como transitoriamente tras cirugía cardiaca, con buenos resultados en ambos casos. La indicación más frecuente es la disfunción sistólica inducida por estimulación, donde ha mostrado su eficacia. En pacientes con ventrículo único y en aquellos con ventrículo derecho sistémico, la TRC ha demostrado acortar la duración del QRS, aunque solo en estos últimos ha mejorado significativamente la fracción de eyección.
ConclusionesEl tamaño no es el único factor diferencial entre niños y adultos a la hora de considerar un procedimiento de ablación. Existen otros aspectos que se deben tener en cuenta, como una distribución distinta de los sustratos, el desarrollo futuro de un miocardio aún inmaduro y un potencial riesgo superior de complicaciones vasculares y bloqueo AV. En centros con experiencia, la ablación pediátrica ha mostrado una tasa de éxito de alrededor del 90% en la mayoría de las series y los sustratos, con una baja tasa de complicaciones asociadas al procedimiento.
En cuanto al implante de dispositivos, la complejidad del sustrato anatómico en el caso cardiopatías congénitas complejas y las cirugías previas contribuyen a una gran variabilidad en estos pacientes, lo que, unido a la escasez de ensayos clínicos, hace que las guías de práctica clínica sean de limitada evidencia científica. Por ello, las indicaciones y las técnicas de implante deben adaptarse de forma individualizada a cada paciente.