Se describe la forma de presentación, el diagnóstico y la resolución quirúrgica de un caso poco frecuente de aneurisma de seno de Valsalva. Se presenta el caso de una paciente femenina de 64 años con antecedentes de dos cirugías, una por ductus arterioso a los 12 años y la otra por una ventana aortopulmonar a los 16 años. Se encontraba asintomática. En un control de ecocardiografía, se observa válvula aórtica trivalva, insuficiencia leve y dilatación aneurismática del seno de Valsalva izquierdo. Realizamos una angiotomografía, la cual informó de un gran aneurisma de 88,9 mm saliendo de la coronaria izquierda de dicho seno. El cateterismo mostró un aneurisma de seno de Valsalva izquierdo, sin lesiones angiográficas. Decidimos realizar una intervención quirúrgica con circulación extracorpórea (canulación aórtica, cava y seno coronario). La paciente presentaba un aneurisma de gran tamaño con hematoma en el seno de Valsalva sobre el ostium de la coronaria izquierda, se extrajo el hematoma y se observó tejido sanioso en vía de fistulizarse hacia la aurícula izquierda. Se realizó la técnica de Yacoub con preservación valvular y un reimplante coronario izquierdo, así como la exclusión del aneurisma. El ecocardiograma intraoperatorio mostró buena competencia valvular e insuficiencia leve. La mujer presentó buena evolución, por lo cual se le dio el alta al séptimo día. Fue un caso complejo debido a la patología en sí y por ser una reoperación cardiaca. Existen varias formas de resolución, todos los componentes del complejo de la raíz aórtica deben considerarse y la técnica debe adaptarse a cada paciente. Aunque el abordaje quirúrgico óptimo sigue siendo controvertido, la competencia a largo plazo de la válvula aórtica parece seguir siendo la principal preocupación de los aneurismas de seno de Valsalva.
We describe the diagnostic and surgical resolution of a rare case of Valsalva sinus aneurysm. Sixty four (64) year old female patient with history of two previous surgery, one due to ductus arteriosus at age of 12 and an aortopulmonary window at age 16. Echocardiography control shows a severe dilatation of the left Valsalva sinus in a trivalve aortic valve with trivial insufficiency. Angiotomography reported a large aneurysm of left Valsalva sinus (88.9 mm) with coronary left main involved. Coronariography showed the same as TC without angiographic coronary lesions. Heart team dessision was surgical resolution with extracorporeal circulation (aortic cannulation, cava and coronary sinus). Patient presented a large aneurysm with great amount of thrombus in the left Valsalva sinus. The hematoma and thrombus was removed. Yacoub technique was performed with valvular preservation and left coronary reimplantation and exclusion of aneurysm. The intraprocedure trans esofagic echocardiogram showed trivial aortic insufficiency. Patient was discharged at seven days after procedure. There are several techniques for this pathology resolution. All components of the aortic root complex must be considered, and the technique must be adapted to each specific case. Although the optimal surgical approach remains controversial, long-term competence of the aortic valve appears to remain the main concern of Valsalva sinus aneurysms surgical treatment.
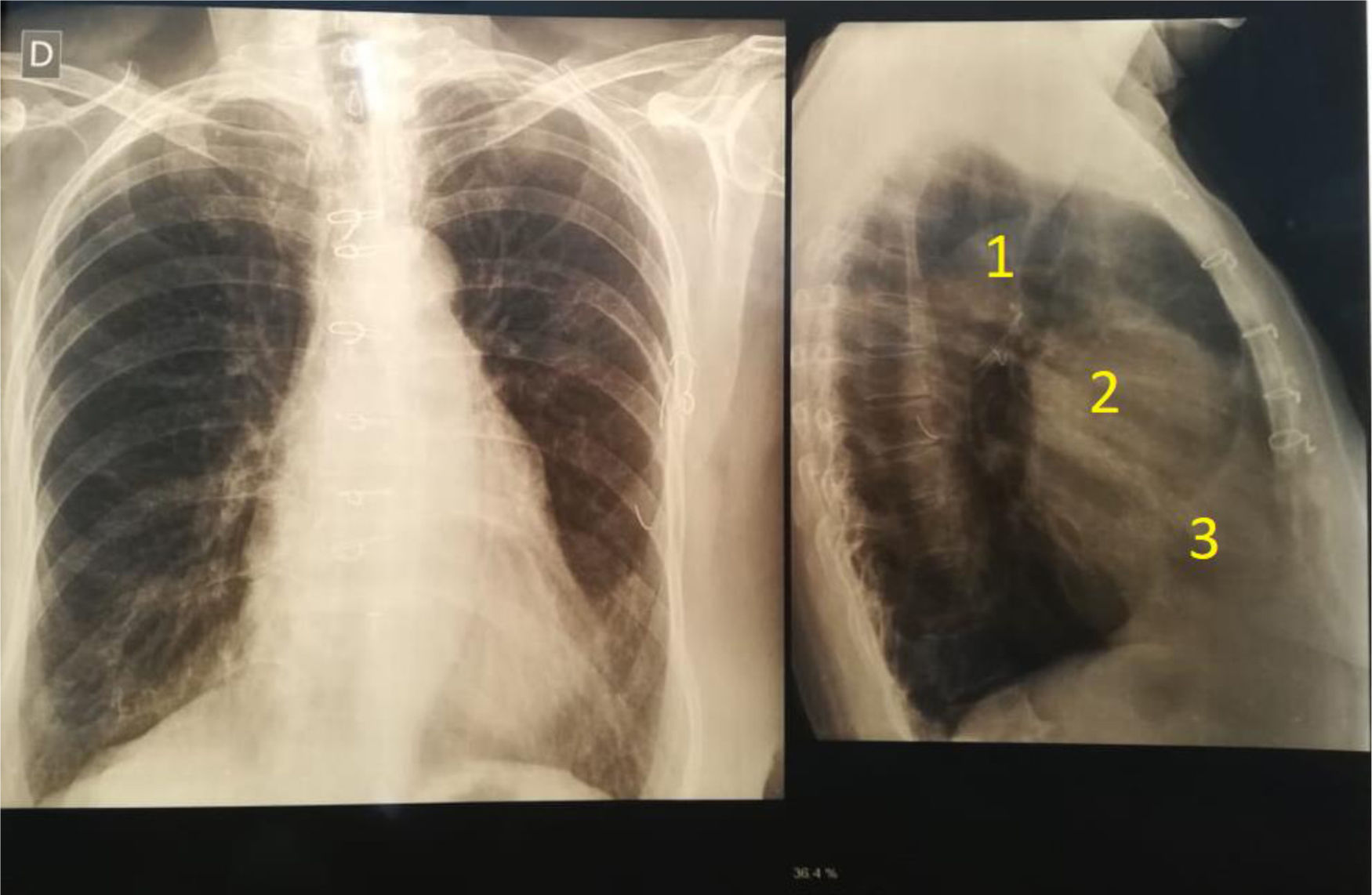
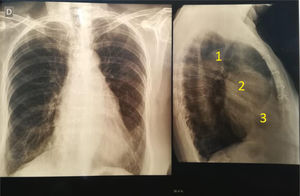
Paciente femenina de 64 años con antecedente de dos cirugías previas, una por ductus arterioso a los 12 años y otra por una ventana aortopulmonar a los 16 años. Se encontraba asintomática. En el examen físico cardiovascular, se detectaron ruidos cardiacos rítmicos, normofonéticos, sin edemas, ni disnea. El electrocardiograma mostró ritmo sinusal a 80 lpm, con signos de hipertrofia ventricular. En la radiografía de tórax, en la proyección frente, no se observan anormalidades con un índice cardiotorácico conservado y alambres de cirugía previa. En el perfil, aparece un gran aneurisma de raíz aórtica (fig. 1).
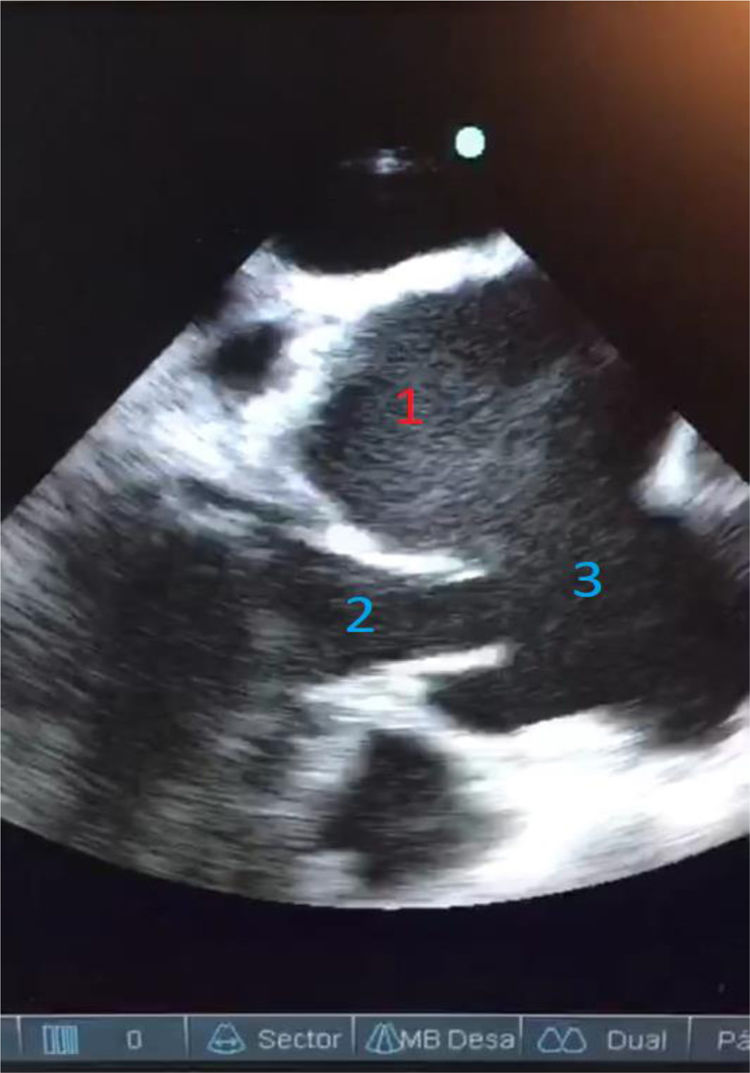
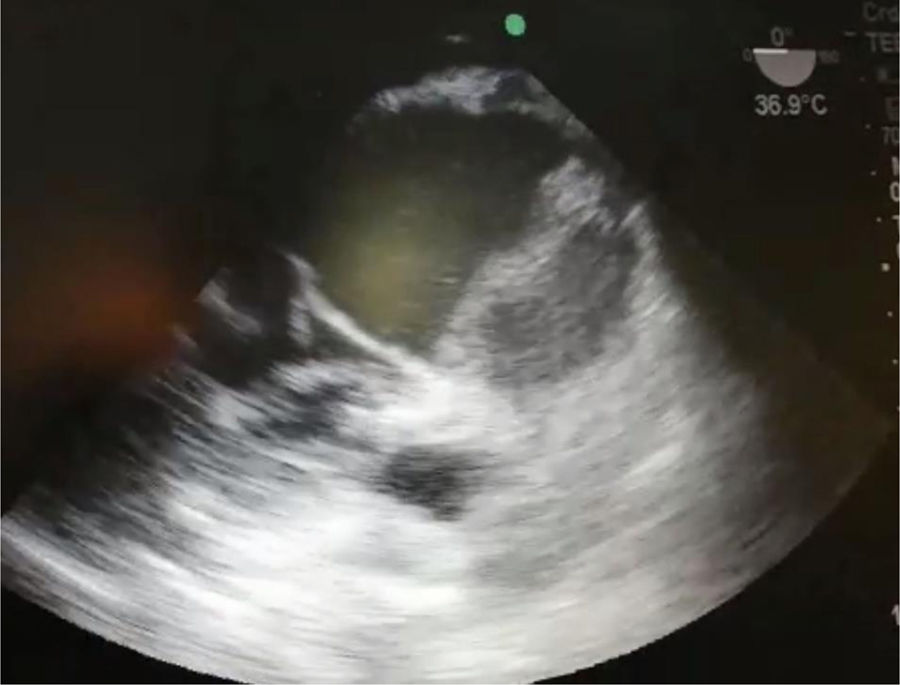
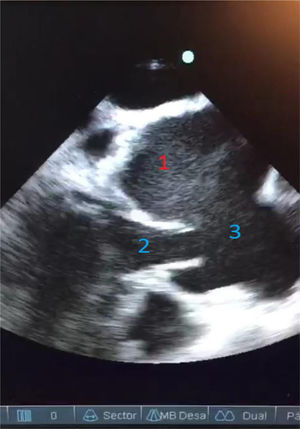
En un control de ecocardiografía, se observa válvula aórtica trivalva, insuficiencia leve y dilatación aneurismática del seno de Valsalva izquierdo. Buena función ventricular. Sin dilatación ventricular (fig. 2).
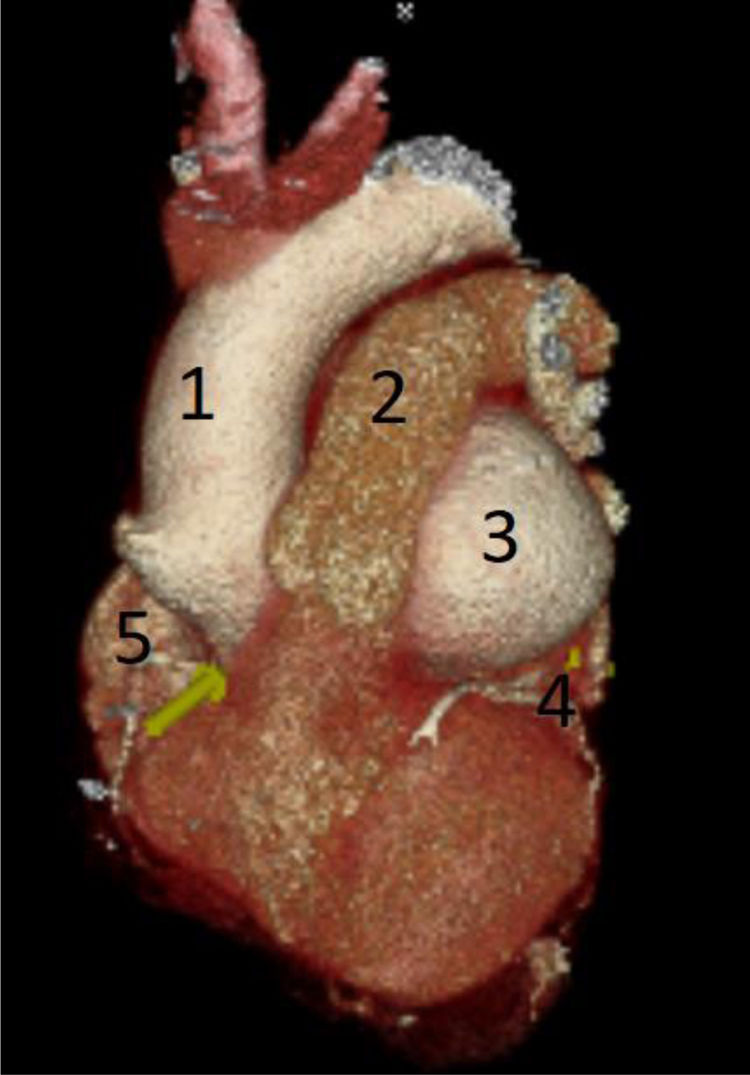
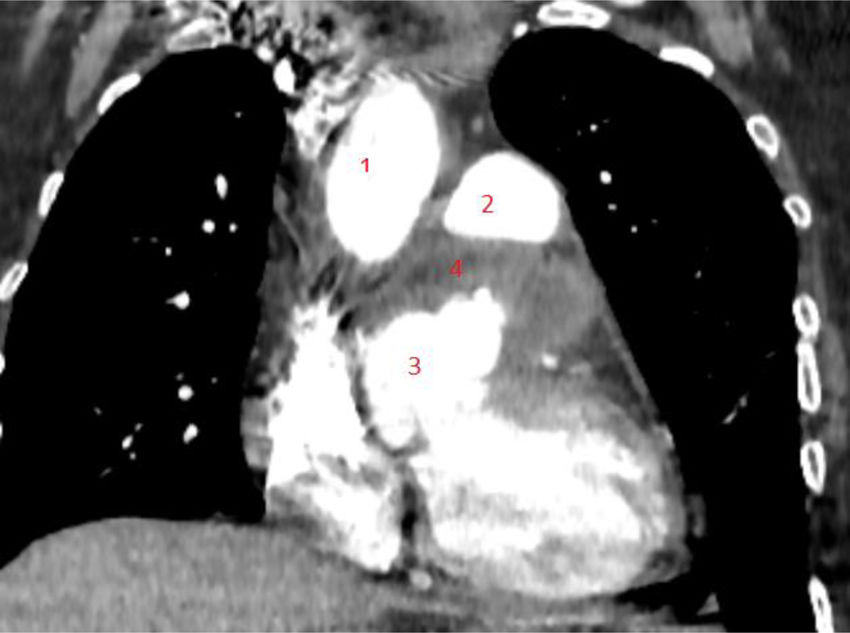
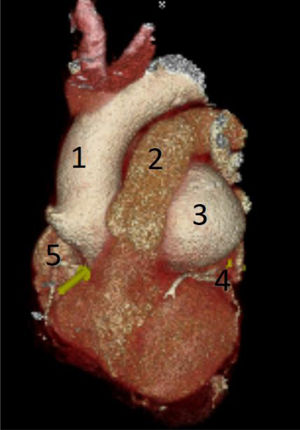
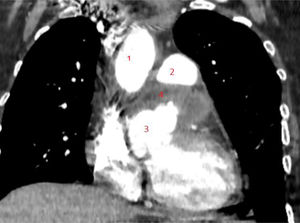
Realizamos una angiotomografía, la cual informó de un aneurisma de gran tamaño de seno de Valsalva izquierdo de 88,9 mm, que se encuentra por detrás del tronco de la arteria pulmonar y por delante de la aurícula izquierda. Se observa la coronaria izquierda saliendo en la porción distal del aneurisma. El cayado aórtico y la aorta descendente resultan con diámetros dentro de la normalidad (fig. 3).
Reconstrucción de tomografía donde se observa gran ASV izquierdo por detrás de la arteria pulmonar y por delante de la aurícula izquierda. 1) Aorta ascendente. 2) Tronco de arteria pulmonar. 3) ASV izquierdo. 4) Arteria coronaria izquierda. 5) Arteria coronaria derecha.
ASV: aneurisma de seno de Valsalva.
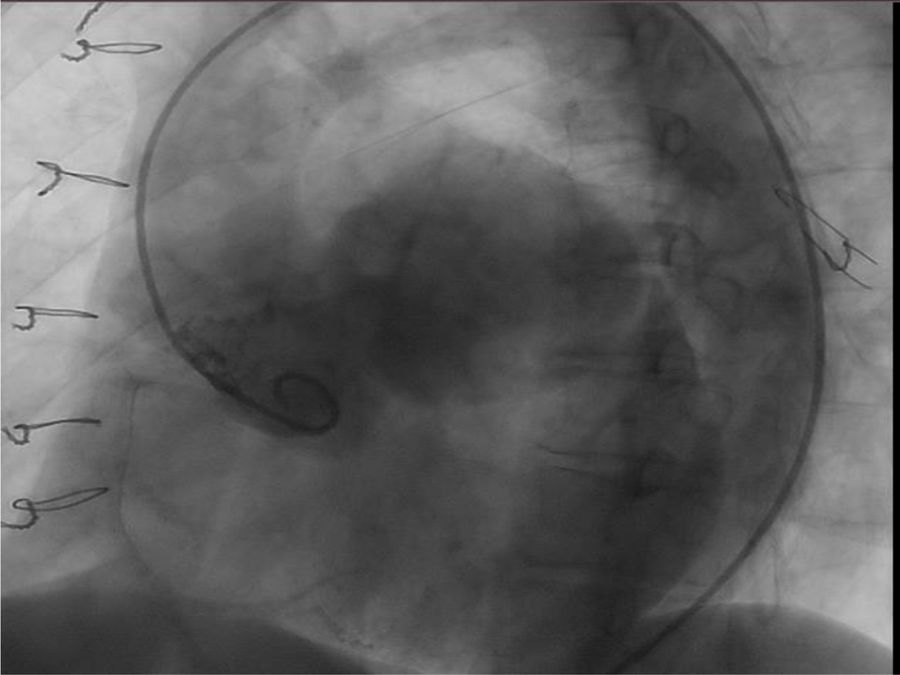
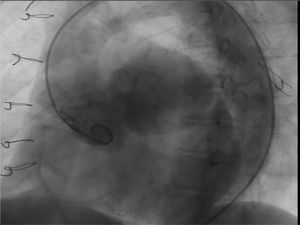
El cateterismo mostró el aneurisma con gran dilatación del seno coronario izquierdo con implante de arteria coronaria izquierda a dicho nivel del saco aneurismático. La coronaria derecha tenía características normales. Se objetiva insuficiencia valvular leve (fig. 4).
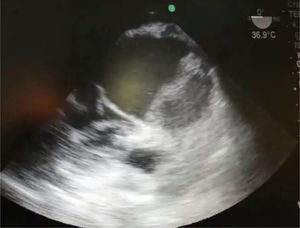
En la reunión de heart team, se plantearon varias alternativas dentro de las cuales estaba la endovascular o la quirúrgica. Había varios aspectos a tener en cuenta para la resolución del aneurisma. Uno de ellos, era la coronaria izquierda naciendo del fondo de este, ello llevaba a un gran problema endovascular, dado que no se podía excluir ese aneurisma sin afectarla. El otro componente en juego era la válvula aórtica que se encontraba solo con insuficiencia leve y en buenas condiciones, también generaba dudas sobre la resolución endovascular, si podría llegar a afectarla. Por todo lo mencionado, considerando la posibilidad de conservar la válvula y el reimplante de la coronaria izquierda, se decidió optar por la conducta quirúrgica, asumiendo el riesgo que acarrea una reoperación, dado que era la tercera cirugía cardiaca y, además, con la posibilidad de afectación de la válvula, lo cual llevaría al reemplazo. En el intraopertorio, realizamos un ecocardiograma donde se evidencia gran dilatación asociada al hematoma dentro de aneurisma (fig. 5).
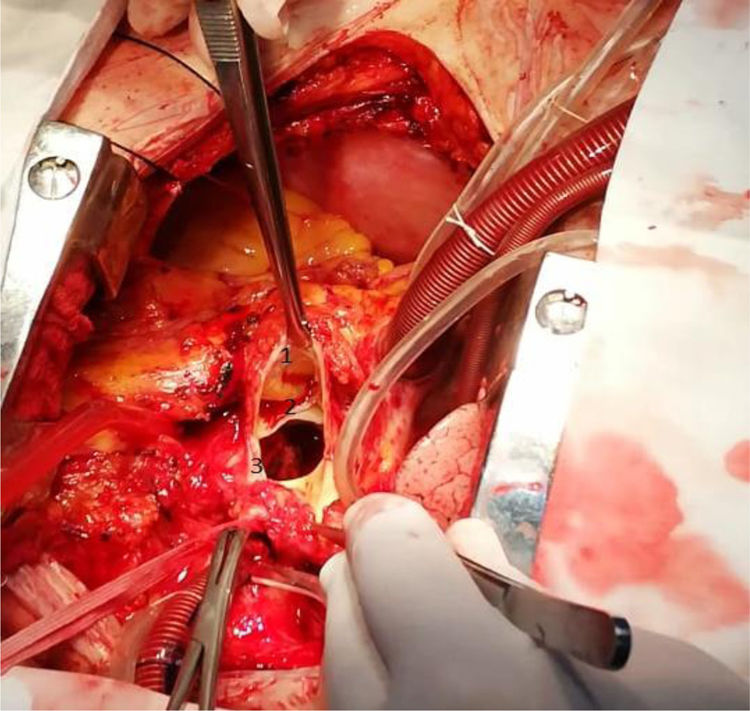
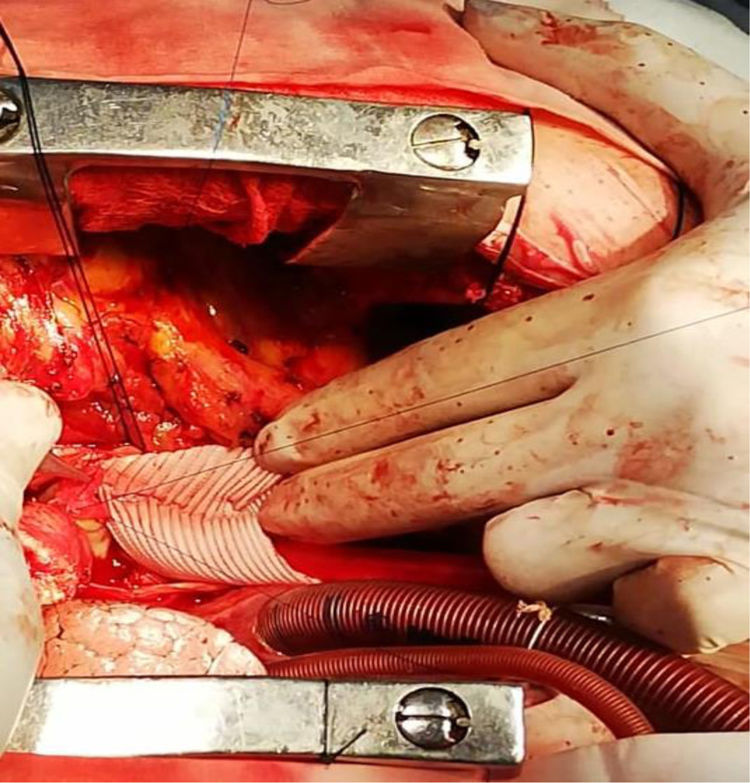
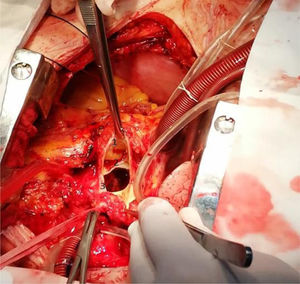
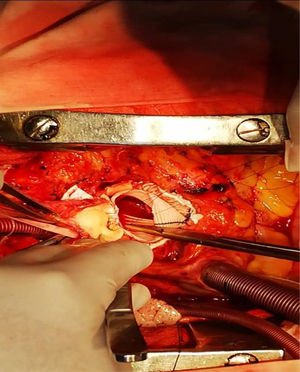
Realizamos una esternotomía con sierra oscilante, por medio de la cual encontramos abundantes adherencias por tratarse de una reoperación. Este procedimiento se efectuó con circulación extracorpórea (canulación aórtica, cava, seno coronario y vent en la arteria pulmonar). Posteriormente, continuamos con la aortotomía, en la cual se presentó un gran aneurisma hacia el seno coronario izquierdo (fig. 6).
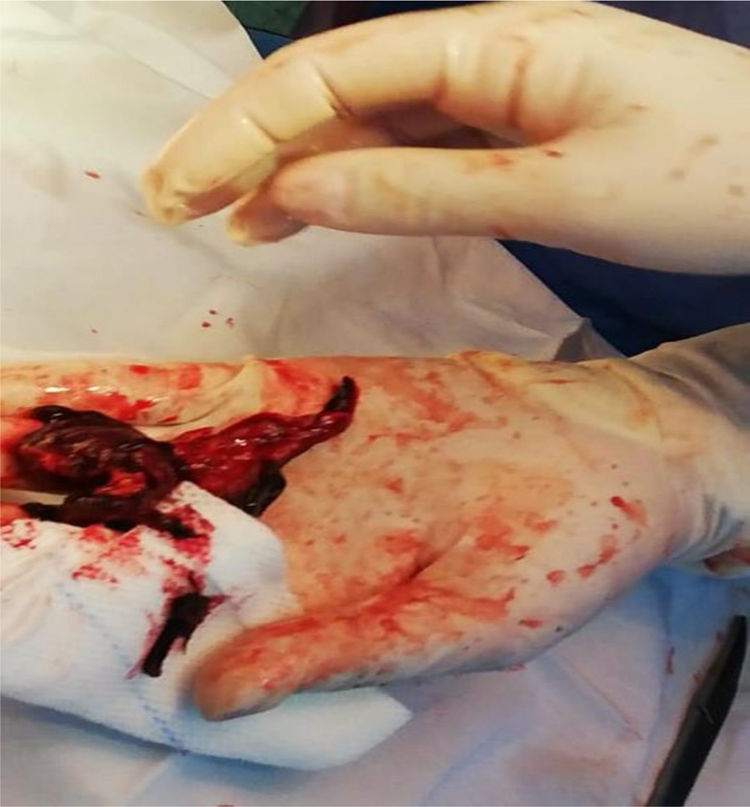
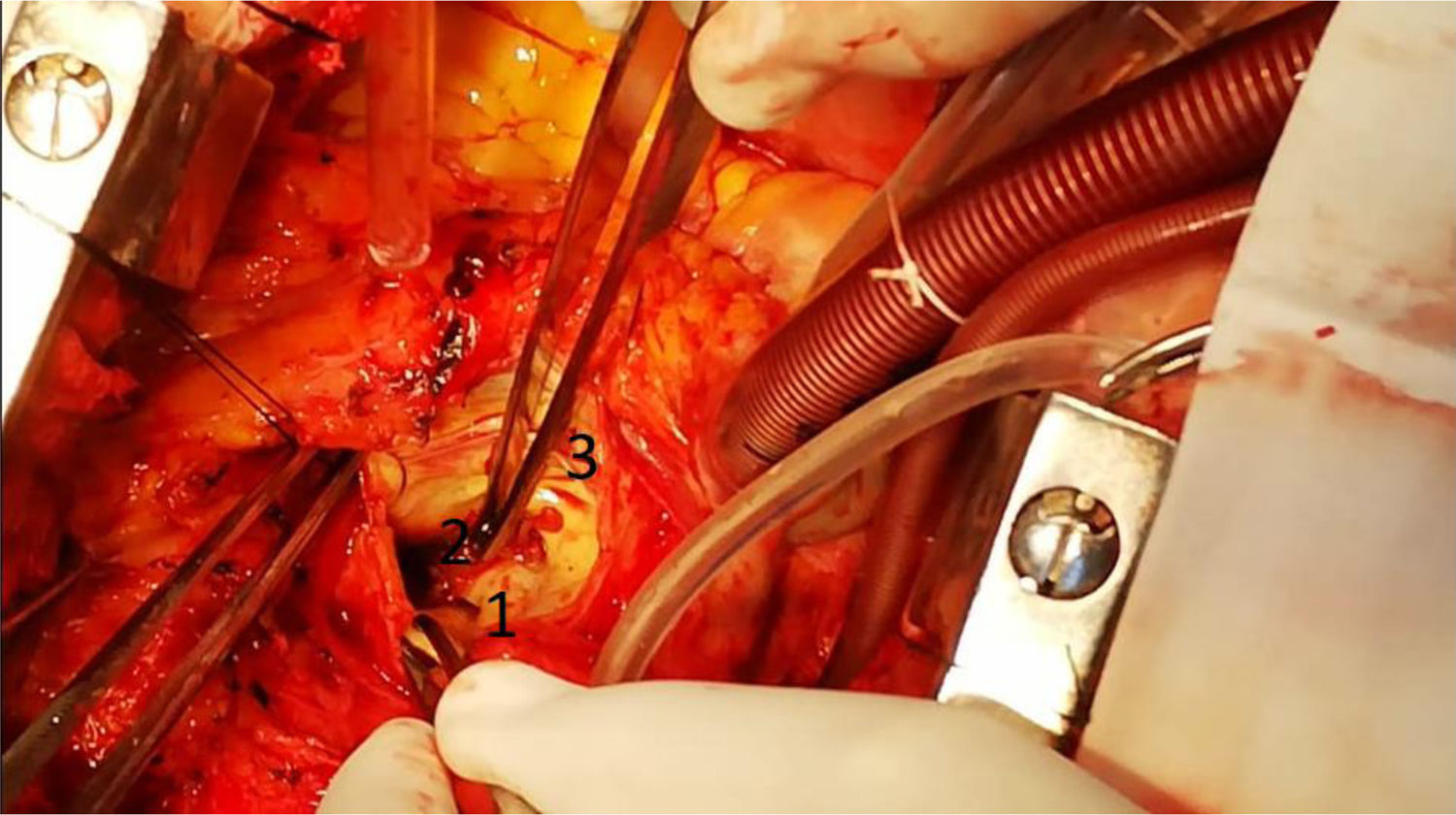
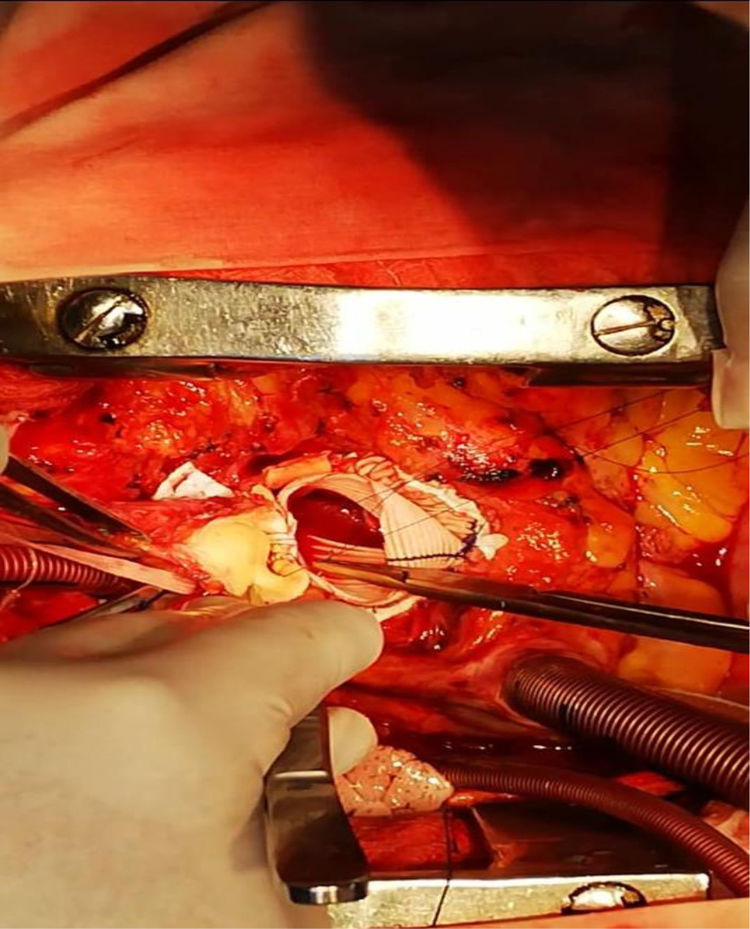
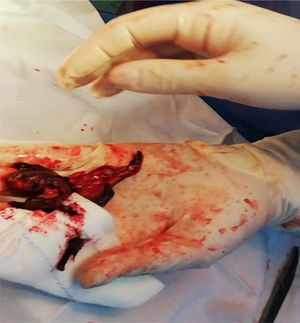
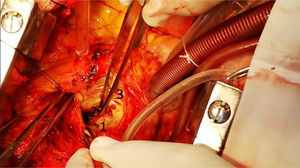
Dentro del aneurisma, retiramos un abundante hematoma sobre el ostium de la coronaria izquierda, se extrajo el hematoma (fig. 7) y se observó tejido sanioso en vía de fistulizarse hacia la aurícula izquierda (fig. 8).
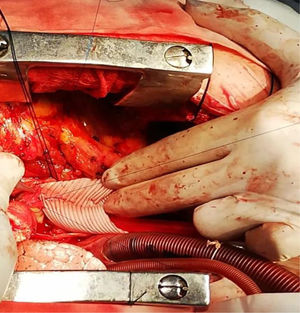
Con respecto a la coronaria izquierda, se pudo liberar del fondo del aneurisma, por lo cual se logró reimplantar sin tensión en la prótesis de Dacrón. La válvula era de aspecto sano trivalva y se colocó la prótesis de Dacrón sin afectarla, comprobando la buena funcionalidad luego de concluir la sutura en la raíz. Posteriormente, se realizó la técnica de Yacoub con preservación valvular y el reimplante coronario izquierdo, así como la exclusión del aneurisma del seno de Valsalva (ASV). El procedimiento se llevó a cabo con el tubo de Dacrón número 28. (figs. 9 y 10). El ecocardiograma intraoperatorio mostró buena competencia valvular e insuficiencia leve. El postoperatorio fue de buena evolución, la paciente fue extubada a las tres horas después de la intervención, sin sangrado significativo. Se dio el alta al séptimo día.
A los seis meses, la paciente se encontraba asintomática para ángor y disnea, y se realizó un control con angiotomografía donde se observó la aorta y los senos de Valsalva con adecuada morfología, sin signos de fuga ni aneurisma (fig. 11).
ComentariosEl ASV es una dilatación anormal de la raíz aórtica ubicada entre el anillo de la válvula aórtica y la unión sinotubular. Esto ocurre como consecuencia de la debilidad de la lámina elástica de la capa media de la aorta. La función de los senos normales es evitar la oclusión de los ostium de las arterias coronarias durante la sístole cuando se abre la válvula aórtica. El diámetro del seno normal es inferior a 4,0 cm para los hombres y 3,6 cm para las mujeres. El ASV puede ser congénito o adquirido. Suelen estar aislados, en raras ocasiones, se describen aneurismas de dos o tres senos de Valsalva1. La ruptura del ASV es una complicación potencialmente fatal.
EtiologíaEl ASV puede ser congénito o adquirido (degenerativo, inflamatorio no infeccioso e infeccioso, traumático e iatrogénico.) El ASV congénito posee algunas alteraciones genéticas que incluyen la mutación de la fibrilina que causa el síndrome de Marfan, permitiendo el debilitamiento de las fibras elásticas, mutaciones de los receptores de los factores de crecimiento transformante beta (TGFβ), causando el síndrome de Loeys-Dietz, relacionado con alteraciones en la elastina y colágeno. También se ha vinculado el síndrome de Ehlers-Danlos con un trastorno en la síntesis del colágeno tipo III que lleva a fragilidad vascular.
Las formas adquiridas pueden ser degenerativas como es el debilitamiento de la pared vascular por desaparición de miocitos de la túnica media y síntesis insuficiente de componentes de la matriz extracelular. Esto ocurre, principalmente, en el contexto de isquemia de la pared vascular en el caso de trombosis de la vasa vasorum y engrosamiento de la pared como en la formación de placas ateromatosas. La hipertensión arterial se relaciona con estenosis de las arteriolas que suministran sangre a la vasa vasorum, lo que produce una disminución de aporte de oxígeno a la pared vascular que conduce al debilitamiento de la misma, culminando en la formación de aneurisma.
Entre las formas adquiridas inflamatorias no infecciosas están las vasculitis de grandes vasos como la arteritis de células gigantes (ACG), la enfermedad de Takayasu (ET), el síndrome IgG4, la policondritis recurrente y el síndrome de Cogan. Se describe en frecuencia muy inferior en patologías como espondiloartropatías, Behcet, artritis reumatoide, lupus (LES) y casos aislados en sarcoidosis, granulomatosis con poliangeitis (PG, antiguo Wegener), poliarteritis nodosa2 y en el síndrome antifosfolípido.
Las etiologías infecciosas se han relacionado con: a) propagación de procesos infecciosos contiguos; b) embolización séptica en casos de infecciones severas por hongos o en casos de endocarditis infecciosa y c) infección directa de la pared vascular por microorganismos que se conducen en el torrente sanguíneo como en la sífilis que causa endarteritis obliterante en la etapa terciaria de la enfermedad. Se asocian con otras cardiopatías: comunicación interventricular (CIV) en 30 a 60% y anomalías de la válvula aórtica, tales como la insuficiencia aórtica (RA) (20 a 30%), válvula bicúspide (10%), estenosis aórtica (6,5%), así como estenosis pulmonar (9,7%), coartación (6,5%), persistencia de conducto arterioso (3,2%), insuficiencia tricúspidea (3,2%) y defecto interatrial.
EpidemiologíaLa tasa estimada de ASV es de aproximadamente el 0,09% de la población general, tomando como base las grandes series de autopsias. Los ASV comprenden hasta el 3,5% de todos los defectos cardiacos congénitos. La rotura puede ser espontánea, después de trauma, de ejercicio físico extremo o de endocarditis. La frecuencia de rotura del ASV varía según su localización: 60% en el seno derecho, 42% en el no coronario y 10% en el seno izquierdo y ocurren principalmente al ventrículo derecho (60%), aurícula derecha (29%), atrio izquierdo (6%), ventrículo izquierdo (4%) o pericardio (1%). La rotura extracardiaca es rara, comúnmente fatal, ocurre hacia el pericardio o al espacio pleural y es más frecuente en los ASV adquiridos. Los hombres tienen cuatro veces más probabilidades de verse afectados que las mujeres. Hay mayor incidencia en grupos asiáticos3.
FisiopatologíaLa historia natural es evolutiva. Primero, el aneurisma protruye sin causar alteración alguna, el prolapso avanza, crece y, aún sin rotura, puede ocasionar obstrucción por su tamaño, tanto en el tracto de salida del ventrículo derecho (VD), de entrada o por compresión coronaria. Eventualmente, la rotura ocurre y da como resultado, casi siempre, un cortocircuito de izquierda a derecha cuya magnitud dependerá del área de rotura; cuando es muy grande, la sobrecarga aguda puede conducir a la insuficiencia cardiaca y, en ocasiones, a la muerte.
ClínicaLos pacientes que tienen ASV pueden estar completamente asintomáticos o bien presentar síntomas no específicos, como disnea, dolor en el pecho, palpitaciones o pérdida del conocimiento. Los hallazgos del examen físico, generalmente, no están presentes, a menos que el aneurisma sea grande o se haya roto. La exploración física de los enfermos con ASV roto típicamente revela un soplo continuo en el mesocardio; sin embargo, puede auscultarse solo un soplo sistólico o un soplo sistólico combinado con un soplo diastólico. Los ASV no rotos, normalmente, no provocan soplo alguno. Se han descrito casos de compresión de la arteria coronaria que provoca un infarto del miocardio, en ocasiones, fatal. El ASV también se ha caracterizado como asiento de endocarditis infecciosa.
EvaluaciónLa tomografía computarizada cardiaca es la prueba de elección para cuantificar el tamaño y la morfología del ASV. La ecocardiografía, generalmente transesofágica, demostrará el flujo y el significado hemodinámico, tiene una certeza diagnóstica de 75 y 90%, respectivamente, para los ASV rotos y no rotos, permite discriminar el tamaño, seno de origen, punto de terminación, gravedad, mecanismo de la insuficiencia valvular, presencia de anormalidades cardiacas o vasculares asociadas, así como la orientación de la conducta quirúrgica. La resonancia magnética cardiaca demostrará también la anatomía y la importancia hemodinámica. Los pacientes se someterán a una angiografía coronaria antes de la cirugía para evaluar la anatomía coronaria. Aquellos con bajo riesgo de enfermedad coronaria pueden tener una evaluación de la anatomía coronaria mediante tomografía computarizada cardiaca. Los pacientes con riesgo intermedio o alto de enfermedad coronaria generalmente se someterán a un cateterismo cardiaco para evaluar el posible injerto de derivación en el momento de la cirugía. La única clasificación formal para los ASV es la propuesta por Sakakibara y Konno en 19624, que consiste en cuatro tipos, según el seno coronario afectado y la zona en la que protruyen o se rompen (tabla 1).
Clasificación para los aneurismas del seno de Valsalva propuesta por Sakakibara y Konno (año 1962)
| Tipo I. Conecta el seno de la Valsalva derecho y el tracto de salida del ventrículo derecho debajo de la válvula pulmonar. |
| Tipo II. Conecta el seno de Valsalva derecho y el ventrículo derecho en la crista supraventricularis. |
| Tipo IIIa. Conecta el seno de Valsalva derecho y la aurícula derecha. |
| Tipo IIIv. Conecta la zona posterior del seno de Valsalva derecho y el ventrículo derecho. |
| Tipo III a+v. Conecta el seno de Valsalva derecho y ambos, aurícula derecha y ventrículo derecho. |
| Tipo IV. Conecta el seno de Valsalva no coronario y la aurícula derecha. |
El tratamiento médico de la ruptura es insuficiente para la terapia definitiva; debe servir de puente para ayudar a estabilizar temporalmente a los pacientes hasta que esté disponible una terapia quirúrgica. El tratamiento médico implica abordar las arritmias, según sea necesario, así como la endocarditis y la insuficiencia cardiaca si están presentes. Los pacientes con ASV roto suelen sucumbir a su estado de enfermedad dentro del año de diagnóstico, debido a insuficiencia cardiaca congestiva en el contexto de derivación de izquierda a derecha. La corrección puede realizarse mediante aortotomía, desde el interior de la estructura involucrada o ambas. Este abordaje combinado es el más efectivo y el más usado porque permite la resección intracardiaca del aneurisma, el cierre del defecto septal ventricular y la reparación de la válvula aórtica, si es necesario. Los ASV no rotos que producen arritmias malignas, infección, obstrucción de arterias coronarias o de tractos de salida ventriculares tienen indicación quirúrgica. La velocidad de progresión del aneurisma es un factor para considerar en la decisión. Por lo tanto, la presencia de un ASV no roto, aun si es asintomático o detectado casualmente, es una indicación de intervención quirúrgica en la mayoría de los casos. En los últimos años, ha surgido como nueva alternativa el cierre percutáneo, con múltiples informes de casos individuales o series de casos con buenos resultados a corto y mediano plazo. Se prefiere el tratamiento quirúrgico cuando existe una RA significativa o una CIV. La cirugía sigue siendo el método preferido de tratamiento del ASV roto. La ruptura obliga a una evaluación quirúrgica urgente, ya que los pacientes pueden deteriorarse rápidamente.
Existen varias técnicas para intervenir el ASV, dependiendo de las estructuras involucradas. Además del cierre del aneurisma, lo que se trata es de la preservación valvular. Se ha descrito la realización de técnicas de David5 y Yacoub, y también en casos de compromiso valvular grave se han realizado las técnicas de Bentall de Bono o Cabrol. En las guías de la Sociedad Europea de Cardiología del 20146, las indicaciones para la cirugía se basan principalmente en el diámetro aórtico y se extraen de los hallazgos hechos en la historia natural al sopesar el riesgo de complicaciones frente al de la cirugía electiva. La cirugía está recomendada para pacientes con síndrome de Marfan y diámetro aórtico máximo ≥ 50 mm. Para personas con otros factores de riesgo, como antecedente familiar de disección, crecimiento > 3 mm/año (en varios exámenes, utilizando la misma técnica y con confirmación en otra), regurgitación aórtica grave o intención de gestar, se acepta un umbral más bajo de 45 mm. Los sujetos con manifestaciones marfanoides por enfermedad del tejido conectivo, sin criterios de Marfan completos, han de ser tratados como pacientes con Marfan.
Se proponen intervenciones precoces para diámetros aórticos > 42 mm en pacientes con síndrome de Loeys-Dietz. Aquellos con síndrome de Ehlers-Danlos se exponen a un riesgo alto de sufrir complicaciones aórticas, aunque ningún dato disponible indica un umbral específico para realizar una intervención. Los pacientes con válvula aórtica bicúspide (VAB) y diámetro aórtico máximo ≥ 55 mm deben someterse a cirugía. Estos individuos corren menos riesgo de sufrir complicaciones que los pacientes con Marfan. Puede aceptarse un umbral más bajo, de 50 mm, para personas con otros factores de riesgo, como antecedente familiar, hipertensión sistémica, coartación de aorta o aumento del diámetro aórtico > 3 mm/año, y también en función de la edad, el peso corporal, las comorbilidades y el tipo de cirugía. Con independencia de la etiología, los pacientes con diámetros aórticos máximos ≥ 55 mm han de ser intervenidos quirúrgicamente. En sujetos con un tamaño corporal pequeño, en especial aquellos con síndrome de Turner, ha de tenerse en cuenta un diámetro aórtico indexado de 27,5 mm/m2 de superficie corporal. También, se pueden considerar umbrales más bajos de los diámetros aórticos en pacientes de riesgo bajo, siempre y cuando la reparación de la válvula se lleve a cabo en un centro experimentado. Para personas con indicación de cirugía de válvula aórtica, se pueden emplear umbrales más bajos para sustituciones aórticas concomitantes (> 45 mm) en función de la edad, el tamaño corporal, la etiología de la enfermedad valvular, la forma intraoperatoria y el grosor de la aorta ascendente. Las indicaciones quirúrgicas para la enfermedad de válvula aórtica se abordan en detalle en guías específicas. La elección entre sustitución total de la aorta ascendente, incluida la raíz aórtica, mediante reimplante coronario y sustitución segmentaria de la aorta por encima de la unión sinotubular depende de los diámetros en diferentes localizaciones de la aorta, sobre todo en los senos de Valsalva. En caso de sustitución total, la opción entre la intervención de preservación valvular y un injerto compuesto acompañado de prótesis valvular depende del análisis tanto de la función como de la anatomía de la válvula aórtica, el tamaño y la localización del aneurisma de aorta torácico (AAT), la esperanza de vida, el estado de anticoagulación deseado y la experiencia del propio equipo quirúrgico.
Recomendación 2014 de la Sociedad Europea de CardiologíaLa mortalidad quirúrgica varía de 1,9 a 3,6%. Las tasas de supervivencia son cercanas al 90% después de 15 años. Uno de los artículos donde se observa mucha experiencia es el de Yan et al. donde identificaron un total de 160 pacientes con edad media de (30 ± 12) años y 112 (70%) de ellos masculinos. El origen del SVA del seno coronario derecho se encontró en 108 pacientes (67,5%), el seno no coronario en 51 (31,9%), y el seno coronario izquierdo en uno (0,6%). La rotura de SVA hacia el ventrículo derecho se identificó en 89 (55,6%) casos, la aurícula derecha en 61 (38,1%), la ventrículo izquierdo en dos (1,3%) y sin rotura en ocho (5,0%). Se encontró CIV y RA en 59 (37%) y 45 (28%) pacientes, respectivamente. Se realizó un reemplazo de válvula aórtica (AVR) en 23/45 (51%) y valvuloplastia aórtica (AVP) en 9/45 (20%) personas. Tuvieron tres muertes hospitalarias (1,9%) y dos fallecimientos tardíos. El 84% de los sujetos fueron seguidos durante (17,6 ± 4,2) años. La supervivencia actuarial fue del 94% a los 10 años y 88% a los 20 años7.
ConclusiónPresentamos un caso muy poco frecuente de aneurisma de seno coronario izquierdo, complejo dada la patología en sí y por ser una reoperación cardiaca. Aunque el abordaje quirúrgico óptimo sigue siendo controvertido, la competencia a largo plazo de la válvula aórtica parece seguir siendo la principal preocupación de los aneurismas de seno de Valsalva. La técnica debe adaptarse a cada paciente.
Conflicto de interesesEl autor declara no tener ningún conflicto de intereses.