En los últimos años, la técnica de implante TAVI empleando la proyección overlapping-cusp o proyección de superposición de cúspides (POC) se ha postulado como una nueva alternativa para el implante más alto de las bioprótesis autoexpandibles.
El objetivo de la presente revisión consiste en describir la técnica POC y analizar la experiencia actual reportada de forma comparativa con la técnica coplanar.
Los procedimientos TAVI con bioprótesis autoexpandibles mediante la técnica de POC se han mostrado seguros y se han asociado con un mejor alineamiento comisural y una profundidad de implantación protésica más alta en comparación con la técnica estándar, lo que conlleva menores tasas de trastornos de conducción e implante de marcapasos permanente. No obstante, esta técnica se ha asociado a mayores dosis de radiación durante el procedimiento.
In recent years, TAVI using the cusp overlap projection, or cups-overlap technique (POC), has been postulated as a new alternative for the higher implantation of self-expanding bioprostheses.
The aim of this review is to describe the POC technique and to analyze the reported experience in comparison with the coplanar or standard technique.
TAVI procedures with self-expanding bioprostheses using the POC technique have been shown to be safe and have been associated with better commissural alignment and a higher prosthetic implantation depth, which leads to lower rates of conduction disorders and permanent pacemaker implantation. However, this technique has been associated with higher radiation doses during the procedure.
En la actualidad, el implante de válvula aórtica transcatéter (TAVI) constituye una opción terapéutica de la valvulopatía aórtica severa en pacientes con riesgo quirúrgico bajo, tal y como indican las guías clínicas europeas y americanas de diagnóstico y tratamiento de valvulopatías1,2. Si bien los resultados del tratamiento TAVI han mejorado progresivamente a lo largo de las dos últimas décadas, la aparición de bloqueo de rama izquierda (BRI) completo persistente y la tasa de implante de marcapasos permanente (IMP) continúan siendo complicaciones frecuentes tras TAVI, situándose entre el 10-39% y el 6-32%, respectivamente3. Tanto el BRI persistente de nueva aparición como el IMP tras TAVI se asocian con un mayor riesgo de mortalidad por todas las causas y de hospitalización por insuficiencia cardiaca en el primer año de seguimiento4. Además, el BRI también se asocia con un aumento del riesgo de muerte cardiaca, así como con la necesidad de IMP en el primer año de seguimiento4. Aunque carecemos de estudios a largo plazo, el potencial impacto clínico de este tipo de complicaciones en pacientes con una expectativa de vida larga tras TAVI supone un importante aliciente para buscar estrategias que disminuyan la incidencia de trastornos de conducción tras el TAVI. Se han identificado diversos predictores de riesgo asociados al paciente o al procedimiento en relación con la aparición tanto de BRI persistente como de necesidad de IMP. Entre ellos, destacan la existencia preoperatoria de bloqueo de rama derecha, bloqueo auriculoventricular, calcificación del tracto de salida del ventrículo izquierdo, septo membranoso corto; y como factores modificables: sobredimensión protésica, implante bajo de bioprótesis y el tipo prótesis empleado5,6. En este sentido, se ha reportado que la disminución del ratio entre el tamaño de la prótesis y el anillo valvular aórtico, para evitar la sobredimensión protésica, podría aumentar la incidencia de fuga paravalvular7, por lo que la mejor opción para reducir el riesgo de BRI e IMP sería el implante más alto de las bioprótesis valvulares aórticas transcatéter.
En relación con las proyecciones radiológicas empleadas en el procedimiento TAVI, mediante la proyección tricúspide coplanar estándar (PTCE) se logran buenos posicionamientos de las prótesis balón-expandibles: la prótesis transcatéter se centra longitudinalmente a nivel del plano anular y se libera en el plano perpendicular al anillo aórtico. En contraposición, la liberación de las prótesis autoexpandibles se produce de forma asimétrica desde la cúspide no coronaria (CNC) hacia la cúspide coronaria izquierda (CCI)8. Por tanto, es muy complicado lograr una liberación precisa que ajuste distancias de 2-3mm de profundidad de implante protésico sin aumentar considerablemente el riesgo de migración de la prótesis.
En los últimos años, la técnica de implante TAVI empleando la proyección overlapping-cusp o proyección de superposición de cúspides (POC) se ha postulado como una nueva alternativa para el implante más alto de las bioprótesis autoexpandibles.
El objetivo de la presente revisión consiste en describir la técnica POC y analizar la experiencia actual reportada de forma comparativa con la técnica PTCE.
Proyecciones radiológicas para TAVI: PTCE y POCLa fluoroscopia continua representa el gold standard para el control por imagen de la liberación de prótesis mediante TAVI, siendo la proyección estándar tricúspide coplanar (PTCE) la técnica tradicionalmente empleada y que ha mostrado muy buenos resultados fundamentalmente con prótesis balón-expandibles9. En la PTCE, la cúspide coronaria derecha (SCD) se sitúa en medio del plano valvular, entre la CCI y la cúspide coronaria derecha (CCD) (fig. 1). El correcto alineamiento de las tres cúspides en el mismo plano se considera un aspecto crucial para lograr precisión en el posicionamiento de la bioprótesis en relación con las estructuras circundantes, fundamentalmente en las prótesis autoexpandibles8,10. En raíces aórticas cuya morfología presenta un trayecto más horizontal puede resultar más complicado lograr dicho alineamiento. En este sentido, además del estudio complementario mediante tomografía computarizada multicorte (TCMC) para optimizar las proyecciones radiológicas, resulta muy útil el uso de la técnica follow the right cusp rule, descrita por Kasel et al.11.
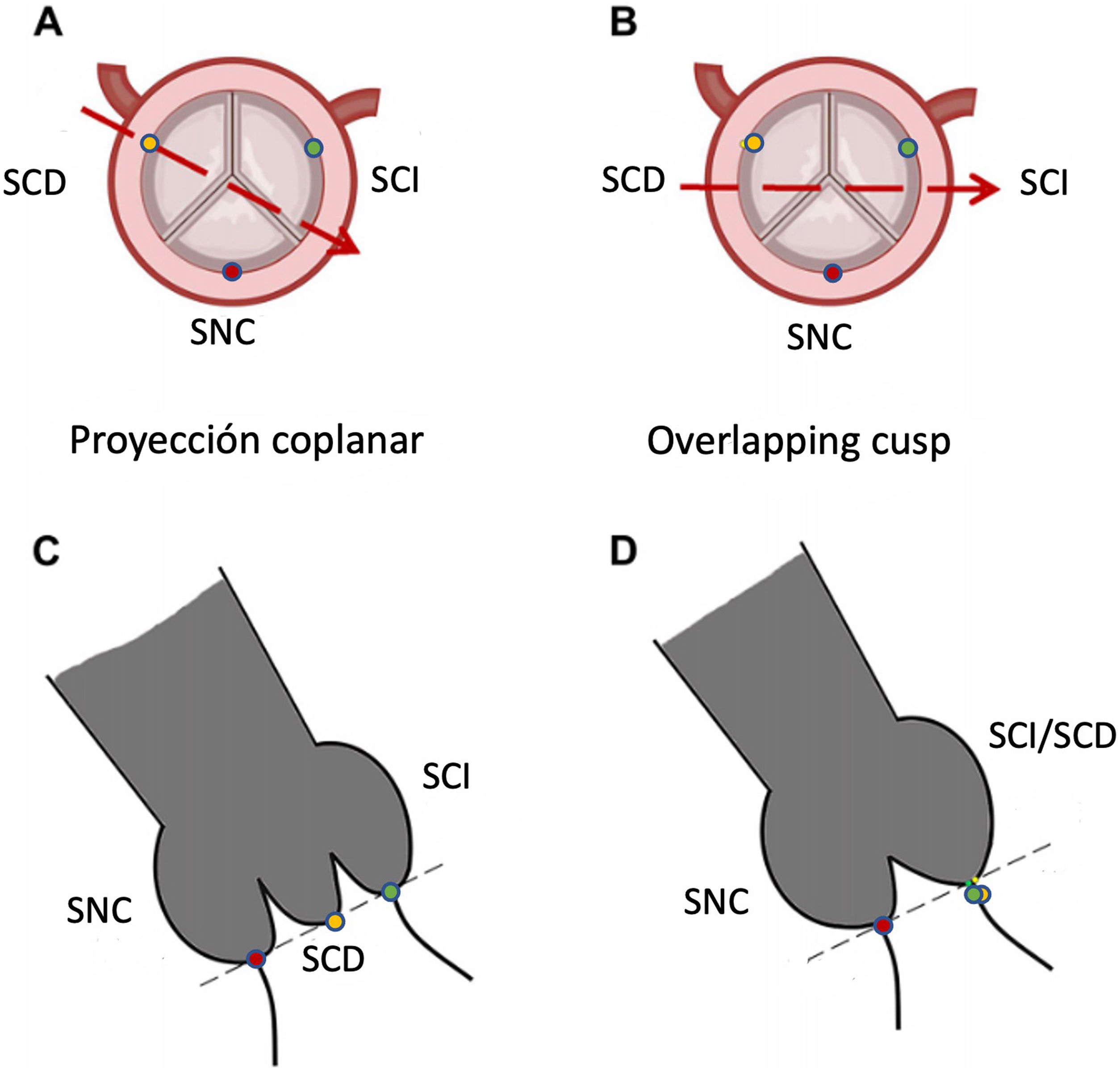
Esquema de la proyección de superposición de cúspides (POC) y de la proyección estándar tricúspide coplanar (PTCE). A,B)Representación en el eje transversal de la visión fluoroscópica (línea discontinua roja) en ambas proyecciones. C,D)Visión esquemática de la proyección fluoroscópica de la POC y la PTCE.
SCD (punto amarillo): cúspide seno coronario derecho; SCI (punto verde): cúspide seno coronario izquierdo; SNC (punto rojo): cúspide seno no coronario.
Modificado de Chen et al.10, Creative Commons Atribution License (CC BY).
La proyección overlapping-cusp o proyección de superposición de cúspides (POC) en implante TAVI fue presentada por primera vez en 201612. En 2018, Tang et al. reportan sus resultados con la POC para el implante TAVI con prótesis expandible Core Valve /Evolut THV system8,10. Se trata de una proyección radiológica en la cual la CCD se sitúa en superposición con la CCI (figs. 1 y 2). Durante el implante de las prótesis autoexplandibles, debido a que su longitud es mayor que las balón-expandibles, se produce una liberación de forma asimétrica desde la CNC hacia la cúspide coronaria izquierda (CCI)8,10. De forma comparativa con la PTCE, la proyección POC logra ofrecer diferentes ventajas. En primer lugar, el uso de una proyección caudal/craneal elimina el error de paralaje del catéter. Además, el catéter se posiciona de forma natural hacia la curvatura mayor de la raíz aórtica y, por tanto, se presenta más centrado a través de la válvula aórtica. La proyección POC consigue una liberación de la prótesis transcatéter en una visión verdaderamente coplanar, eliminando por tanto el error de paralaje del sistema de liberación a través de la válvula. La visión que ofrece la POC de la CNC permite una gran precisión en el alineamiento protésico así como en la profundidad de implante de la bioprótesis, evitando el riesgo de implantes muy bajos o de migración protésica (pop-out)14,15. De forma más precisa, el procedimiento TAVI con prótesis autoexpandible con POC permite un implante más elevado del dispositivo de forma estadísticamente significativa (diferencia media estandarizada=−0,324, IC95%: −0,469 a −0,180)10. Recientemente, el grupo de Pascual et al.6 reportó un implante más alto de la prótesis autoexpandible, asociado con menores alteraciones de la conducción e IMP, con el empleo de la técnica de implante mediante POC. Se trata de un estudio con un buen diseño para la evaluación cuidadosa de la profundidad de implante de las bioprótesis transcatéter, puesto que no existe un criterio uniforme en la literatura. La profundidad de implante medida desde la CNC hasta la prótesis fue estadísticamente menor con el uso de la técnica POC en comparación con la PTCE (4,77 ±2,22mm vs 5,71±3,07mm, respectivamente, p=0,011). En las mediciones de borde más profundo (la mayor distancia desde la CNC o desde la CCI hasta la prótesis) o la media aritmética desde CCI y CNC, se muestra una tendencia a menor profundidad de implante con la técnica POC frente a la PTCE, si bien no se alcanzó diferencia estadísticamente significativa6.
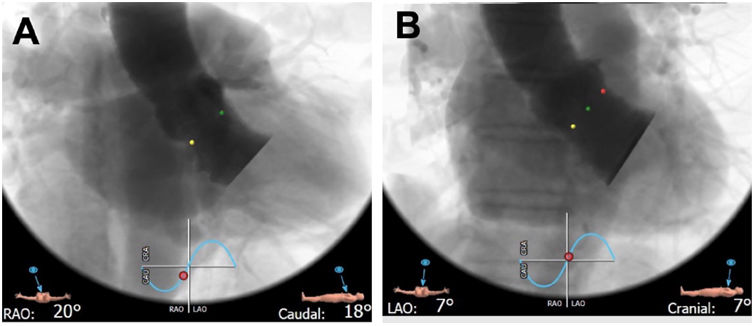
A)Proyección radiológica de superposición de cúspides (POC). B)Proyección radiológica estándar tricúspide coplanar (PTCE). Cúspide coronaria derecha (punto rojo), cúspide coronaria izquierda (punto rojo) y cúspide no coronaria (punto amarillo). En la proyección POC se superponen la cúspide coronaria derecha e izquierda y se aísla la cúspide coronaria derecha, contribuyendo a la eliminación del error de paralaje del dispositivo y a la elongación del tracto de salida del ventrículo izquierdo.
Modificado de Maier et al.13, Creative Commons Atribution License (CC BY).
A pesar de los avances tecnológicos en el diseño y la liberación de las prótesis valvulares aórticas transcatéter, los trastornos de ritmo cardíaco y de implante de marcapasos permanente (IMP) tras TAVI constituyen un problema muy relevante, fundamentalmente en el caso de las prótesis autoexpandibles. En el estudio Evolut Low Risk Trial, la incidencia de IMP a 30días tras implante de prótesis autoexpandible fue del 17,4%, frente a la incidencia del 6,6% de IMP a 30días tras TAVI con prótesis balón-expandible, reportada en el estudio PARTNER39,16.
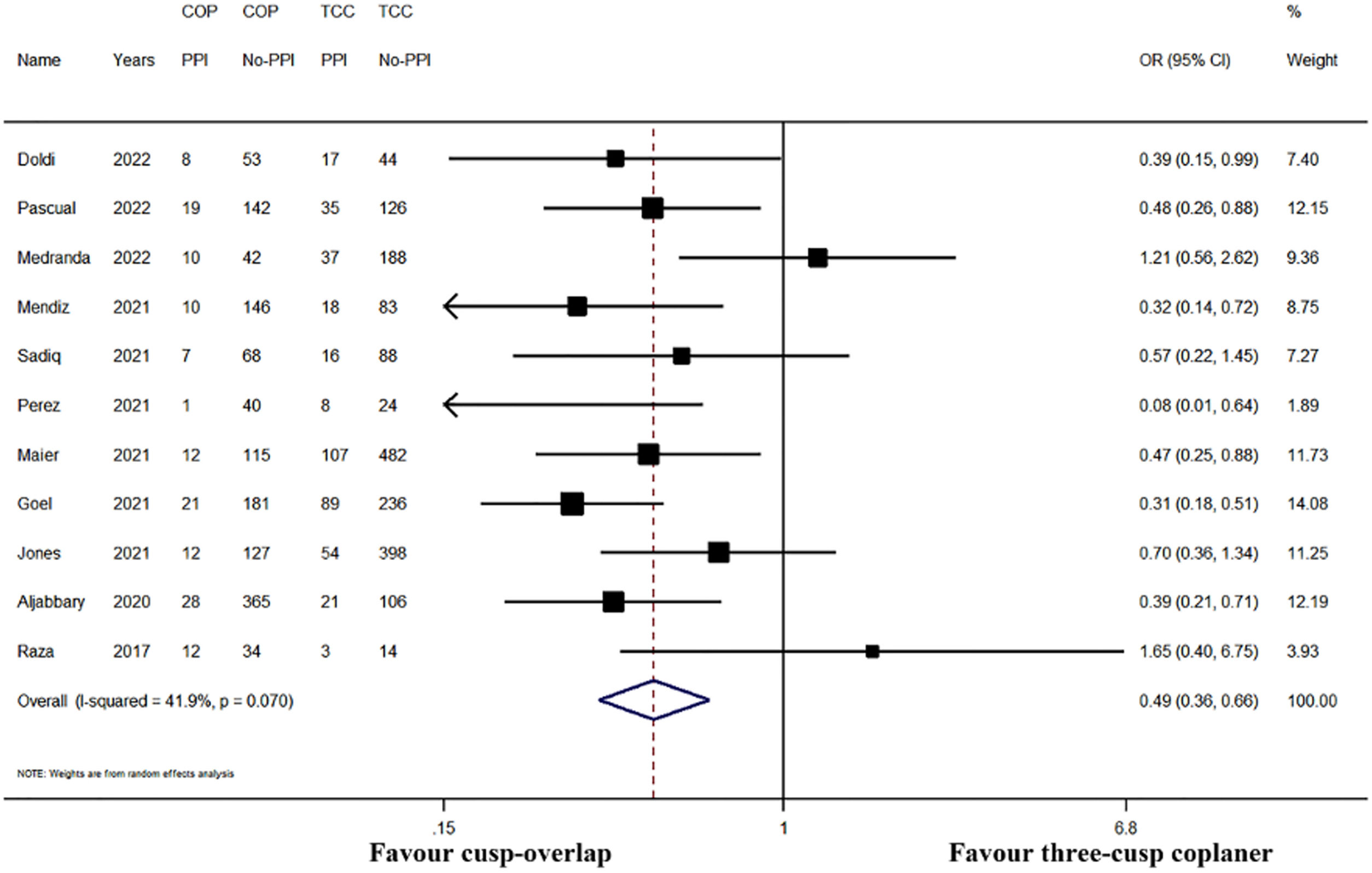
En un reciente metaanálisis reportado por Chen et al.10 se observó que la POC redujo de forma estadísticamente significativa un 45% el riesgo de IMP postoperatorio en comparación con la técnica estándar PTCE (RR: 0,544, IC95%: 0,418-0,718, p<0,001). En la figura 3 se muestran los resultados de los 11 estudios analizados en el metaanálisis en relación con la tasa de IMP tras TAVI mediante técnica POC con prótesis autoexpandible10.
Metaanálisis sobre la tasa de implante de marcapasos permanente (PPI). CI, intervalo de confianza.
COP: proyección overlapping-cusp; OR: odds ratio; TCC: proyección tres cúspides coplanar.
Las barras representan el intervalo de confianza al 95%.
Modificado de Cheng et al.10, Creative Commons Atribution License (CC BY).
Debido a la mayor longitud de las bioprótesis autoexpandibles, durante su proceso de liberación contactan en primer lugar a nivel de la cúspide del SNC del plano anular, por lo que esta cúspide actúa como punto de apoyo. Desde este punto, el despliegue de la prótesis progresa hacia la curvatura mayor de la raíz aórtica y finalmente la prótesis contacta con la CCI10. El tejido del sistema de conducción y el septo membranoso se localizan bajo los senos no coronario y coronario derecho, por lo que la proyección POC aporta una correcta visualización para aumentar la precisión del despliegue de la prótesis. Además, el tracto de salida del ventrículo izquierdo se despliega mediante la proyección COP, contribuyendo a la precisión de la profundidad de despliegue (fig. 2A).
POC y alineamiento comisuralA diferencia del implante quirúrgico de las bioprótesis valvulares aórticas en las que se alinean las comisuras nativas y protésicas, las bioprótesis transcatéter se han implantado durante muchos años sin tener en cuenta su orientación. El alineamiento comisural entre las comisuras nativas y protésicas se define en base a cuatro categorías: alineadas (ángulo de desviación entre las neocomisuras protésicas y comisuras nativas 0° a 15°), mal alineamiento leve (ángulo de desviación de 15° a 30°), moderado (ángulo de desviación de 30° a 45°) o severo (ángulo de desviación de 45° a 60°)17. Un mal alineamiento moderado o severo podría suponer la superposición de las neocomisuras protésicas con los ostia coronarios17,18. Esta situación aumenta el riesgo de complicaciones en pacientes jóvenes que con posterioridad precisen intervenciones coronarias percutáneas o reintervenciones TAVI (valve in valve). Asimismo, un mal alineamiento severo podría aumentar el riego de fuga periprotésica así como una sobrecarga de estrés a los velos protésicos19. Por lo tanto, mejorando el alineamiento comisural en el procedimiento TAVI se facilitaría el eventual acceso a las arterias coronarias así como procedimientos TAVI futuros y, por otra parte, se favorecería una mejor hemodinámica y mayor durabilidad de las bioprótesis17-19.
En el estudio COMALING de Bieliauskas et al.18 se evaluó el impacto del uso de la técnica POC en 60 pacientes sometidos a procedimientos TAVI con las prótesis autoexpandibles Evolut R/PRO (Medtronic), ACURATE neo2 THV (Boston Scientific) y Portico THV (Abbott). En este estudio se obtuvo una alineación comisural óptima o mal alineamiento leve (<30°) en 53 pacientes (88%) utilizando la técnica de implantación de TAVI con POC. Por tanto, en la actualidad la técnica de superposición de cúspides se postula como la alternativa ideal para lograr la alineación comisural en TAVI con prótesis autoexpandibles. No obstante, es necesario validar en estudios más amplios la seguridad y la aplicabilidad a gran escala del movimiento de torque o torsión activa del catéter de liberación para intentar optimizar el alineamiento comisural en el anillo aórtico durante el despliegue de las prótesis transcatéter. Bieliauskas et al.18 sugieren que un sistema de liberación más flexible, como Acurate neo2 y Portico, podrían ser más susceptibles a la rotación en el anillo en comparación con el sistema Evolut, más rígido. Sin duda, los futuros diseños de sistemas de liberación de prótesis autoexpandibles favorecerán el alineamiento comisural (fig. 4)15.
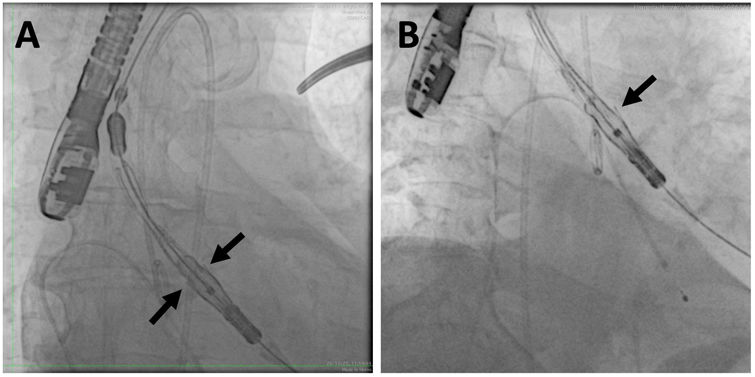
Imágenes de fluoroscopia durante el procedimiento TAVI con prótesis autoexpandible Acurate neo2 (Boston Scientific), que presenta un diseño específico para lograr el alineamiento comisural mediante la orientación de las marcas protésicas en dos proyecciones diferentes. A)Protección tricúspide coplanar estándar (PTCE): la bioprótesis se rota hasta observar dos marcas simétricas (flechas negras). B)Proyección overlapping-cusp: se observa una marca a nivel de la curvatura menor (flecha negra).
Dado que la proyección POC permite una mejor precisión en implantes más altos de TAVI con prótesis autoexpandibles, se puede plantear la posibilidad de que conllevaría un potencial aumento del riesgo de migración protésica (pop-out), fuga periprotésica, necesidad de implante de un segundo dispositivo o incremento adicional del riesgo periprocedimiento. En un metaanálisis sobre TAVI con prótesis autoexpandible con la técnica POC reportado por Chen et al.10, el riesgo de fuga periprotésica, la necesidad de implante de un segundo dispositivo, la aparición de bloqueo de rama izquierda, el tiempo de fluoroscopia y los eventos clínicos (mortalidad y eventos neurológicos) fueron similares a los del grupo TAVI con técnica estándar PTCE. En este metaanálisis, en 2 pacientes del total de 363 se produjo migración de la prótesis con la técnica POC frente a 3 pacientes del total de 279 procedimientos TAVI con técnica estándar PTCE (OR: 0,602, IC95%: 0,113-3,206, p=0,584). No obstante, el grupo de Maier et al.20 reporta que el procedimiento TAVI con prótesis autoexpandible con POC se asocia a tasas superiores de reposicionamiento valvular comparado con la técnica estándar (57,8% vs. 16,2%, p<0,001). En este sentido, en el metaanálisis de Chen et al.10 se mostró que la dosis de radiación fue superior en el grupo TAVI con POC frente a la técnica estándar (diferencia media estandarizada=0,394, IC95%: 0,296-0,572, p<0,001). El incremento de dosis de radiación para la obtención de la POC posiblemente esté relacionado con la propia curva de aprendizaje de la POC o con la posibilidad de realizar un ajuste más preciso con esta proyección.
POC: limitacionesExisten varias potenciales desventajas asociadas con el implante TAVI mediante la técnica POC. El implante más elevado de las prótesis transcatéter podría provocar una tasa más alta de migración protésica o pop-out. Sin embargo, este fenómeno no se ha corroborado en las series publicadas hasta ahora. En términos prácticos, la técnica POC ofrece una visión más exacta de la profundidad real de la prótesis en relación con la CNC. Se sugiere una profundidad de implantación de 3-5mm en relación con la CNC. Esta profundidad de implante también proporciona protección frente al potencial acortamiento de la bioprótesis durante la posdilatación, cuando es necesaria21. La implantación más elevada de las prótesis autoexpandibles también podría dificultar o impedir futuros abordajes percutáneos de los ostia coronarios. Este fenómeno adquiere mayor relevancia en pacientes jóvenes que puedan desarrollar cardiopatía isquémica y precisar cateterismos coronarios. El acceso al ostium coronario se compromete debido a la proximidad del stent de la bioprótesis o bien por los propios velos aórticos calcificados impactados en la raíz aórtica. El estudio exhaustivo mediante TCMC antes del procedimiento es crucial para evitar complicaciones obstructivas a nivel de los ostia coronarios22. No obstante, el desarrollo de los nuevos dispositivos de liberación facilita la orientación valvular para tratar de lograr el alineamiento comisural (fig. 4)17.
Por otra parte, la técnica POC tiene las limitaciones inherentes de la vista fluoroscópica oblicua anterior derecha (RAO)/vista fluoroscópica caudal (CAU). De esta forma, no se evalúa correctamente la tensión sobre el catéter de liberación y su ubicación a lo largo de la curvatura interna o externa de la aorta. Por ello, existen centros que abogan por usar una combinación de dos puntos de vista simétricos para controlar más fácilmente la profundidad de implante y la tensión en el catéter antes del despliegue definitivo, ofreciendo una evaluación más completa de la posición de la prótesis a lo largo de la raíz aórtica y el anillo valvular23. Además, la vista RAO/CAU también puede disminuir la calidad de la imagen fluoroscópica en pacientes con sobrepeso. En estos casos, la vista estándar de tres cúspides o una vista oblicua anterior izquierda/craneal que superpone las cúspides derecha y no coronaria podrían ser más efectivas8.
Finalmente, debe tenerse en cuenta que el empleo de la técnica COP es relativamente reciente, por lo que para evaluar su eficacia serían necesarios nuevos estudios con mayor tamaño muestral y seguimiento.
ConclusionesLos procedimientos TAVI con bioprótesis autoexpandibles mediante la técnica POC se han mostrado seguros y se han asociado con un mejor alineamiento comisural y una profundidad de implantación protésica más alta, lo que conlleva menores tasas de trastornos de conducción e IMP. No obstante, esta técnica se ha asociado a mayores dosis de radiación durante el procedimiento, probablemente en relación con la curva de aprendizaje de la técnica.
En definitiva, la técnica POC constituye en la actualidad una buena alternativa para optimizar la profundidad de implante y el alineamiento comisural de las bioprótesis transcatéter autoexpandibles, especialmente a medida que la TAVI se expande a la población de bajo riesgo y con mayor esperanza de vida.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.