La incidencia de estenosis anastomótica tras cirugía colorrectal es variable por las diferentes definiciones que existen de ella. En la mayoría de las ocasiones son asintomáticas y en el caso de que presenten sintomatología se manifiestan como cuadro suboclusivo.
Caso clínicoPresentamos el caso de un paciente de 80 años intervenido de neoplasia de recto que, tras cierre de ileostomía, presentó cuadro suboclusivo ocasionado por estenosis de anastomosis colorrectal. Esta estenosis se trató con dilatación endoscópica, ocasionando una perforación anastomótica con neumoperitoneo, retroneumoperitoneo y neumotórax. Tras la estabilización del paciente, la perforación se manejó con medidas conservadoras que lograron resolver el cuadro de manera satisfactoria.
ConclusionesSe han descrito diversas opciones terapéuticas para el tratamiento de las estenosis anastomóticas, entre las que destacan: resección quirúrgica, empleo de dilatadores, colonoscopia dilatadora. Todas las opciones terapéuticas pueden conllevar una perforación colónica. La resolución en función de la estabilidad del paciente permitirá desde un manejo conservador, como el caso que presentamos, hasta una intervención quirúrgica.
The incidence of anastomotic stricture varies due to the different definitions given to the condition. In most cases they are asymptomatic, and if there are symptoms, they are usually those of a partial intestinal obstruction.
Case reportThe case is presented of an 80 year old patient who underwent a lower anterior resection for rectal neoplasm. After ileostomy closure, he presented with subocclusive symptoms caused by stenosis of colorectal anastomosis. This stenosis was managed with endoscopic dilations, and one of these dilations produced an anastomotic perforation with pneumoperitoneum, retropneumoperitoneum, and pneumothorax. Once the patient was clinically and haemodynamically stable, the perforation was treated with conservative measures, resolving the complication satisfactorily.
ConclusionsThe literature describes several management options for colorectal anastomoses strictures, such as surgical resection, rubber dilators, endoscopic dilation, all of which might produce colonic perforation. Its management ranges from conservative measures to surgical intervention.
La incidencia de perforaciones iatrogénicas durante la práctica de una colonoscopia varía desde el 0.016%1 descrito en las colonoscopias diagnósticas hasta el 5% en el caso de colonoscopias terapéuticas. El manejo de este tipo de perforaciones es variable y permite diferentes estrategias según el estado clínico del paciente y de las medidas de soporte disponibles en el medio, con posibilidad de optar por diversas estrategias que varían desde el tratamiento conservador hasta el abordaje quirúrgico.
Presentamos un caso clínico con perforaciones iatrogénicas, que no obstante lo aparatoso clínico-radiológico, fue posible un tratamiento conservador en un ámbito hospitalario con control intensivo durante las primeras horas.
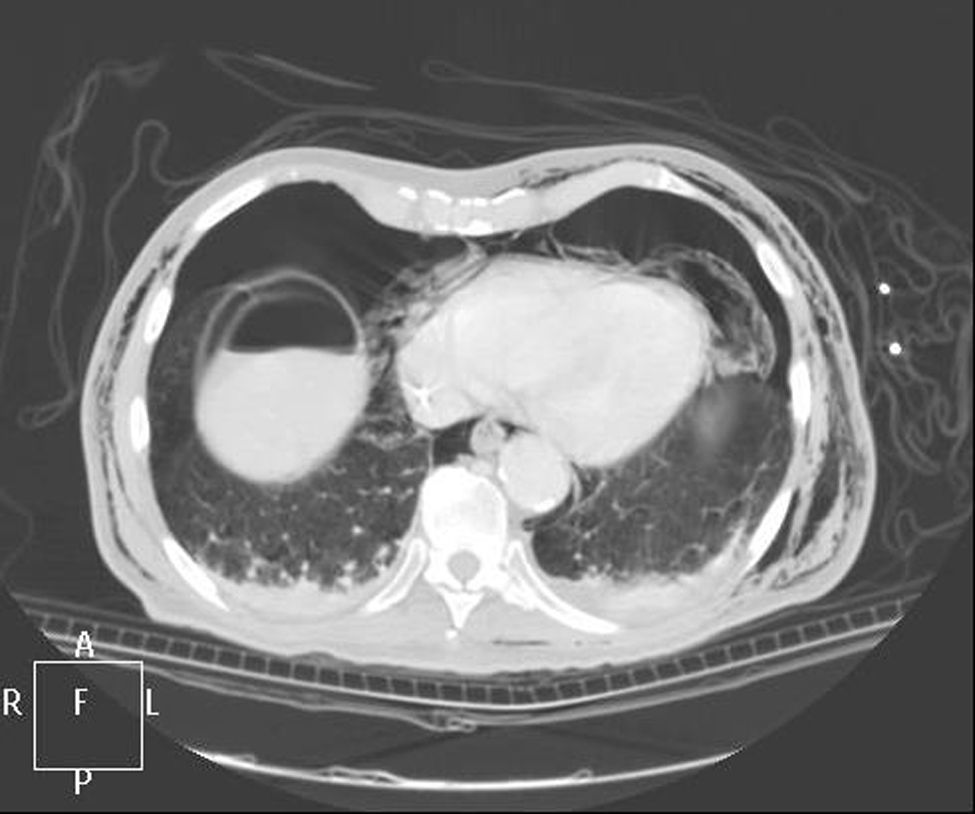
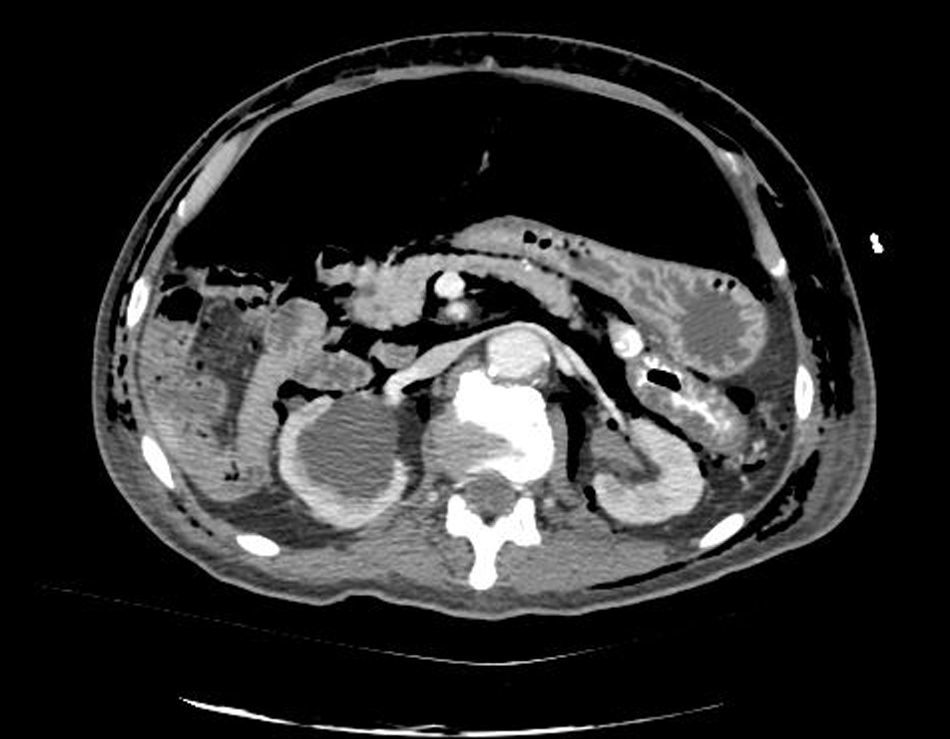
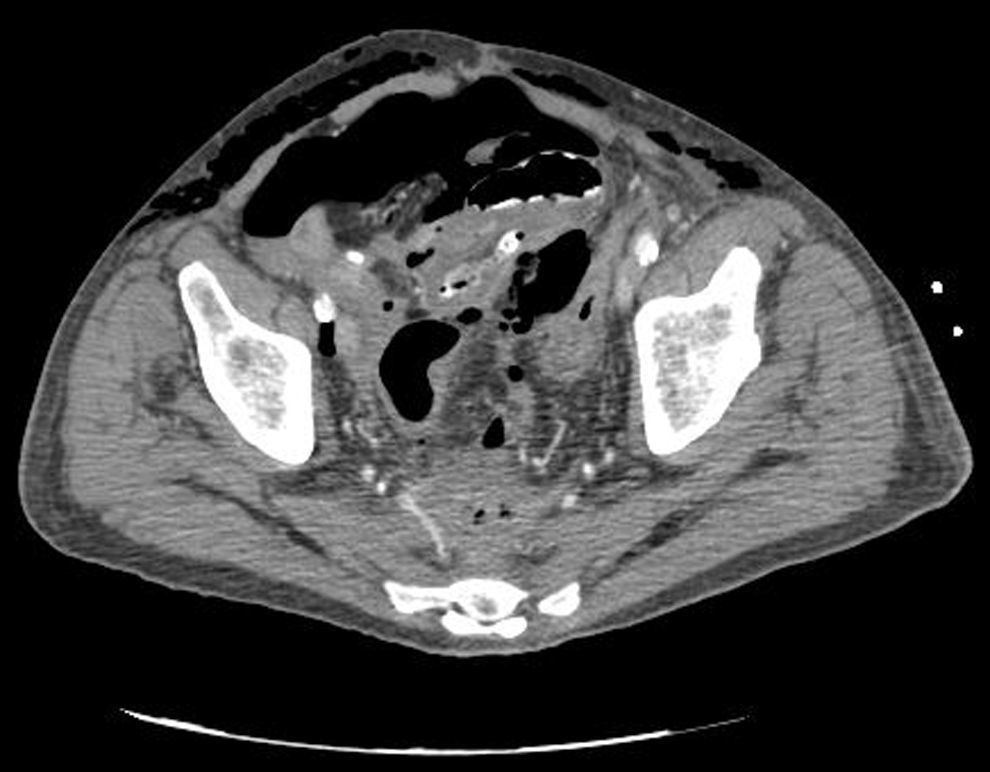
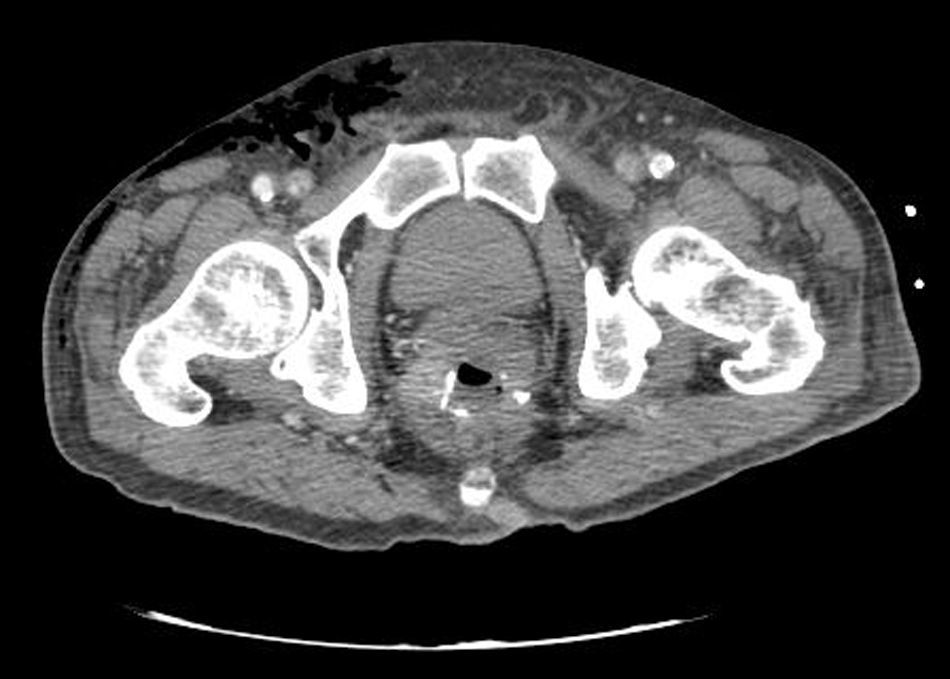
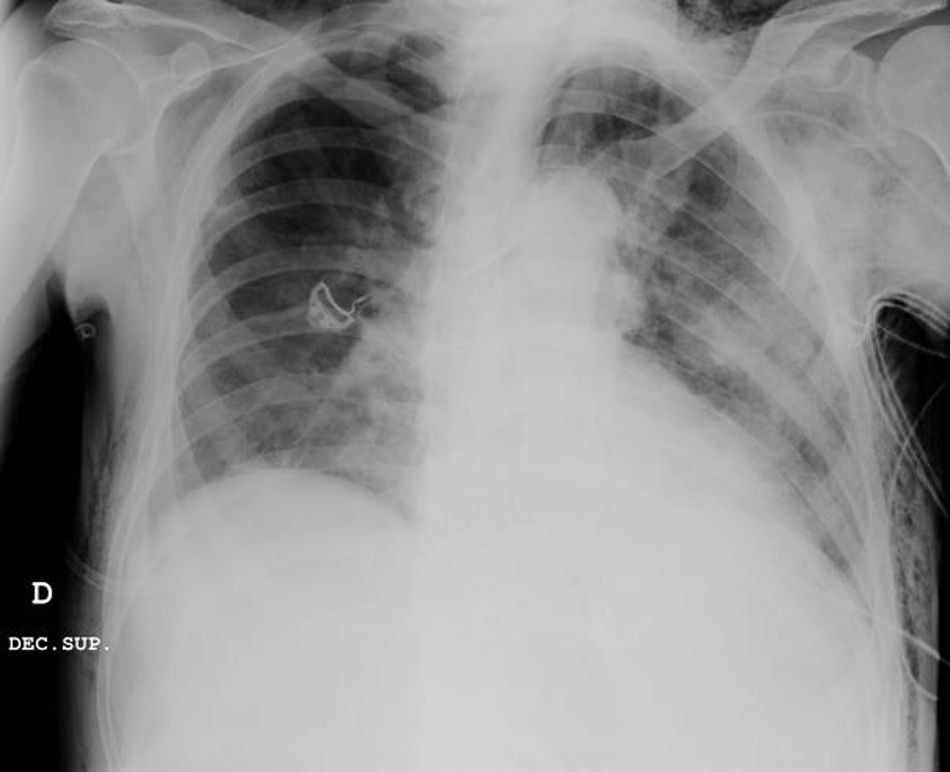
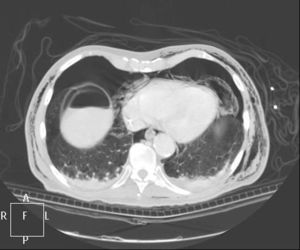
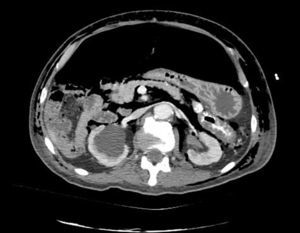
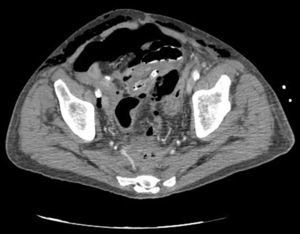
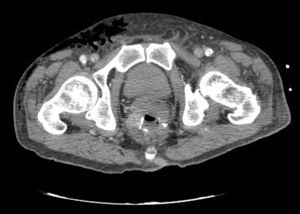
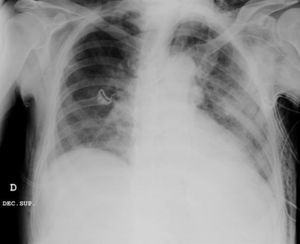
Caso clínicoPresentamos el caso de un paciente de 80 años con antecedentes de hipertensión arterial sistémica, intervenido en 2003 de un aneurisma de aorta abdominal infrarrenal. Valorado en el Servicio de Digestivo por presentar rectorragias ocasionales, es diagnosticado endoscópicamente de adenocarcinoma de recto de alto grado a 6-7 cm de margen anal. Se completa el estudio mediante tomografía axial computada, la cual mostró neoplasia de recto con afectación de los ganglios perirrectales y aneurisma de la aorta abdominal infrarrenal con trombo intraluminal. Una vez valorado por el Servicio de Oncología, que consideró que no ameritaba tratamiento neoadyuvante, por lo tanto se interviene quirúrgicamente practicándose una resección anterior baja de recto con escisión mesorrectal total laparoscópica y reconstrucción del tránsito mediante anastomosis latero-terminal mecánica (grapadora circular quirúrgica de calibre 28 mm) e ileostomía de protección en asa a nivel de fosa ilíaca derecha. El resultado de la anatomía patológica es adenocarcinoma de recto de alto grado pT3N2a (GL 5+/14) estadio C de Dukes. En el postoperatorio se observó una fuga subclínica que se trató y resolvió de manera conservadora. Tres meses después, se programó el cierre de la ileostomía tras comprobar mediante tacto rectal y anuscopia la integridad y normalidad de la anastomosis. El segundo día postoperatorio, tras la reconstrucción del tránsito digestivo, el paciente presentó distensión abdominal, náuseas y vómitos. Se realizó una radiografía de abdomen en la que se apreciaron niveles hidroaéreos de intestino delgado y grueso. Bajo la sospecha de estenosis anastomótica, se lleva a cabo una rectoscopia en la que se confirma dicha sospecha y se procede a realizar una dilatación neumática mediante colonoscopia. Dicha dilatación es laboriosa, con dificultad para identificar la anastomosis (probablemente por ser latero-terminal) y el fondo de saco ciego del cierre lateral. El paciente, durante el procedimiento, se encontraba sedado y en ese momento solo se apreció importante distensión abdominal, la cual se atribuye a la distensión abdominal que se atribuye a distensión colónica por la ingente insuflación de aire durante el prolongado procedimiento. En ningún momento el endoscopista determinó perforación alguna. Dos horas después del procedimiento, el personal de enfermería informó que el paciente presentaba signos clínicos de: hipotensión arterial, taquicardia y sudoración. A la exploración física del paciente se identificó: distensión abdominal con crepitación palpable a nivel torácico y del hemiabdomen inferior; acompañado de inestabilidad hemodinámica y con discreta obnubilación del paciente; lo que determinó su traslado a la Unidad de Cuidados Intensivos, donde se ha estabilizado al paciente con las medidas necesarias y sin la administración de fármacos vasoactivos, el estudio diagnóstico se integró con una tomografía axial computada toracoabdominopélvica que evidenció un importante neumo- y retroneumoperitoneo con neumomediastino (figs. 1–4). Y con un estudio simple de rayos X simple de tórax se determinó un neumotórax bilateral discreto (fig. 5).
Debido a la edad del paciente y a que se logró estabilizar clínicamente con tratamiento conservador, se determinó continuar con: ayuno total, sonda nasogástrica, hidroterapia, oxigenoterapia y la administración de antibióticos de amplio espectro. Una vez estabilizado el paciente se procedió a la eliminación del neumoperitoneo mediante punción percutánea con abocath No. 14 a nivel de epigastrio, manteniendo vigilancia estrecha con la monitorización del paciente y mediante estudios de laboratorio y radiológicos seriados.
Al tercer día de su ingreso en la Unidad de Cuidados Intensivos, el paciente evolucionó clínicamente en forma favorable, y se verificó con los estudios de laboratorio y radiológicos correspondientes, razón por la cual se le trasladó al Servicio de Cirugía, donde se regularizó su tránsito intestinal con una exploración abdominal normal, por lo que se determina su alta hospitalaria, 10 días después de su ingreso. Después de 6 meses de seguimiento ambulatorio del paciente, en los que se realizaron controles de rectoscopias seriadas, no han sido necesarias dilataciones neumáticas endorrectales; no obstante el no haberse demostrado la localización de la perforación.
DiscusiónSe estima entre el 4 y el 10% la incidencia de estenosis sintomáticas anastomóticas que se manifiestan como obstrucción intestinal parcial o completa1.
La primera opción terapéutica en aquellos pacientes con estenosis anastomóticas tanto benignas como malignas es la dilatación endoscópica de la anastomosis con o sin la colocación de stents expandibles o la resección de los tejidos estenóticos por vía endoscópica si existe una estenosis de alto grado benigna2 y, en los casos en los que no sean efectivas estas medidas, será necesaria la resección quirúrgica. Aunque la dilatación endoscópica es el tratamiento de elección, esta puede provocar una serie de efectos adversos no deseados como la reestenosis, formación de abscesos o la perforación, que es la complicación más grave tras este procedimiento.
La incidencia de perforaciones oscila en torno al 5% tras colonoscopias terapéuticas, según diferentes series3. Ante el diagnóstico de una perforación tras una dilatación endoscópica, se puede optar por diversas estrategias terapéuticas: manejo conservador, cierre endoscópico endoanal de la perforación3,4 o intervención quirúrgica. En el caso que presentamos, la dilatación mediante colonoscopia resultó muy laboriosa, quizá por el tipo de anastomosis (latero-terminal) y la fuga previa y, aunque en última instancia efectiva, conllevó como efecto secundario una perforación que se manejó de manera conservadora; este tipo de tratamiento debe reservarse para pacientes con: buen estado general, con preparación colónica, y sin signos de peritonitis y clínicamente estable; lo cual podría ser considerado para pacientes inestables, como el caso de referencia. No obstante, se recomienda en estos casos, las medidas necesarias de apoyo en la Unidad de Cuidados Intensivos para el control y vigilancia estrecho del paciente con tratamiento conservador, en caso contrario se deberá proceder a una revisión quirúrgica.
El manejo conservador está sustentado en el reposo digestivo, hidroterapia, y la administración de antibióticos de amplio espectro y demás medidas que sean precisas según las manifestaciones clínicas del paciente. El éxito del tratamiento conservador oscila entre el 33 y el 73% y debe ser evidente a las 24-48 h de su instauración, puesto que, en caso contrario, será necesario plantearse una actitud más agresiva3,5,6. En este paciente se planteó una opción conservadora al disponer de una Unidad de Cuidados Intensivos que permitió su control estrecho durante las primeras 48 h en las que se le realizó el drenaje percutáneo del neumoperitoneo y se le hicieron las medidas de soporte necesarias, con las que se obtuvo una adecuada respuesta clínica, lo que permitió mantener el tratamiento conservador como una primera opción terapéutica, evitando la revisión quirúrgica, con la consiguiente morbimortalidad. Si en nuestro paciente hubieran fallado las medidas conservadoras, o se hubiera producido de nuevo una estenosis, dada su edad y debido a que era una anastomosis baja, nuestra actitud hubiera sido la realización de una resección y una colostomía en fosa ilíaca izquierda.
La reestenosis presenta una incidencia del 15% de los pacientes intervenidos de cáncer de recto según Suchan7, aunque este dato es muy variable en la literatura debido a diferentes e irregulares métodos de seguimiento.
Por otro lado, las estenosis benignas cuya incidencia varía entre el 3 y el 30%8 están directamente relacionadas con los siguientes factores de riesgo: A) La realización de anastomosis mecánicas que está asociada con mayores depósitos de colágeno e inflamación, lo que puede favorecer la aparición de estenosis8. B) La realización de anastomosis termino-terminales frente a las latero-terminales, debiendo ser estas últimas las de elección cuando la anastomosis sea por debajo de 8 cm9. C) El haber presentado signos de fuga anastomótica o fuga subclínica, con la consecuente sepsis pélvica que favorece la aparición de fibrosis de los tejidos perianastomóticos10,11. D) El sexo masculino, por la dificultad técnica que conlleva en ciertos casos la pelvis del varón12. E) Portar una ostomía de protección12, debido a la falta de tránsito intestinal en esa región.
La práctica estandarizada en nuestra unidad siempre que realizamos resecciones rectales bajas y siempre que las características anatómicas del paciente y quirúrgicas lo permitan es la realización de una anastomosis «tension-free» mecánica latero-terminal con dispositivo de 31 mm, evitando dispositivos de menor calibre y realizando comprobación sistemática de la estanqueidad de la anastomosis, con refuerzo ocasional mediante varios puntos de sutura (seda 3/0). Al paciente que presentamos, aunque se le realizó una anastomosis mecánica latero-terminal mediante un dispositivo de calibre que consideramos adecuado (grapadora circular quirúrgica de calibre 28 mm), presentó un íleo postoperatorio en la primera cirugía, con exteriorización de contenido purulento por el drenaje, que interpretamos como una fuga subclínica bien tolerada y resuelta bajo tratamiento conservador, que a lo largo de la evolución posterior interpretamos como causa principal de la estenosis anastomótica. Si sumamos a este hecho el uso de un cabezal de calibre intermedio, nos hace pensar que, en ciertas ocasiones y ante ciertas complicaciones en el postoperatorio de cirugía colorrectal, el estudio previo de la anastomosis de forma ambulatoria mediante la prueba de imagen13,14 y rectoscopia rutinaria es no solo obligado15 sino que permite la dilatación previa al cierre ileostómico, que disminuye la morbilidad durante el postoperatorio del segundo tiempo quirúrgico.
Como conclusión, creemos importante comprobar toda anastomosis colorrectal baja previa al cierre ileostómico, procedimiento simple que puede realizarse de forma ambulatoria mediante exploración digital, anuscopia y rectoscopia rígida. Sin embargo, como en el caso que presentamos, esta comprobación no fue capaz de descartar la estenosis. Por otro lado, cabe contemplar, ante una perforación anastomótica tras su manipulación endoscópica, la posibilidad del tratamiento conservador si la situación clínica del paciente lo permite, en un medio hospitalario que disponga de los medios adecuados.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.