La cirugía laparoscópica ha remplazado gran variedad de procedimientos que anteriormente se realizaban con técnica abierta o convencional, debido a su mínima invasión, incisiones pequeñas y rápida recuperación. Sin embargo, el aumento de la presión intraabdominal por el neumoperitoneo con dióxido de carbono causa alteraciones: cardiovasculares, respiratorias, endocrinas y renales.
ObjetivoEvaluar el efecto nefroprotector del telmisartán, un antagonista de los receptores AT1 de la angiotensina II, en la filtración glomerular en cirugía laparoscópica.
Material y métodosEstudio analítico prospectivo, aleatorizado, doble ciego, en pacientes intervenidos mediante colecistectomía laparoscópica electiva. Se aleatorizaron en 2 grupos, el grupo de tratamiento recibió 40mg de telmisartán por vía oral en dosis única 2 h antes de la cirugía y el otro grupo, placebo.
ResultadosSe analizaron 20 pacientes por grupo (n=40) con una media de edad de 32.65 en el grupo de tratamiento. La creatinina plasmática no mostró cambios significativos en los distintos tiempos en los que se tomó la muestra, pero la depuración de creatinina al final de la cirugía (196.415±56.507 vs. 150.1995±75.081; p=0.034) y a las 2 h potsoperatorias (162.105±44.756 vs. 113.235±31.228; p=≤ 0.001) presentaron datos estadísticamente significativos, que apoyan el aumento de la función renal con el grupo de telmisartán.
ConclusionesEl uso de telmisartán, un antagonista de los receptores AT1 de la angiotensina II, ofrece medidas nefroprotectoras durante la cirugía laparoscópica.
Laparoscopic surgery has begun to replace a great number of procedures that were previously practiced using open or conventional techniques. This is due to the minimal invasion, small incisions, and short time recovery. However, it has come to knowledge, that the increase in intra-abdominal pressure due to carbon dioxide pneumoperitoneum during laparoscopic surgery causes cardiovascular, respiratory, endocrine, and renal alterations.
ObjectiveTo evaluate the nephroprotective effect of telmisartan, an angiotensin II AT1 receptor antagonist, on glomerular filtration in laparoscopic surgery.
Material and methodsAnalytical prospective, randomised, double-blind study was conducted on patients undergoing elective laparoscopic cholecystectomy. They were randomised into 2 groups, with the treatment group receiving a single dose of 40mg telmisartan orally 2hours prior to surgery, and the placebo group.
ResultsThere were 20 patients in each group (n=40), with a mean age of 32.65 years in the treatment group. Plasma creatinine did not show any significant change in the different time lapse in which blood samples were taken, but creatinine clearance at the end of surgery (196.415±56.507 vs. 150.1995±75.081; p=0.034), and at 2 h postoperative period (162.105±44.756 vs. 113.235±31.228; p≤0.001) was statistically significant, which supports an increase in renal function in the telmisartan group.
ConclusionThe use of telmisartan, an angiotensin II AT1 receptor antagonist, offers renal protection during laparoscopic surgery.
El papel de la cirugía laparoscópica se ha expandido en los últimos años. Esta técnica de mínima invasión para cirugías complejas y corta recuperación, se ha popularizado. La incidencia anual de colecistolitiasis es aproximadamente de 1/200 personas. La colecistectomía es el tratamiento de elección en colecistolitiasis sintomática. Cada año más de 500,000 colecistectomías son realizadas en los Estados Unidos y 600,000 en Reino Unido. Aproximadamente el 80% de las colecistectomías son realizadas por laparoscopia1,2.
El neumoperitoneo es una condición no fisiológica que causa aumento de la presión intraabdominal; el aumento de presión es transmitido a los órganos intraabdominales, incluyendo los riñones. Una presión intraabdominal superior a 10mm/Hg presenta transitoriamente: oliguria, disminución del filtrado glomerular y del flujo sanguíneo renal1,3.
El CO2 insuflado durante la cirugía laparoscópica es rápidamente absorbido dentro de la circulación, lo que resulta en acidosis respiratoria y cambios hemodinámicos. También compromete la circulación capilar en órganos intraabdominales. El aumento en la presión intraabdominal causa alteraciones respiratorias, cardiovasculares y renales. El flujo sanguíneo en la arteria mesentérica, esplénica, hepática y perfusión renal disminuye con el aumento de la presión intraabdominal3–5.
ObjetivoEvaluar el efecto de telmisartán, un antagonista de los receptores AT1 de angiotensina II, en la filtración glomerular en pacientes operados con cirugía laparoscópica electiva con neumoperitoneo, usando dióxido de carbono.
Material y métodosEstudio analítico prospectivo, longitudinal, aleatorizado, controlado, doble ciego, en pacientes intervenidos mediante colecistectomía laparoscópica electiva, que ingresaron en el periodo comprendido entre septiembre de 2015 y enero de 2016 en el Hospital Universitario Universidad Autónoma de Nuevo León (UANL), en Monterrey (Nuevo León, México).
La población de estudio incluyó a pacientes mayores de 18 años, ASA I y II (clasificación de la American Society of Anesthesiologists), o intervenidos mediante colecistectomía laparoscópica, atendidos en el Servicio de Cirugía General del Hospital Universitario (UANL). Los pacientes con enfermedad renal, diabetes mellitus, enfermedad hepática, uso de antihipertensivos o conversión de la colecistectomía a técnica abierta fueron excluidos.
Se dividió de manera aleatorizada en 2 grupos, con apoyo del programa Microsoft Excel 2007; el grupo 1, de tratamiento, recibió 40mg por vía oral de telmisartán en dosis única, 2 h antes de la cirugía, y el grupo 2 recibió placebo. Al ingreso se aleatorizaron en 2 grupos a través de un sobre cerrado y recibieron una cápsula por vía oral en dosis única, 2 h antes de la cirugía. El estudio fue aprobado por el Comité de Ética e Investigación de la institución y se obtuvo consentimiento informado escrito de cada paciente.
Se recolectaron datos generales y demográficos. Se registraron: peso, talla, índice de masa corporal y clasificación ASA.
Los pacientes recibieron anestesia general estándar para colecistectomía laparoscópica. Se administraron 0.05-0.15mg/kg de midazolam, 2-20 ug/kg de fentanilo, seguidos de 1.7-2.4mg/kg de propofol. Se buscó la relajación muscular con atracurium 0.4-0.5mg/kg. La anestesia fue mantenida con isofluorano (0.8-1.2 vol/%) y mezcla de aire y oxígeno (índice 0.40). La ventilación en asisto-control con frecuencia y volumen tidal, suficiente para mantener normocapnia (35-38mmHg). Después de la anestesia general se colocó sonda Foley y sonda nasogástrica. La monitorización del paciente incluyó: capnografía, oximetría de pulso, electrocardiografía y medida de presión arterial no invasiva. La colecistectomía laparoscópica se realizó con neumoperitoneo con dióxido de carbono, con una presión mantenida a 15mmHg y un índice de 1 a 1.5l/min.
Las variables hemodinámicas incluyeron: frecuencia cardiaca y presión arterial media, las cuales fueron registradas según los siguientes tiempos: (T0) antes de la inducción de la anestesia; (T1) después de la inducción de la anestesia, pero antes de la intubación traqueal; (T2) 5 min después de la intubación traqueal, (T3) inmediatamente después de colocar el neumoperitoneo; (T4) 15 min después del neumoperitoneo; (T5) 30 min después del neumoperitoneo; (T6) 45 min después del neumoperitoneo; (T7) después del retirar el neumoperitoneo; (T8) 30 min después de retirar el neumoperitoneo; (T9) a las 24h postoperatorias y (T10) a las 48h postoperatorias.
Los niveles de creatinina fueron medidos: antes de la cirugía, al final del neumoperitoneo, a las 2, 24, y 48 horas, postoperatorias.
Diuresis, depuración o aclaramiento de creatinina corregida (CrCl) y fracción de excreción de sodio (FENA) fueron calculados al finalizar el neumoperitoneo y a las 2 h postoperatorias.
La diuresis fue calculada dividiendo el volumen urinario y el tiempo de recolección urinaria. La depuración de creatinina corregida fue calculada de acuerdo con la fórmula CrCl=(UCr×UVol)/(PCr×Tmin), donde UCr es la concentración de creatinina urinaria, UVol es el volumen urinario, PCr es la concentración de creatinina plasmática y Tmin es el tiempo de recolección urinaria. CrCl fue corregido de acuerdo con el área de superficie corporal, CrCl×1.73 m2/área de superficie corporal. La fracción de excreción de sodio (FENA) fue calculada de acuerdo con la siguiente fórmula: FENA=(UNa×PCr)/(PNa×UCr)×100, donde UNa es la concentración de sodio urinario y PNa es la concentración de sodio en plasma.
La depuración de creatinina antes de la cirugía, a las 24 y a las 48 h postoperatorias, fue calculada con la ecuación modificada de Cockcroft-Gault, corregida por el área de superficie corporal (fórmula de Cockcroft-Gault×1.73 m2/área de superficie corporal). Fórmula de Cockcroft-Gault: para hombres CrCl=[(140-edad)×peso×1.2]/Cr en plasma y para mujeres CrCl=[(140-edad)×peso]/Cr en plasma.
El tiempo anestésico, la hidratación transoperatoria y la duración de la cirugía fueron registrados. La intensidad del dolor postoperatorio fue evaluada con la escala visual análoga del dolor de 10 puntos, y se registró en la primera hora, a las 3, 6, 12, 24 y a las 48h después de la cirugía.
Análisis estadístico. Se evaluaron las variables por separado utilizando la prueba de chi cuadrada con coeficiente de Pearson, en caso de variables categóricas y la prueba de t de Student, en caso de variables continuas. Un valor de p<0.05 se consideró significativo.
Utilizando una fórmula para prueba de hipótesis y diferencia de 2 medias, con un valor zα de 1.96 con nivel de significación del 95% para 2 colas, y un valor zβ de 0.84 con una potencia de 80%, se obtuvo una muestra de 20 participantes por grupo. El análisis estadístico se realizó con SPSS versión 20 (SPSS, Inc. Armon, NY, EE. UU.).
ResultadosSe incluyó a 43 pacientes, de los cuales 3 fueron excluidos por conversión de la cirugía a técnica convencional. Se analizaron 20 pacientes por grupo (n=40). Las características basales de los pacientes y las variables quirúrgicas fueron comparables y homogéneas (tabla 1).
Características biométricas y quirúrgicas
| Variable | Grupo 1 Telmisartán (n=20) | Grupo 2 Placebo (n=20) |
|---|---|---|
| Edad | 32±12.12 | 35.5±12.1 |
| Hombre/mujer | 3/17 | 2/18 |
| Peso | 73±14.95 | 74±11.38 |
| Talla | 161±7.67 | 160±6.42 |
| IMC | 26.57±6.26 | 28.92±4.95 |
| ASA I/II | 18/2 | 20/0 |
| Duración de la anestesia | 102.85±34.12 | 104.6±35.7 |
| Duración de la cirugía | 72.6±33.57 | 72.05±29.85 |
| Hidratación transoperatoria | 517.5±121.69 | 507.5±97.7 |
ASA: clasificación de la American Society of Anesthesiologists; IMC: índice de masa corporal.
Los datos son presentados como mediana y desviación estándar.
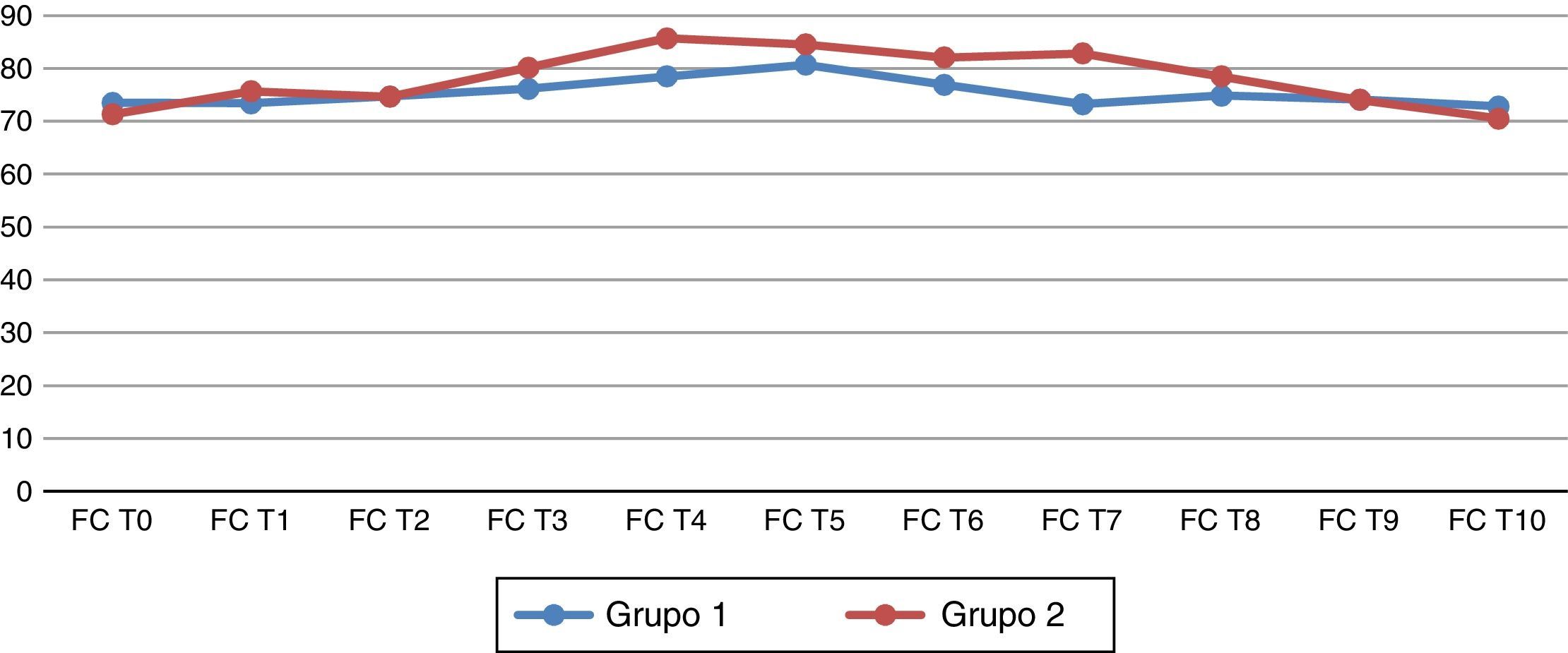
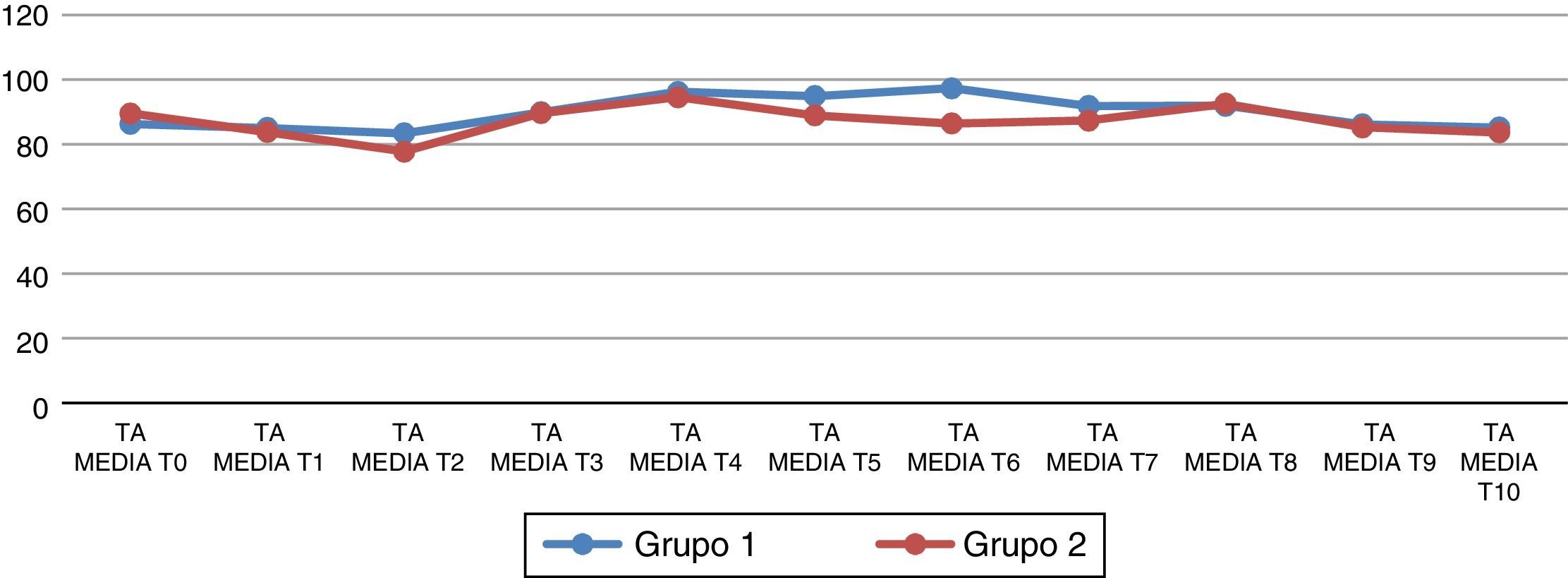
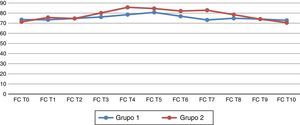
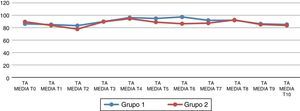
Al analizar las variables hemodinámicas, se observa que la frecuencia cardiaca al retirar el neumoperitoneo (T7) presenta cambios estadísticamente significativos en el grupo de telmisartán (p=0.026) (fig. 1). La presión arterial media (PAM) 45 min después del neumoperitoneo (T6) presenta cambios estadísticamente significativos respecto al grupo 2 (p=0.044) (fig. 2).
Frecuencia cardiaca basal y en los diferentes tiempos del estudio. (T0) antes de la inducción de la anestesia; (T1) después de la inducción de la anestesia, pero antes de la intubación traqueal; (T2) 5 min después de la intubación traqueal; (T3) inmediatamente después de colocar el neumoperitoneo; (T4-T6) 15, 30 y 45 min después del neumoperitoneo; (T7) después del retirar el neumoperitoneo; (T8) 30 min después de retirar el neumoperitoneo; (T9) a las 24h postoperatorias y (T10) a las 48h postoperatorias.
Presión arterial media (PAM) basal y en los diferentes tiempos del estudio. (T0) antes de la inducción de la anestesia; (T1) después de la inducción de la anestesia, pero antes de la intubación traqueal; (T2) 5 min después de la intubación traqueal; (T3) inmediatamente después de colocar el neumoperitoneo; (T4-T6) 15, 30 y 45 min después del neumoperitoneo; (T7) después de retirar el neumoperitoneo; (T8) 30 min después de retirar el neumoperitoneo; (T9) a las 24h postoperatorias y (T10) a las 48h postoperatorias.
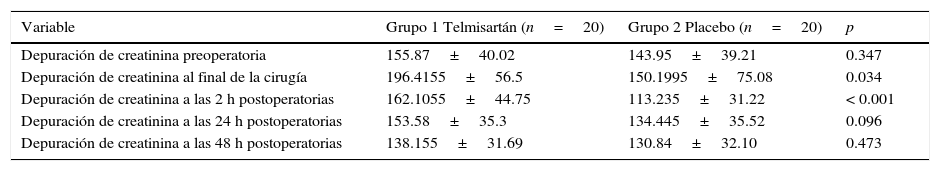
Al analizar la creatinina plasmática, esta no mostró cambios significativos en los distintos tiempos en los que se tomó la muestra (p=0.114), pero la depuración de creatinina al final de la cirugía (p=0.034) y a las 2 h postoperatorias (p=≤ 0.001) presentaban cambios estadísticamente significativos en el grupo de telmisartán (tablas 2 y 3).
Valores de la creatinina plasmática en los diferentes tiempos de recolección del estudio
| Variable | Grupo 1 Telmisartán (n=20) | Grupo 2 Placebo (n=20) | p |
|---|---|---|---|
| Creatinina preoperatoria | 0.625±0.18 | 0.645±0.13 | 0.697 |
| Creatinina al final de la cirugía | 0.74±0.15 | 0.745±0.13 | 0.913 |
| Creatinina 2 h postoperatorias | 0.645±0.15 | 0.7±0.12 | 0.229 |
| Creatinina 24 h postoperatorias | 0.62±0.13 | 0.69±0.13 | 0.114 |
| Creatinina 48 h postoperatorias | 0.685±0.13 | 0.705±0.14 | 0.647 |
Los datos son presentados como mediana y desviación estándar.
Valores de la depuración de creatinina en los diferentes tiempos de recolección del estudio
| Variable | Grupo 1 Telmisartán (n=20) | Grupo 2 Placebo (n=20) | p |
|---|---|---|---|
| Depuración de creatinina preoperatoria | 155.87±40.02 | 143.95±39.21 | 0.347 |
| Depuración de creatinina al final de la cirugía | 196.4155±56.5 | 150.1995±75.08 | 0.034 |
| Depuración de creatinina a las 2 h postoperatorias | 162.1055±44.75 | 113.235±31.22 | < 0.001 |
| Depuración de creatinina a las 24 h postoperatorias | 153.58±35.3 | 134.445±35.52 | 0.096 |
| Depuración de creatinina a las 48 h postoperatorias | 138.155±31.69 | 130.84±32.10 | 0.473 |
Los datos son presentados como mediana y desviación estándar.
La diuresis al final de la cirugía (p=0.005) y a las 2 h postoperatorias (p=0.003) presentaron cambios significativos en el grupo de telmisartán (tabla 4).
Valores de la diuresis en los diferentes tiempos de recolección
| Variable | Grupo 1 Telmisartán (n=20) | Grupo 2 Placebo (n=20) | p |
|---|---|---|---|
| Diuresis al final de la cirugía | 1.379±0.73 | 0.8035±0.44 | 0.005 |
| Diuresis a las 2 h postoperatorias | 0.9555±0.44 | 0.57±0.32 | 0.003 |
Los datos son presentados como mediana y desviación estándar.
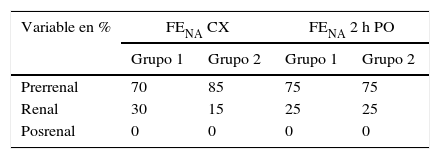
Se observó que la fracción de excreción de sodio (FENA), el 70% de los pacientes del grupo 1 y el 85% del grupo 2 presentaron lesión prerrenal al finalizar la cirugía y el 75% de los pacientes de ambos grupos presentaron lesión prerrenal a las 2 h postoperatorias, lo que muestra un cambio funcional o fisiológico, posiblemente influido por el procedimiento quirúrgico (tabla 5).
Porcentaje de los pacientes según la clasificación por la fracción de excreción de sodio (FENA)
| Variable en % | FENA CX | FENA 2 h PO | ||
|---|---|---|---|---|
| Grupo 1 | Grupo 2 | Grupo 1 | Grupo 2 | |
| Prerrenal | 70 | 85 | 75 | 75 |
| Renal | 30 | 15 | 25 | 25 |
| Posrenal | 0 | 0 | 0 | 0 |
FENA: clasificación por la fracción de excreción de sodio; PO: postoperatorio.
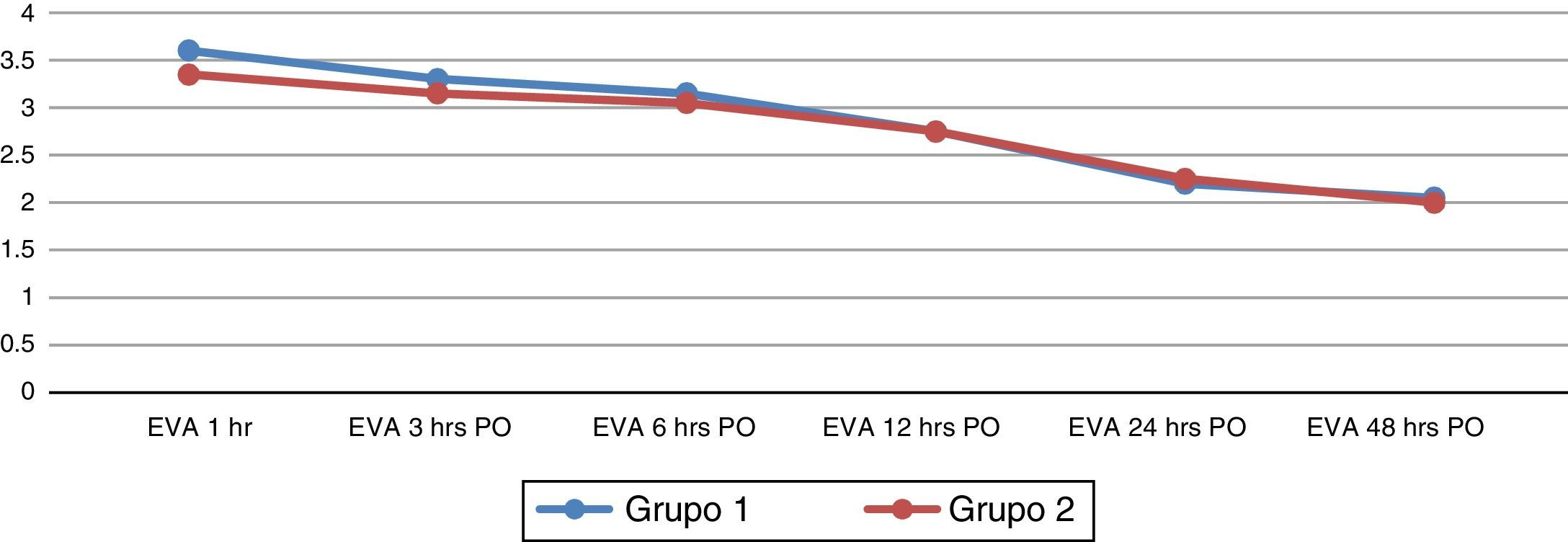
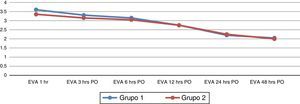
No hay evidencia significativa en los resultados de la escala visual análoga del dolor en ambos grupos, en los distintos tiempos en los que se aplicó (fig. 3). No se encontró asociación entre los grupos y las variables analizadas mediante la prueba de chi cuadrada al 95% de confianza. No se registraron complicaciones ni efectos adversos durante el estudio.
DiscusiónLos antagonistas de los receptores de la angiotensina II (ARA II) son un grupo de antihipertensivos que ha aparecido en los últimos tiempos, para el tratamiento de la hipertensión arterial y de la insuficiencia cardiaca. Los principales que se han comercializado son: candesartán, eprosartán, irbesartán, telmisartán y valsartán. Actúan bloqueando la unión de la angiotensina II a los receptores de tipo 1 de la angiotensina II (AT1), presentes en numerosos tejidos como: muscular liso, glándula adrenal y miocardio. Como consecuencia, inhiben su efecto vasopresor y liberador de aldosterona6–8.
El neumoperitoneo produce una disminución del volumen pulmonar total, de la capacidad residual y de la complianza pulmonar, lo que facilita el desarrollo de atelectasias. La insuflación de CO2 en la cavidad abdominal provoca hipercapnia, debida a la difusión del gas a través del peritoneo, y causa hipoxemia, hipercapnia y acidosis respiratoria; además, produce alteraciones hemodinámicas significativas y reduce el gasto cardíaco, entre un 10 y un 30%9.
En nuestro estudio los grupos analizados fueron homogéneos, y es interesante que la frecuencia cardiaca, al retirar el neumoperitoneo (T7), presente cambios hemodinámicos favorables y cardioprotectores, al reducir la frecuencia cardiaca (73.25±11.70 vs. 82.85±14.33; p=0.026).
Al analizar la presión arterial media (PAM) 45 min después del neumoperitoneo (T6) del grupo de telmisartán, este presenta un aumento de la PAM (97.31±20.100 vs. 86.435±11.549; (p=0.044). La PAM se considera como la presión de perfusión de los órganos corporales, y un valor > 60mmHg es suficiente para satisfacer su demanda. Aunque no está del todo claro el mecanismo exacto de la elevación de la PAM en el grupo de tratamiento, sabemos que el neumoperitoneo y la posición de Trendelenburg producen: un aumento de la PAM, la presión venosa central, la presión arterial pulmonar media, la presión de enclavamiento capilar pulmonar y la resistencia vascular sistémica. La administración perioperatoria de ARA II conlleva un riesgo de hipotensión grave bajo los efectos de la anestesia, particularmente tras la inducción. Sin embargo, algunos estudios demuestran que la actividad simpática puede causar un aumento de la presión arterial y un aumento de la frecuencia cardiaca en individuos normotensos, durante el procedimiento quirúrgico10. Sin embargo, la importancia clínica de estas acciones podría ser en un futuro la base para la selección de un determinado ARA II, debido a que no disponemos de estudios comparativos en pacientes normotensos con el uso de los distintos ARA II, que nos permitan conocer todas sus propiedades, ni si alguno de ellos presenta ventajas sobre el resto.
El flujo sanguíneo renal y la filtración glomerular disminuyen a menos del 50% durante la cirugía laparoscópica. Este descenso del flujo sanguíneo se ha encontrado también en los vasos mesentéricos y en otros órganos como: el hígado, páncreas, estómago, bazo e intestino.
La diuresis disminuye, lo que es atribuido al aumento de la actividad de la renina y la compresión directa de la vena cava inferior, de la vasculatura y del parénquima renal por el neumoperitoneo. Esto se observa en el estudio de Koivusalo et al.3 en el que comparan la disminución de la función renal usando un método de retracción de la pared abdominal versus un método convencional de neumoperitoneo11.
Usando telmisartán durante la cirugía laparoscópica observamos que la diuresis, y la depuración de creatinina tienen cambios significativos como nefroprotector al final de la cirugía y a las 2 h del procedimiento.
La importancia de la perfusión renal y las secuelas patofisiológicas durante el neumoperitoneo ha aumentado especialmente con la introducción de la donación renal, mediante la nefrectomía laparoscópica5,12,13.
Los ARA II presentan un buen perfil de seguridad, el telmisartán se absorbe rápidamente por vía oral, alcanza su Cmáx al cabo de 0.5-1 hora y disminuye la resistencia vascular renal, especialmente en la resistencia de las arteriolas aferentes, lo que resulta en un aumento del flujo sanguíneo renal14–16.
ConclusionesEs importante la detección temprana de la función renal alterada o limítrofe en pacientes que serán tratados mediante procedimientos laparoscópicos, para ofrecerles medidas nefroprotectoras. Algunos estudios demuestran los efectos del neumoperitoneo sobre los cambios hemodinámicos y de perfusión visceral durante la cirugía laparoscópica, los cuales muchas de las veces son reversibles espontáneamente.
En conclusión, demostramos que el uso de telmisartán, un antagonista de los receptores AT1 de la angiotensina II (ARA II), ofrece medidas nefroprotectoras durante la cirugía laparoscópica. Estudios futuros serán necesarios para determinar la nefroprotección de los distintos medicamentos en el mercado, así como en pacientes nefrópatas intervenidos mediante cirugía laparoscópica.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Queremos expresar un agradecimiento especial al equipo de enfermeras y cirujanos del área de cirugía ambulatoria del Hospital Universitario UANL por la paciencia y colaboración para la realización de este estudio.