La colecistitis aguda (CA) constituye una indicación frecuente de colecistectomía. Las circunstancias locales y ciertas características de los pacientes provocan unas altas tasas de fracaso y complicaciones de la colecistectomía laparoscópica (CL) y, a pesar de la experiencia ganada, aún no disponemos de una lista de indicaciones pormenorizada que permita minimizarlas.
Material y métodoEmpleamos el análisis de la adecuación RAM para evaluar 2 opciones, la CL y la colecistectomía abierta (OC). Un panel de expertos analizó su idoneidad tras una revisión de la bibliografía, una reunión de consenso y 2 rondas de puntuaciones sobre diferentes situaciones clínicas. Se analizó la puntuación sobre cada escenario para establecer el grado de adecuación de cada opción.
ResultadosTras la reunión presencial quedaron definidos 64 escenarios, lográndose un acuerdo en las indicaciones en el 67,18% de ellos. En el 86,04% de los escenarios el acuerdo fue por adecuación de las indicaciones. Cuando la colecistectomía estuvo indicada siempre lo fue por laparoscopia, mientras que solo en ocasiones lo fue por laparotomía. En pacientes con menos de 72 h de evolución se consideró apropiada siempre la CL cuando se presentasen con sepsis, o bien sin ella pero con datos ecográficos de CA complicada.
ConclusionesSigue existiendo incertidumbre respecto al manejo de la CA, en especial respecto al momento de la intervención y la vía de abordaje, particularmente en pacientes frágiles y con evoluciones de la clínica superiores a las 72 h. El método RAND puede ayudar a tomar decisiones sobre la adecuación de distintas opciones terapéuticas.
Acute cholecystitis (AC) is a common indication for cholecystectomy. Local circumstances and certain patient characteristics lead to high failure rates and complications in laparoscopic cholecystectomy (LC), and despite the experience gained, we still do not have a detailed list of indications which could minimise them.
Material and methodWe used the RAND/UCLA Appropriateness Method (RAM) to evaluate 2 options, LC and open cholecystectomy (OC). An expert panel analysed its suitability after a literature review, a consensus meeting, and 2 rounds of scores on different clinical situations. The score of each scenario was analysed to establish the appropriateness level of each option.
ResultsAt the end of the meeting there were 64 defined scenarios, with an agreement being reached on the indications in 67.18% of them. In 86.04% of the scenarios, the agreement was due to the appropriateness of the indications. When cholecystectomy was indicated, it was always by laparoscopy, while it was only occasionally by laparotomy. In patients with less than 72h of onset, LC was always considered appropriate when there was sepsis, or even without this if the ultrasound data showed complicated AC.
ConclusionsThere is still uncertainty as regards the management of AC, especially as regards the timing of the operation and the surgical approach, particularly in frail patients and with a clinical onset greater than 72h. The RAND method can help to make decisions on the appropriateness of different therapeutic options.
Más del 90% de las colecistitis agudas (CA) están relacionadas con la colelitiasis1, de las que entre el 1 y el 4% se vuelve sintomáticas cada año, un 20% por desarrollar CA2. Tras un primer episodio de CA es frecuente que se vuelvan a producir otros3, pero su incidencia ha caído debido a la mejor aceptación de la colecistectomía laparoscópica (CL) como tratamiento para la colelitiasis sintomática4. El 60% de los pacientes afectos de CA son mujeres, pero se presenta con mayor frecuencia de lo esperado en hombres y con episodios más severos5. La CL es considerada el «patrón oro» del tratamiento de la colelitiasis sintomática y durante los primeros años de su implantación, la presencia de CA se consideró una contraindicación para este abordaje6. Posteriormente, parece haber quedado demostrado que la CL en estos pacientes es viable, segura y coste-efectiva al ser comparada con la colecistectomía abierta (OC) o el tratamiento en 2 etapas (antibióticos y colecistectomía diferida)3,7,8. Sin embargo, la CL precoz aún no parece haber sido adoptada como rutinaria en la CA, por falta de consenso entre los profesionales o ausencia de guías clínicas específicas9.
Con la intención de proporcionar una herramienta de ayuda para la toma de decisiones, siguiendo un método RAM (RAND Appropriateness Method, método Delphy modificado de la Universidad de California), se estableció el nivel de adecuación de las estrategias terapéuticas analizadas (OC o CL), para diferentes situaciones clínicas.
Material y métodoSe analizó la adecuación para 2 indicaciones terapéuticas: extirpación de la vesícula mediante laparoscopia (CL) y extirpación por vía abierta (OC). Para definir los criterios del uso adecuado de ambas opciones aplicamos el método RAM, uno de los más respetados al definir la adecuación de la asistencia médica10–12. Este método consiste en puntuar, por parte de profesionales contrastados, la adecuación de las intervenciones terapéuticas evaluadas (aquí, la CL y la OC), aplicadas a escenarios clínicos concretos, tomando siempre en consideración la mejor evidencia aportada por una revisión sistemática de la bibliografía (elaborada por un equipo independiente). Ha demostrado, específicamente, su utilidad para establecer los algoritmos de toma de decisiones en temas relacionados con la salud12–17. No es un método de consenso, sino que trata de identificar grados de acuerdo o desacuerdo para cada indicación terapéutica, evaluándola estadísticamente, identificando también puntos discrepantes que representan una llamada para futuras investigaciones.
En este caso fueron seleccionados profesionales implicados en la asistencia de pacientes con CA (tabla 1), elegidos en base a su reconocido prestigio profesional, su diversidad geográfica, su capacidad de trabajo en equipo, la diferente tipología de sus centros laborales de origen y la ausencia de conflictos de intereses.
Miembros de panel de expertos
| Especialidad | Nombre | Institución/hospital | Ciudad |
| Gastroenterólogos | Dr. Rafael Bañares Cañizares | Hospital Universitario Gregorio Marañón | Madrid |
| Dr. Antonio Naranjo Rodríguez | Hospital Universitario Reina Sofía | Córdoba | |
| Cirujanos | Dr. Esteban Cugat Andorrá | Hospital de la Mutua de Terrasa | Barcelona |
| Dr. Juan Ruiz Castillo | Hospital Universitario San Cecilio | Granada | |
| Dr. Julio Santoyo Santoyo | Hospital Universitario Carlos Haya | Málaga | |
| Dr. Eduardo Targarona Soler | Hospital de la Santa Creu i San Pau | Barcelona | |
| Dr. Antonio Torres García | Hospital Clínico San Carlos | Madrid |
Se hizo una búsqueda exhaustiva en las bases de datos Biblioteca Cochrane Plus 2006, MEDLINE y PubMed (1964-2005) y EMBASE (1974-2005) con una síntesis crítica de las publicaciones, sobre la cirugía laparoscópica en el tratamiento de la CA. La Agencia de Evaluación de Tecnologías Sanitarias de Andalucía (AETSA) publicó, de forma independiente, un informe sobre la laparoscopia aplicada a las enfermedades hepato-biliares, que incluye el resultado de dicha revisión, en la dirección web http://www.juntadeandalucia.es/salud/servicios/contenidos/nuevaaetsa/up/ETSA_P_2008_2_Laparoscopia.pdf. Simultáneamente, 3 cirujanos digestivos expertos tanto en cirugía laparoscópica como en cirugía hepato-bilio-pancreática elaboraron la lista de escenarios clínicos, describiendo las distintas situaciones en las que podría presentarse un paciente con CA. Cada indicación debía ser lo suficientemente exhaustiva como para que todos los pacientes se pudiesen clasificar en categorías autoexcluyentes; homogéneas, pues la decisión terapéutica debiera ser igual para todos los pacientes clasificados en la misma categoría y manejables, para que los panelistas pudieran valorarlas en un tiempo razonable.
Adecuación, inadecuación o incertidumbreEl concepto de adecuación se determinó a partir del peso relativo de los beneficios de cada procedimiento frente a sus riesgos potenciales, para cada escenario. Una indicación se consideró adecuada si el beneficio que aportaba era superior a sus consecuencias negativas, por un margen lo suficientemente amplio como para que valiese la pena, mientras que se consideró inadecuada si sus riesgos superaban sus potenciales beneficios. Si el panel no logró un consenso sobre el balance riesgo/beneficio, el procedimiento fue calificado como incierto.
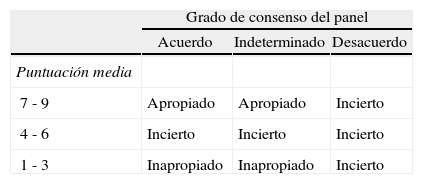
Los panelistas usaron una escala de 9 puntos para evaluar cada escenario, de forma que se puntuó con 1 aquello que se consideró extremadamente inadecuado y con 9 lo totalmente adecuado. Se calcularon las medianas de las puntuaciones para cada indicación, de forma que si se situó en el intervalo 7-9, la indicación se clasificó como «adecuada»; en el intervalo 1-3 se consideró «inadecuada» y en el intervalo 4-6, «dudosa».
Reunión presencial y segunda ronda de puntuacionesLos panelistas puntuaron individualmente, según su experiencia y los datos ofrecidos por la revisión bibliográfica. Posteriormente fueron reunidos para discutir los resultados de esa primera ronda de puntuaciones y modificar los escenarios que estimasen. El acuerdo del panel no era obligatorio y las puntuaciones podrían ser diferentes, pero las valoraciones totalmente opuestas podrían entenderse como una interpretación errónea del escenario y se resolvieron durante la reunión presencial. Establecida la lista final de escenarios, se votó en segunda ronda, de forma individual y anónima, estableciéndose las medianas para cada uno.
Consenso final del panel de expertosEn las definiciones finales de adecuación se adoptaron las directrices propuestas por la RAND para paneles con 7 componentes12. Según esto, existió acuerdo cuando no más de un panelista puntuó una indicación fuera del rango que contenía la mediana (1-3, 4-6, o 7-9). Existió desacuerdo cuando 2 puntuaron una indicación en el rango 7-9, pero al menos otros 2 en el rango 1-3. Cuando no existió acuerdo ni desacuerdo se clasificó como «indeterminado».
Se clasificaron como adecuadas aquellas indicaciones puntuadas en el rango 7-9 sin desacuerdo, inadecuadas las que tuvieron una mediana de 1-3 sin desacuerdo e indeterminadas todas las situadas en la mediana de 4-6, junto a todas aquellas que se definieron como «con desacuerdo», cualquiera que fuese la mediana (tabla 2).
ResultadosLista de indicaciones y análisis de las opciones terapéuticasTras la revisión de las indicaciones realizada durante la reunión presencial quedaron definidas 64 situaciones clínicas, seleccionadas en función de las siguientes variables: signos clínicos de sepsis, tiempo transcurrido desde el inicio de los síntomas, presencia de comorbilidades, calidad de vida previa, datos ecográficos de complicación o posible asociación de inmunodepresión (tabla 3). La calidad de vida se determinó por el índice de Karnofsky, que describe los niveles de actividad e independencia utilizando una escala de 0 a 10018. Se entendió como Karnofsky basal el que el paciente tenía 72 h antes del inicio de los síntomas. En el grupo de CA «sin signos de sepsis», solo los pacientes «sin comorbilidad» fueron subdivididos en función de su estado inmunológico.
Definiciones
| Signos de sepsis: Ta > 39 °C o <36 °C, hipotensión arterial (tensión arterial sistólica menor de 100mmHg), trastornos de la coagulación, oliguria, trastorno del nivel de consciencia, peritonismo intenso local o generalizado |
| Ecografía de CA complicada: líquido libre perivesicular o peritoneal en ausencia de ascitis o hepatopatía, perforación vesicular, colecciones perivesiculares o hepáticas yuxtavesiculares, datos de gangrena vesicular (desprendimiento de la mucosa, gas o disrupción de la pared) |
| Comorbilidad: enfermedad cardiológica limitante, enfermedad respiratoria limitante, deterioro cognitivo avanzado, ASA IV |
| Inmunodepresión: diabetes mellitus, toma de medicación corticoidea o inmunosupresora, enfermedad con inmunocompromiso |
Tras el debate que se originó durante la reunión presencial los panelistas decidieron modificar sus opiniones en 17 escenarios (26,56%). El panel de expertos logró un acuerdo en el 67,18% de las indicaciones, considerando adecuadas el 57,81% de las mismas e inadecuadas el 9,37%. El resultado fue indeterminado en el 32,81% de los escenarios, de acuerdo con la normativa RAND.
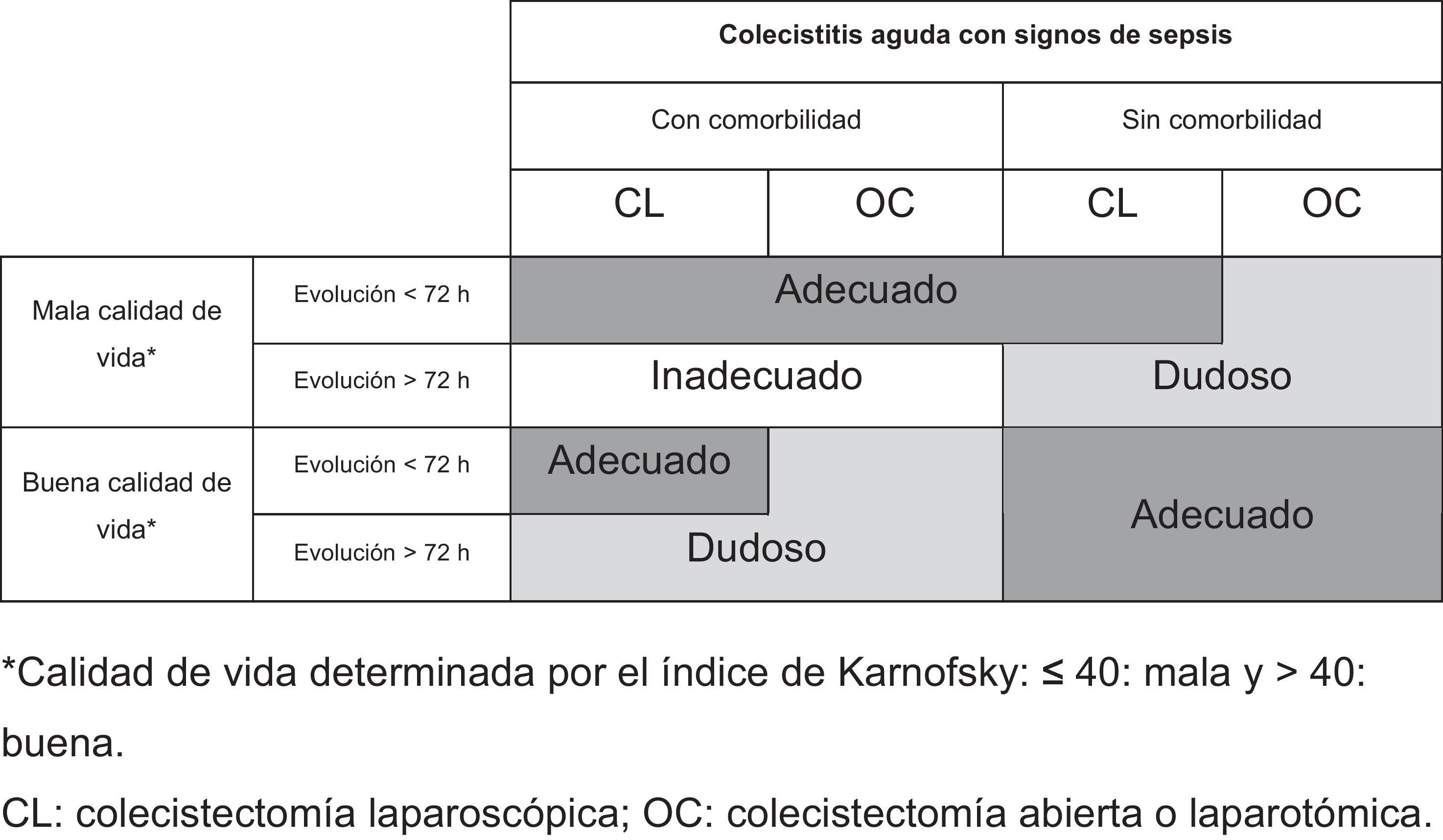
Análisis final de la adecuaciónAdecuación de la colecistectomía laparoscópicaEn pacientes que se presentasen con signos de sepsis, se consideró un tratamiento adecuado para todos cuyos síntomas llevasen menos de 72 h, de forma independiente de la comorbilidad o la calidad de vida previos. Cuando la evolución fuese superior a las 72 h, la indicación se valoró como adecuada solo para pacientes sin comorbilidad y buena calidad de vida previa (tabla 4).
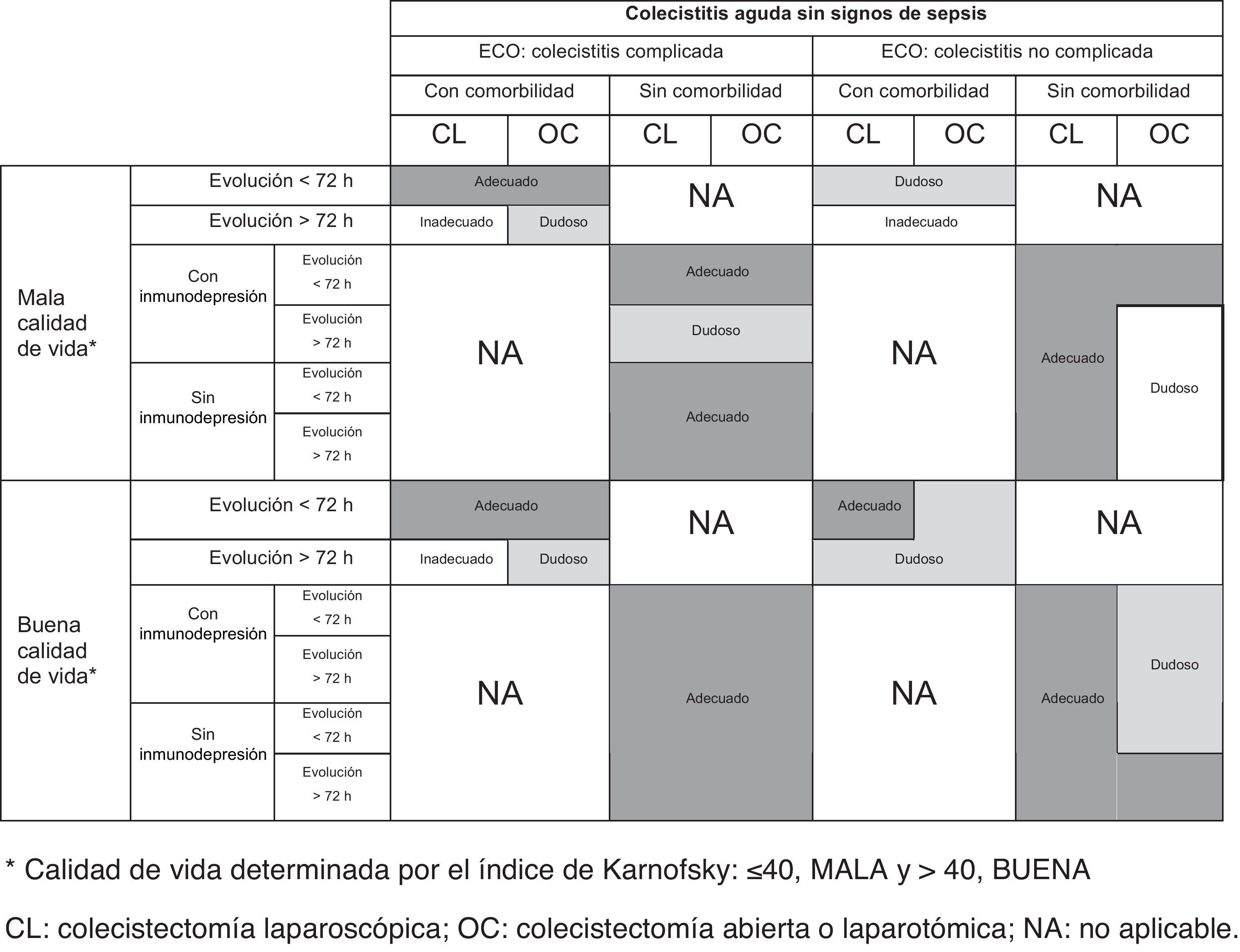
Cuando se presentasen sin sepsis y la ecografía mostrase datos de complicación, la indicación se consideró siempre adecuada cuando los síntomas llevasen menos de 72 h. Con más de 72 h solo fue apropiada para pacientes sin comorbilidad, con mala calidad de vida y sin inmunosupresión, o bien en los que asociasen buena calidad de vida, independientemente de la inmunodepresión. Si en la ecografía no apareciesen datos de complicación, la opción se valoró siempre como adecuada en pacientes sin comorbilidad, sin que influyesen las demás variables. En los que asociasen comorbilidad solo se consideró apropiada para pacientes con buena calidad de vida y menos de 72 h de evolución (tabla 5).
Adecuación de la colecistectomía laparotómicaEn ningún supuesto fue considerada una opción apropiada aislada, como sí ocurrió, a veces, con la CL. Para pacientes presentados con sepsis, se consideró adecuada en aquellos con comorbilidad, mala calidad de vida y una evolución menor a las 72 h, o bien para aquellos sin comorbilidad y buena calidad de vida, independientemente del tiempo de los síntomas (tabla 4).
Para los pacientes que se presentasen sin signos de sepsis y con datos ecográficos de complicación, los escenarios apropiados fueron los mismos que para la CL. Además, la OC se estimó también oportuna en ausencia de datos de complicación ecográfica o comorbilidades, para pacientes con mala calidad de vida, con inmunodepresión asociada y menos de 72 h de clínica, o bien para los de buena calidad de vida, sin inmunodepresión y clínica superior a 72 h (tabla 5).
DiscusiónAntes de la generalización de la laparoscopia, el tratamiento de las CA más aceptado había sido la OC precoz19. Después de imponerse la CL para la colelitiasis sintomática se iniciaron los primeros intentos para la CA, pero la inflamación y la necrosis que suele acompañarla, que añaden una considerable dificultad técnica, hicieron que los resultados no fuesen tan alentadores. Retornaron, así, estrategias terapéuticas en 2 tiempos («enfriamiento» mediante antibióticos y colecistectomía diferida), con la intención de que los pacientes pudiesen beneficiarse aun de las nuevas técnicas de acceso mínimo. La adquisición de experiencia en laparoscopia, los progresos tecnológicos (cámaras y monitores de alta definición, insufladores de alto flujo, calentadores del CO2) y los resultados globales discutibles con las propuestas en 2 tiempos llevaron a que estos planteamientos fuesen reconsiderados. Así, parece ya claro que, de forma general, la CL resulta superior a la OC en términos de costes, mortalidad, estancia hospitalaria, dolor y tamaño de la cicatriz20. De similar forma, parece también claro que la CL precoz frente a la diferida ofrece beneficios en cuanto al acortamiento de las estancias hospitalarias21–23, con porcentaje de complicaciones similares, teniendo en cuenta que también beneficia al grupo de pacientes (20-23%) en los que la evolución clínica resulta desfavorable y obliga a reconsiderar la postura inicial conservadora, sometiendo al paciente a una colecistectomía, no siempre por vía laparoscópica20,21. Sin embargo, estas conceptos han de ser analizados detenidamente, ya que los estudios hacen referencia, mayoritariamente, a la CA llamada «simple». Frente a ella hemos de tener en cuenta otros escenarios, como la presentación en forma de CA «grave» o las circunstancias particulares de algunos pacientes, que pueden, en ocasiones, condicionar una tasa elevada de fracaso de la técnica laparoscópica24. Múltiples factores han sido relacionados con la probabilidad de encontrar una CA «grave» tales como el tiempo de evolución de los síntomas, la coexistencia de comorbilidades, la escasa calidad de vida o los datos desfavorables de los estudios complementarios. De cualquier modo, hay también indicios de que la CL puede ser beneficiosa para algunos de estos pacientes24,25, si bien hasta el momento no han sido definidas las variables que permitan seleccionar a los mejores candidatos.
Hemos empleado el método de análisis de la conveniencia de la corporación RAND/UCLA, que ya ha demostrado su utilidad para establecer los algoritmos de toma de decisiones en temas relacionados con la salud12–17 y que aúna los beneficios de una revisión bibliográfica sistemática con la opinión de expertos. No es un método de consenso, sino que trata de identificar grados de acuerdo o desacuerdo para cada indicación mediante análisis estadístico, identificando también puntos discrepantes.
El acuerdo general del panel del 67,18% evidencia la dificultad que entraña conseguir un consenso en ausencia de una evidencia potente en favor de una u otra opción terapéutica. La mayoría de los publicaciones sobre CA comparan la colecistectomía precoz frente a la tardía3,21,23 o la CL frente a la OC26–28, si bien no abordan situaciones clínicas específicas. Por otra parte, en este estudio no se valora si para un determinado escenario una técnica es superior a otra, sino que se evalúa la pertinencia del empleo de cada técnica individualizada para ese caso concreto.
Para aquellos pacientes presentados con signos de sepsis y una evolución de la clínica inferior a las 72 h existió unanimidad en relación con la pertinencia de la intervención quirúrgica, lo que concuerda con la bibliografía al respecto29. En todos estos casos fue considerada apropiada la CL, mientras que la OC solo fue aceptada en los supuestos de pacientes con comorbilidades y mala calidad de vida o con tan buen estado general (sin comorbilidades y con buena calidad de vida) que el beneficio de la resolución rápida del procedimiento mediante una intervención, en ambos supuestos, aunque no fuese de acceso mínimo, superaría sus potenciales inconvenientes o los de la propia evolución del proceso tratado solo con medidas conservadoras (antibioterapia, colecistostomía percutánea...). La CL por CA grave parece asociarse con una mayor tasa de conversión, aunque suele estar relacionada con la experiencia del cirujano, por lo que debería ser un factor decisivo en la elección de una u otra vía de abordaje26,30. En estas circunstancias, la CL también se ha relacionado con una mayor tasa global de complicaciones, lo que habrá de tenerse en cuenta en pacientes con enfermedad cardiovascular, en los que el neumoperitoneo puede afectar a su estado hemodinámico, si bien el beneficio del acceso mínimo suele justificar su empleo para aquellos que mantengan una hemodinámica estable31. En pacientes con más de 72 h de clínica solo se consideró apropiada la cirugía para los que asociasen comorbilidades y presentasen buena calidad de vida, en sus 2 modalidades (CL y OC) (tabla 6).
Análisis de la adecuación de la cirugía agrupada por escenarios
| Situaciones en las que se consideró adecuada solo la CL |
| - En CA con signos de sepsis: siempre en casos con evolución clínica inferior a 72 h y dependiendo de la comorbilidad asociada |
| ○ Si la tiene, cuando coexiste mala calidad de vida |
| ○ Si no la tiene, cuando la calidad de vida es buena |
| - En CA sin signos de sepsis: cuando la ecografía muestre datos de colecistitis no complicada y teniendo en cuenta las comorbilidades |
| ○ Si las tiene, cuando la calidad de vida es buena y la clínica menor de 72 h |
| ○ Si no las tiene, en función de la calidad de vida previa |
▪ Si es mala, para cualquier paciente con más de 72 h de evolución o para los que lleven menos y no asocien inmunodepresión |
▪ Si es buena, para cualquier paciente con menos de 72 h de evolución o para los que lleven más y asocien inmunodepresión |
| Situaciones en las que se consideraron adecuadas tanto la CL como la OC |
| - En CA con signos de sepsis: |
| ○ Cuando coexisten comorbilidades y mala calidad de vida, siempre que los síntomas lleven menos de 72 h |
| ○ Si no hay comorbilidades y la calidad de vida es buena, independientemente del tiempo de evolución de los síntomas |
| - En CA sin signos de sepsis: |
| ○ Con datos ecográficos de CA complicada, valorando las comorbilidades |
▪ Cuando coexisten, siempre que la evolución de los síntomas sea inferior a 72 h |
▪ Cuando no las hay, para todos los pacientes excepto los que presentan mala calidad de vida, inmunodepresión y una evolución de los síntomas superior a las 72 h |
| ○ Sin datos ecográficos de CA complicada y si no se asocian comorbilidades, dependiendo de la calidad de vida previa |
| • si es mala, cuando coexista inmunodepresión y la evolución sea inferior a 72 h |
| • si es mala, cuando no coexista inmunodepresión y la evolución sea superior a 72 h |
CA: colecistitis aguda; CL: colecistectomía laparoscópica; OC: colecistectomía abierta o laparotómica.
Para los pacientes que inicialmente no presentasen sepsis y la clínica fuese inferior a las 72 h se consideró también apropiada la intervención quirúrgica, exceptuando aquellos con ecografía no complicada, comorbilidades y mala calidad de vida, en los que se consideró dudosa. Esta consideración se debió, probablemente, a que en estos pacientes la colecistostomía32 o los antibióticos podrían considerarse válidos. Fueron apropiadas tanto la CL como la OC, salvo para los casos con ecografía sin complicaciones y buena calidad de vida, en los que la única opción apropiada fue la CL (la OC se consideró dudosa). Este tipo de pacientes se adapta al tipo recogidos por la mayoría de los estudios en los que, desde hace tiempo, quedó demostrado que la CL para CA, dentro de las primeras 72 h desde el inicio de los síntomas, ofrece ventajas importantes. De forma similar, la CL también fue la única opción quirúrgica considerada oportuna para pacientes sin comorbilidades, sin inmunodepresión y sin complicaciones ecográficas asociadas, pero con mala calidad de vida.
En estos mismos casos, sin sepsis asociada, cuando los pacientes presentasen una evolución de los síntomas superior a las 72 h, la indicación quirúrgica fue menos uniforme, considerándose la cirugía inapropiada o dudosa en la mayor parte de supuestos. La CL solo se estimó válida en casos sin complicación ecográfica y sin comorbilidades, pero con mala calidad de vida, o bien con buena calidad de vida e inmunodepresión.
FinanciaciónEste trabajo ha sido financiado por el Ministerio de Sanidad y Consumo Español a través del plan de calidad para el Sistema Nacional de Salud.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Queremos agradecer su colaboración a los miembros del panel de expertos y al moderador de la reunión presencial: Dr. Salvador Rufian Peña (Hospital Reina Sofía, Córdoba, España), Dr. Rafael Bañares Cañizares (Hospital Universitario Gregorio Marañón, Madrid, España), Dr. Antonio Naranjo Rodríguez (Hospital Universitario Reina Sofía, Córdoba, España), Dr. Esteban Cugat Andorrá (Hospital de la Mutua de Terrasa, Barcelona, España), Dr. Juan Ruiz Castillo (Hospital Universitario San Cecilio, Granada, España), Dr. Julio Santoyo Santoyo (Hospital Carlos Haya, Málaga, España), Dr. Eduardo Targarona Soler (Hospital de la Santa Creu y San Pau, Barcelona, España), Dr. Antonio Torres García (Hospital Clínico San Carlos, Madrid, España).