El objetivo del presente trabajo es describir nuestra experiencia en la cirugía del uréter y la vejiga en pacientes con carcinoma de ovario primario y recurrente sometidas a procedimientos de peritonectomía y administración de quimioterapia intraperitoneal intraoperatoria hipertérmica (HIPEC).
Pacientes y métodoSobre una base de datos prospectiva construida al comienzo del programa de carcinomatosis peritoneal en nuestro centro, se seleccionaron aquellas pacientes en las que fue preciso realizar maniobras quirúrgicas sobre uréter distal o la vejiga. Siete pacientes cumplían este requisito y fueron incluidas en el estudio. Desde diciembre de 2007 hasta abril de 2011 fueron incluidas para la realización de citorredución de máximo esfuerzo y HIPEC 81 pacientes diagnosticadas de carcinoma de ovario primario o recurrente.
ResultadosEn siete pacientes, con una mediana de edad de 46 años (40-71), fue necesaria la realización de algún gesto quirúrgico sobre el uréter o la vejiga. Cuatro pacientes fueron intervenidas por recurrencia de la enfermedad ovárica y en otras 3 pacientes la indicación fue el rescate quirúrgico, tras cirugía no óptima en otro centro. En 4 de ellas existía afectación tumoral directa del tracto urinario inferior. Tres pacientes (42%) de la serie desarrollaron al menos una complicación postoperatoria.
ConclusiónLa realización de procedimientos de peritonectomía que incluye la eventual resección del uréter o la vejiga y la posterior aplicación de HIPEC en un grupo seleccionado de pacientes con diseminación peritoneal por carcinoma de ovario puede realizarse con cifras razonables de morbilidad postoperatoria. Estos gestos quirúrgicos pueden ser necesarios para la consecución de una cirugía óptima.
The objective of the present work is to describe our experience in the surgery of the ureter and bladder in patients with primary and recurrent ovarian cancer subjected to peritonectomy procedures and the administration of hyperthermic intraoperative intraperitoneal chemotherapy (HIIC).
Patients and methodThose patients who required surgical procedures on the distal ureter or bladder, were selected from a prospective data base constructed at the beginning of the peritoneal carcinomatosis program in our centre. Seven patients fulfilled this requirement and were included in the study. A total of 81 patients diagnosed with primary or recurrent ovarian cancer from December 2007 to April 2011 were included for maximum effort cytoreduction and HIIC.
ResultsIt was necessary to perform some surgical manoeuvre on the ureter or bladder in seven patients, with a median age of 46 years (40-71). Four patients were operated on due to recurrence of the ovarian disease and in the other 3 patients the indication was surgical rescue after non-optimal surgery in another centre. There was direct tumour involvement of the lower urinary tract in 4 of them. Three patients (42%) in the series developed at least one postoperative complication.
ConclusionThe performing of peritonectomy procedures that include the eventual resection of the ureter or bladder, and the subsequent application of HIIC in a selected group of patients with peritoneal dissemination due to an ovarian carcinoma can be done with reasonable rates of postoperative morbidity. These surgical procedures may be necessary to achieve optimal surgery.
El tratamiento locorregional de la carcinomatosis peritoneal (CP) en pacientes seleccionados con neoplasias gastrointestinales y ginecológicas ha experimentado en las dos últimas décadas un avance importante. La utilización de quimioterapia intraperitoneal intraoperatoria hipertérmica (HIPEC) tras la realización de procedimientos extensos de citorreducción quirúrgica ha conseguido supervivencias superiores al 90% a los 5 años en pacientes con pseudomixoma peritoneal1 y superiores al 60% en pacientes con mesotelioma peritoneal2. En la diseminación peritoneal del cáncer de colon, tratada con citorreducción e HIPEC Verwaal et al publicaron en 2003 y revisaron los resultados posteriormente en 2008, el único estudio prospectivo y aleatorizado concluido que existe en la actualidad. En este estudio se comunicó una mejora en la supervivencia libre de enfermedad y global a favor de las pacientes tratadas con cirugía e HIPEC, en comparación con el grupo de pacientes tratadas convencionalmente con quimioterapia sistémica con intención paliativa, sin cirugía3. Otro estudio prospectivo y aleatorizado llevado a cabo por Elías et al, con quimioterapia intraperitoneal postoperatoria precoz (EPIC) no pudo ser concluido ya que los pacientes seleccionados se negaban a formar parte del estudio ante la posibilidad de recaer por el azar en el grupo de tratamiento convencional, que no incluía la quimioterapia intraperitoneal, lo que llevó a suspenderse tras el reclutamiento de 35 pacientes. A pesar de ello este estudio sirvió para poner de manifiesto la superioridad del tratamiento intraperitoneal frente al esquema estándar, basado en una actitud abstencionista y quimioterapia paliativa4,5.
En pacientes con carcinoma de ovario avanzado, primario o recurrente, no existe en la actualidad ningún estudio prospectivo y aleatorizado que demuestre que usar HIPEC tras una citorreducción óptima sea superior a no hacerlo y los trabajos publicados hasta la actualidad ofrecen una gran heterogeneidad en cuanto al tipo de pacientes incluidos así como en el esquema utilizado durante la HIPEC. No obstante, los resultados obtenidos son esperanzadores, con supervivencias superiores al 60% a los 5 años de seguimiento6.
La realización de resecciones gástricas7, hepáticas8,9 y pancreáticas10 durante la citorreducción previa al tratamiento con HIPEC ha sido descrita con aceptables tasas de morbimortalidad. La experiencia respecto a la cirugía del tracto urinario en pacientes con carcinomatosis peritoneal es escasa11. En carcinoma de ovario avanzado primario o recurrente, hasta un 5% de las pacientes pueden necesitar cirugía de resección del uréter distal o la vejiga durante la cirugía.
El objetivo del presente trabajo es describir nuestra experiencia en la cirugía del uréter y la vejiga en pacientes con carcinoma de ovario primario y recurrente sometidas a procedimientos de peritonectomía y administración de HIPEC.
Pacientes y métodoDesde diciembre de 2007 hasta abril de 2011 fueron incluidas para la realización de citorredución de máximo esfuerzo e HIPEC 81 pacientes diagnosticadas de carcinoma de ovario primario o recurrente. Todas las pacientes fueron evaluadas e intervenidas por el mismo equipo quirúrgico. Se realizó estudio de extensión preoperatorio de la enfermedad con TAC torácica y abdominal. La realización de un PET se restringió a los casos en los que existían dudas acerca de la presencia de enfermedad extraperitoneal. Se incluyeron para la realización de dicho procedimiento pacientes con buena situación basal, (ECOG performance status 0-2), adecuada función cardiaca, renal, hepática y hematológica y con enfermedad peritoneal a priori resecable en función de las pruebas de imagen preoperatorias. Sobre una base de datos prospectiva construida al comienzo del programa de carcinomatosis peritoneal en nuestro centro, se seleccionaron aquellas pacientes en las que fue preciso realizar maniobras quirúrgicas sobre uréter distal o la vejiga. Siete pacientes cumplían este requisito y fueron incluidas en el estudio.
Protocolo quirúrgico y manejo postoperatorioBajo anestesia general, se practicó una cistostopia con cateterización de ambos uréteres en quirófano. El protocolo quirúrgico incluyó una laparotomía amplia xifopúbica, valorándose la extensión de la enfermedad peritoneal. La estadificación del grado de extensión tumoral en la cavidad abdominal se realizó según el índice de carcinomatosis peritoneal (PCI) de Sugarbaker. En todas las pacientes se siguió la misma sistemática quirúrgica, comenzando la cirugía en la región pélvica, practicando una pelviperitonectomía que incluía el útero y ambos anejos si estos no habían sido extirpados previamente, así como el fondo de saco de Douglas. Si el rectosigma estaba afecto, también se procedió a su resección en bloque con anastomosis colorrectal mecánica. El uso de ostomías de protección de las anastomosis colorrectales quedó restringido a pacientes con resección rectal baja. Posteriormente se realizó la citorreducción del resto de la cavidad peritoneal, practicando sistemáticamente una omentectomía supramesocólica completa. La linfadenectomía pélvica y paraaórtica se reservó a pacientes con enfermedad ganglionar macroscópica sospechosa en la TAC preoperatoria o en aquellas pacientes en las que se confirmó con biopsia intraoperatoria mediante cortes por congelación la presencia de ganglios afectos. Tras evaluar el grado de afectación del tracto urinario, se procedió a la resección del uréter o la vejiga en aquellos casos en los que era posible conseguir una citorreducción óptima del resto de la cavidad peritoneal. La realización de una anastomosis ureteroureteral termino-terminal o una ureteroneocistostomía quedó tutorizada sistemáticamente por un catéter doble J. La apertura accidental de la vejiga durante las maniobras de disección fue resuelta con sutura continua de la misma en 3 planos con material reabsorbible. Una sonda vesical se mantuvo durante 15 días para minimizar los efectos del reflujo vesicoureteral y reducir la tensión de las suturas por la distensión vesical. Se utilizó un drenaje abdominal en la pelvis. El resultado de la citorreducción se evaluó en función del Completeness Cytoreductive Score (CCS) de Sugarbaker, considerando la cirugía óptima CC-0 cuando tras la citorreducción de la cavidad peritoneal no quedó ningún residuo tumoral macroscópico y óptima CC-1 si el residuo tumoral al final de la cirugía era menor de 2,5mm en su diámetro mayor. La aplicación de HIPEC solamente se contempló en aquellos casos en los que se consiguió la cirugía óptima CC-0 y CC-1. Los catéteres ureterales se retiraron antes de la salida de la paciente del quirófano.
Quimioterapia intraperitoneal intraoperatoria hipertérmicaSe utilizó como citostático intraperitoneal el paclitaxel, a dosis de 60 mg/m2 de superficie corporal. El uso de cisplatino a dosis de 75 mg/m2 de superficie corporal se indicó cuando la paciente había desarrollado previamente alergias a taxanos durante la quimioterapia sistémica previa12,13. El citostático se diluyó para su perfusión en 3 litros de líquido de diálisis (Dialisan®). Tras la citorreducción se posicionó la cavidad peritoneal según la técnica del «coliseum», manteniéndose en el circuito de perfusión un flujo constante de 0,5-0,7 l/min durante 60 min. Dos termómetros intraabdominales monitorizaron la temperatura dentro de la cavidad peritoneal durante la perfusión, que se mantuvo constante entre 42-43°C. Se utilizó un termómetro esofágico para monitorizar la temperatura central de la paciente.
Morbilidad postoperatoriaLos datos referentes a la morbimortalidad fueron recogidos de forma prospectiva. Los eventos adversos fueron clasificados de acuerdo con los criterios de toxicidad del Instituto Nacional del Cáncer Comon Toxicity Criteria (versión 3.0). Se consideraron complicaciones menores aquellas que precisaron para su resolución tratamiento médico (grado II) y complicaciones moderadas aquellas que precisaron procedimientos invasivos, como un drenaje percutáneo guiado por ECO/TAC, colocación de un tubo de drenaje pleural o endoscopia terapéutica (grado III). Las complicaciones graves (grado IV) precisaron para su resolución una nueva intervención quirúrgica o el ingreso de la paciente en UCI.
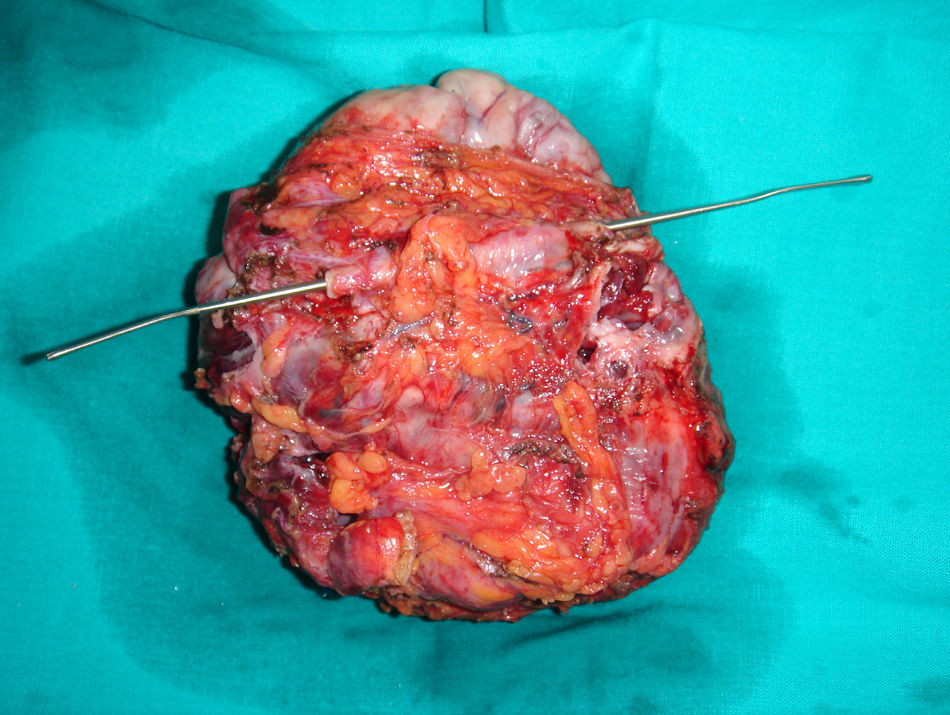
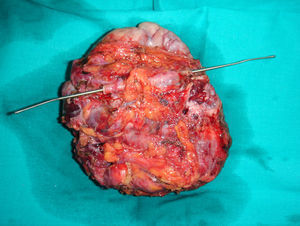
ResultadosEn siete pacientes, con una mediana de edad de 46 años (40-71), fue necesaria la realización de algún gesto quirúrgico sobre el uréter o la vejiga. Cuatro pacientes fueron intervenidas por recurrencia de la enfermedad ovárica, otras 2 pacientes la indicación fue el rescate quirúrgico y en una paciente se administró quimioterapia sistémica neoadyuvante previa a una primera cirugía citorreductora (cirugía de intervalo). En 4 de ellas existía afectación tumoral directa del tracto urinario inferior (fig. 1). Esta última paciente presentaba, previamente a ser remitida a nuestro centro, una ligadura iatrogénica del uréter izquierdo acontecida durante la realización de una laparotomía diagnóstica previa en otro hospital. En esta paciente, la ligadura pasó inadvertida durante la cirugía inicial y fue descubierta en el postoperatorio, precisando la colocación de una nefrostomía percutánea. Ninguna de las pacientes con afectación tumoral del uréter o la vejiga presentaba sintomatología urinaria preoperatoria. En las restantes dos pacientes se produjo una apertura accidental de la vejiga durante las maniobras de disección pélvica, que se resolvió intraoperatoriamente. El tipo de cirugía realizada en cada paciente está reflejada en la tabla 1. Los datos referentes a la edad, indicación quirúrgica, PCI, resultado tras la citorreducción, morbilidad postoperatoria, tiempo de seguimiento y estado actual de las pacientes incluidas en la serie están reflejadas en la tabla 2.
Tipo de cirugía practicada y gestos quirúrgicos realizados sobre el uréter o la vejiga de la orina en las pacientes de nuestra serie
| Paciente | Cirugía | Cirugía sobre uréter/vejiga |
| 1 | Peritonectomía completa, omentectomía mayor y menor, resección de rectosigma y citorreducción del meso del intestino delgado | Apertura accidental de la vejiga. Cierre simple |
| 2 | Pelviperitonectomía, omentectomía, peritonectomía diafragmática derecha, resección 100 cm de yeyuno distal e íleon proximal, esplenectomía y citorreducción del meso del intestino delgado | Resección parcial de cúpula vesical. Cierre simple |
| 3 | Pelviperitonectomía, omentectomía, peritonectomía diafragmática derecha, hemicolectomía derecha, colecistectomía y citorreducción del meso del intestino delgado | Apertura accidental de la vejiga. Cierre simple |
| 4 | Pelviperitonectomía, omentectomía y citorreducción del meso del intestino delgado. Resección de implante en antigua cicatriz | Resección 5 cm uréter distal. Ureteroneocistostomía (fig. 1) |
| 5 | Pelviperitonectomía. Linfadenectomía pélvica derecha, omentectomía | Resección parcial extramucosa uréter derecho. Colocación de catéter doble J para proteger la pared del uréter |
| 6 | Pelviperitonectomía, omentectomía, peritonectomía diafragmática derecha, colecistectomía | Resección parcial de cúpula vesical. Cierre simple |
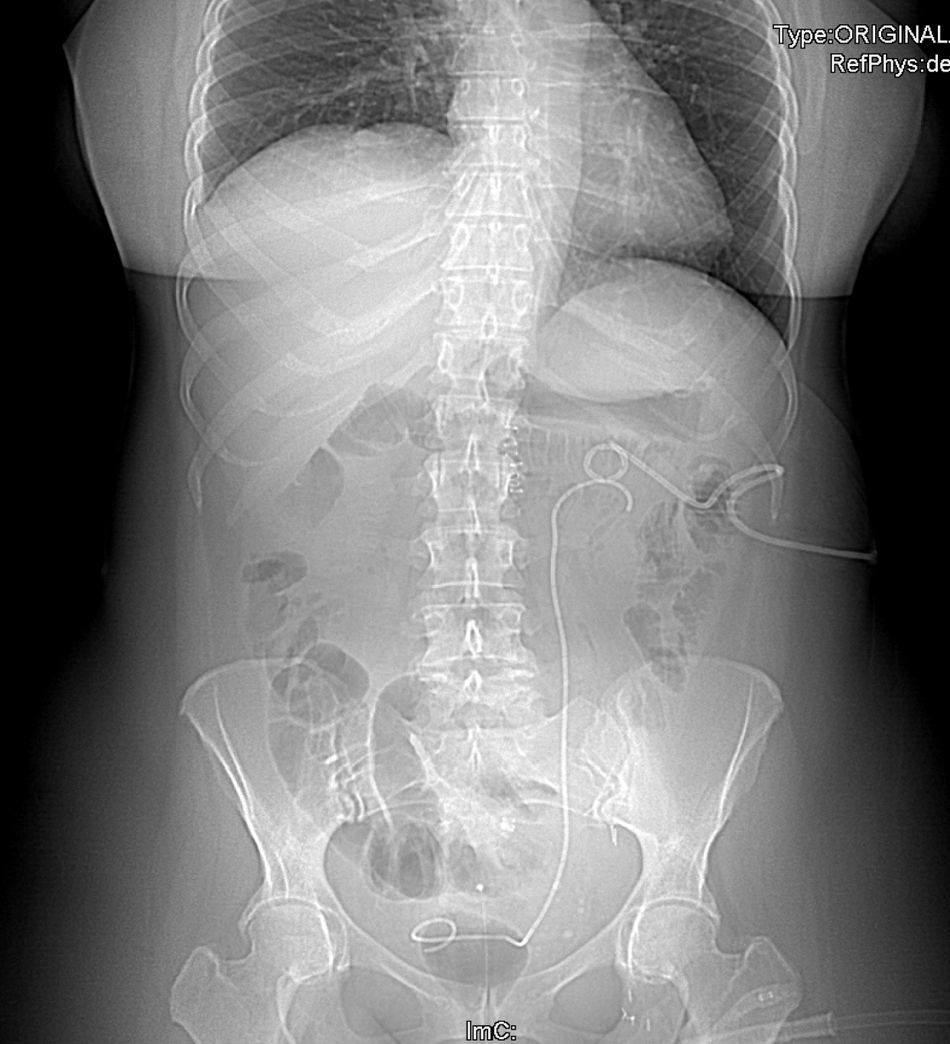
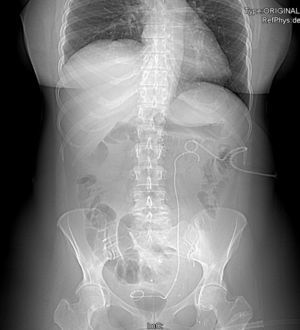
| 7 | Peritonectomía completa, histerectomía y doble anexectomía, colectomía subtotal, citorreducción del meso del intestino delgado, colecistectomía, esplenectomía. | Identificación de porción del uréter ligado, resección segmentaria con anastomosis ureteroureteral termino-terminal tutorizada con catéter doble J (fig. 2) |
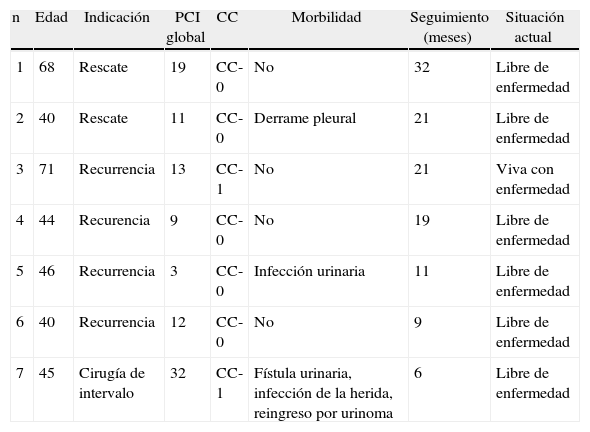
Edad, tipo de cirugía, índice de carcinomatosis peritoneal global, resultados tras la citorreducción, morbilidad postoperatoria, tiempo de seguimiento y estado actual de las pacientes incluidas en la serie
| n | Edad | Indicación | PCI global | CC | Morbilidad | Seguimiento (meses) | Situación actual |
| 1 | 68 | Rescate | 19 | CC-0 | No | 32 | Libre de enfermedad |
| 2 | 40 | Rescate | 11 | CC-0 | Derrame pleural | 21 | Libre de enfermedad |
| 3 | 71 | Recurrencia | 13 | CC-1 | No | 21 | Viva con enfermedad |
| 4 | 44 | Recurencia | 9 | CC-0 | No | 19 | Libre de enfermedad |
| 5 | 46 | Recurrencia | 3 | CC-0 | Infección urinaria | 11 | Libre de enfermedad |
| 6 | 40 | Recurrencia | 12 | CC-0 | No | 9 | Libre de enfermedad |
| 7 | 45 | Cirugía de intervalo | 32 | CC-1 | Fístula urinaria, infección de la herida, reingreso por urinoma | 6 | Libre de enfermedad |
Tres pacientes de la serie desarrollaron al menos una complicación postoperatoria. Una paciente desarrolló un derrame pleural cuantioso, secundario a la peritonectomía diafragmática practicada y fue necesaria la colocación de un drenaje torácico. Aparecieron 2 complicaciones urinarias, una complicación grado II (infección urinaria en una paciente) y otra de grado III (fístula urinaria), esta última en la paciente con ligadura iatrogénica del uréter en la que se practicó una anastomosis ureteroureteral (fig. 2). Esta última paciente desarrolló además una infección de la herida quirúrgica. Aunque la pieloureterografía percutánea a través de la nefrostomía demostró la ausencia de fuga en el postoperatorio previo al alta hospitalaria, fue necesario el reingreso de la misma por fiebre, detectándose en la TAC practicada de forma urgente, la presencia de una colección adyacente a la anastomosis ureteral compatible con urinoma. Dicha colección fue resuelta con la colocación de un drenaje radiológico, cesando progresivamente la emisión de orina por el mismo, siendo posible posteriormente su retirada. La fístula urinaria se resolvió de forma conservadora manteniendo la nefrostomía abierta durante 40 días, pudiendo proceder a su retirada tras la comprobación mediante urografía directa a través de la propia nefrostomía de la ausencia de fuga del contraste.
DiscusiónDesde la descripción por parte de Sugarbaker12 del tratamiento quirúrgico con intención curativa de la carcinomatosis peritoneal mediante la realización de procedimientos extensos de peritonectomía y administración intraoperatoria de HIPEC el manejo de los pacientes con enfermedad maligna peritoneal por carcinomatosis colorrectal3–5, pseudomixoma peritoneal1 y mesotelioma peritoneal2 ha sufrido un giro de 180 grados. Este procedimiento se ha aplicado con creciente frecuencia también en pacientes con diseminación peritoneal de origen ovárico7,9. El esquema terapéutico difundido por Sugarbaker propone una máxima citorreducción quirúrgica, que elimina la enfermedad macroscópica, acompañada en el mismo acto operatorio de la administración de HIPEC con el objetivo de erradicar la enfermedad microscópica diseminada, causante de las recidivas detectadas en el seguimiento de las pacientes10.
En carcinoma de ovario avanzado, todavía no existe ningún trabajo prospectivo y aleatorizado publicado que demuestre con suficiente nivel de evidencia, que el asociar HIPEC tras una citorreducción de máximo esfuerzo mejora los resultados respecto a no hacerlo. No obstante, los buenos resultados comunicados en la literatura hacen que la indicación en esta afección crezca con fuerza en la actualidad14. La comunidad científica actual acepta la máxima citorreducción quirúrgica como piedra angular del tratamiento del carcinoma de ovario avanzado, primario o recurrente12,14. La afectación del diafragma, el hilio hepático, la afectación difusa de la serosa del intestino delgado y la afectación de la raíz del mesenterio son los principales obstáculos para conseguir una citorreducción óptima15–17. Se han descrito tasas de afectación diafragmática del 42% de casos en los que la enfermedad está limitada en la pelvis y hasta en un 71% de los casos en los que hay enfermedad fuera de la pelvis en áreas diferentes al diafragma17. La cirugía sobre el uréter y la vejiga, por su localización anatómica, es necesaria hasta en un 5% de las pacientes intervenidas.
La experiencia comunicada tras citorreduccción e HIPEC en la resección del tracto urinario (uréter y vejiga) es escasa. Sugarbaker comunicó el uso de la transureteroureterostomía con razonables tasas de morbilidad en 11 pacientes con carcinomatosis peritoneal tratadas con citorreducciones quirúrgicas extensas e HIPEC18. Smeenk comunicó 7 casos en los que existía compromiso del tracto urinario en pacientes con pseudomixoma peritoneal tratadas con citorreducción e HIPEC11. Entre los factores de riesgo para presentar compromiso tumoral del tracto urinario se han descrito la presencia de una intensa afectación tumoral en la pelvis y el haber sido sometidas a cirugía pélvica previamente, lo que habría determinado una diseminación tumoral al retroperitoneo. En referencia a los trabajos publicados en carcinoma de ovario tratado con citorreducción e HIPEC, estos incluyen la resección del uréter y la vejiga en el cómputo global de los procedimientos quirúrgicos comunicados en cada serie (tabla 3)19–21.
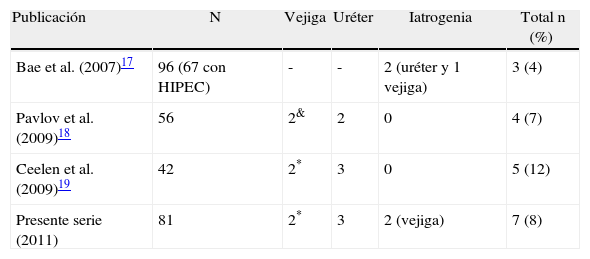
Procedimientos quirúrgicos sobre uréter y vejiga durante cirugía citorreductora y quimioterapia intraperitoneal intraoperatoria hipertérmica en pacientes con carcinoma de ovario avanzado y recurrente
| Publicación | N | Vejiga | Uréter | Iatrogenia | Total n (%) |
| Bae et al. (2007)17 | 96 (67 con HIPEC) | - | - | 2 (uréter y 1 vejiga) | 3 (4) |
| Pavlov et al. (2009)18 | 56 | 2& | 2 | 0 | 4 (7) |
| Ceelen et al. (2009)19 | 42 | 2* | 3 | 0 | 5 (12) |
| Presente serie (2011) | 81 | 2* | 3 | 2 (vejiga) | 7 (8) |
*Resección parcial; &exenteración pélvica.
Tras la resección del uréter, la técnica utilizada para la restauración del flujo urinario dependerá de múltiples factores: el grado funcional de ambos riñones, la localización en la que el uréter se encuentra comprometido, las características anatómicas del uréter contralateral y el grado de afectación de la vejiga. Los principios que deben regir la técnica reconstructiva continúan siendo la escisión completa de lesiones patológicas, la seguridad del aporte vascular del uréter, el drenaje correcto y la realización de la anastomosis con el uréter espatulado y libre de tensión uniendo mucosa con mucosa22. Cuando la lesión ureteral se encuentra por debajo del cruce del uréter con la arteria ilíaca común, existen numerosas alternativas para la resolución de la continuidad del flujo urinario. En general, se debe intentar evitar la anastomosis termino-terminal del uréter, dado el mayor índice de complicaciones que presenta posteriormente, fundamentalmente la estenosis. A menudo es preferible el reimplante ureteral a vejiga realizando una vejiga psoica (psoas hitch) si el cabo del uréter se encuentra por debajo del cruce de los vasos ilíacos o utilizando un colgajo de vejiga (Boari) si se encuentra por encima de estos. En otras ocasiones el extremo ureteral puede ser suficientemente caudal como para permitir un reimplante tras la liberación de la vejiga sin tener que realizar otra manipulación de esta. En caso de lesiones de los tercios medio y superior del uréter (por encima de la pelvis) si el defecto es pequeño pueden ser reparadas mediante ureteroureterostomía termino-terminal espatulada y en caso de pérdidas extensas de uréter con otras medidas como la movilización del riñón, la transureteroureterostomía, el autotrasplante y la sustitución con intestino delgado puden ser necesarias23. Creemos que después de estos procedimientos es imprescindible el uso de un catéter doble J. La opción de la transureteroureterostomía o cruce ureteral cobra además especial importancia en lesiones altas con radioterapia pélvica previa18. La interposición de un asa de intestino delgado (ileocistoplastia) es preferible en pacientes en las que además del uréter se asocia una resección extensa de la vejiga o existe riesgo de una vejiga de escasa capacidad por el volumen resecado de la misma.
En conclusión, la realización de procedimientos de peritonectomía que incluye la resección del uréter o la vejiga cuando es necesaria y la posterior aplicación de HIPEC en pacientes con diseminación peritoneal por carcinoma de ovario avanzado puede realizarse con cifras razonables de morbilidad postoperatoria. Estos gestos quirúrgicos pueden ser necesarios para la consecución de una cirugía óptima.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.