Introducción
El hallazgo de gas venoso portal (GVP) está asociado tanto a condiciones benignas como a otras potencialmente letales que precisan cirugía. El gas venoso portal intrahepático (GVPH) fue descrito por primera vez en neonatos con enterocolitis necrosante en 1955 por Wolf y Evans1. En 1960 Susman y Senturia describieron el primer caso en adultos2. Desde entonces, el número de casos publicados ha ido en aumento debido a la mejora de los métodos diagnósticos que incluyen la tomografía computarizada (TC) y la ecografía3-8. El GVPH se puede asociar con isquemia intestinal (43%), con unas tasas de supervivencia global de entre el 25 y el 44% debido a la severidad del proceso, así como con una amplia variedad de procesos no isquémicos2-5,9 que presentan unas tasas de mortalidad < 29%10,11. Se hace una revisión de la bibliografía para definir el significado clínico del hallazgo de gas en el territorio venoso portal, así como el papel que juega la laparotomía exploradora urgente.
Etiología
En el adulto, la existencia de gas en el territorio venoso portal se ha descrito asociado con una amplia variedad de entidades clínicas (tabla 1)3,5,7,12-24, entre las más frecuentes hay que destacar la isquemia intestinal (43%), la dilatación del tracto digestivo (12%), los abscesos intraabdominales o retroperitoneales (11%)12 y la enfermedad inflamatoria intestinal (8%)13. En el niño se han descrito, en la enterocolitis necrosante, algunas malformaciones gastrointestinales como la enfermedad de Hirschprung24 y la cateterización de la vena umbilical13,15.
La tasa de mortalidad varía según el proceso subyacente, y puede alcanzar hasta un 75% en el caso de isquemia intestinal, que varía según el grado y extensión de la necrosis3,4,7,16,25,26. Existe una serie de condiciones no letales, como la enfermedad de Crohn no complicada, la pancreatitis, los traumatismos abdominales16,17,27,28 y las complicaciones de procedimientos endoscópicos que pueden manejarse mediante tratamiento conservador5,19,29-32; sin embargo, otras como la enfermedad inflamatoria intestinal severa, la obstrucción intestinal con estrangulación, las lesiones traumáticas de estructuras vasculares intestinales32 y los tumores3,33 precisan un tratamiento quirúrgico. La supervivencia en los casos potencialmente letales depende del tratamiento adecuado de la enfermedad de base asociada con el GVPH3,5,24.
Fisiopatología
La etiopatogenia del GVPH no está del todo aclarada y para ello habría que responder a 2 consideraciones, origen del gas y vía de llegada al sistema venoso portal34. El gas se compone de una mezcla variable de aire ingerido, gases intestinales, como metano, hidrógeno, dióxido de carbono o nitrógeno, y gases producto del metabolismo bacteriano intestinal8. Tanto un incremento de presión en el interior de la luz intestinal, como ocurre tras un traumatismo abdominal severo17, una endoscopia o una obstrucción intestinal, como una alteración de la barrera mucosa, en el caso de un carcinoma o una ingestión por cáusticos8, puede permitir que el gas diseque la pared y que entre en el sistema portal a través de las venas mesentéricas2-5,13,16,29,32. Estos 2 mecanismos fueron demostrados por Shaw et al2,35 en 1967 en un modelo canino. Cualquier cambio en la barrera mucosa, como puede suceder en la enfermedad de Crohn, en una úlcera gástrica, en una inmunodeficiencia congénita o adquirida, o bien tras una terapia inmunosupresora o citotóxica, puede llevar a una alteración de la pared de los vasos y del tejido circundante que evite su colapso y que facilite la entrada de aire6,16,34,36.
Un tercer mecanismo es mediado por bacterias formadoras de gas, fundamentalmente de tipo Clostridium, que son especialmente capaces de crecer y sobrepasar la submucosa a través de pequeños defectos mucosos en un intestino isquémico o infartado2,3,21,37-39.
El GVPH puede ir asociado a neumatosis intestinal13, un hallazgo radiológico descrito por primera vez por Du Vernoi en 173040, y que se caracteriza por la acumulación de gas en la pared intestinal. Se trata de un indicio más que de un diagnóstico definitivo, que sugiere la presencia de una patología intraabdominal severa como una enterocolitis necrosante34,41 pero que no tiene un valor predictivo de su severidad2,4,34, y se ha asociado con isquemias reversibles2,4,6,16,40,42.
Se ha descrito asociación de gas en la vena porta con gas en las venas cava superior e inferior, mesentérica superior e inferior, hemorroidal e ilíaca interna2,43. Según Mallens et al43, una cantidad importante de gas puede causar una obstrucción temporal de los sinusoides portales y un cortocircuito portosistémico. También se ha observado ecográficamente el paso del gas a tiempo real desde la vena porta a través del hígado hasta la circulación sistémica44.
Se han observado numerosos casos de gas en la vena porta intrahepática transitorios, sin consecuencias clínicas (enfermedad inflamatoria intestinal, dilatación aguda gástrica, traumatismo violento abdominal, tras inserción de catéteres de yeyunostomía)2,9,43.
Diagnóstico
La imagen de GVPH puede verse en una radiografía convencional, mediante ultrasonografía o TC7,13,45. La radiografía abdominal simple puede detectar grandes cantidades de GVPH o gas intestinal intramural, pero su eficacia es inferior a la de la ecografía o TC, las cuales permiten una detección precoz de pequeñas cantidades de gas en el tracto portal2,46. El hallazgo de GVPH en una radiografía simple sugiere un mal pronóstico y se asocia comúnmente con isquemia intestinal5,8,46. Esta prueba es más sensible si se realiza con el paciente en decúbito lateral izquierdo2,4,5.
En la ecografía, el GVPH aparece como numerosas y pequeñas imágenes hiperecogénicas con sombra acústica intermitente2,5,8,13,25,46-48. El gas, dentro del sistema venoso portal, tiene un flujo sanguíneo centrífugo que aparece en la periferia hepática y se extiende hasta 2 cm de la cápsula hepática. Por el contrario, el gas en el tracto biliar sigue una dirección centrípeta que aparece más centralmente en el hígado5,13,30. La ultrasonografía da una información adicional a tiempo real que permite la observación del desplazamiento hepatófugo o hepatópeto2,49, y el diagnóstico es más difícil cuando existe hipertensión portal debido al desplazamiento más lento de las burbujas aéreas hasta la periferia hepática2,50. Es importante hacer un diagnóstico diferencial ante una historia de anastomosis biliodigestiva previa, papilotomía endoscópica, endoprótesis biliar o fístula coledocointestinal2,51.
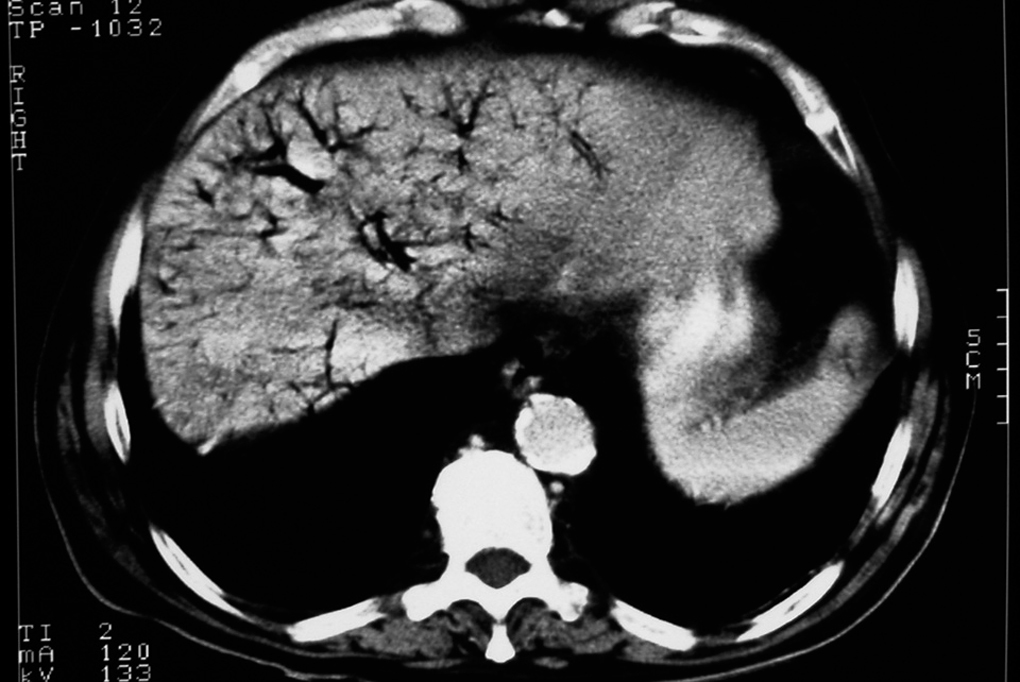
La TC abdominal da el diagnóstico en la mayoría de los casos donde el GVPH aparece como ramificaciones hipodensas en la periferia subcapsular hepática, fundamentalmente en el lóbulo izquierdo5,7,30 (fig. 1), y es capaz de detectar pequeñas cantidades de gas, lo que permite un tratamiento quirúrgico precoz5,31. La TC abdominal con contraste tiene una sensibilidad del 64% y una especificidad del 92% en el diagnóstico de isquemia intestinal26,52. Los signos intestinales de necrosis son más específicos con la TC que con la ecografía. En caso de necrosis intestinal el gas generalmente produce una imagen de microburbujas, mientras que en los casos inocuos puede ser lineal o arracimada, más grande y más esférica2. Sin embargo, estos signos no son específicos. El uso de la ventana pulmonar complementaria en la TC abdominal puede ser valioso cuando se sospecha neumatosis intestinal2,53.
Fig. 1. Tomografía computarizada en la que se observa la presencia de gas en el árbol portal.
En ausencia de una indicación clínica para una laparotomía urgente, la angiografía mesentérica es la prueba de elección ante la sospecha de isquemia mesentérica aguda26,52.
Tratamiento
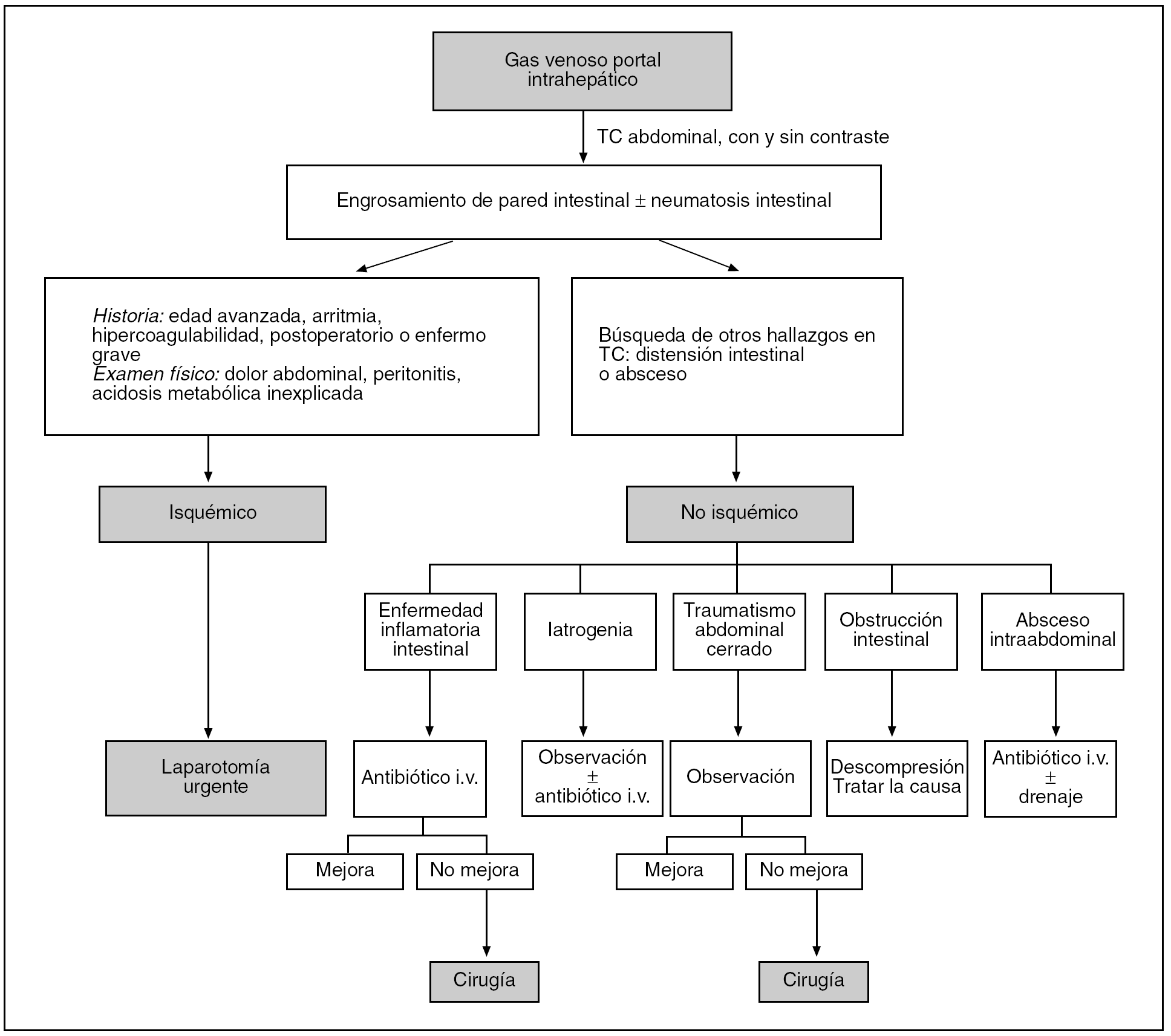
La presencia de factores predisponentes, como la edad, la arritmia cardíaca, un estado de hipercoagulabilidad, un postoperatorio o una situación de enfermedad grave, junto con una clínica de dolor abdominal, con o sin signos de irritación peritoneal o acidosis metabólica inexplicada, pueden alertar sobre la sospecha de una isquemia mesentérica26. Por ello, estará indicada una laparotomía exploradora en todo paciente en el que se sospeche una isquemia intestinal en base a los diferentes hallazgos radiológicos y clínicos2,5,29. El pronóstico viene determinado por la extensión del infarto transmural y la demora entre el diagnóstico y el tratamiento2,3,5,32, de forma que la supervivencia puede ser de hasta un 50% cuando el diagnóstico se realiza dentro de las primeras 24 h o < 30% cuando se retrasa26,52. Por otra parte, se podrá evitar una laparotomía exploradora en todas las condiciones no isquémicas asociadas con una evolución clínica favorable, a excepción de algunas entidades como la enfermedad inflamatoria intestinal complicada, la obstrucción intestinal con estrangulación o los traumatismos intestinales con lesión vascular, en cuyo caso será preciso una intervención quirúrgica urgente. En la figura 2 se expone un algoritmo de decisión para el diagnóstico y tratamiento de los pacientes con gas venoso portal intrahepático.
Fig. 2. Algoritmo de diagnóstico y tratamiento para pacientes con hallazgo radiológico de gas venoso portal intrahepático. TC: tomografía computarizada; i.v.: intravenoso.
Conclusiones
El reconocimiento de GVPH en el adulto no es por sí mismo un factor predictivo de mortalidad8,54,55. Además, no hay una correlación directa entre la cantidad de GVPH y la mortalidad. Se trata de un signo radiológico más que diagnóstico3,5,13. Cuando se detecta GVPH, es importante diferenciar una isquemia mesentérica grave, con tasas de mortalidad que alcanzan el 56%13,56, de otras causas no isquémicas más benignas57. Para ello, la TC puede revelar una serie de signos que incluyen engrosamiento de pared, hematoma intramural, dilatación de asas intestinales llenas de líquido, neumatosis intestinal34, edema mesentérico, ascitis, presencia de gas venoso mesentérico y portal o tromboembolia mesentérica arterial o venosa26,52. Sin embargo, la mayoría de estos hallazgos no son específicos y deben ocurrir en asociación con una sospecha clínica de isquemia mesentérica para que puedan considerarse significativos.
Correspondencia: Dr. L.A. Magrach Barcenilla.
Servicio de Cirugía General y Aparato Digestivo.
Hospital Santiago Apóstol.
Olaguibel, 29. 01004 Vitoria. Álava. España.
Correo electrónico: lmagrach@euskalnet.net
Manuscrito recibido el 22-11-2004 y aceptado el 19-10-2005.