La perforación tardía del miocardio (PTM) secundaria a un electrodo de un dispositivo electrónico cardiaco implantable (DECI) es infrecuente1,5. El manejo en este escenario no está unificado en la literatura actual. El presente trabajo tiene como objetivo presentar nuestra experiencia en cinco pacientes.
MétodosSe reclutaron todos los pacientes desde enero de 2018 hasta octubre de 2020 con el diagnóstico de PTM secundario a un DECI. Se consideró PTM cuando el evento se produjo 15días posterior al implante del dispositivo, previa constatación de migración del electrodo mediante pruebas de imagen respecto a su ubicación inicial.
ResultadosPresentamos una serie de 5 pacientes con una edad media de 79 años (DE7), 3 varones, con una mediana de 47días hasta la perforación. Las características basales de los pacientes, dispositivo, indicación del implante y clínica se exponen en la tabla 1.
Características de los pacientes, de los dispositivos y de la presentación clínica
| Caso | Edad | Sexo | Indicación de implante | Dispositivo | Tipo de fijación | Sitio de estimulación y perforación | Tiempo trascurrido hasta el diagnóstico (días) | Signo o síntoma principal |
|---|---|---|---|---|---|---|---|---|
| 1 | 72 | Varón | MI con FEVI <30% | DAI-TRC | Activo | Ápex VD | 30 | Taponamiento cardiaco |
| 2 | 88 | Varón | Bloqueo A-V | MP bicameral | Activo | Ápex VD | 56 | Taponamiento cardiaco |
| 3 | 77 | Varón | MHnO con TVMNS | DAI bicameral | Activo | Orejuela AD | 47 | Hemotórax derecho (disnea) |
| 4 | 74 | Mujer | Bloqueo A-V completo | MP bicameral | Activo | Ápex VD | 395 | Síncope |
| 5 | 86 | Mujer | Bloqueo A-V 2:1 | MP bicameral | Activo | Ápex VD | 28 | Ausencia de captura del MP en ECG |
AD: aurícula derecha; A-V: auriculoventricular; DAI-TRC: desfibrilador automático implantable - Terapia de resincronización cardiaca; ECG: electrocardiograma; FEVI: fracción de eyección del ventrículo izquierdo; MHnO: miocardiopatía hipertrófica no obstructiva; MI: miocardiopatía isquémica; MP: marcapasos; TVMNS: taquicardia ventricular monomorfa no sostenida; VD: ventrículo derecho.
Tres de los pacientes eran portadores de un marcapasos bicameral, uno de un DAI-TRC y otro de un DAI. En cuatro casos la perforación fue del ventrículo derecho (VD), tres secundaria al electrodo ventricular del marcapasos y uno por el electrodo ventricular del DAI-TRC. En el paciente del DAI la perforación fue de la pared libre de la aurícula derecha.
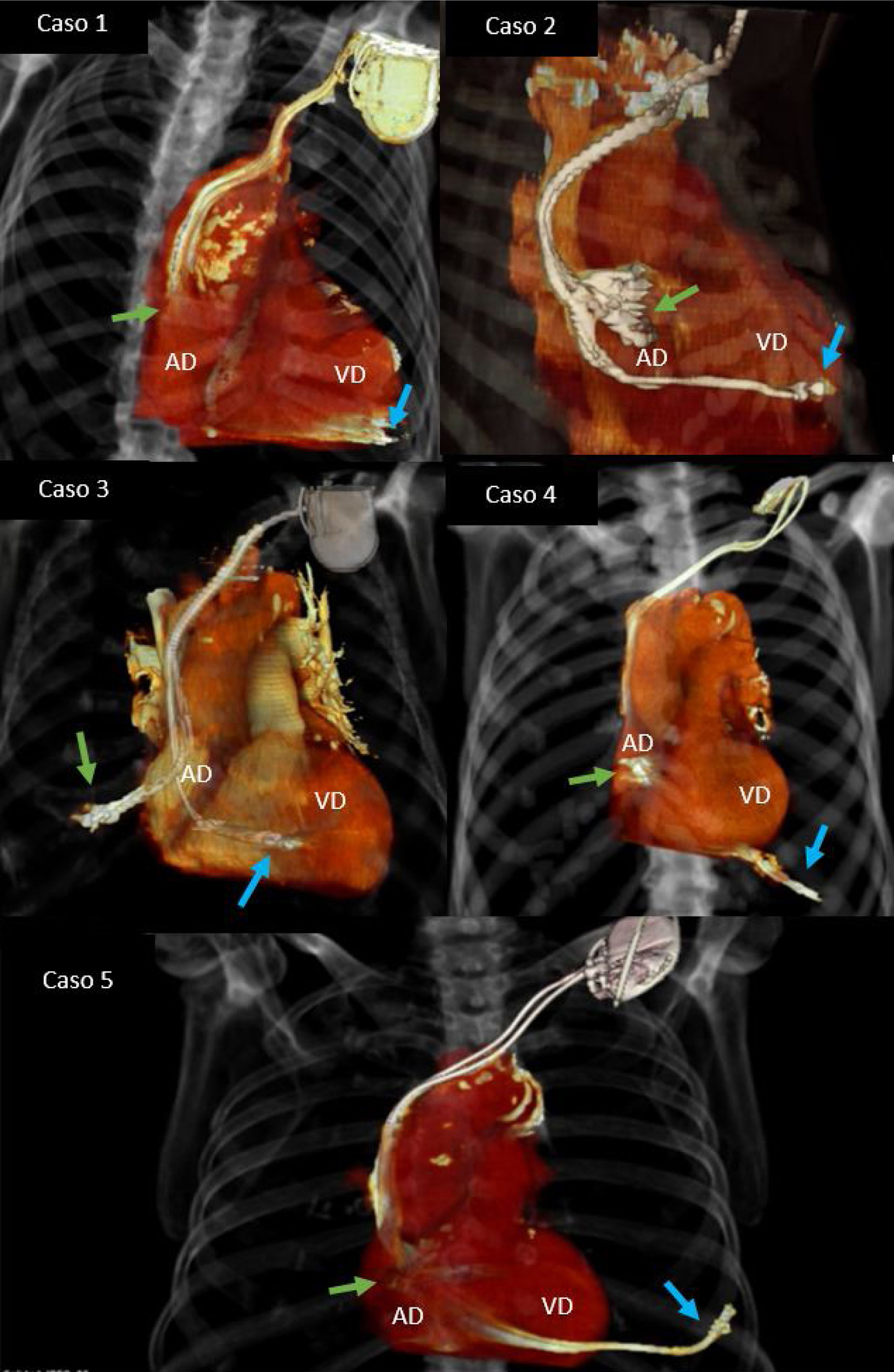
A todos los pacientes se les realizó una radiografía de tórax para confirmar el desplazamiento de los electrodos respecto a su posición original. Se solicitó una TAC para identificar la localización exacta del electrodo y descartar complicaciones concomitantes (fig. 1). Se revisaron los umbrales de los electrodos posterior al implante para confirmar el normo-funcionamiento de estos y descartar así una perforación aguda que haya pasado inadvertida.
En todos los casos el manejo fue similar, con algunas peculiaridades en el manejo preoperatorio según la presentación de la clínica. En el caso1 se realizó una pericardiocentesis ecoguiada con un catéter de pigtail para aliviar el taponamiento cardiaco. En el caso2 se realizó una ventana pericárdica vía subxifoidea durante el acto quirúrgico. En el caso3 se drenó el hemotórax derecho con un tubo de tórax.
Técnica quirúrgicaBajo anestesia general. Se preparó el tórax anterior para una posible esternotomía. Se prepararon ambas ingles para disponer de accesos por vasos femorales. Se canalizaron la arteria y la vena femoral, dejando un introductor de 4Fr y 6Fr, respectivamente, para canular percutáneamente en caso de requerir circulación extracorpórea por una complicación mayor.
Mediante tracción simple se retiró el electrodo hasta la vena cava superior. Una vez descartada la presencia de sangrado activo mediante monitorización invasiva y ecocardiografía transesofágica (ausencia de derrame pericárdico o pleural), se procedió a recolocar nuevamente los electrodos. Los electrodos ventriculares del marcapasos se recolocaron a nivel del tracto de salida del VD, del DAI-TRC se reimplantó en el ápex y el auricular se implantó en la orejuela de la AD.
Todos los pacientes salieron extubados y sin necesidad de soporte vasoactivo y/o inotrópico. No se registraron complicaciones intraoperatorias.
En los casos del hemotórax y derrame pericárdico se retiraron los drenajes a las 24h y fueron dados de alta a las 48h. En los otros dos casos el alta fue a las 24h. Se realizó una radiografía de tórax y una ecocardiografía transtorácica para descartar complicaciones. Todos los pacientes fueron dados de alta a domicilio en buenas condiciones. El seguimiento clínico se completó al mes y a los 6meses, con ausencia de morbimortalidad.
DiscusiónEl propósito de este estudio fue analizar todos los pacientes intervenidos en nuestro centro con el diagnóstico de PTM secundario a DECI y describir las características clínicas, la presentación de los síntomas y dar a conocer el manejo protocolizado realizado en nuestro centro.
La PTM es una complicación inusual con una incidencia reportada del 0,1-0,8%, y nuestra incidencia es del 0,1%2-4. La PTM se ha clasificado de forma arbitraria en: aguda (primeras 24h), subaguda (entre 24h y un mes) y tardía (posterior al mes)2,5. Otros autores proponen la clasificación de: agudo (primeros 15días) y tardío (más de 15días)6. En nuestro caso hemos optado por esta última, ya que consideramos que la actitud terapéutica no difiere entre subaguda y tardía.
Algunos factores de riesgo de perforación son: implante en la pared libre de la AD o el ápex del VD, sexo femenino, obesidad, edad mayor a 75años, anticoagulantes, implante de electrodos de fijación activa1. Algunos de estos factores coinciden en nuestra serie.
La presentación clínica es variada, desde la disfunción del marcapasos hasta el paciente con taponamiento cardiaco. Los signos que sugieren PTM son aumento de umbrales, fallo de captura y/o censado de los electrodos. En la radiografía de tórax, desplazamiento de los electrodos, que pueden ser tan evidentes como migración a otras cavidades. En el ecocardiograma, derrame pericárdico e incluso la presencia del electrodo en el saco pericárdico. La TAC aporta información detallada del recorrido del electrodo y confirma el diagnóstico en casos dudosos.
El manejo de la PTM varía considerablemente: extracción del electrodo mediante cirugía (toracotomía, esternotomía o videotoracoscopia con reparación concomitante de la pared), tracción simple, o incluso actitud expectante, absteniéndose de extraer el electrodo. Todas con buenos resultados7.
Nuestro enfoque es conservador, retirando el electrodo, con preparación para cirugía emergente, sin suponer un riesgo aumentado y evitando la comorbilidad propia del abordaje quirúrgico.
ConclusionesEn los casos de PTM por un electrodo de un DECI, la movilización y la recolocación del mismo en un entorno quirúrgico adecuado ofrece buenos resultados.
Aunque no tuvimos complicaciones de sangrado activo o rotura de miocardio, la principal limitación de nuestra serie es el escaso número de casos debido a lo inusual de esta complicación, por lo que no recomendamos la movilización de los electrodos en una área no quirúrgica.
El manejo de la PTM debe estar correctamente protocolizado, ajustándose a la disponibilidad de equipos y personal de cada centro.