Introducción
Durante los últimos 20 años se han ido adquiriendo nuevos conocimientos en la fisiopatología e historia natural de la pancreatitis aguda. El curso clínico de la pancreatitis aguda varía desde una forma leve y transitoria (pancreatitis edematosa) hasta una enfermedad grave y potencialmente mortal (pancreatitis necrótica). La pancreatitis grave se asocia con fallo orgánico múltiple y/o complicaciones locales tales como necrosis, formación de abscesos o seudoquistes1.
La pancreatitis grave llega a representar el 15-20% de los casos. Las primeras 2 semanas después del inicio de la sintomatología, esta forma grave está caracterizada por el desarrollo de un síndrome de respuesta inflamatoria sistémica. La necrosis pancreática se desarrolla en los primeros 4 días de la enfermedad, mientras que la infección de esta necrosis se presenta, en la mayoría de los casos, a partir de la segunda y la tercera semanas. Cabe destacar que el 70% de todos los pacientes desarrollan la infección alrededor de la cuarta semana después del inicio de la enfermedad2. Además, el riesgo de la infección aumenta en relación con la extensión de la necrosis, tanto intra como extrapancreática2,3. La infección de la necrosis pancreática sigue siendo el principal factor de riesgo para el desarrollo del fallo orgánico múltiple3-5.
El tratamiento de la pancreatitis aguda grave durante las primeras fases de la enfermedad es únicamente médico, con el objeto de mantener la estabilidad hemodinámica y cardiovascular. El desarrollo de la infección en la necrosis pancreática es el principal determinante de la morbilidad y mortalidad en las fases tardías de la enfermedad, por lo que se recomienda la administración profiláctica de antibióticos cuando la necrosis es mayor del 30%. La última revisión de la Biblioteca Cochrane continúa recomendando la utilización profiláctica de antibióticos en casos de pancreatitis aguda grave6.
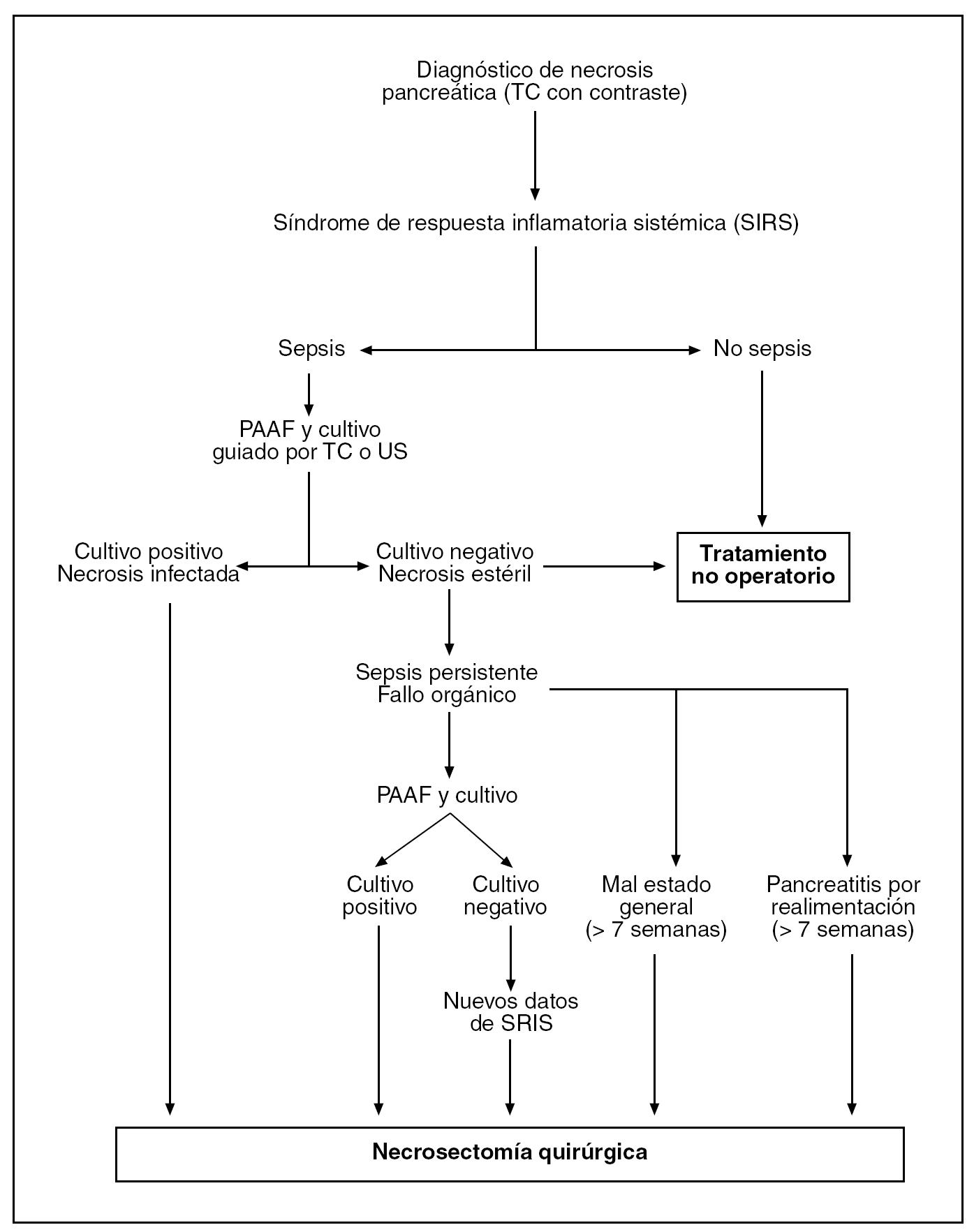
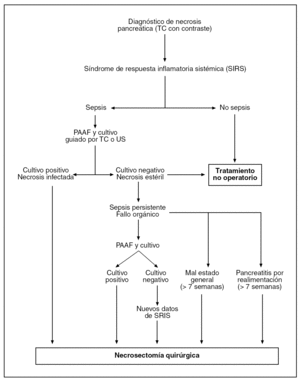
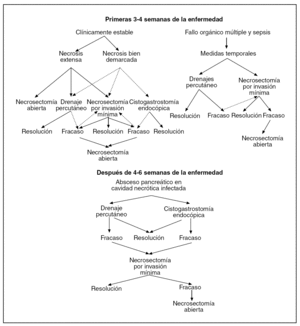
Una vez que se ha desarrollado la necrosis pancreática es de suma importancia diferenciar entre la presencia o no de infección del área de necrosis. Generalmente, la necrosis pancreática infectada se puede sospechar en aquellos pacientes que desarrollan signos clínicos de sepsis7. Sin embargo, para llegar al diagnóstico de certeza, es necesario realizar en estos pacientes una punción-aspiración con aguja fina (PAAF) del tejido pancreático o peripancreático, guiada por tomografía computarizada (TC) o ecografía5,7. La PAAF es un método seguro y fiable para poder diferenciar entre la necrosis estéril y la infectada8. Es de suma importancia resaltar que únicamente aquellos pacientes con signos clínicos de sepsis deberían de ser sometidos a PAAF, ya que existe el riesgo potencial de infección secundaria relacionada al procedimiento. En la figura 1 se explica el algoritmo que utilizamos en nuestra institución en aquellos pacientes que desarrollan el cuadro clínico de sepsis9.
Fig. 1. Algoritmo terapéutico en pacientes con pancreatitis aguda grave. PAAF: punción-aspiración con aguja fina; TC: tomografía computarizada; US: ultrasonidos.
Aunque en la actualidad la mayoría de los pacientes sobrevive a la fase inicial de la pancreatitis aguda grave debido a los avances en el tratamiento en las unidades de cuidados intensivos (UCI), es en la etapa tardía cuando el riesgo de sepsis se va incrementado5,10. Mientras que la intervención quirúrgica debe realizarse únicamente en casos seleccionados durante las dos primeras semanas de la enfermedad11, la cirugía y los procedimientos de acceso mínimo son de gran importancia en las etapas tardías de la enfermedad.
Indicaciones para cirugía
Necrosis pancreática infectada
Tanto la presencia de necrosis pancreática infectada como el desarrollo de complicaciones sépticas secundarias a la infección pancreática son indicaciones bien establecidas para el tratamiento quirúrgico5,12,13. En estos pacientes, la mortalidad es superior al 30%, y más del 80% de las defunciones en estos pacientes con pancreatitis se debe a complicaciones sépticas2,5,14. En centros especializados en cirugía del páncreas, la mortalidad se ha logrado disminuir hasta un 10-20% gracias al tratamiento quirúrgico apropiado5,13-16.
Necrosis estéril
En la mayoría de los pacientes, el tratamiento conservador suele ser adecuado5,7,16; sin embargo, algunos pacientes con necrosis pancreática estéril no mejoran a pesar del tratamiento en la UCI. Se ha aceptado de manera general que los pacientes con persistencia o desarrollo de fallo orgánico a pesar del tratamiento intensivo se benefician del tratamiento quirúrgico7, pero no existe un consenso acerca de cuándo considerar que el paciente no presenta respuesta al tratamiento en la UCI. Adicionalmente, la cirugía puede indicarse de manera excepcional en los casos raros de fallo orgánico múltiple de aparición rápida y progresiva en los primeros días de desarrollo de la pancreatitis aguda, a pesar del tratamiento adecuado en la UCI (pancreatitis aguda fulminante)7. Desafortunadamente, en estas circunstancias, debido al pobre pronóstico que tiene esta clase de pacientes, así como a la falta de datos publicados, no está bien establecido cuál es el tratamiento óptimo, ya sea quirúrgico y/o conservador.
Momento adecuado para la cirugía
Se considera que la cirugía debe realizarse lo más tardíamente posible desde el inicio de la enfermedad7. El principal razonamiento es la menor dificultad que existe para identificar en este período de la enfermedad el límite entre el tejido necrótico del parénquima pancreático viable. Estos datos son de gran importancia para limitar la extensión del desbridamiento quirúrgico. De esta forma se disminuye el riesgo de la hemorragia intra y postoperatoria asociada a la necrosectomía. Esta cirugía conservadora minimiza la pérdida de tejido pancreático para evitar en un futuro el desarrollo de una insuficiencia pancreática exocrina y/o endocrina.
Se han descrito tasas de mortalidad de hasta el 65% con la cirugía en fases tempranas de la pancreatitis grave2,17, lo cual pone en duda el beneficio de la intervención durante los primeros días después del inicio de la enfermedad. En el único estudio prospectivo y aleatorizado que compara la cirugía precoz (48-72 h del inicio de los síntomas) frente a cirugía tardía (al menos 12 días después del inicio) en pacientes con pancreatitis grave, se observó una mortalidad del 56 frente al 27%, respectivamente17. Aunque esta diferencia no fue estadísticamente significativa, este estudio fue detenido debido al riesgo elevado que confería la cirugía temprana. Por lo tanto, únicamente en el caso de necrosis pancreática infectada demostrada o en los casos raros de complicaciones graves, como la hemorragia masiva o la perforación de la víscera hueca, se deberá realizar la intervención quirúrgica5-7.
Técnicas de necrosectomía pancreática abierta
El objetivo es controlar el foco séptico y disminuir la liberación de mediadores proinflamatorios. Un principio plenamente aceptado es el abordaje quirúrgico que combine el desbridamiento y la eliminación, en los días del postoperatorio, de los residuos necróticos y de los exudados retroperitoneales. La necrosectomía puede realizarse mediante 4 técnicas distintas: a) taponamiento abierto18; b) lavados repetidos por etapas13; c) lavado cerrado continuo en la transcavidad de los epiplones y del retroperitoneo, y d) taponamiento cerrado16.
Necrosectomía/desbridamiento
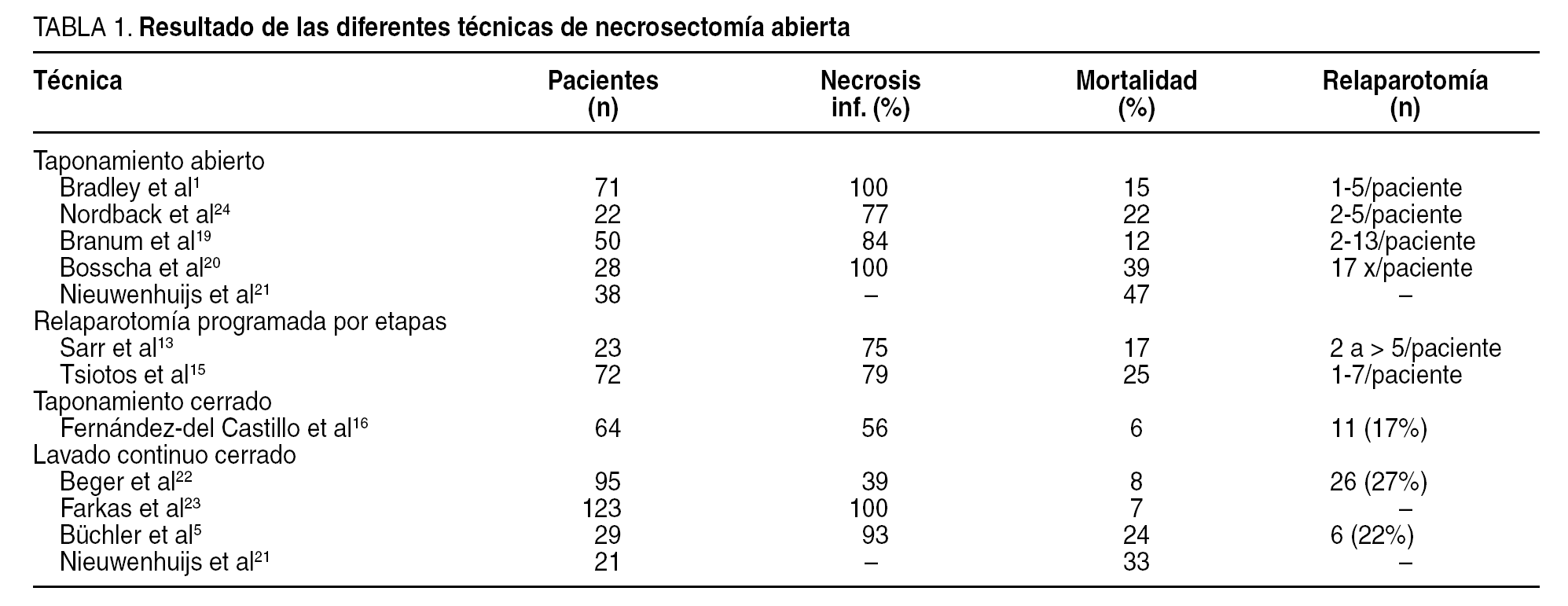
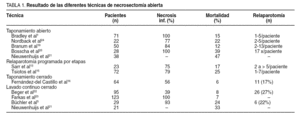
Aunque las 4 técnicas difieren en la manera en que se crean los espacios y de los medios que se utilizan para permitir la salida de los detritos, la técnica de la necrosectomía es esencialmente la misma. En cirujanos con experiencia, se han descrito tasas de mortalidad inferiores al 15%2,5,13,15,16,18-24 (tabla 1).
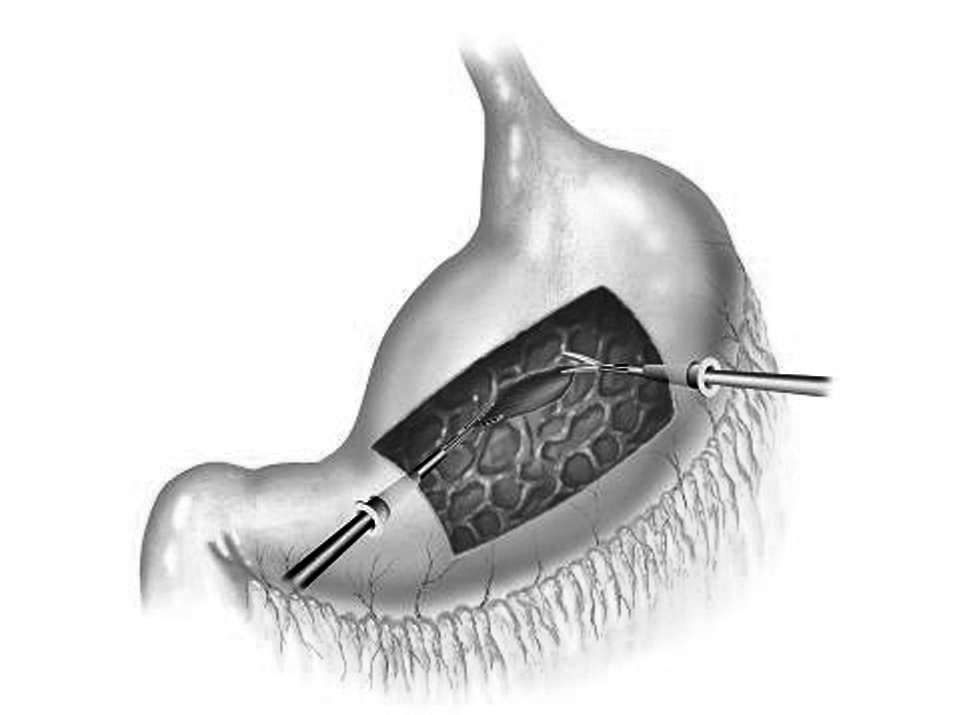
Tradicionalmente, la necrosectomía se ha llevado a cabo mediante abordaje abierto. Una incisión en la línea media permite la valoración de la totalidad de la cavidad abdominal, para una completa irrigación-lavado y la realización de otros procedimientos, en casos necesarios. Una vez que se accede a la cavidad abdominal, el ligamento gastrocólico se secciona lo más proximal posible a la curvatura mayor del estómago, con el objetivo de exponer el área pancreática y localizar el área de necrosis. El desbridamiento se lleva a cabo con gran cuidado y con el objetivo de resecar únicamente el tejido desvitalizado, y evitar el riesgo de complicaciones hemorrágicas graves. Una vez que el tejido necrótico es resecado, el retroperitoneo se irriga con varios litros de solución salina.
Taponamiento abierto. La cavidad abdominal se cubre con apósitos no adherentes y se empaqueta. El paciente es llevado al quirófano cada 48 h para continuar con el desbridamiento y taponamiento hasta que no se encuentre presencia alguna de necrosis. Estas intervenciones sucesivas pueden llevarse a cabo bajo sedación en la UCI, en algunos casos, hasta la aparición de tejido de granulación. En este momento, se colocan drenajes y la cavidad puede cerrarse, procediendo entonces a realizar los lavados con el abdomen ya cerrado25.
Laparotomía de repetición con lavados. Se llevan a cabo reoperaciones planeadas para repetir el procedimiento hasta completar la exéresis de todo el tejido desvitalizado, hasta que el cirujano quede convencido de que el proceso de inflamación local y de necrosis esté controlado. Para facilitar el acceso a la cavidad, se han utilizado cremalleras incorporadas a la pared abdominal. Finalmente, puede efectuarse el cierre primario retardado, previa colocación de drenajes en la zona peripancreática13.
Las otras 2 técnicas, la necrosectomía y el lavado cerrado continuo en la zona del retroperitoneo5,23, y el taponamiento cerrado16 son métodos de gran eficacia para eliminar de manera continua la necrosis pancreática residual.
Lavado cerrado continuo del retroperitoneo y de la transcavidad de los epiplones. Para realizar el lavado cerrado postoperatorio, se colocan dos o más drenajes de doble luz (20-24 Fr) y tubos de caucho o silicona de una luz (28-32 Fr) desde ambos lados del abdomen, dirigidos con la punta hacia la cola del páncreas, detrás del colon descendente, y hacia la zona de la cabeza del páncreas y el colon ascendente. A través de los drenajes se instila el lavado, mientras que el drenaje se facilita a través de los tubos de mayor calibre, para permitir también la salida de los detritos. Los ligamentos gastrocólico y duodenocólico se reaproximan para crear un espacio retroperitoneal cerrado apropiado para la irrigación-lavado. Se utilizan 35-40 l de líquido de lavado con solución salina. Según la evolución del paciente y las características del líquido drenado, el volumen del líquido de lavado se reduce de manera progresiva. Los drenajes normalmente se retiran al cabo de 2 o 3 semanas5,22.
Taponamiento cerrado. Esta técnica sigue el mismo principio que el lavado continuo postoperatorio, ya que permite la salida relativamente sencilla de los detritos. Una vez que todo el tejido ha sido eliminado y el abdomen ha sido irrigado con solución salina, la cavidad residual se rellena con múltiples drenajes de Penrose rellenos de gasa, así como de drenajes aspirativos cerrados. Los drenajes se extraen hacia los lados del paciente, procurando que estén situados en las zonas más declive, para favorecer el drenaje espontáneo. Los drenajes pueden retirarse de manera sucesiva después de un mínimo de 7 días de drenaje continuo. Al mismo tiempo, los drenajes empaquetados con gasa pueden retirarse de manera gradual, para permitir el cierre progresivo de la cavidad16.
Qué técnica ofrece mayores ventajas
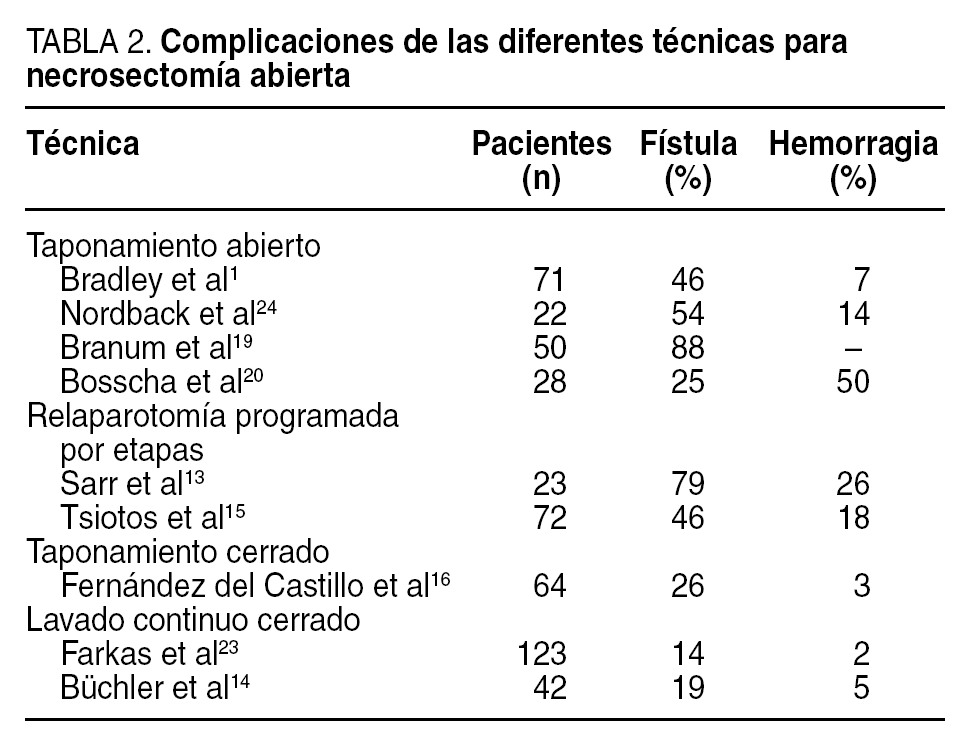
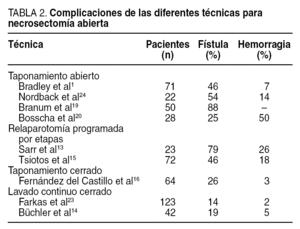
Aunque la incidencia de sepsis abdominal recurrente ha disminuido de manera significativa al comparar estas técnicas con la técnica de necrosectomía simple, la morbilidad postoperatoria permanece alta con las técnicas de taponamiento abierto y las laparotomías de repetición (tablas 1 y 2). Existe una correlación directa entre las intervenciones quirúrgicas repetidas y la morbilidad, incluida la aparición de fístulas, estenosis del tracto gastrointestinal, hernias incisionales y hemorragia. El desarrollo de fístulas pancreáticas y colónicas es significativamente mayor después de estas técnicas cuando se comparan con la necrosectomía con lavado continuo cerrado o con el taponamiento cerrado5,13,16,25 (tabla 2). Por lo tanto, las primeras 2 técnicas serían particularmente útiles cuando la intervención se lleva a cabo de manera inicial en el curso de la pancreatitis necrosante antes de que haya ocurrido una delimitación de la necrosis. Estos 2 procedimientos deberían de considerarse únicamente en los casos raros en que es necesario un desbridamiento temprano7.
Las técnicas de lavado continuo cerrado y el taponamiento cerrado tienen la ventaja de eliminar de manera progresiva en el tiempo la necrosis pancreática residual7. De esta manera, se evitan las laparotomías repetidas y se disminuye la morbilidad relacionada con el desarrollo de fístulas y las secuelas de hernias incisionales (tablas 1 y 2). Los resultados de estas dos estrategias quirúrgicas son comparables respecto a la necesidad de reoperación, la morbilidad y la mortalidad, por lo que la elección de una u otra depende de la preferencia del cirujano. En nuestra institución, usamos de manera rutinaria el lavado continuo cerrado que fue exitoso en el 80% de los casos. Actualmente, la necrosectomía con el lavado continuo cerrado del retroperitoneo y de la transcavidad de los epiplones es el abordaje más frecuentemente utilizado7,11.
En diferentes series quirúrgicas se publican resultados muy dispares, a pesar de utilizar aparentemente unos métodos similares, lo cual ejemplifica la dificultad para poder comparar estas técnicas (tablas 1 y 2). Los porcentajes de mortalidad publicados varían entre el 10 y el 20%20. En ausencia de estudios aleatorizados, es imposible determinar la influencia que pueden tener otros factores tales como la selección de pacientes, la comorbilidad, el tratamiento preoperatorio con técnicas percutáneas y las situaciones clínicas que motivaron la indicación quirúrgica.
Sin embargo, esta mortalidad, que raramente es inferior al 20% después de las técnicas de cirugía convencional, aumenta de manera significativa en aquellos pacientes con necrosis infectada y fallo orgánico. Cuando el fracaso orgánico es superior a 3 órganos, la mortalidad de la cirugía es del 80-90%. En este tipo de pacientes con necrosis pancreática y fracaso orgánico tenemos las siguientes opciones26:
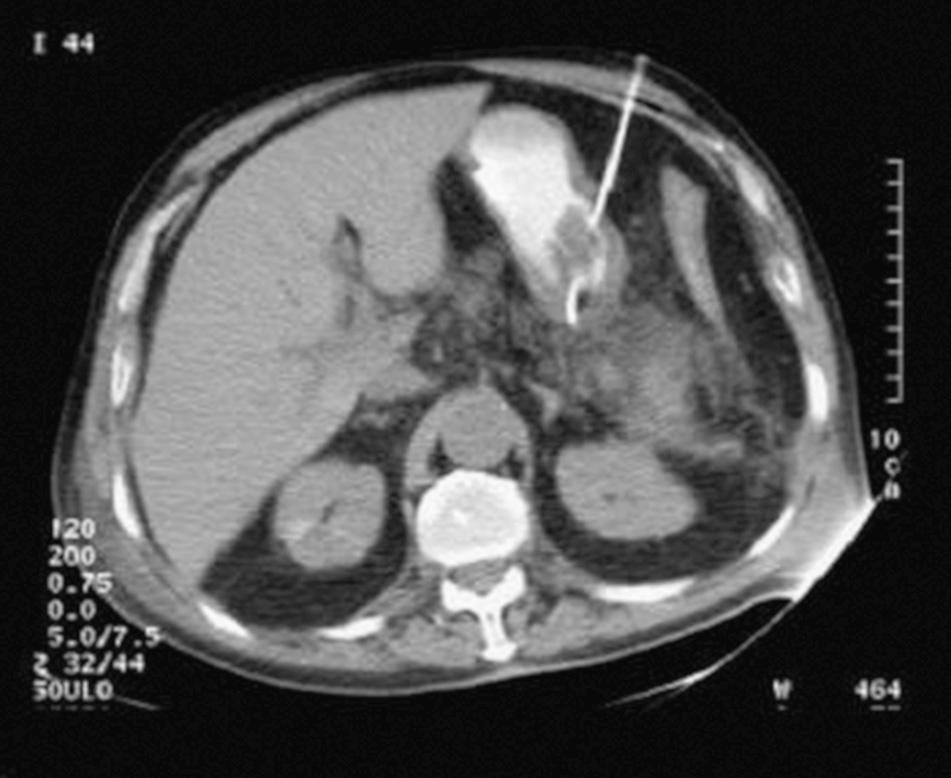
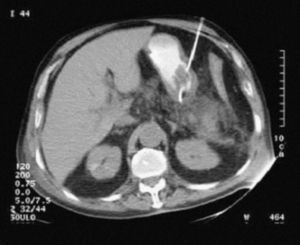
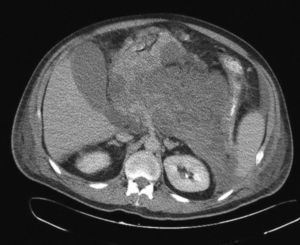
1. Drenaje percutáneo. Este procedimiento combina el drenaje guiado por TC, dilatación del trayecto de drenaje y lavado continuo27. Esta técnica de radiología intervencionista utiliza una media de 4 drenajes por paciente. El porcentaje de éxito como tratamiento definitivo de la necrosis infectada varía ampliamente entre el 14 y el 86%, con una morbilidad y una mortalidad muy bajas. El éxito de este método de drenaje está en relación con el esfuerzo del radiólogo y la disponibilidad del servicio de radiología para efectuar un seguimiento continuo de la eficacia del tratamiento. Esta técnica también puede utilizarse como medida transitoria o temporal para que el paciente se encuentre en las mejores condiciones de recibir un tratamiento quirúrgico (fig. 2).
Fig. 2. Drenaje percutáneo en un paciente con una necrosis pancreática infectada de localización retrogástrica.
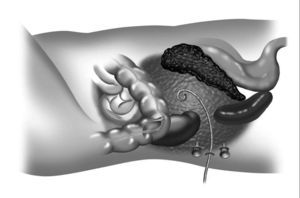
2. Cistogastrostomía endoscópica. Este método se basa en la realización de un drenaje transmural, utilizando ecografía endoscópica y dilatación del trayecto del drenaje, combinado con un lavado de la cavidad necrótica a través de un drenaje que sale por la nariz28. Este procedimiento es de gran efectividad para disminuir el componente líquido del área de necrosis pero tiene un efecto limitado en la eliminación del componente sólido de la necrosis. Por ello, su efectividad podría esperarse en necrosis bien limitada y como medida temporal para poner en condiciones adecuadas a los pacientes para un tratamiento quirúrgico.
3. Necrosectomía laparoscópica o retroperitoneoscópica. El desbridamiento del área necrótica mediante abordajes de invasión mínima puede realizarse por una vía retrogástrica y retrocólica o a través del estómago29,30,31. Hemos efectuado estas técnicas en 15 pacientes con necrosis infectada > 50%, con una mortalidad del 10%. Tres de estos pacientes necesitaron una reintervención laparoscópica. Estos abordajes son de gran utilidad en aquellos pacientes con necrosis pancreática bien localizada y con fracaso orgánico. En estos casos, es de gran eficacia la combinación de un drenaje percutáneo que permita controlar la infección durante un cierto tiempo, y el abordaje laparoscópico como control definitivo de la eliminación del tejido necrótico, seguido de lavados continuos a través de los drenajes.
Gambiez et al32 y Castellanos et al33 han descrito con éxito la necrosectomía por vía lumboscópica. En este método se utiliza un mediastinoscopio de 23 cm de longitud que se introduce a través de una incisión en la base de la 12.a costilla, y a través de éste se realiza el desbridamiento de la necrosis mediante visión directa. La mortalidad quirúrgica es de un 10%, con una morbilidad escasa. Sin embargo, es necesario efectuar las maniobras de drenaje de manera repetitiva, que pueden realizarse en la mayoría de los casos dentro de la UCI (figs. 3 y 4).
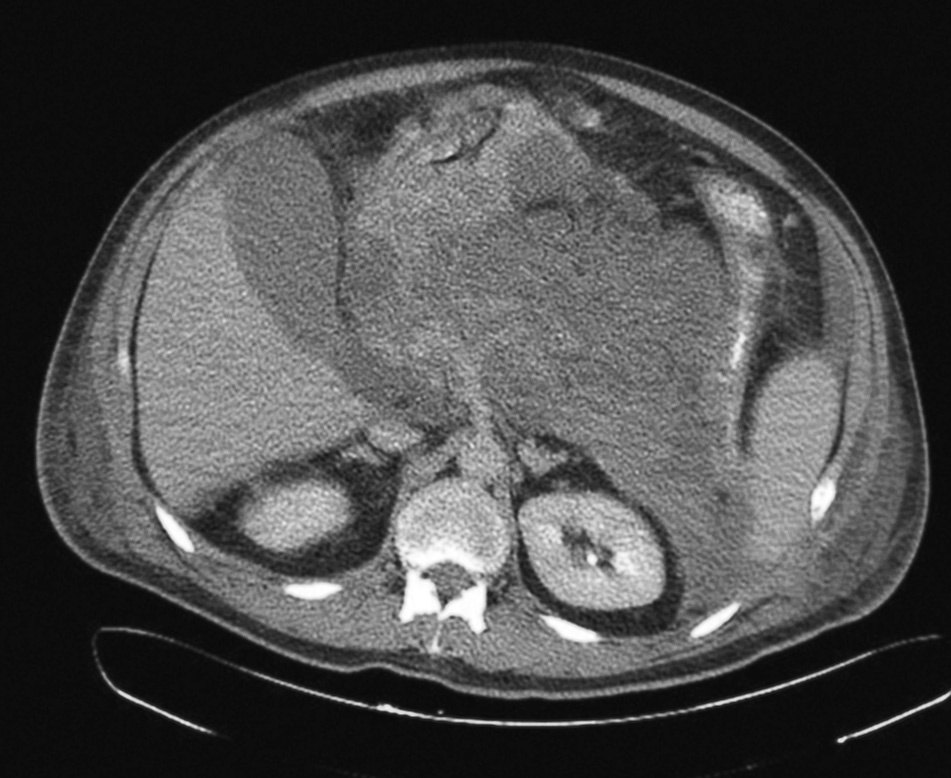
Fig. 3. Necrosis pancreática que se extiende al espacio esplenorrenal. Esta situación es la adecuada para el drenaje por vía retroperitoneal.
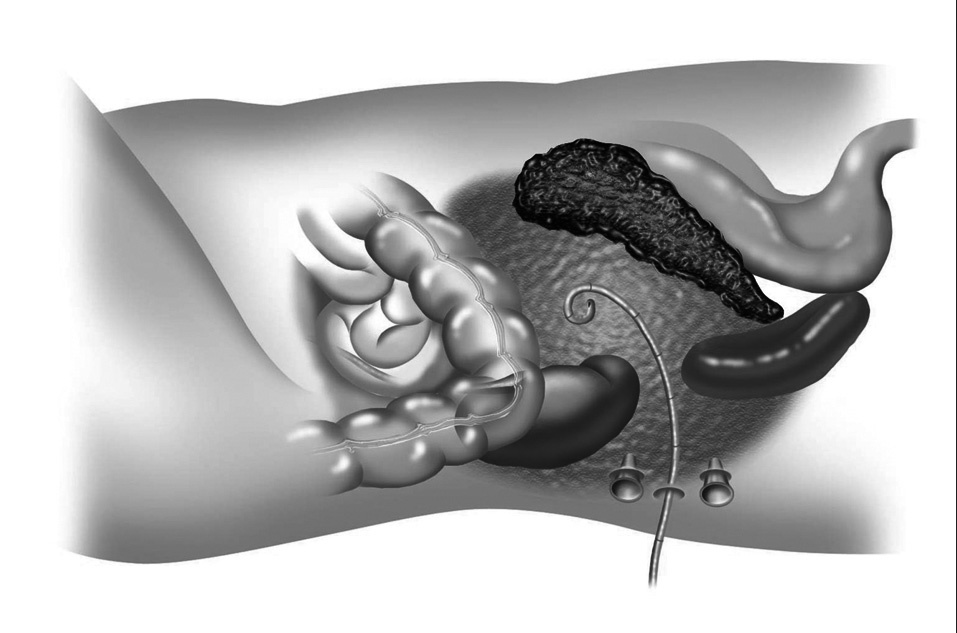
Fig. 4. Posición del paciente en decúbito lateral. Una vez se ha localizado el área de necrosis por tomografía computarizada se deja un drenaje. En la intervención quirúrgica se coloca un trócar guiado por el drenaje percutáneo y otros 2 trócares para realizar la necrosectomía y el lavado.
Carter et al34 han descrito la necrosectomía percutánea, mediante una dilatación del trayecto del drenaje percutáneo y la colocación de una óptica urológica: se efectúan lavados con gran cantidad de líquido y se procede a la aspiración de la cavidad necrótica. Este procedimiento es repetido cada 7-10 días hasta conseguir limpiar por completo la cavidad35,36.
Entre las ventajas de este procedimiento está la desaparición progresiva del fracaso orgánico y una notable disminución de la estancia de los pacientes en la UCI.
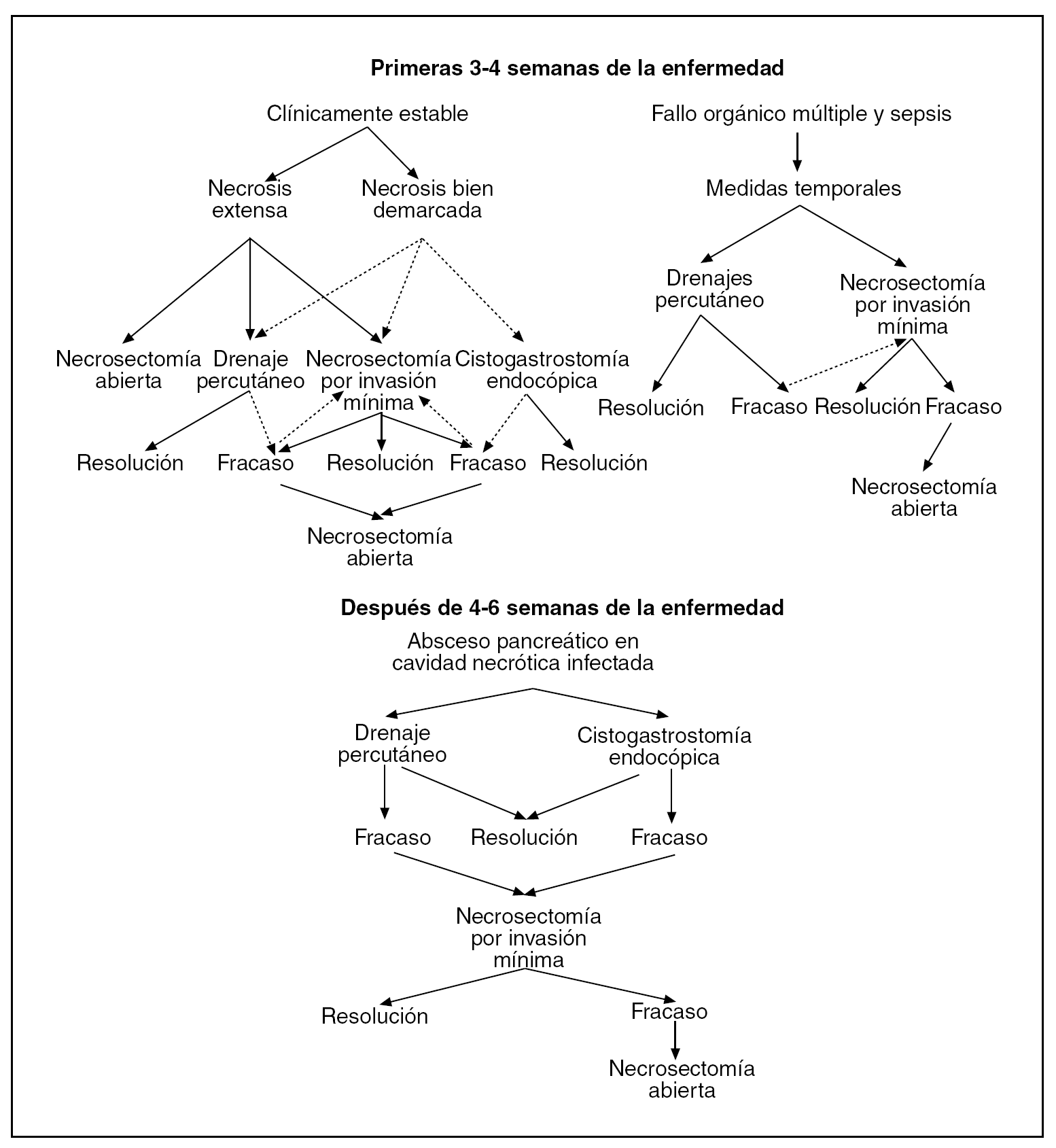
En la actualidad, el cirujano dispone de una serie de opciones que le permita una disminución de la mortalidad de los pacientes con pancreatitis necrótica infectada extensa. El tratamiento antibiótico es una medida de sostén eficaz pero no suficiente. Las opciones terapéuticas deben tener en cuenta la posibilidad de alternativas terapéuticas de radiología intervencionista (drenaje percutáneo) y endoscópicas (cistogastrostomía endoscópica) que permitan la recuperación de los pacientes hasta conseguir las mejores condiciones para realizar el tratamiento quirúrgico definitivo. Si bien la necrosectomía por la laparotomía es una técnica segura y eficaz en un gran número de pacientes, supone un gran trauma para estos pacientes con fracaso orgánico. Por todo ello, la cirugía mínimamente invasiva tiene como atractivo el minimizar el trauma operatorio y conseguir la misma eficacia que se consigue con la necrosectomía abierta. En la figura 5 se expone una propuesta de tratamiento que tiene en consideración las variables clínicas26:
Fig. 5. Estrategia terapéutica en pacientes con necrosis pancreática infectada, según sus variables clínicas.
1. Los pacientes en situación clínica estable pueden presentarse con una necrosis extensa o una necrosis bien delimitada. En el primer caso, la necrosectomía convencional es una buena opción, si bien también puede optarse por el drenaje percutáneo o el abordaje mínimamente invasivo. Nosotros creemos que en pacientes con necrosis bien delimitada, el tratamiento inicial debería ser el drenaje mediante la radiología intervencionista y dejar la cirugía convencional o la cirugía mínimamente invasiva para aquellos casos en los que fracasan los métodos radiológicos.
2. En pacientes con fracaso multiorgánico y sepsis, la cirugía convencional conlleva una mortalidad tan elevada que debe postergarse a la espera de la eficacia de los métodos de drenaje en la radiología intervencionista. El fracaso de esta técnica podría seguirse de una cirugía mínimamente invasiva para mejorar las condiciones generales del paciente. Este abordaje de acceso mínimo puede acompañarse de éxito, pero un fracaso de llevar a la necrosectomía abierta.
3. El grupo de pacientes que a partir de las 4 o 6 semanas del inicio de la enfermedad presentan un absceso pancreático incluido en una extensa área de necrosis, se benefician de los métodos de radiología intervencionista. El fracaso de estos métodos obligaría a un tratamiento quirúrgico mediante un abordaje mínimamente invasivo (figs. 6 y 7). La cirugía convencional debe quedar siempre como una opción válida en los casos de fracaso de estas estrategias menos invasivas.
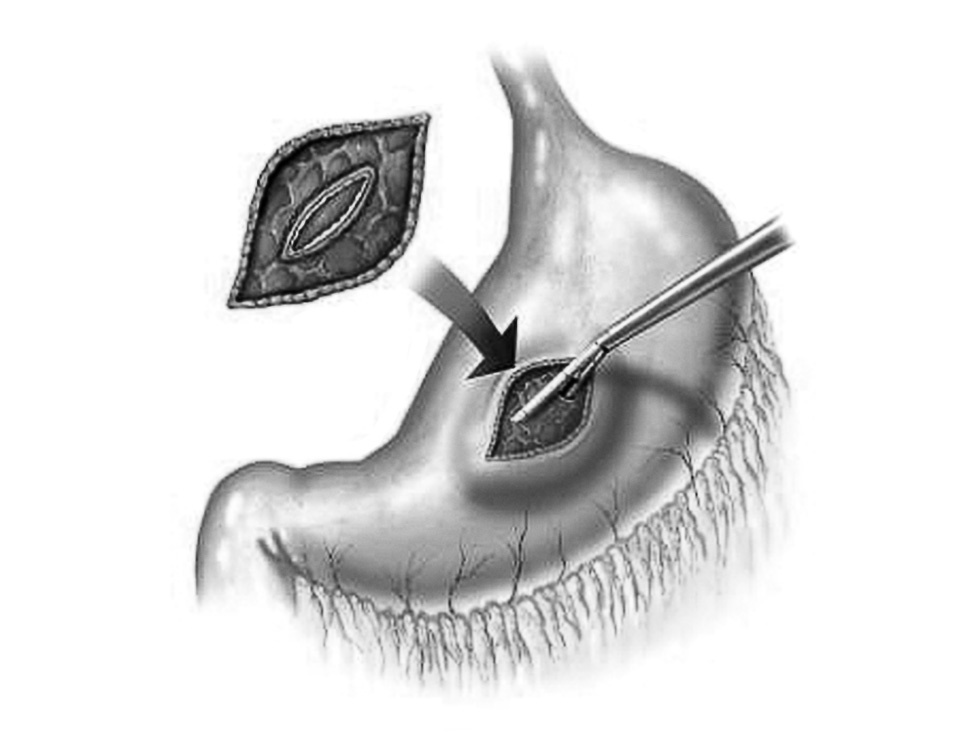
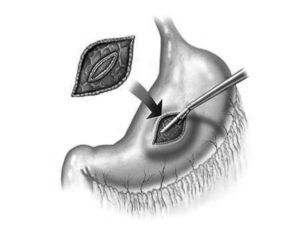
Fig. 6. Abordaje transgástrico por vía laparoscópica para el drenaje de un absceso retrogástrico, con apertura de la cara anterior y posterior del estómago.
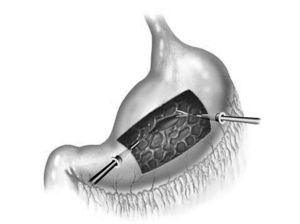
Fig. 7. Técnica laparoscópica de drenaje cistogastrostomía por vía transgástrica. Colocación intragástrica de 2 trócares, uno para la entrada de la óptica y otro para la entrada de los instrumentos de trabajo
Esta búsqueda de nuevos métodos de tratamiento de la necrosis infectada extensa está justificada por el advenimiento de las nuevas tecnologías en las especialidades tanto de la radiología como de la cirugía. Estos nuevos procedimientos tendrían como objetivos: a) evitar grandes incisiones quirúrgicas que puedan asociarse a algunas complicaciones, tales como hernia incisionales y fístulas intestinales; b) una recuperación postoperatoria más rápida; c) disminuir el dolor; d) disminución de la estancia en la UCI, y e) disminuir la estancia intrahospitalaria.
Sin embargo, en la actualidad no disponemos de datos que apoyen que estas propuestas son mejores que las técnicas convencionales. La utilización de los nuevos tratamientos debe regirse por programas de investigación clínica.
Correspondencia: Prof. Dr. L. Fernández-Cruz.
Catedrático de Cirugía. Departamento de Cirugía.
Universidad de Barcelona.
Hospital Clínic i Provincial de Barcelona.
Villarroel 170, Escalera 6, 4.a planta. 08036 Barcelona. España.
Correo electrónico: lfcruz@clinic.ub.es
Manuscrito recibido el 22-12-2005 y aceptado el 11-5-2006.