La endoscopia flexible (EF) es un procedimiento de gran utilidad para el manejo diagnóstico y terapéutico de lesiones del tracto digestivo superior. A pesar de que su uso intraoperatorio se ha extendido con el paso de los años, su empleo por parte de cirujanos es aún limitado en nuestro medio. Las oportunidades de capacitación en EF varían ampliamente entre instituciones, especialidades y países.
La endoscopia intraoperatoria (EIO) presenta ciertas peculiaridades que aumentan su complejidad respecto a la EF estándar. La realización de EIO repercute positivamente en los resultados quirúrgicos aportándoles seguridad y calidad así como disminución de las complicaciones asociadas a estas técnicas. Debido a sus innumerables ventajas, su uso intraoperatorio por parte de cirujanos es actualmente un proyecto vigente en muchos países y forma parte de un futuro próximo en otros, extendiéndose su uso dentro de la especialidad de cirugía general gracias a la creación de proyectos de formación mejor estructurados.
En este manuscrito se realiza una revisión y puesta al día de las indicaciones y utilidades de la endoscopia digestiva alta intraoperatoria en la cirugía esofagogástrica.
Flexible endoscopy (FE) plays a major role in the diagnosis and treatment of gastrointestinal disease. Although its intraoperative use has spread over the years, its use by surgeons is still limited in our setting. EF training opportunities are different among many institutions, specialties, and countries.
Intraoperative endoscopy (IOE) presents peculiarities that increase its complexity compared to standard EF. IOE has a positive impact on surgical results, due to increased safety and quality, as well as a reduction in the complications. Due to its innumerable advantages, its intraoperative use by surgeons is currently a current project in many countries and is part of the near future in others because of the creation of better structured training projects.
This manuscript reviews and updates the indications and uses of intraoperative upper gastrointestinal endoscopy in esophagogastric surgery.
Con el paso de los años la cirugía se ha convertido en una disciplina menos invasiva y más segura, que expande sus herramientas para optimizar resultados. En este sentido, el empleo intraoperatorio de la endoscopia flexible (EF) es un abordaje utilizado que aporta claros beneficios como adyuvante en la cirugía.
En 1880 el cirujano austriaco Mikulicz1 describió el uso del gastroscopio y describió el cáncer gástrico endoscópicamente. Desde estos inicios, la EF se ha desarrollado exponencialmente y su uso se ha extendido a múltiples procedimientos. De esta forma, la miotomía endoscópica peroral (POEM) para el tratamiento de la acalasia fue descrita en 2010 en Japón por el cirujano Haruhiro Inoue2 y a día de hoy un gran porcentaje de cánceres gástricos precoces se tratan mediante resección endoscópica mucosa (REM)3, mediante disección endoscópica submucosa (ESD) o mediante el procedimiento DEILO, descrito recientemente por Mochiki et al.4.
La endoscopia intraoperatoria (EIO) puede no solo ser de gran utilidad, sino, en algún caso, imprescindible para completar el procedimiento quirúrgico con seguridad, formando parte inseparable de él, como es el caso del establecimiento de límites de resección o identificación de lesiones de difícil visualización de forma extraluminal; sin contar con otras circunstancias, como la comprobación de la integridad de la anastomosis o descartar complicaciones intraoperatorias. Esta técnica queda relegada en la actualidad para su uso en algunas situaciones de urgencia y resolución de problemas, siendo realizada en la mayor parte de los centros por médicos digestólogos especializados5.
En este manuscrito se realiza una revisión sobre la capacitación en EF en cirugía general y una actualización de las indicaciones y de los posibles beneficios de la endoscopia digestiva en la cirugía esofagogástrica.
Endoscopia digestiva alta intraoperatoriaUtilidad de la endoscopia intraoperatoriaLa disponibilidad para acceder a la realización de una EIO de forma inmediata durante el desarrollo de procedimientos quirúrgicos en el tracto digestivo superior repercute de forma positiva en aumentar la seguridad y reducir los tiempos y las posibles complicaciones asociadas a la cirugía.
La realización de un procedimiento completo incluye la inspección del esófago, del estómago y del duodeno. La duración mínima recomendada de la exploración por algunos expertos es de 7minutos, habiéndose demostrado que los endoscopistas que empleaban más tiempo detectaban mayor número de lesiones premalignas gástricas (OR: 2,5), cáncer y lesiones con displasia (OR: 3,42)6. En el caso de su empleo intraoperatorio, la técnica puede ser más dirigida, obviando áreas ya exploradas previamente en otras endoscopias y centrándose en la patología y en el procedimiento específico.
Entre las ventajas e indicaciones generales del uso de la EIO en cirugía esofagogástrica se encuentran:
- -
Identificar la anatomía intraluminal y relacionarla con los hallazgos extraluminales de la cirugía.
- -
Permitir la adecuada calibración del órgano antes de la extirpación de lesiones o la confección de anastomosis.
- -
Permitir identificar lesiones in situ y comprobar la resección completa con márgenes de seguridad, evitando resecciones extensas innecesarias.
- -
Permitir la evaluación intraluminal del resultado quirúrgico una vez finalizado el procedimiento.
- -
Permitir la evaluación de la estanqueidad de la anastomosis, y descartar sangrados y posibles lesiones iatrogénicas.
Para realizar una EIO deben tenerse en cuenta algunas consideraciones que la diferencian del procedimiento estándar.
Es realizada en un paciente con intubación orotraqueal, por lo que el grado de dificultad puede verse incrementado. Los tubos endotraqueales deben asegurarse al lado derecho de la boca para llevar a cabo la exploración y se coloca un bloque de mordida en concierto con el dispositivo de vía aérea7. La posición del paciente cambia, presentándose en algunas ocasiones en decúbito supino, lateral, prono o semiprono, lo que dificulta en ocasiones el acceso. La colocación de la torre y del aparataje necesario para realizar la endoscopia dentro del quirófano debe adecuarse a la disposición espacial, sin olvidar los aspectos ergonómicos para el explorador. Además, debe tenerse en cuenta que la instilación de un exceso de aire/CO2 puede dificultar el abordaje quirúrgico al distender el estómago y el intestino delgado y la luz del laparoscopio puede dificultar o disminuir en ocasiones la calidad de la visión endoscópica.
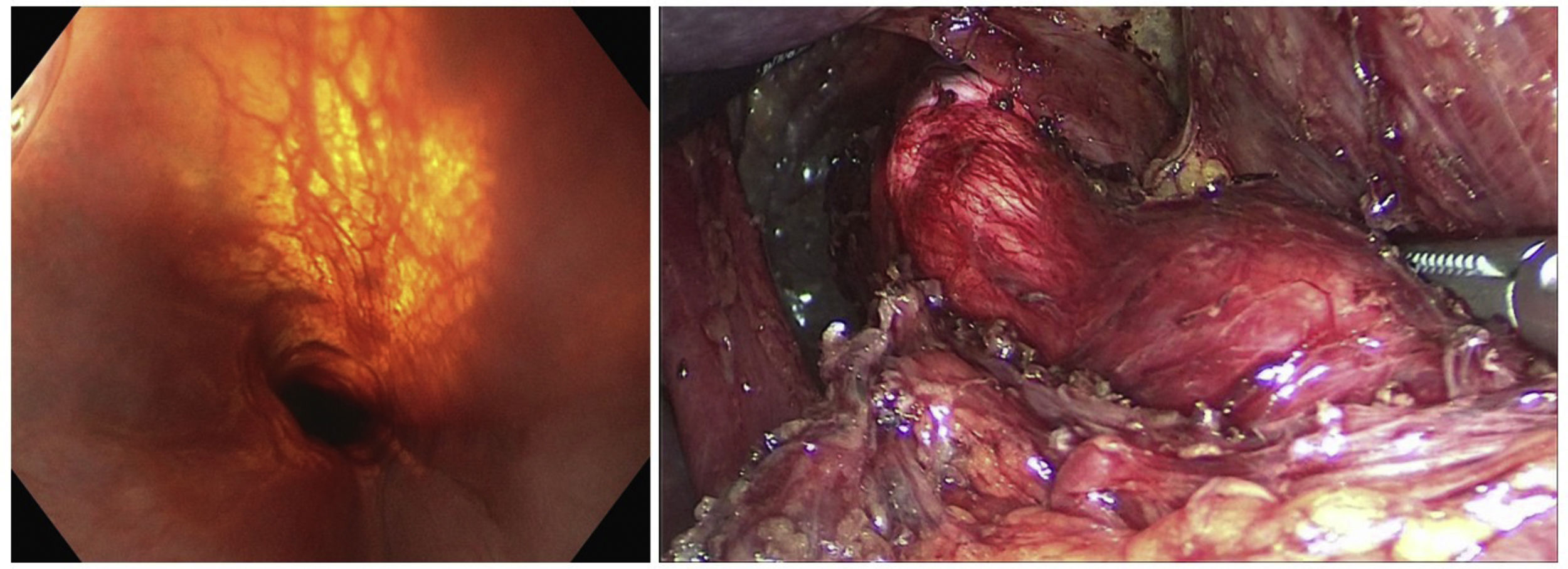
Escenarios más habituales para su usoCirugía de la acalasiaEn el caso del tratamiento quirúrgico de la acalasia, la realización de una EIO permite evaluar la calidad y la extensión de la miotomía8, permitiendo ampliar la longitud de la misma tanto en sentido craneal hacia el esófago como distalmente hacia al estómago, o incluso evaluando fibras musculares circulares que no hayan sido seccionadas que aparecen más marcadas al distender y transiluminar el esófago con el endoscopio (fig. 1) (Vídeo 1).
Además, la EIO permite identificar perforaciones mucosas inadvertidas durante la realización de la miotomía9, permitiendo realizar su sutura y aumentando así la seguridad del procedimiento.
Del mismo modo, permite evaluar el estado de la unión esofagogástrica antes y después de realizar la funduplicatura aconsejada en estos pacientes para evitar el reflujo gastroesofágico y que marca la diferencia en resultados funcionales frente a la miotomía realizada por vía endoscópica (POEM). En estudios comparativos, la técnica POEM y la miotomía de Heller laparoscópica presentan resultados similares en términos de eficacia, complicaciones y necesidad de analgesia, reduciéndose el tiempo del procedimiento en el caso de POEM10.
En los últimos años la incorporación de la manometría intraoperatoria mediante el dispositivo endoFLIP permite evaluar manométricamente el estado de la miotomía y la unión esofagogástrica. Estudios con mayor número de casos, con evaluación de los resultados a largo plazo y bien diseñados son necesarios para determinar su verdadera rentabilidad11,12.
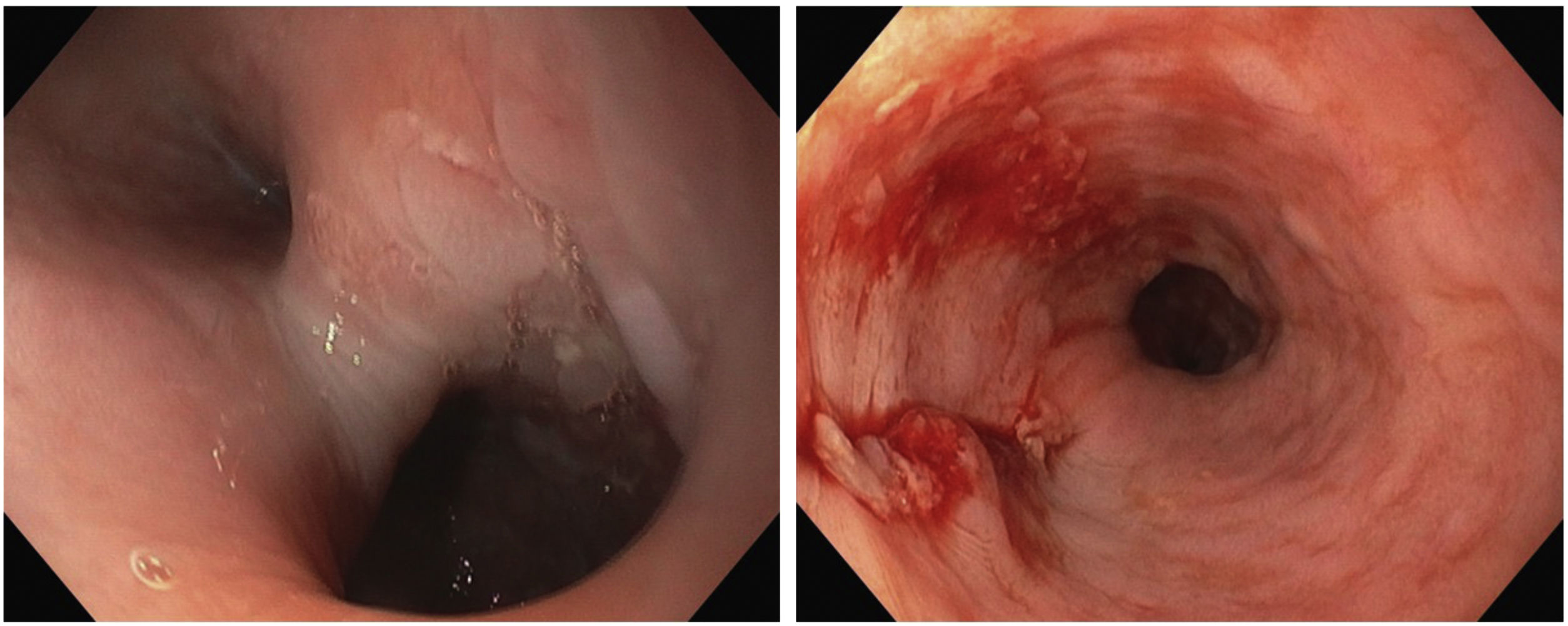
Cirugía de los divertículos esofágicosEl empleo de la EIO durante la cirugía de los divertículos esofágicos es de gran utilidad para diagnosticar con precisión la localización del divertículo, definiendo el inicio de su cuello y ayudando a su identificación al producir la insuflación y transiluminación con el endoscopio (Vídeo 2). Además de descartar otras posibles lesiones o alteraciones asociadas, la EIO permite limpiar los restos de alimentos que pueden quedar retenidos en el fondo y en el cuello diverticular, facilitando que la sección del cuello diverticular se realice en un tejido sin restos que puedan interferir en el grapado. Además, permite evaluar la resección completa del divertículo y comprobar que la luz esofágica no se encuentre reducida tras su sección (fig. 2), punto importante en diferentes tipos de cirugías que conlleven resecciones parciales13.
Como ocurre en la cirugía de la acalasia, la EIO en estos pacientes permite evaluar la extensión de la miotomía hasta el cuello del divertículo y descartar posibles perforaciones de la mucosa14.
Por otro lado, la endoscopia se emplea actualmente con finalidad terapéutica en el manejo de los divertículos de Zenker, realizándose la sección del tabique muscular con endograpadora15 o selladora bipolar16. En casos seleccionados ha demostrado resultados satisfactorios con resolución de la sintomatología cercana al 90% de los casos17. La POEM también ha sido descrita como tratamiento de los divertículos de tercio medio esofágico, aunque las publicaciones se limitan a series cortas de casos18,19.
Cirugía de los tumores submucososLos tumores submucosos esofagogástricos son infrecuentes: representan menos del 10% de todos los tumores localizados en esta estructura, siendo los leiomiomas los más frecuentes20.
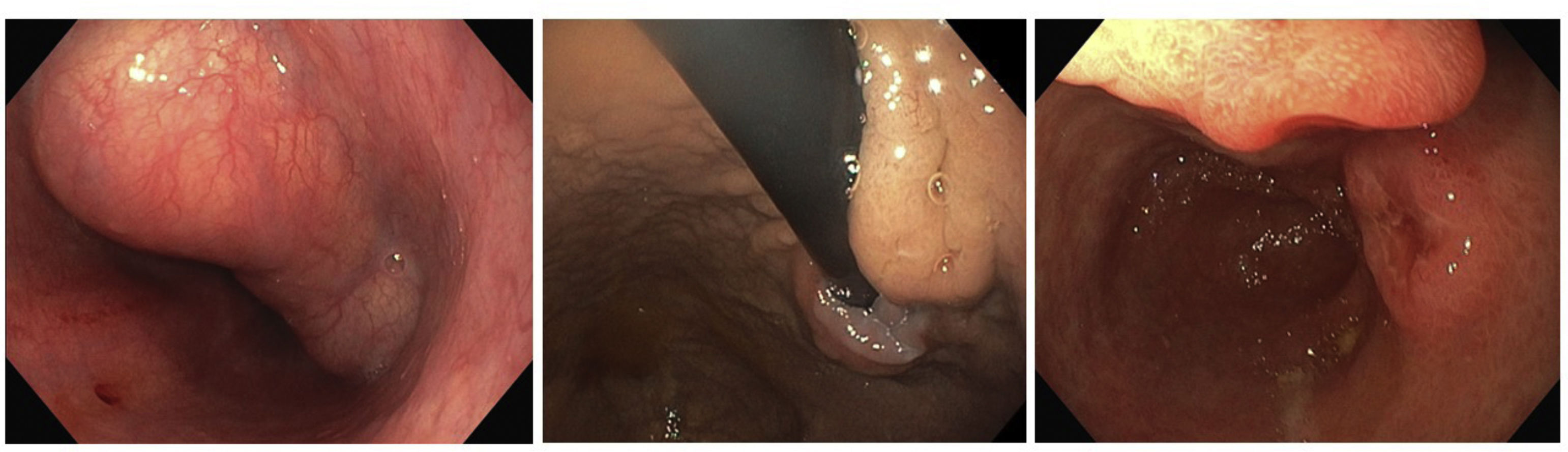
La EIO ha sido empleada para identificar intraoperatoriamente el tumor (fig. 3A), facilitar su enucleación y comprobar la integridad de la mucosa tras la resección21,22 (Vídeo 3).
Algunos grupos describen el empleo y la colocación por vía endoscópica de un balón que al inflarlo endoluminalmente facilita que el tumor protruya hacia el exterior ayudando a su enucleación toracoscópica de forma segura23.
Del mismo modo que en otro tipo de lesiones esofágicas, ha sido descrito el abordaje exclusivamente endoscópico para realizar la exéresis de este tipo de tumores, mediante la inyección de una sustancia en el interior de la mucosa esofágica con el objetivo de separar el tumor de la submucosa y posteriormente extirparlo24.
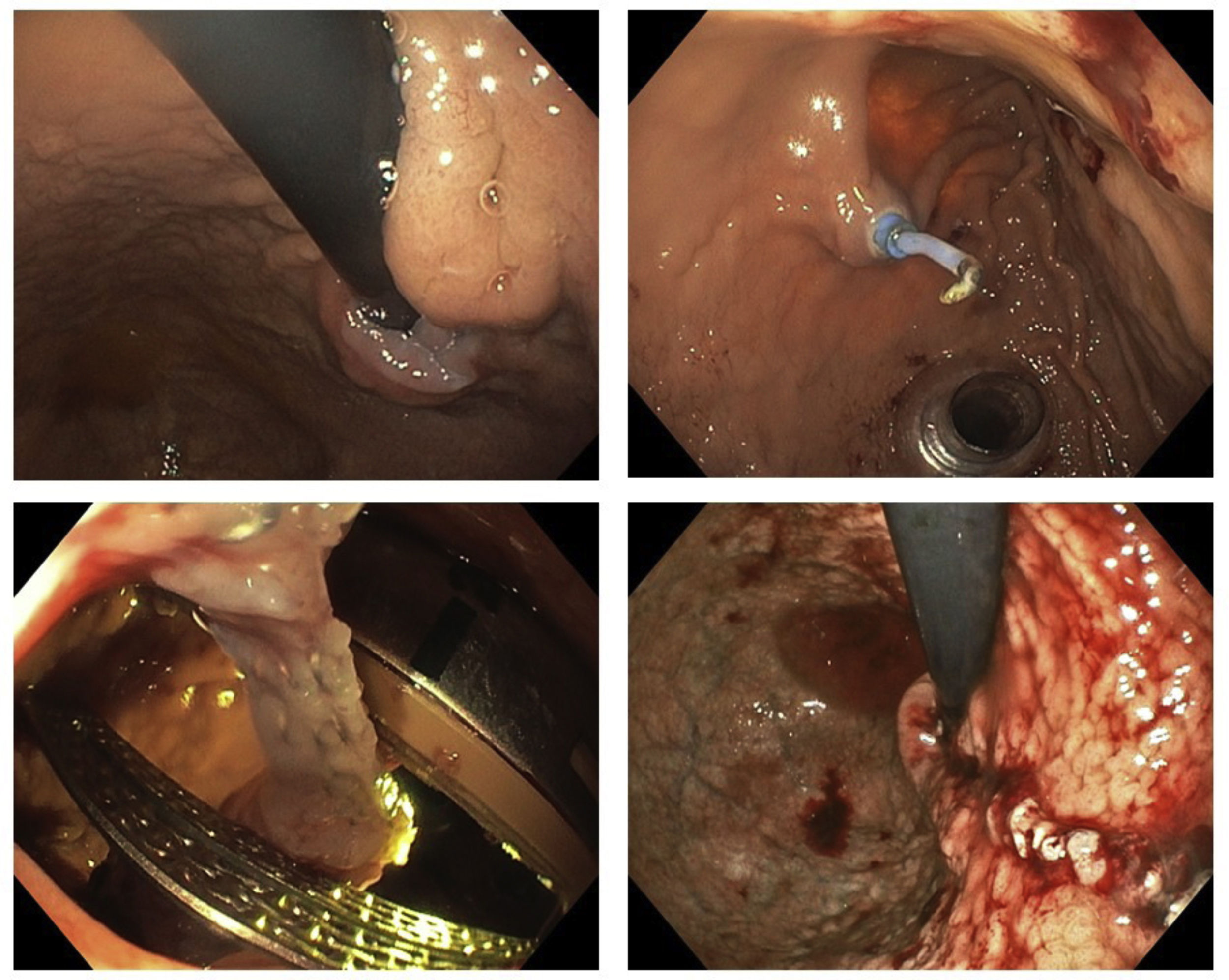
En el caso de los tumores GIST el abordaje endoscópico intraoperatorio resulta de gran utilidad para establecer la localización exacta de la lesión (fig. 3B), y en casos seleccionados puede emplearse para realizar resecciones combinadas transgástricas o por vía puramente endoscópica, sobre todo en localizaciones como la unión esofagogástrica (fig. 4A) o la región antropilórica, que supondrían una cirugía más agresiva.
A)Visión endoscópica de tumoración submucosa próxima a la unión esofagogástrica. B)Visión endoscópica de gastrostomía y colocación transgástrica de los trócares de laparoscopia. C)Visión endoscópica de la sección realizada con endograpadora. D)Visualización endoscópica de la línea de sección.
La resección endoscópica incluye diferentes modalidades, como la resección endoscópica de la mucosa (REM), la disección endoscópica submucosa (ESD), la excavación endoscópica submucosa (ESE), la resección endoscópica de espesor total (EFTR) y la resección endoscópica mediante tunelización submucosa (STER)25. La ESD se considera una técnica eficaz para los GIST; sin embargo, para los tumores que se originan en la capa muscular propia profunda pueden usarse la ESE y la EFTR26. La STER generalmente se usa para tratar los GIST de cardias, ya que protege la integridad de la mucosa27. En ocasiones es difícil determinar los límites del tumor mediante la laparoscopia, recomendándose en estos casos una técnica que combina la resección gástrica laparoscópica con la endoscopia intraluminal (LECS)28 (fig. 4B,C).
Cirugía de cáncerLa EIO resulta de gran utilidad para la identificación de lesiones tumorales que no son palpables o visibles por toracoscopia o laparoscopia y que no han sido marcadas previamente (fig. 3C).
Del mismo modo, permite evaluar la extensión endoluminal del tumor garantizando bordes proximales y distales libres de tumor macroscópico. En el caso de los adenocarcinomas de esófago distal que asientan sobre un esófago de Barrett, la EIO permite identificar la extensión de la metaplasia evitando abandonar áreas de posible afectación fuera del área de resección quirúrgica.
En lesiones localizadas en la mucosa sin afectación ganglionar y sin factores de riesgo, las técnicas de resección endoscópica han sido descritas y son aplicadas con resultados oncológicos satisfactorios y con un bajo índice de complicaciones. La más extendida es la ESD, con una tasa de remisión local completa que varía entre el 80 y el 99%29 y una tasa de supervivencia libre de enfermedad que se encuentra entre el 87 y el 100%30. Las complicaciones asociadas, como hemorragias, perforaciones (0-2%) y estenosis, son raras, y generalmente se manejan endoscópicamente con éxito31.
Tras la parte resectiva de este tipo de cirugías es necesario proceder a la reconstrucción del tránsito mediante la confección de diferentes anastomosis digestivas. Con el empleo de la EIO se pueden evaluar de forma segura este tipo de anastomosis, descartando la existencia de algún defecto o advirtiendo una fuga aérea al introducir el endoscopio y colocar la anastomosis sumergida en suero fisiológico (fig. 5). Diferentes estudios muestran que la realización de EIO disminuye el riesgo de fugas postoperatorias y se considera la mejor prueba para testar la anastomosis de forma intraoperatoria32-35. El empleo de la EIO en la valoración de la integridad de la anastomosis en cirugía de colon ha demostrado una reducción de las complicaciones36,37.
A)Visión endoscópica de anastomosis gastroyeyunal mecánica laterolateral. B)Visión endoscópica de anastomosis esofagoyeyunal terminolateral mecánica con CEEA de 25mm. C)Visualización endoscópica de anastomosis esofagogástrica terminolateral mecánica con CEEA de 25mm (a nivel cervical).
Además, se puede evaluar el calibre de la anastomosis descartando posibles estenosis, así como descartar posibles focos hemorrágicos en la línea de grapado34,38.
En el caso de esofagectomías, la EIO permite además evaluar la mucosa de la plastia utilizada para la reconstrucción, descartando la presencia de áreas de isquemia o lesiones de mucosa, sangrado, perforación, tanto en la línea de sección para la confección de la gastroplastia, como en la zona de la piloroplastia si se ha realizado. Además, la EIO permite descartar la presencia de posibles torsiones de la plastia ocasionadas durante su ascenso al tórax o al cuello o acodamientos en plastias redundantes.
Cirugía del reflujo esofagogástricoEn este tipo de cirugía, la EIO permite advertir posibles complicaciones secundarias al reflujo o alteraciones anatómicas asociadas, como la hernia de hiato.
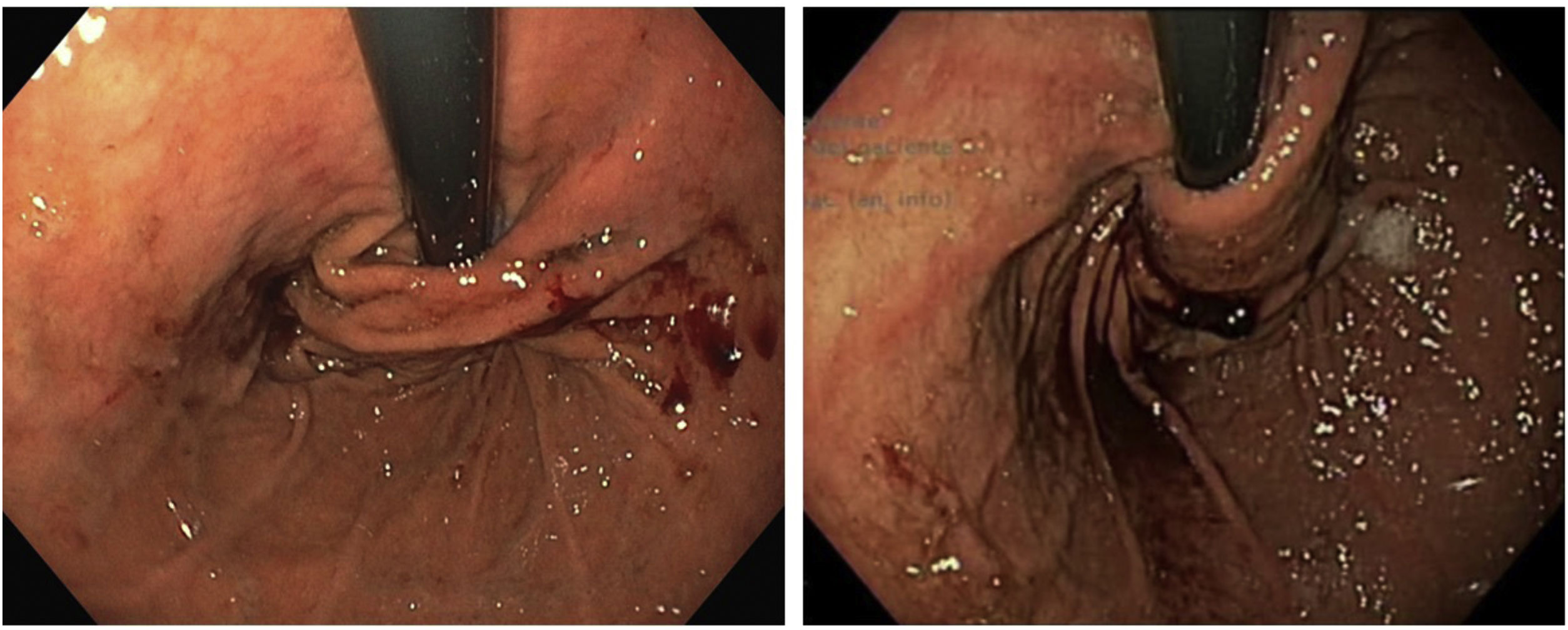
Una vez realizada la disección quirúrgica, la EIO permite comprobar la adecuada longitud esofágica (descartando la presencia de un esófago corto), la presencia de suficiente esófago abdominal, la localización exacta de la unión esofagogástrica (al identificar la unión escamocolumnar) para realizar la funduplicatura en una correcta posición y, una vez realizada esta, evaluar su competencia (grado en que la funduplicatura abraza el endoscopio al realizar una retrovisión) y descartar una presión elevada (resistencia al pasar el endoscopio por la unión esofagogástrica) que puedan comprometer los resultados postoperatorios (fig. 6) (Vídeo 4).
En algunas series se describe que, con el empleo intraoperatorio de la EIO, en el 28% de los procedimientos se realizó alguna corrección durante la cirugía y en el 2,5% se cambió el tipo de funduplicatura a realizar para evitar estenosis o angulaciones39.
Donde la EIO adquiere mayor importancia es en la cirugía de revisión, donde permite diagnosticar el problema que obliga a la reintervención, identificar la luz esofágica por transiluminación durante la adhesiolisis y evaluar la calidad de la nueva funduplicatura, descartando posibles perforaciones o lesiones mucosas.
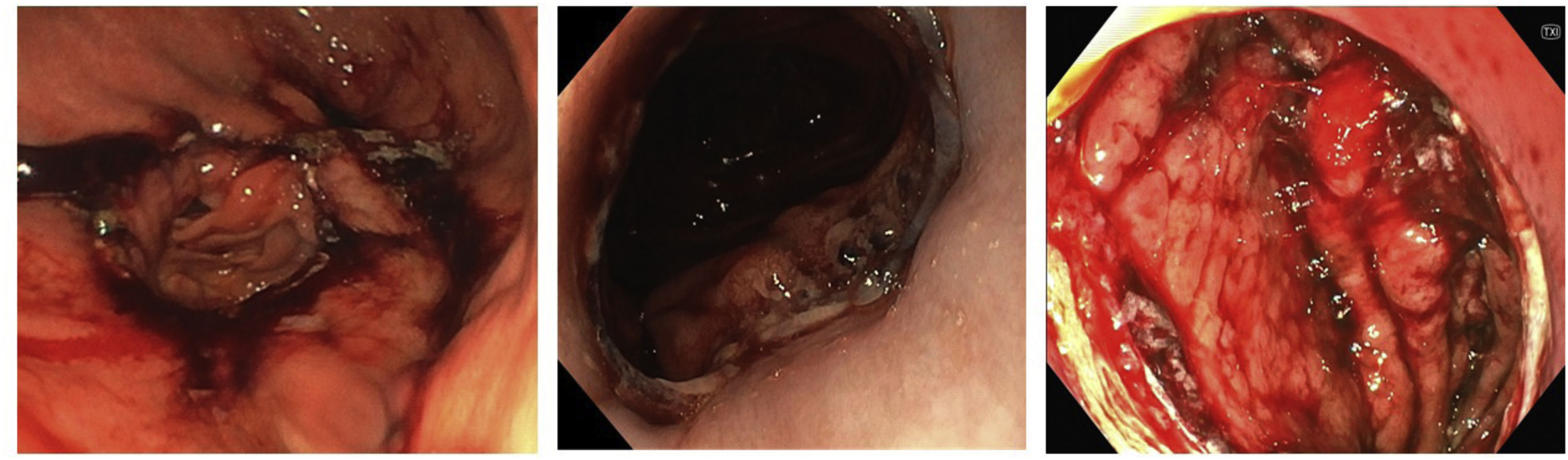
Cirugía por lesiones de cáusticosLa endoscopia digestiva alta (EDA) es la mejor prueba para evaluar la mucosa del esófago, del estómago y del duodeno, y su papel es crucial en el manejo de pacientes con lesiones por ingesta de cáusticos. En estos pacientes ya se pueden advertir alteraciones mucosas a partir de las 6horas de la ingesta. A partir de las 48horas, esta prueba debe realizarse con precaución por el riesgo de perforación. En general se recomienda su realización temprana, porque alrededor del 30% de los pacientes con ingestión de cáusticos no tendrán lesión en el esófago y pueden ser dados de alta rápidamente40,41. No se aconseja su realización en caso de obstrucción de la vía aérea o distrés respiratorio grave, lesiones graves en la hipofaringe, perforación de víscera hueca o inestabilidad hemodinámica.
A pesar de las ventajas que la tomografía computarizada (TC) ofrece en el diagnóstico de las posibles complicaciones y necrosis del tracto digestivo42, el uso de la EIO ayuda a la evaluación in situ de la localización y de la gravedad de las lesiones para tomar una decisión sobre la extensión y el tipo de resección quirúrgica a llevar a cabo.
Durante el seguimiento de estos pacientes, la EDA puede ayudar a valorar la aparición de nuevas lesiones, estenosis o incluso neoplasias.
El tratamiento endoscópico de las estenosis secundarias a la ingesta de cáusticos generalmente se realiza 3semanas después de la ingesta, no debiendo demorarse más allá de 8semanas, cuando el tejido cicatricial está completamente formado y el resultado de la dilatación endoscópica no suele ser satisfactorio43. A pesar de existir una amplia variedad de dilatadores, todos parecen tener una tasa de éxito comparable (25-95%), en función de la gravedad de la estenosis44,45, y una tasa de perforación del 0,1 al 0,4%46.
En el caso de estenosis refractarias se han empleado otras técnicas, como electrocisión47, inyección intralesional de esteroides48, inyección de mitomicina-C49 y stent esofágico (tasa de éxito: 33%; tasa de migración: 40%)50.
Posibles complicaciones asociadas a la endoscopia intraoperatoriaA pesar de las ventajas descritas de la EIO, este procedimiento no está exento de posibles complicaciones, tales como el sangrado y la perforación, entre otras. Para evitarlas, el cirujano y el personal de quirófano deben estar adecuadamente capacitados y formados con el uso, el cuidado, el mantenimiento, la descontaminación y la solución de posibles problemas de equipo y con las herramientas comúnmente utilizadas51.
Empleo, aprendizaje y acreditaciónLas oportunidades de capacitación en EF varían ampliamente entre instituciones, especialidades y países. A pesar de ser una capacitación obligatoria en la residencia quirúrgica de países como América del Norte, Australia y países de Asia, en otras partes del mundo los cirujanos no tienen acceso a la práctica de la EF durante su formación ni en el desarrollo posterior de su asistencia profesional52-54.
Situación actual en EspañaEn nuestro país la realización de esta exploración es llevada a cabo en la mayor parte de los centros por médicos digestólogos especializados en endoscopia, siendo escasos los centros en los que los cirujanos son los responsables de realizar esta exploración con fines diagnósticos.
Actualmente los programas de formación de los médicos residentes de cirugía general y del aparato digestivo son insuficientes para la formación en EF.
Debido a las ventajas que ofrece la EF, el acceso a la formación, a la acreditación de competencias y a la experiencia práctica debe ser fomentado con mayor intensidad desde sociedades científicas y quirúrgicas. Los pasos hacia una experiencia de capacitación más uniforme y adecuada deben incluir abordar las políticas actuales del Consejo de Acreditación para la Educación Médica de Graduados (ACGME), utilizar de manera eficiente los recursos disponibles, incluidos los simuladores, e instituir un plan de estudios de endoscopia estandarizado y validado que incorpore las recomendaciones de las sociedades de cirugía y gastrointestinales55.
Como intento de expandir su uso e implementar esta técnica en nuestros quirófanos, la Asociación Española de Cirujanos ha diseñado un programa formativo en EIO para cirujanos digestivos. Este programa consta de 5 fases, y se puso en marcha en diciembre de 2020, por lo que en unos años podrán evaluarse los resultados de esta iniciativa y el grado de implementación de este procedimiento en nuestra rutina laboral.
Situación actual en otros paísesEn Canadá la capacitación en endoscopia es parte del plan de estudios básico en la residencia de cirugía general, realizando los cirujanos generales aproximadamente el 50% de todos los procedimientos endoscópicos56. A pesar de ello, en una encuesta realizada sobre el aspecto formativo en endoscopia, el 47% de los cirujanos informaron que la capacitación actual en endoscopia es inadecuada y el 39% de los residentes de cirugía no se sentían preparados para realizar endoscopia debido a una formación deficiente54,57.
En América, los cirujanos generales realizan endoscopias tanto diagnósticas como terapéuticas no intraoperatorias. The American Board of Surgery (ABS) reconoció la necesidad de incorporar la formación en endoscopia en la residencia de cirugía general, y en 1985 recomendó un mínimo de 29 casos realizados por el residente durante su formación, que posteriormente aumentó a 35 endoscopias digestivas altas (EDA) y 50 colonoscopias. La Sociedad Americana de Cirujanos Generales y Endoscopistas (SAGES) desarrolló el programa de Fundamentos de Cirugía Endoscópica (FES), puesto en marcha en 2010, a fin de estandarizar y evaluar la formación en endoscopia58.
En la Unión Europea de Médicos Especialistas (UEME) la formación en EF forma parte del currículum del cirujano general, aunque no es equiparable en todos los países. En 2014 el Instituto de Investigación contra el Cáncer Digestivo (IRCAD) participó en el desarrollo de un diploma universitario utilizando métodos de educación avanzada, de un año de duración, para ofrecer tanto a cirujanos como a gastroenterólogos una formación de alta calidad en EF. El plan de estudios combina el aprendizaje online, las prácticas y el seguimiento clínico59. En el Reino Unido el programa de acreditación en EDA es común para cirujanos y gastroenterólogos, y para poder obtener la competencia y su práctica independiente se requieren 200 procedimientos y acceder a la acreditación mediante DOPS (Direct Observation of Procedural Skills)60.
En muchos países de Asia la formación en endoscopias se encuentra dentro del programa formativo del residente61, aunque todavía falta una estrategia estandarizada para la enseñanza62, siendo los médicos generales los que realizan el mayor número de endoscopias.
ConclusiónLa EIO es una técnica que presenta importantes beneficios que aportan seguridad a los procedimientos quirúrgicos en la patología esofagogástrica y debería ser implementada por los cirujanos en su actividad quirúrgica habitual.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.