La enfermedad arterial periférica es una manifestación común de la aterosclerosis sistémica que se asocia a un mayor riesgo cardiovascular. Dado que los pacientes con enfermedad arterial periférica pueden presentar asimetría o ausencia de pulsos, aún estando asintomáticos, ante un evento coronario agudo en estos pacientes debemos realizar el diagnóstico diferencial con la disección de aorta.
Peripheral arterial disease is a common manifestation of systemic atherosclerosis that is associated with increased cardiovascular risk. When presented in the context of an acute coronary syndrome a differential diagnosis with aorta dissection should be made, because peripheral arterial disease may be asymptomatic despite the absence or asymmetry of femoral pulses.
La enfermedad arterial periférica (EAP) es una patología de difícil diagnóstico por ser, la mayoría de las ocasiones, subclínica. Según la guía española de consenso multidisciplinar en EAP de extremidades inferiores, su prevalencia en la población española se sitúa entre el 4,5 y el 8,5% según las series, de la que el 3,8-24,5% es silente y el 6-29,3% suele presentarse como claudicación intermitente1.
Teniendo en cuenta que la diabetes, la hipertensión arterial, el tabaquismo o la hiperlipidemia están presentes en la mayoría de los casos2, que la incidencia de EAP teniendo, en cuenta la edad y el sexo, sigue una distribución similar a la enfermedad coronaria con una relación hombre-mujer 2:1 en todos los grupos de edad3 y que la cardiopatía isquémica es la principal causa de muerte tardía4, su diagnóstico en estadios subclínicos resulta fundamental. Igualmente, dado que la ausencia o asimetría de pulsos sin clínica asociada (estadio i de la clasificación clínica de Leriche-Fontaine, ya sea porque la obstrucción del vaso no es completa o porque se han desarrollado mecanismos de compensación a expensas de arterias colaterales) puede simular una disección de aorta en un paciente con un evento coronario agudo, debemos tener en cuenta esta asociación en el diagnóstico diferencial del dolor torácico.
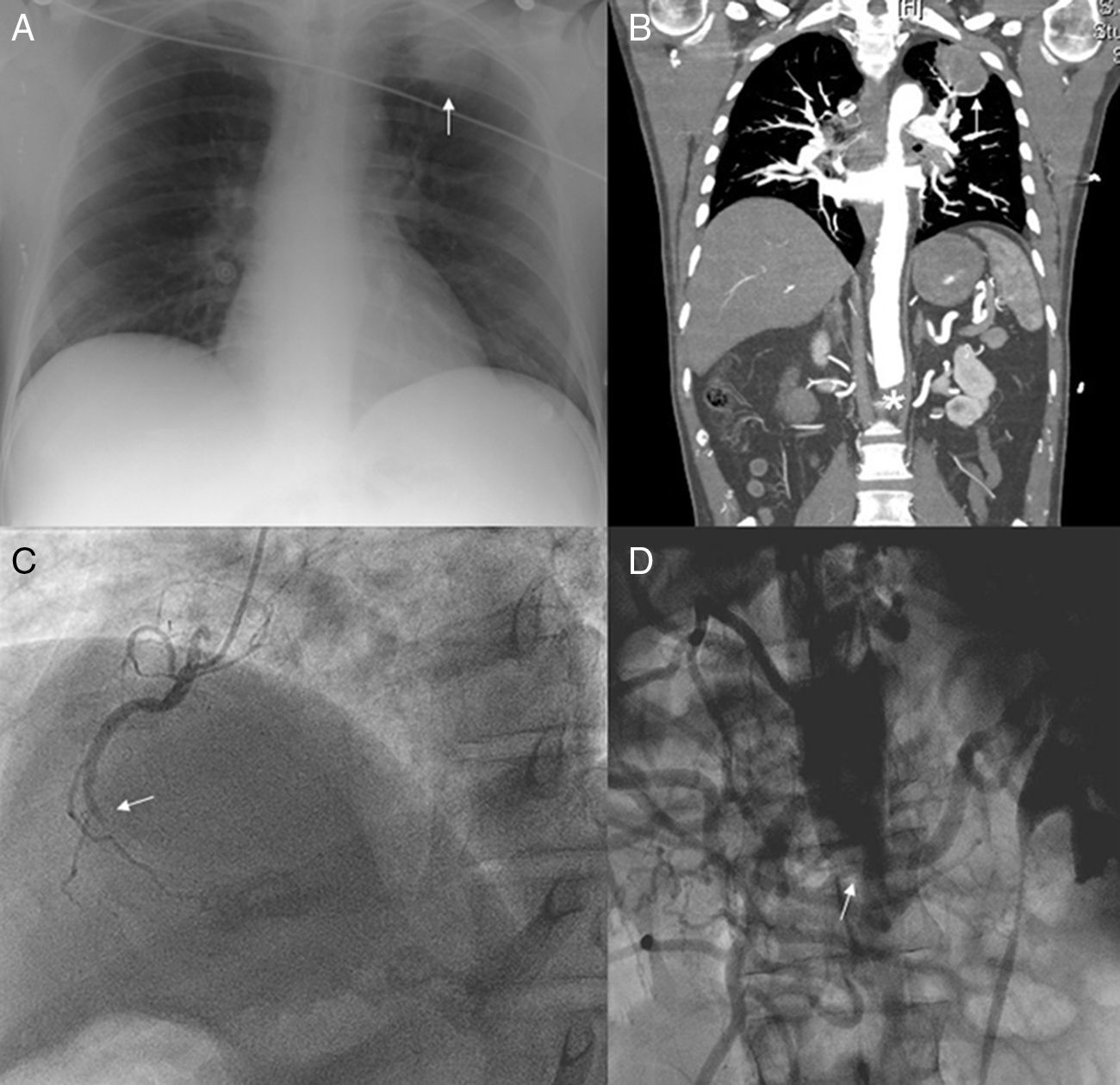
Caso clínicoVarón de 57 años de edad, sin factores de riesgo cardiovascular, salvo fumador de 30 cigarrillos/día, y sin antecedentes de cardiopatía isquémica ni EAP, que ingresa por dolor centrotorácico de características isquémicas asociado a cortejo vegetativo de una hora de evolución. Al ingreso se evidenció en el electrocardiograma elevación del ST en la cara inferior, hipocinesia inferior en la ecocardiografía y una masa en el lóbulo superior izquierdo en la radiografía de tórax (fig. 1A). Debido a la presencia hipertensión arterial severa de difícil control y a la ausencia de pulsos femorales, asociada a dolor abdominal difuso, se decidió la realización de una tomografía computarizada (TC) toracoabdominal con el fin de descartar la existencia de disección de aorta. En esta se confirmó la presencia de una masa pulmonar, sospechosa de neoplasia, y la existencia de una oclusión de la aorta abdominal a nivel infrarrenal (fig. 1B) sin datos de disección. Ante estos hallazgos, y ante la dificultad en el control de la presión arterial, se decidió la realización de un cateterismo cardiaco urgente por vía radial. En este se evidenció la oclusión de la arteria coronaria derecha (fig. 1C), que se recanalizó con el implante de 2 stents convencionales, y la oclusión de la aorta abdominal a nivel infrarrenal con abundante circulación colateral (fig. 1D).
A) Radiografía de tórax en posteroanterior evidenciando una masa a nivel del lóbulo superior izquierdo (flecha). B) Tomografía computarizada toracoabdominal, corte coronal, donde se evidencian la masa pulmonar (flecha) y la oclusión de la aorta a nivel abdominal (asterisco). C) Coronariografía (oblicua anterior derecha) en la que se evidencia oclusión de la coronaria derecha a nivel de tercio medio (flecha). D) Aortografía abdominal (anteroposterior) donde se evidencia oclusión a nivel de la aorta abdominal (flecha) con abundante circulación colateral.
La aterosclerosis, la tromboangitis obliterante (enfermedad de Buerger), la enfermedad de Takayasu y de Horton, la degeneración quística de la media, la fibrosis periarterial idiopática retroperitoneal o las arteritis específicas pueden conllevar al desarrollo de EAP. Sin embargo, la aterosclerosis es la causa más frecuente y la responsable del 95% de los casos. En estos pacientes, los factores de riesgo preponderantes son la diabetes mellitus, la hipertensión arterial, la dislipidemia y el tabaquismo3,5,6. Uno de cada 3-4 pacientes diabéticos tipo ii presenta EAP, un 20-40% hipertensión arterial y entre un 60 y un 77% dislipidemia1,4. Por otro lado, el tabaquismo es el factor de riesgo modificable más importante, aumentando el riesgo de tener EAP en 2-6 veces1, presentando hasta un 50% de los pacientes con EAP síntomas asociados de enfermedad cerebrovascular o coronaria7.
Cuando se evidencia obliteración aortoilíaca, como ocurre en el caso descrito, los hallazgos patológicos característicos suelen ser lesiones arteroscleróticas progresivas de la pared de la aorta abdominal, con trombosis superpuesta, que afecta en mayor o menor grado a la bifurcación aortoilíaca y se extiende en sentido proximal sin afectar a las arterias renales. Esta forma clínica es de presentación precoz, normalmente entre los 35 y 55 años, y afecta a los varones en una relación 3:1 con respecto a las mujeres, siendo los factores de riesgo cardiovascular más prevalentes la hiperlipidemia y el tabaquismo5.
Aunque dentro del diagnóstico diferencial de la arteriopatía aortoilíaca debemos incluir dolores neurológicos (como lumbociáticos, las hernias discales o las lesiones del plexo crural) y osteomusculares (como la osteoartritis, la sacroilitis o la coxartrosis) —ya que la sintomatología en estos pacientes suele ser la claudicación en las masas musculares de glúteos, muslos y gemelos e impotencia en el varón si hay afectación bilateral (síndrome de Leriche)—, ante un síndrome coronario agudo debemos tener en cuenta otras posibilidades diagnósticas, como la disección de aorta.
La disección de aorta suele asociarse a hipertensión arterial en el 80-90% de los casos, el déficit de pulsos es frecuente (un 50% en la disección de aorta proximal y un 15% en la disección de aorta distal) y el infarto de miocardio suele ser de localización inferior (1-2%)8, 3 de los hallazgos presentes en nuestro paciente. En estos casos, realizar una adecuada historia clínica, exploración física (con evaluación de los pulsos, coloración y temperatura de las extremidades, presencia o ausencia de atrofia muscular y cicatrización tórpida de las heridas) conjuntamente con pruebas de imagen, como la ecocardiografía o la TC, nos ayudará a realizar un diagnóstico correcto. Igualmente, debemos tener en cuenta que el tabaquismo, uno de los factores de riesgo más importantes para desarrollar EAP, es también la principal causa de neoplasia pulmonar.
ConclusiónLa arteriopatía periférica puede conllevar retos diagnósticos y terapéuticos en pacientes con un síndrome coronario agudo. Realizar una adecuada historia clínica, apoyada en pruebas de imagen nos permitirá realizar un diagnóstico diferencial adecuado y plantear el mejor abordaje terapéutico.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesNo existe conflicto de interés por parte de los autores. Ninguno de los autores ha recibido financiación. Todos los autores han participado en la interpretación de los datos, la redacción del artículo y la aprobación final de la versión a publicar.