La anemia es una manifestación común en los pacientes con insuficiencia renal crónica (IRC) y un hallazgo constante en los pacientes crónicos en hemodiálisis.
Los factores que contribuyen a la aparición de la anemia en pacientes con IRC son insuficientes producción y secreción renal de eritropoyetina (EPO), alteración de la eritropoyesis por la presencia de toxinas uréticas y disminución de la vida media del eritrocito 1,2.
Además, los pacientes con IRC en hemodiálisis o diálisis peritoneal continua ambulatoria (CAPD) sufren un incremento de la pérdida de sangre debido a su propia diálisis y a la toma de muestras para el laboratorio. También, la pérdida de sangre debido a lesiones gastrointestinales y a la utilización de anticoagulantes y antitrombóticos es frecuente en los pacientes con IRC. Las hemorragias gastrointestinales tienen una prevalencia del 18, el 7,3 y el 6,3 % en pacientes de prediálisis, diálisis peritoneal y hemodiálisis, respectivamente 3,4.
La corrección de la anemia en pacientes con IRC mejora la supervivencia, disminuye la morbilidad y aumenta la calidad de vida 5,6.
La terapia con agentes estimuladores de la eritropoyesis (ESA) ha representado un avance para el tratamiento de la anemia en pacientes con IRC, pero requiere depósitos de hierro apropiados y una movilización rápida del hierro para abastecer las necesidades eritropoyéticas. Además, el tratamiento con agentes estimuladores de la eritropoyesis es costoso. De acuerdo con el estudio epidemiológico PRESAM (Pre-dialysis Survey of Anaemia Management), la administración de hierro está asociada con un aumento de la respuesta a la eritropoyetina 7, y un suplemento insuficiente de hierro está asociado a la necesidad de dosis más altas de eritropoyetina (agente estimulador de la eritropoyesis).
La concentración de hemoglobina objetivo recomendada en pacientes anémicos con IRC son > 11 g/dl, según las guías European Best Practice Guidelines for the Management of anaemia. En estos pacientes, cifras de hemoglobina > 11 g/dl se pueden alcanzar con una nutrición adecuada y una administración de hierro apropiada 6.
La corrección de la anemia renal con agentes estimuladores de la eritropoyesis está frecuentemente asociada a una disminución progresiva de la concentración de hierro y a un déficit funcional de hierro. En muchos pacientes con IRC, especialmente los que están en diálisis, el tratamiento con hierro oral no consigue cubrir las demandas eritropoyéticas ni mantener depósitos de hierro efectivos. Los pacientes con IRC no presentan una correcta absorción gastrointestinal del hierro, especialmente en pacientes urémicos. Además, frecuentemente no hay conformidad con el hierro oral debido a la elevada aparición de efectos adversos o intolerancia. En estos casos la administración de hierro intravenoso es esencial para asegurar la efectividad del tratamiento de la anemia renal y favorecer la respuesta al tratamiento con ESA.
Las guías terapéuticas, Best Practice Guidelines for the Management of Anaemia in Patients with Chronic Renal Failure, recomiendan la utilización de hierro intravenoso como la vía de administración más adecuada para el tratamiento de la anemia renal en pacientes en hemodiálisis y consideran la preparación hierro sacarosa intravenoso (Venofer®) como la preparación de hierro intravenoso más segura 6.
El hierro sacarosa intravenoso es un complejo que posee una estabilidad adecuada que le permite un intercambio competitivo y rápido del hierro entre el hierro sacarosa y las proteínas selectivas fijadoras de hierro, tales como la transferrina y la ferritina. De esta manera, el hierro se distribuye rápidamente y se incorpora a los órganos diana, lo que asegura una rápida corrección del déficit férrico 8. Estas propiedades del hierro sacarosa intravenosos son cruciales en pacientes con una necesidad clínica de liberación rápida de hierro a los depósitos de hierro, con una anemia por déficit de hierro debido a un aporte insuficiente de hierro o pérdida de hierro, que no toleran el hierro oral o por falta de cumplimiento del tratamiento con hierro oral. En los pacientes en tratamiento con eritropoyetina, mediante la administración de hierro sacarosa intravenoso se puede conseguir la optimización de la eritropoyesis y reducir significativamente los requerimientos de eritropoyetina y, por lo tanto, los costes del tratamiento 9.
La propiedades farmacológicas del complejo hierro sacarosa le confieren un perfil de toxicidad favorable. El perfil de seguridad y tolerabilidad del hierro sacarosa intravenoso ha sido demostrado en la experiencia clínica durante más de 3 décadas. El hierro sacarosa intravenoso es seguro y bien tolerado en el tratamiento y la prevención de la anemia por déficit de hierro 10-12. Además, los índices de reacciones de hipersensibilidad debidas a la administración de hierro sacarosa son extremadamente bajos en comparación con las de las demás preparaciones de hierro parenteral, como hierro dextrano o hierro gluconato 13,14.
Pacientes en prediálisis
El 60 % de los pacientes con IRC que inician la diálisis presenta déficit de hierro, del cual el 39 % es déficit real de hierro y el 22 %, déficit funcional de hierro 7.
El tratamiento con hierro intravenoso ha sido reconocido hasta ahora como una terapia para la anemia de pacientes crónicos en hemodiálisis, especialmente en los pacientes tratados con ESA, mientras que su función en la anemia de pacientes con IRC en prediálisis resultaba desconocida.
Actualmente se han realizado distintos estudios que demuestran que la administración de hierro intravenoso en pacientes con IRC en prediálisis mejora la anemia renal y reduce la dosis necesaria de ESA, en ausencia de reacciones adversas.
Mircescu et al 15 trataron a 60 pacientes con IRC moderada en prediálisis con 200 mg de hierro sacarosa intravenoso, una vez al mes durante 1 año, y observaron un incremento significativo de las concentraciones de hemoglobina (de 9,7 ± 1,1 a 11,3 ± 2,5 g/dl), un aumento de la ferritina sérica (de 98,0 a 442,5 mg/l) y de TSAT (de 21,6 ± 2,6 a 33,6 ± 3,2 %). Además, no empeoró la función renal y tampoco se observaron efectos adversos del tratamiento. Por lo tanto, concluyeron que el tratamiento con hierro sacarosa mejora los valores de hierro y parece ser efectivo y seguro para la corrección de la anemia de pacientes con IRC en prediálisis, evitando el tratamiento con ESA. Resultados similares fueron observados por Silverberg et al 16, cuando administraron 200 mg de hierro sacarosa una vez al mes durante 5 meses, a pacientes en prediálisis no respondedores al tratamiento con hierro oral.
Posteriormente, esos mismos autores demostraron que el tratamiento de pacientes en prediálisis con hierro-sacarosa junto con bajas dosis de ESA era más rápido y efectivo que el tratamiento sólo con hierro sacarosa. Después de tratar a 90 pacientes con IRC en prediálisis durante 5 semanas con 200 mg una vez a la semana junto con 2.000 IU de rHuEPO, observaron que el 80 % de los pacientes aumentó el hematocrito en un 3 % 17.
Con el objetivo de comparar la eficacia del tratamiento con hierro oral diario y la eficacia del tratamiento con hierro sacarosa intravenoso semanal en pacientes anémicos con IRC en prediálisis tratados con ESA, se realizó un estudio en el que 96 pacientes tratados con rHuEPO recibieron hierro sulfato oral 325 mg t.i.d una vez al día, durante 29 días, o 200 mg de hierro sacarosa intravenoso una vez a la semana, durante 5 semanas. Los resultados obtenidos fueron que los pacientes tratados con hierro sacarosa presentaron un incremento superior de la concentración de ferritina y de hemoglobina que los pacientes tratados con hierro oral, que no aumentaron los depósitos de hierro. No se detectaron efectos adversos graves 18.
De ese estudio se concluye que el tratamiento con hierro sacarosa intravenoso de pacientes anémicos en prediálisis permite incrementar, de forma rápida y segura, los depósitos de hierro y alcanzar concentraciones de hemoglobina > 11 g/dl, tal como recomiendan las guías terapéuticas: Revised European Best Practice Guidelines for the Management of Anaemia in Patients with Chronic Renal Failure 6.
En resumen, el tratamiento de la anemia en pacientes con IRC en prediálisis con hierro sacarosa es un tratamiento eficaz que evita la necesidad de utilizar ESA, por lo que resulta un tratamiento coste-efectivo. Éste es un aspecto económico de gran importancia en países como Rumanía, en los que sólo se permite la administración de rHuEPO cuando el paciente está en hemodiálisis. Además, el tratamiento con hierro sacarosa intravenoso es la alternativa terapéutica para pacientes que no toleran el tratamiento con hierro oral, capaz de corregir la anemia y mejorar la calidad de vida del paciente. La administración de hierro sacarosa en pacientes de prediálisis es un tratamiento seguro, como se demuestra en el estudio de Macdougall et al 19, en el que tras la administración de 2.297 inyecciones de 200 mg de hierro sacarosa, durante 2 min, a 657 pacientes en prediálisis, no se reportaron reacciones adversas graves. Ese estudio nos muestra que la administración de hierro sacarosa intravenoso en bolo durante 2 min es una práctica clínica segura y eficaz para el tratamiento de la anemia renal y permite ahorrar tiempo y costes.
En los últimos años se ha comenzado a dar importancia a la relación entre IRC, insuficiencia cardíaca congestiva (ICC) y la anemia. La combinación de estas afecciones forma un círculo vicioso en el que cada una de ellas empeora las otras. La anemia en los pacientes con ICC está asociada a un incremento de mortalidad y de hospitalización. En los pacientes ICC anémicos, disminuye la función cardíaca y se asocia a un mayor deterioro de la función renal que en los pacientes no anémicos 20. Varios estudios publicados han demostrado que un tratamiento adecuado de la ICC, junto con un tratamiento para la corrección de la anemia mediante la administración de ESA y hierro oral o intravenoso, puede mejorar la función cardíaca, la función renal y la calidad de vida y reducir la frecuencia de hospitalización y la dosis de diuréticos requeridos. Un estudio prospectivo en 26 pacientes con ICC y anemia mostró que la corrección de la anemia con ESA y hierro intravenoso mejoró la función ventricular izquierda y el estadio de la NYHA, disminuyó la tasa de hospitalizaciones y permitió disminuir las dosis de furosemida 21. En un ulterior estudio controlado, en 32 pacientes con anemia se observó que las cifras de creatinina sérica permanecían estables en los 16 pacientes control en los que se corrigió la anemia con ESA y hierro sacarosa intravenoso, mientras que aumentaron significativamente en los pacientes que permanecieron con anemia 22. Resultados similares fueron observados en otro estudio que incluyó a 179 pacientes con anemia e ICC, de los que la mitad eran diabéticos 23.
Estos estudios confirman la corrección de la anemia con el tratamiento con hierro sacarosa combinado con ESA en pacientes con ICC, y mejora la función cardíaca.
Pacientes en hemodiálisis
Como ya se ha comentado, la deficiencia de hierro en pacientes con IRC puede comenzar ya antes de iniciar tratamiento con diálisis. Esta deficiencia se hace más acusada en los pacientes ya sometidos a hemodiálisis debido a múltiples causas (pérdidas por sangrado gastrointestinal, sangrado de los puntos de punción, sangre retenida en el dializador, múltiples análisis, etc.). El uso de eritropoyetina ha potenciado aún más este problema debido al rápido incremento en las necesidades de movilización de hierro. Los suplementos orales de hierro generalmente no son suficientes para aportar la suficiente cantidad de hierro para cubrir estas necesidades, así que se hace necesario el tratamiento con hierro sacarosa intravenoso. Recientemente se han publicado varios estudios que confirman la seguridad y la eficacia del uso de hierro intravenoso en este tipo de pacientes.
En el North American Clinical Trial 24, se estudia el uso de hierro sacarosa intravenoso en 77 pacientes en hemodiálisis con anemia por déficit de hierro, aun estando en tratamiento con rHuEPO, e incluye 10 casos con antecedentes de reacciones anafilácticas a hierro dextrano. Todos los pacientes recibieron una dosis total de 1.000 mg de hierro sacarosa intravenoso repartidos en dosis de 100 mg de hierro en 10 sesiones de diálisis. El incremento de hemoglobina se evidenció ya tras 3 dosis de hierro sacarosa y persistió hasta al menos 5 semanas después de la décima dosis. Durante esas 5 semanas posteriores a la finalización del tratamiento, el 78 % de los pacientes alcanzaron los valores de hemoglobina objetivo (> 11 g/dl), con recuperación de las cifras de porcentaje de saturación de la transferrina y de ferritina. En cuanto a aspectos de seguridad: al 91 % de los pacientes se les administró hierro intravenoso en bolo durante 5 min. No hubo necesidad de interrumpir el tratamiento por acontecimientos adversos en ningún caso y no se detectaron acontecimientos adversos graves. Este estudio confirma los datos previos de eficacia y seguridad de hierro sacarosa intravenoso en el tratamiento de la anemia por deficiencia de hierro en pacientes hemodializados en tratamiento con ESA.
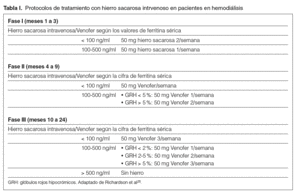
Con el objetivo de lograr un mejor ajuste del tratamiento con hierro sacarosa intravenoso y eritropoyetina (rHuEPO) en estos pacientes, Richardson et al 25 han publicado recientemente un artículo en el que se pretendía evaluar el valor predictivo de las concentraciones de ferritina sérica y el porcentaje de glóbulos rojos hipocrómicos (%GRH) durante un período de 24 meses. Se administró hierro sacarosa a una cohorte de pacientes en hemodiálisis (n = 228) para lograr una hemoglobina objetivo que cumpliese los estándares de la UK Renal Association con el 85 % de hemoglobina $ 10 g/dl. Tanto la dosis de hierro como la de EPO se ajustaban mensualmente mediante protocolos informatizados. En el caso del hierro intravenoso, se utilizaron 3 protocolos diferentes y en todos ellos el tratamiento fue interrumpido cuando los valores de ferritina superaron los 500 ng/ml (tabla I).
A todos los pacientes se les administró rHuEPO por vía subcutánea para alcanzar una concentración media de hemoglobina de 11,5 g/dl, estableciéndose un valor umbral de hemoglobina (11 g/dl) por debajo del cual las dosis de rHuEPO se incrementaban. El valor de hemoglobina por encima del cual las dosis de rHuEPO se redujeron a razón de 1.000 UI/ dosis administrada osciló en 12-13 g/dl. Con estos protocolos de tratamiento se consiguió una disminución media del porcentaje de glóbulos rojos hipocrómicos (el 8 y el 4 %), incrementar los valores medios de ferritina a 480 ng/ml, con un intervalo intercuartílico en 350-650, y disminuir las necesidades medias de rHuEPO de 136 a 72 IU/kg/semana. Este estudio demuestra que, con protocolos adecuados de administración y una adecuada monitorización basada en los valores de ferritina y porcentaje de glóbulos rojos hipocrómicos, se puede optimizar el tratamiento de la anemia sin problemas de toxicidad. Estos datos concuerdan con los publicados por Descombes et al 26 en un estudio de seguimiento a 18 meses en el que el tratamiento con hierro sacarosa intravenoso consiguió mantener los valores de hemoglobina y hematocrito objetivo, con un mantenido y significativo decremento de las necesidades de eritropoyetina.
Además de su eficacia, el tratamiento con hierro sacarosa presenta un mejor perfil de seguridad que presentaciones anteriores de hierro intravenoso 14. Este buen perfil de seguridad se ha descrito incluso en pacientes en hemodiálisis que presentaban intolerancia a hierro dextrano y/o gluconato. La cantidad de hierro sacarosa intravenoso administrado a los 130 pacientes incluidos en el estudio 27 osciló entre 100 y 5.000 mg (mediana, 1.000 mg), administrados en dosis intravenosas de 100-200 mg durante 2-5 min o diluido en suero salino isotónico durante 15-30 min. No se detectó ningún acontecimiento adverso grave. Sólo se comunicó 14 reacciones adversas en 8 pacientes, ninguna de las cuales precisó interrumpir el tratamiento.
Por tanto, lo publicado muestra que el tratamiento con hierro sacarosa intravenoso es eficaz y seguro en el tratamiento de pacientes en hemodiálisis. El hierro sacarosa permite optimizar el tratamiento con ESA en pacientes con anemia por deficiencia de hierro e incluso disminuir las dosis (y por tanto los costes) de estos agentes en tratamientos a largo plazo. Estos datos son aplicables también a pacientes que previamente habían mostrado intolerancia a otras formulaciones de hierro intravenoso.
Diálisis peritoneal
En los pacientes sometidos a diálisis peritoneal (DP), las pérdidas sanguíneas son menores que en los pacientes sometidos a hemodiálisis, y rondan los 250 ml/año (aproximadamente, 100 mg de hierro/ año). En muchos casos, el suplemento con hierro oral resulta ineficaz, como se observa en el artículo de Macdougall et al 28 en que se estudió a más de 600 pacientes en diálisis peritoneal durante 6 meses con suplementos de hierro oral, en los que se observó que un 50 % presentaba anemia por deficiencia de hierro. A diferencia del hierro oral, que no consigue un buen control de la anemia aun cuando se administre combinado con eritropoyetina, el hierro sacarosa intravenoso ha demostrado una rápida y mantenida corrección de la anemia e incluso menor necesidad de eritropoyetina. Estos datos concuerdan con los publicados por Silverberg et al 29, en un subgrupo de 9 pacientes en diálisis peritoneal ambulatoria continua (DPCA), 4 de ellos en tratamiento previo con EPO (61 ± 17 IU/kg/semana), que recibieron tratamiento con hierro sacarosa (100 mg intravenosos 2 veces al mes) durante 6 meses. El tratamiento con Fe consiguió el objetivo de hematocrito > 33 % sin necesidad o con bajas dosis de EPO, sin presentar acontecimientos adversos de relevancia. Estos resultados concuerdan con los publicados posteriormente por Domrongkitchaiporn 30, en que se estudió a 24 pacientes en DPCA anémicos, en tratamiento con Fe oral y EPO durante al menos 3 meses. Se demostró que el tratamiento con Fe intravenoso (2 dosis de 500 mg de Fe intravenoso cada semana) mejoraba las cifras de hemoglobina de estos pacientes. A los 3 meses de instaurado el nuevo tratamiento, se observó un incremento de al menos 1 g/dl en el 71 % de los pacientes. Los datos aportados permiten concluir que el tratamiento con Fe intravenoso restaura la respuesta al tratamiento con EPO en pacientes en DP en tratamiento previo con EPO y Fe oral. La dosis empleada ha sido alta, pero la dosis de eficacia y con menos efectos secundarios se estable entre 200 y 300 mg de Fe intravenoso en infusión 31.
Como en el caso de los pacientes hemodializados, Richardson et al 32 estudiaron el valor predictivo de los valores de ferritina sérica y el %HRC en la administración de hierro sacarosa intravenoso y las necesidades de eritropoyetina en 103 pacientes, sometidos a DPCA durante un período de 13 meses, que presentaban marcadores de deficiencia de hierro a pesar de tratamiento con hierro oral (tabla II).
Con este protocolo se consiguió aumentar la hemoglobina de 11,0 a 11,7 g/dl. La proporción de pacientes con deficiencia absoluta de hierro (ferritina < 100 ng/ml) también disminuyó de 24 al 2 %, así como el %HRC, que se redujo del 4 al 1 %.
Este artículo confirma en pacientes en DPCA lo observado en pacientes con hemodiálisis, una estrategia integrada de EPO y Fe intravenoso incrementa el número de pacientes que alcanzan las cifras de hemoglobina diana según las guías europeas, sin necesidad de aumentar los requerimientos de EPO.
El tratamiento con hierro sacarosa intravenoso ha demostrado en ensayos clínicos corregir la anemia por deficiencia de hierro en pacientes en diálisis peritoneal a tratamiento con hierro oral, sin necesidad de iniciar tratamiento con ESA. Cuando el tratamiento con eritropoyetina se hace necesario, el uso combinado con hierro sacarosa intravenoso permite optimizar el tratamiento disminuyendo las necesidades de eritropoyetina.
Conclusiones
El hierro sacarosa intravenoso es un complejo de hierro sacarosa con una estructura similar a la ferritina que transfiere el hierro de forma específica a las proteínas plasmáticas transferrina y ferritina y lo distribuye de forma rápida y eficaz a los órganos diana (sistema reticuloendotelial).
El hierro sacarosa presenta un buen perfil de seguridad y representa una alternativa al tratamiento con hierro oral de bajo riesgo. No contiene dextrano, lo que impide la inducción de reacciones anafilácticas, observadas previamente con la administración de hierro dextrano intravenoso, y evita la aparición de histotoxicidad, observada con el tratamiento de la anemia por déficit de hierro con complejos lábiles de hierro, tales como hierro gluconato. El hierro sacarosa intravenoso es seguro y bien tolerado en el tratamiento y la prevención de la anemia por déficit de hierro 10-12. Además los índices de reacciones de hipersensibilidad por administración de hierro sacarosa son extremadamente bajos en comparación con los de las demás preparaciones de hierro parenteral como hierro dextrano o hierro gluconato 13,14.
Representa una alternativa terapéutica eficaz y bien tolerada en el tratamiento y la prevención de la anemia por déficit de hierro, sola o en combinación de terapia con ESA, como por ejemplo rHuEPO. La terapia con hierro sacarosa intravenoso es más eficaz y rápida que con hierro oral en el tratamiento de la anemia 33. En cuanto a la salud pública, el hierro sacarosa permite una reducción de las transfusiones sanguíneas postoperatorias y favorece la recuperación de la concentración de hemoglobina. En economía sanitaria, el hierro sacarosa intravenoso acelera la recuperación clínica, por lo que reduce el período de hospitalización de los pacientes.
No existe conflicto de intereses.