Desde los comienzos de la hemodiálisis (HD), era conocido que para realizar una buena técnica sería imprescindible disponer de un buen acceso vascular. Y al revés, también se ha demostrado después que, por muchas mejoras tecnológicas que utilicemos (membranas, líquidos, etc.), no podremos dispensar una buena diálisis si no disponemos de un buen acceso vascular que nos garantice unos flujos sanguíneos adecuados.
Hay que tener en cuenta que los aclaramientos difusivos dependen básicamente de los flujos sanguíneos (QB) utilizados. Y por otro lado, no se puede hacer transportes convectivos importantes si no se dispone de QB elevados. Por eso desde siempre se ha intentando disponer de accesos vasculares adecuados para las necesidades de la HD.
La descripción de Cimino y Brescia en 1966 de la fístula arteriovenosa interna (FAVI) mejoró de forma sustancial los resultados de accesos usados previamente, como la derivación de Scribner, que consistía en un tubo del teflón con una "aguja" en cada extremo. En los períodos entre tratamientos, estas "agujas" se dejaban en su lugar y el tubo permitía la circulación de un flujo de sangre continuo para reducir la coagulación. Pero las derivaciones de Scribner duraban sólo algunos días o semanas.
En 1950 Cimino estaba trabajando en el Bellevue Hospital Center de la ciudad de Nueva York, y detectó la existencia de fístulas vasculares causadas por traumatismos en los veteranos de la guerra de Corea. Observó que tales fístulas no causaban afecciones importantes a los pacientes y además eran lugares de fácil punción para conseguir repetidas muestras de la sangre. Él convenció al cirujano Kenneth Appel para producir fístulas arteriovenosas en pacientes con insuficiencia renal crónica, y el resultado fue un éxito completo. Las derivaciones de Scribner fueron rápidamente reemplazadas por las fístulas de Cimino, y 40 años más tarde siguen siendo el método más eficaz y duradero como acceso a la sangre a largo plazo en los pacientes de diálisis. Tanto es así que las Guías Internacionales y Nacionales siguen recomendando a día de hoy, como primera opción, la realización precoz (filtrados glomerulares < 25 ml/min) de FAVI a los pacientes que deban entrar en programas de HD periódicas.
Pero seguimos teniendo problemas serios para conseguir buenos accesos vasculares mediante FAVI. La causas son de diferente índole: pacientes remitidos tardíamente a consulta de prediálisis, agudizaciones no predecibles, casos con afecciones vasculares graves, enfermos muy seniles, diferentes dificultades técnicas, etc. Sin olvidar la en ocasiones escasa o nula conciencia del problema de los especialistas en cirugía vascular.
Por todos estos motivos, los nefrólogos han respondido de diferente forma según la época; en ocasiones se han convertido en cirujanos vasculares realizando ellos mismos las FAVI o han sido los responsables de practicar otro tipo de accesos vasculares más transitorios, como la colocación de catéteres.
Hoy se sigue considerando que la FAVI es el mejor acceso vascular permanente para HD, aunque la realidad nos dice que es imposible disponer en el 100 % de nuestros enfermos de una buena fístula funcionante y necesitamos catéteres de forma transitoria. Pero lo peor es que cada vez es más frecuente la "imposibilidad absoluta" de disponer de una FAVI en algunos de nuestros pacientes. Esto está obligando (a algunas unidades más que a otras) a utilizar de forma habitual catéteres permanentes como única forma de disponer de acceso vascular para HD.
Aunque las guías no recomiendan los catéteres como forma de acceso vascular permanente, pocos o ninguno de los servicios de HD pueden cumplir con sus recomendaciones. Muy al contrario, cada día se están incrementando el número y el porcentaje de utilización de catéteres permanentes. Y es muy dudoso que algún día podamos prescindir de ellos, por lo que nos tendremos que ir acostumbrando a esta realidad. Pero eso sí, habrá que ir mejorando los resultados tan precarios que hasta ahora se están publicando.
Así como en su día se mejoraron las técnicas quirúrgicas, deberemos progresar en los catéteres a todos los niveles (materiales, diseño, colocación, mantenimiento, etc.). Los resultados se pueden mejorar sustancialmente respecto a los actuales. Y de hecho, están mejorando de forma generalizada. Antes se publicaban duraciones de los catéteres de días o semanas, y ahora la mayoría son de meses. Creo que si las duraciones fuesen de años y con igual o similar número de complicaciones que con las FAVI, estaríamos en situación óptima, aunque sus prestaciones fuesen algo inferiores. Podría ser una muy buena solución para esos pacientes con dificultades para disponer de una buena fístula.
En nuestro centro, por diferentes motivos, no disponemos de un buen número de FAVI funcionantes, aun a pesar de disponer de consulta de prediálisis y que se solicita su realización con tiempos prudenciales. Las fístulas a veces no se realizan o se realizan de forma muy tardía y el porcentaje de fracasos iniciales en la realización de FAVI es extremadamente elevado (alrededor del 50 % de la FAVI realizadas no funciona de inicio, un 20 % funciona de forma precaria y sólo el 30 % se puede considerar aceptable). Por esto, nos hemos visto obligados a la utilización frecuente de catéteres permanentes, y ha sido casi simbólica y testimonial la utilización de catéteres transitorios en nuestros pacientes crónicos. Hemos ido mejorando lentamente en nuestros resultados funcionales y disminuyendo de forma significativa nuestras complicaciones, tanto de colocación como en infecciones u otro tipo de complicaciones crónicas habituales de los catéteres permanentes. Los factores que pueden haber influido en la mejora de nuestros resultados son los materiales, la colocación y el mantenimiento.
Material
Siempre utilizamos el mismo diseño de catéter, un catéter gemelo tipo Twin-Cath de poliuretano. Nos parece que tener experiencia con un tipo de catéter suele mejorar los resultados y dar más habilidad tanto en la colocación como en el mantenimiento.
Los catéteres gemelos separados disponen de un mejor calibre interno y producen menos lesión traumática en la colocación, tanto en la vena como en el túnel y la piel.
Estos catéteres también nos permiten renovar los prolongadores externos cuando se deterioran por el uso, y son más fáciles de recolocar e incluso recambiar si se precisa.
Colocación
Siempre utilizamos de forma preferente la yugular interna derecha. Como segunda opción, la yugular izquierda. Como opciones extraordinarias las subclavias o femorales. El lugar de punción es el vértice inferior externo del triangulo de Sédillot, formado por la clavícula y las dos ramas del esternocleidomastoideo.
Sólo se anestesia el punto de punción del vértice inferior externo del triángulo y el lugar de salida de la piel en zona preesternal. No se debe anestesiar el túnel subcutáneo (no es preciso, pues se practica a través del panículo adiposo), para no lesionar la piel y así evitar tunelitis o cufitis posteriores.
La punción se realiza con técnica retroclavicular, dirigiendo la aguja hacia la zona de la mamilla, y cuanto más se haya girado la cabeza para facilitar la punción más externa dirigiremos la punción de la aguja, hacia la axila e incluso hacia el hombro.
Se realizará técnica de Sheldiger, con colocación de un fiador metálico, también llamado guía.
Dado que se trata de catéteres gemelos separados (Twin-Caths), se recomienda realizar dos pinchazos diferentes y colocar dos fiadores metálicos con una separación de unos 5 mm entre ellos. También se puede realizar con un único pinchazo, colocando primero una guía y después metiendo por esa guía un dilatador que permita introducir una segunda guía en el mismo orificio.
Por cada una de las guías de Sheldinger se introduce un dilatador (normalmente pelador) y se meten los catéteres.
Las puntas de los catéteres deben quedar: el arterial, en la parte alta de aurícula derecha y el venoso, a mitad de la aurícula. Los catéteres deberán subir por cava y salir de la vena a nivel entre la primera costilla y la clavícula (retroclavicular). Darán la vuelta por encima de la clavícula, que sirve de punto de apoyo, para dar la vuelta sin acodarse y para que quede fijo y no se mueva con los movimientos de la cabeza.
Luego se tunelizan por la parte anterior del tórax, por delante del esternón (separándolo así de la axila y las glándulas mamarias), para salir perforando la piel preesternal a nivel equidistante de las dos mamillas. Esto permite salir en una zona con poco panículo adiposo (preesternal), por lo que está más fija y es menos productora de seroma. Ademas, nos separamos de zonas calientes y sudorosas (axilas), que son más contaminantes, y de las glándulas mamarias, para evitar perforaciones y seromas mamarios o infecciones.
Los CUF de los catéteres quedan subcutáneos y por delante de la parrilla costal, a la altura de la primera costilla (o entre ésta y la clavícula en las personas altas) y a la altura de la segunda costilla (o entre ésta y la primera en los pacientes de estatura baja).
Mantenimiento
Para curar los orificios de salida, nunca utilizamos antisépticos como povidonas, yodos o alcoholes porque pueden deteriorar los materiales de los catéteres con su uso continuado y porque resecan la piel, la cuartean y cambian su pH, factores todos ellos que facilitan las infecciones posteriores.
Tampoco utilizaremos para las curas de orificio pomadas (mupirocina), geles o cremas. Éstas hiperhidratan la piel y la maceran, favoreciendo también las infecciones.
La única sustancia que utilizamos (porque no reseca ni macera la piel) es el aceite, que además tiene pH ácido y no modifica la barrera natural, con lo que se mantiene la piel en un correcto estado de hidratación. La primeras semanas, hasta que cicatriza el orificio de salida, se utiliza aceite con antibiótico (tipo aceite ótico + ciprofloxacino). Con estas curas, dado que el aceite tiene mucha tensión superficial, penetra y se eleva pericatéter, llevando el antibiótico hasta los CUF. Con esto evitamos tunelitis y cufitis precoces. Durante este tiempo, los catéteres permanecerán fijados externamente con adhesivos y nunca utilizaremos sedas o puntos en piel o internos.
Después el orificio se cicatriza y se epiteliza, y alrededor del catéter se forma una funda fibrosa, que es la mejor barrera contra la infección. El CUF formará su fibrosis estimulada por el dacrón y no serán necesarios los fijadores externos.
Una vez epitelizados los orificios, las curas se realizarán únicamente con lavado y arrastre con suero fisiológico, a pH 5,5. Secado minucioso posterior y como mucho utilizar para la piel aceite, esta vez sin antibiótico.
Las curas oclusivas se realizarán con gasas recubiertas con apósitos transpirables. Si no transpiran, el propio sudor macera la piel y la hace vulnerable a la infección.
También existen apósitos que permiten la transpiración interna, pero resultan exteriormente hidrófugos, permitiendo las duchas o baños, manteniendo seco el interior del apósito.
Nuestros resultados
Durante el período 1995-abril de 2007, se han colocado en nuestra unidad 106 catéteres, todos del tipo TESIO y en yugular derecha.
Se han retirado 70 catéteres, ninguno por infección: 26 por haber fallecido el paciente (pero con catéter funcionante), 21 por haberse trasplantado, 11 por disponer de fistula arteriovenosa funcionante, 3 por haber mejorado su función renal residual y 9 catéteres se han recambiado (en la misma colocación) por deterioro u otros motivos.No hemos tenido ningún caso de coagulación de catéter o de la vía venosa, así como en ningún caso se ha observado síndrome de cava superior u otro tipo de problema vascular.
La utilización media de los 70 catéteres retirados fue de 723 (2.998-28) días (fig. 1).
Figura 1. Días de utilización y motivos de retirada de 70 catéteres yugulares derechos (período enero 1995-abril 2007).
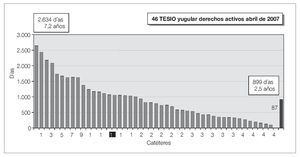
De los 106 catéteres, 46 siguen utilizándose en abril de 2007, con una media de utilización de 899 (2.634-87) días (fig. 2).
Figura 2. Días de utilización de 46 catéteres yugulares derechos, activos en abril de 2005.
Como complicaciones recogidas de los 106 catéteres colocados entre 1995 y abril de 2007, tenemos: en 12 ocasiones se ha recolocado el mismo catéter por mala posición (normalmente salidas subtotales por tracciones bruscas), 3 catéteres se han recambiado por perforaciones espontáneas, 4 pacientes presentaron granuloma en orificio de salida, que se cauterizaron con nitrato de plata, pero en un caso obligó a recolocar un catéter haciendo su salida en zona de piel sana; hemos tenido 14 casos de tunelitis que respondieron al tratamiento antibiótico, en 23 ocasiones presentaron clínica y cultivo de orificios positivos, que se trataron con antibióticos tópicos o sistémicos, y sólo hemos tenido 3 hemocultivos positivos (2 por estafilococo y 1 por Escherichia coli) que respondieron a tratamiento antibacteriano sistémico, sin necesidad de retirar catéter (hemocultivos positivos, 0,0003/1.000 días/paciente).
No hemos tenido hemocultivos positivos en estos últimos 6 años, pese a estar utilizando de forma prevalente unos 45-50 catéteres.
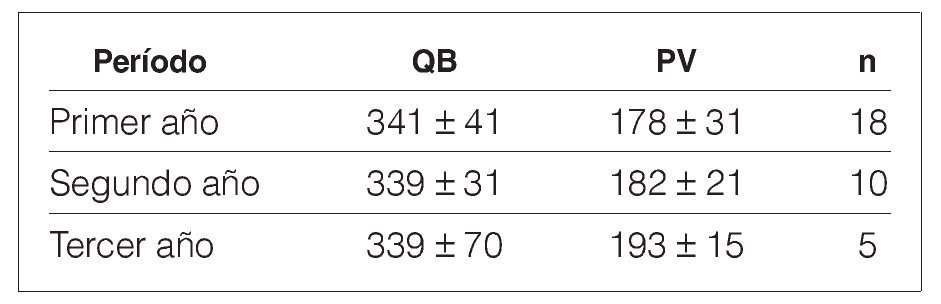
En cuanto a funcionalidad, se han ido evaluando varios catéteres a lo largo de los años de utilización, y no perdían capacidad de flujos de sangre (QB) ni aumentaban su resistencia venosa (PV).
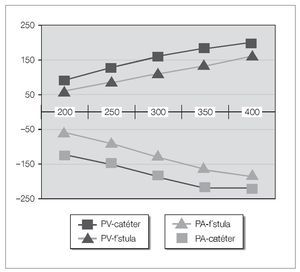
Comparados con las FAVI, para cualquier flujo de sangre (QB), los catéteres tienen presiones arteriales (PA) de succión más negativas y presiones venosas (PV) de retorno más positivas (fig. 3).
Figura 3. Presiones arteriales (PA) y presiones venosas (PV) según flujo de sangre comparando catéteres y fístulas.
Comentario final
Creo que cada día serán más necesarios los catéteres, aunque las guías nos recomienden lo contrario.
Los catéteres de agudos (no tunelizados) se pueden evitar mayoritariamente en los pacientes crónicos y sus complicaciones frecuentes (sobre todo infecciosas) son difíciles de prevenir.
Los catéteres permanentes están mejorando de forma generalizada en sus resultados. Las complicaciones infecciosas, coagulación o infecciosas, pueden reducirse de forma drástica, con mejoras en materiales, colocación y cuidados. En esto último, la formación de la enfermería es básica.
Actualmente los resultados funcionales, comparados con las FAVI, parecen ser inferiores. Pero hay que decir que siempre se compara los catéteres con las FAVI normofuncionantes. Si comparamos los accesos, siempre será mejor un catéter normofuncionante que una FAVI defectuosa. Y el porcentaje de FAVI que no funcionan de forma adecuada suele ser en muchos servicios muy elevado.
Como resumen final, creo firmemente que en el futuro las prestaciones de los catéteres permanentes serán cada día mejores, las complicaciones se reducirán y su duración mejorará notablemente, por lo que su indicación y su prevalencia crecerán en el futuro y para ello deberemos estar preparados.
Correspondencia: Dr. C. Solozábal.
Unidad de Hemodiálisis. Hospital Virgen del Camino. Irunlarrea, s/n. 31008 Pamplona. Navarra. España.
Correo electrónico: carlos.solozabal.campos@cfnavarra.es
Bibliografía general
Brescia MJ, Cimino JE, Appel K, Hurwich BJ. Chronic hemodialysis using venipuncture and a surgically created arteriovenous fistula. N Engl J Med. 1966;275:1089-92.
Ferrari G, Talassi E, Baraldi C, Lombertini D, Tarchini R. Vascular access validity and treatment efficiency in hemodialysis. G Ital Nefrol. 2003;20:22-9.
Gómez Campderá FJ, Polo JR, Sanabia J, Tejedor A. Primer acceso vascular para hemodiálisis en el anciano. Nefrologia. 1995;15:183-5.
Guía de acceso vascular en hemodiálisis. Nefrologia. 2005;25 Supl 1.
Kairaitis LK, Gottlieb T. Outcome and complications of temporary hemodialysis catheters. Nephrol Dial Transplant. 1999;14:1710-4.
Konner K. Vascular access in the 21st century. J Nephrol. 2002; 15 Suppl 6:S28-32.
Locatelli F, Manzoni C, Pozzoni P, Pontoriero G, Filippo L. Clinical dialysis: New problems and new prospects. G Ital Nefrol. 2004; 21:156-64.
NKF-K/DOQI Clinical practice guidelines for vascular access: Am J Kidney Dis. 1997;Suppl 3:157-8.
Perez-Banasco V, Borrego FJ. De la excelencia al caos. Nefrologia. 1995;15:6.
Polkinghorne KR, McDonald SP, Atkins RC, Kerr PG. Vascular access and all-cause mortality: a propensity score analysis. J Am Soc Nephrol. 2004;15:477-86.
Rodriguez JA. Hemodiálisis vascular access in incident patients in Spain. Kidney Int. 2002;62:1475-7.
Schwab SJ, Weiss MA, Rushton F, Ross JP, Jackson J, Kapcian T, et al. Multicenter clinical trial results with LifeSite hemodialysis access system. Kidney Int. 2002;62:1026-33.
Tesio F, Panadello G, De Baz H, Canzi M, De MattiaT, Pasut R. Central vascular access: rational and results. G Ital Nefrol. 2003;20: 30-4.
Tesio F, Panadello G. Long-term vascular access: the Tesio catheter. Contrib Nephrol. 2004;142;153-8.
Vassalotti JA, Faik A, Teodorescu V, Urribarri J. The multidisciplinary approach to hemodialysis vascular access in the Mount Sinai Hospital. Mt Sinai J Med. 2004;71:94-102.