Integrar conocimientos es la tarea fundamental de la educación química y es en este contexto en el cual la investigación en inhibición de corrosión de acero nos brinda la oportunidad de integrar los conocimientos de cinética electroquímica con química orgánica, química analítica instrumental y electrónica vía la construcción de un potenciostato de bajo costo y la utilización de este en el estudio de las propiedades anticorrosivas del sulfato de atropina frente a acero al carbono en solución. Ya que esta experiencia le permitirá al alumno determinar el potencial de corrosión y el comportamiento cronoamperométrico de acero al carbono SAE 1010 en solución de NaCl al 0.9% en volumen en presencia y ausencia de sulfato de atropina en una celda electroquímica estándar de 3 electrodos.
Knowledge integration is the central duty of chemistry education and is in this context where the investigation surrounding steel corrosion inhibition bring us the opportunity to integrate knowledge from electrochemical kinetics, Organic chemistry, Instrumental analytical chemistry and electronics via the construction of a low cost potentiostat and the use of this in studies of the anticorrosive properties of atropine sulphate with carbon steel in solution. Due that this experience is going to allow the student the determination of the corrosion potential and chronoamperometric behavior of carbon steel SAE 1010 in 0.9% NaCl solution in presence and absence of atropine sulphate in a standard electrochemistry cell of three electrodes.
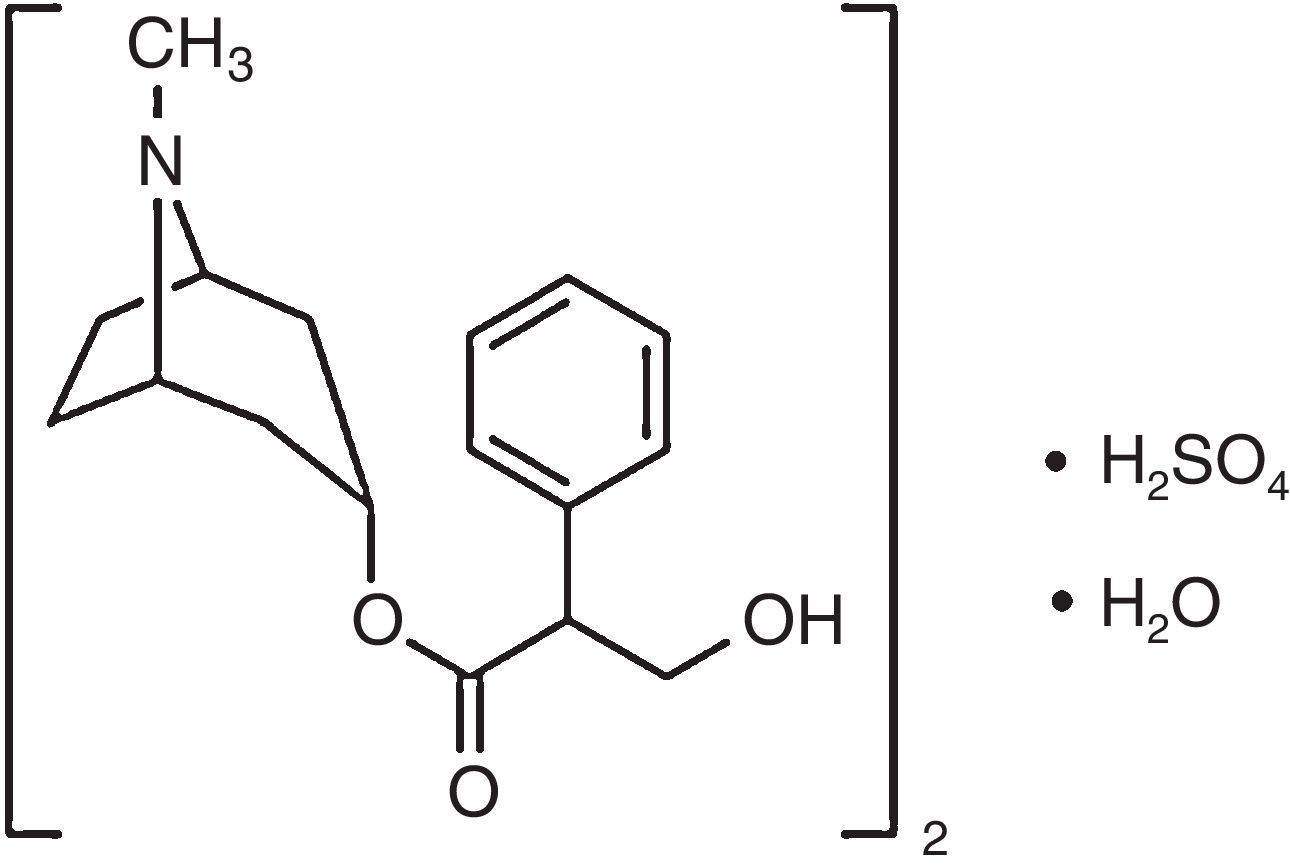
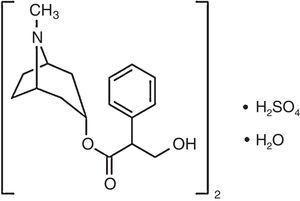
La construcción de un equipo de bajo costo para el laboratorio presenta una doble finalidad; por una parte, que el alumno pueda entender el funcionamiento de los equipos, evitando el concepto de caja negra (Meloni, 2016; Segura, Jiménez y Giraldo, 2016). Y, por otra parte, contar con el número de equipos necesarios para que cada alumno pueda realizar la experiencia práctica de laboratorio en un grupo no mayor de 3 estudiantes en los casos en que el costo comercial de estos equipos es muy elevado (Vilasó, 2014; McClain, 2014). Así se han reportado en la literatura equipos de bajo costo tales como termómetros (Kubínová y S¿légr, 2015), fotómetros (McClain, 2014), pH-metros (Kubínová y S¿légr, 2015) y termocicladores (Mabbott, 2014). En lo que respecta a potenciostatos, Vilasó (2014) construyó un potenciostato de bajo costo y funcionamiento simple, sin utilizar un software para su operación, el cual consiste en un circuito que se compone de una fuente de poder, una resistencia, un reóstato, un multitester básico en función voltímetro, una celda electroquímica de 3 electrodos y otro multitester básico en función de amperímetro. Todo el circuito montado en una caja de plástico desechable (Vilasó, 2014). Por otra parte, Meloni (2016) diseñó y construyó un potenciostato versátil basado en la filosofía off the shelf capaz de realizar experimentos de voltamperometría cíclica que le permitieron calcular el coeficiente de difusión del ferricianuro en disolución acuosa, cuyo valor medido estuvo de acuerdo con el reportado en la literatura, transformando este equipo en una alternativa competitiva no comercial, para efectuar trabajo de laboratorio en los campos de la electrónica y la electroquímica (Meloni, 2016). Respecto de los potenciostatos que han sido diseñados para estudios de corrosión, estos requieren para su construcción conocimientos avanzados en electrónica y programación (Barrero, Amaya, Acevedo, Acevedo, González y Morales, 2004; Roa-Rodríguez, Aperador-Chaparro y Delgado-Tobón, 2015). Por otra parte, el uso de inhibidores de corrosión es uno de los métodos más utilizados para prevenir la corrosión de acero al carbono en contacto con un medio acuoso. Generalmente, el medio en estudio es un medio ácido (ácido clorhídrico o ácido sulfúrico), y la mayoría de los inhibidores de corrosión son compuestos orgánicos que contienen átomos de nitrógeno, azufre u oxígeno en su estructura (Ahamad y Quraishi, 2010). Dentro de los compuestos cuyas propiedades anticorrosivas han sido investigadas están los compuestos farmacéuticos (Vaszilcsin, Ordodi y Borza, 2012; Samide, 2013); un ejemplo de estos es el sulfato de atropina cuya fórmula estructural aparece en la figura 1, del cual se han investigado sus propiedades anticorrosivas en medio ácido (Raja y Sethuraman, 2008), pero no han sido investigadas en soluciones que contengan cloruro de sodio, lo cual resulta vital para entender el comportamiento de estos materiales en condiciones marinas y en el tratamiento industrial de residuos que contengan cloruro (Cáceres, Vargas y Herrera, 2007). Una forma sencilla de verificar la capacidad de inhibición de la corrosión de una molécula es la realización de experimentos cronoamperométricos, en los cuales se polariza el electrodo de acero a un potencial de fijo versus el electrodo de referencia en un tiempo dado y se miden los valores de densidad de corriente en presencia y ausencia del inhibidor; si la densidad de corriente disminuye significativamente en presencia del inhibidor, se concluye que este inhibe la corrosión del acero (Krishnegowda, Venkatesha, Krishnegowda y Shivayogiraju, 2013; de Oliveira, Battistin y Gonçalves, 2012). Así el crear una práctica de laboratorio que investigue las propiedades anticorrosivas de preparaciones farmacéuticas que incluya el uso de un potenciostato de bajo costo construido para tal efecto, no solo posicionaría al alumno en conocimientos, habilidades y destrezas para manejar una determinada técnica (Lagos y Camus, 2016), sino que también le permitiría integrar los conocimientos adquiridos en otras asignaturas de su plan de estudios. Considerando lo anterior, el objetivo del presente trabajo fue la construcción de un potenciostato de bajo costo para estudios de inhibición de corrosión de acero, específicamente la determinación del potencial de corrosión y comportamiento cronoamperométrico en presencia y ausencia de un inhibidor de corrosión.
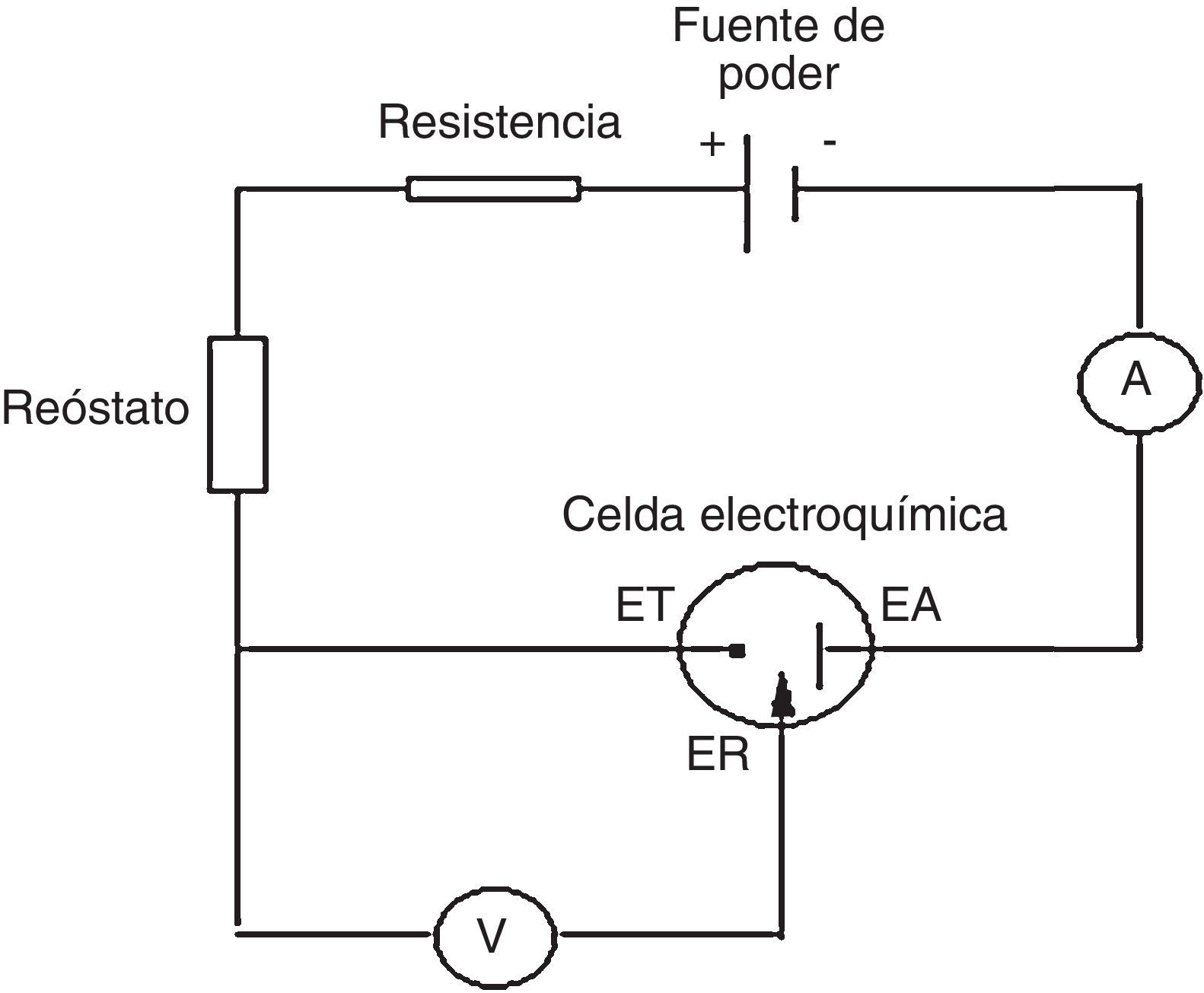
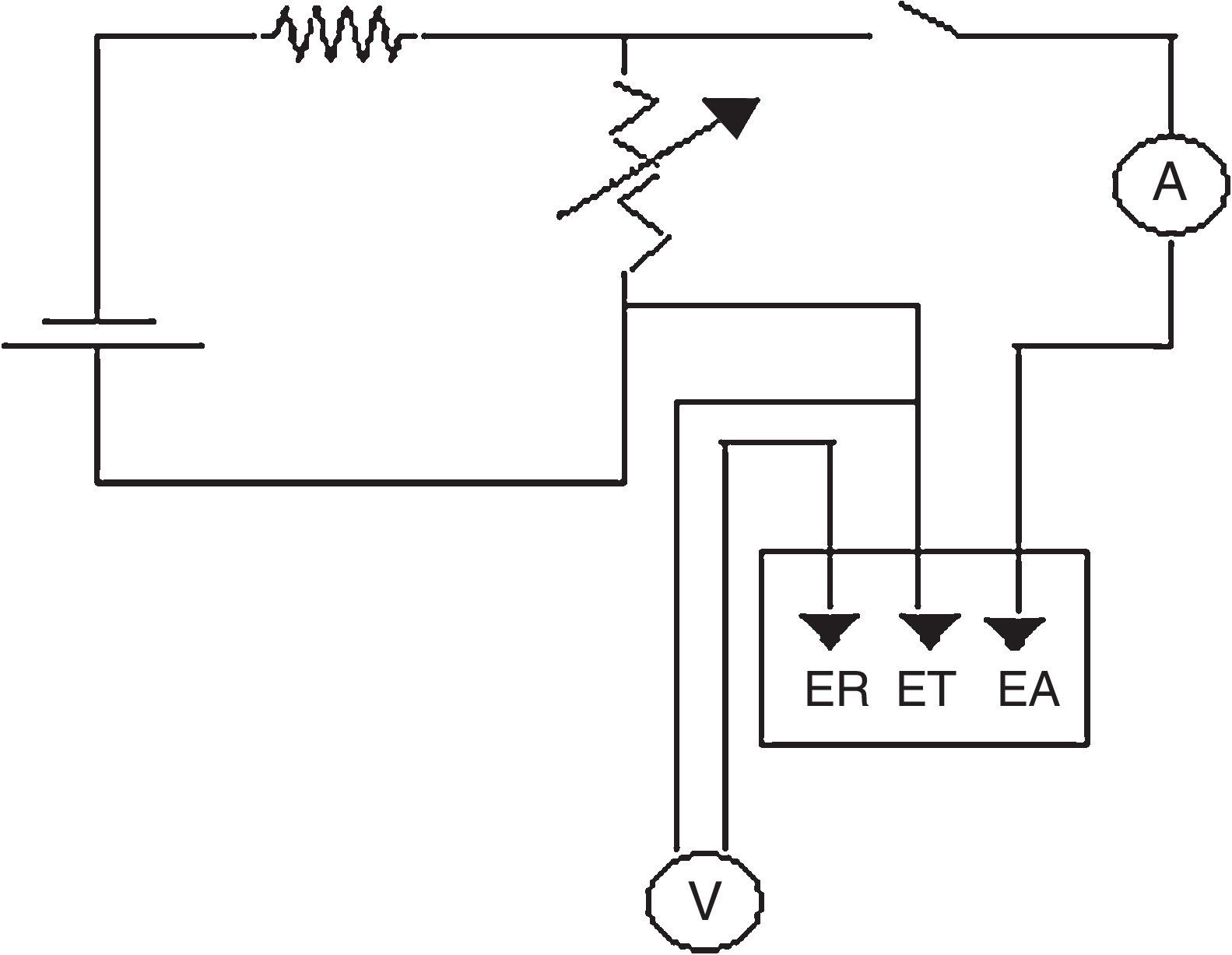
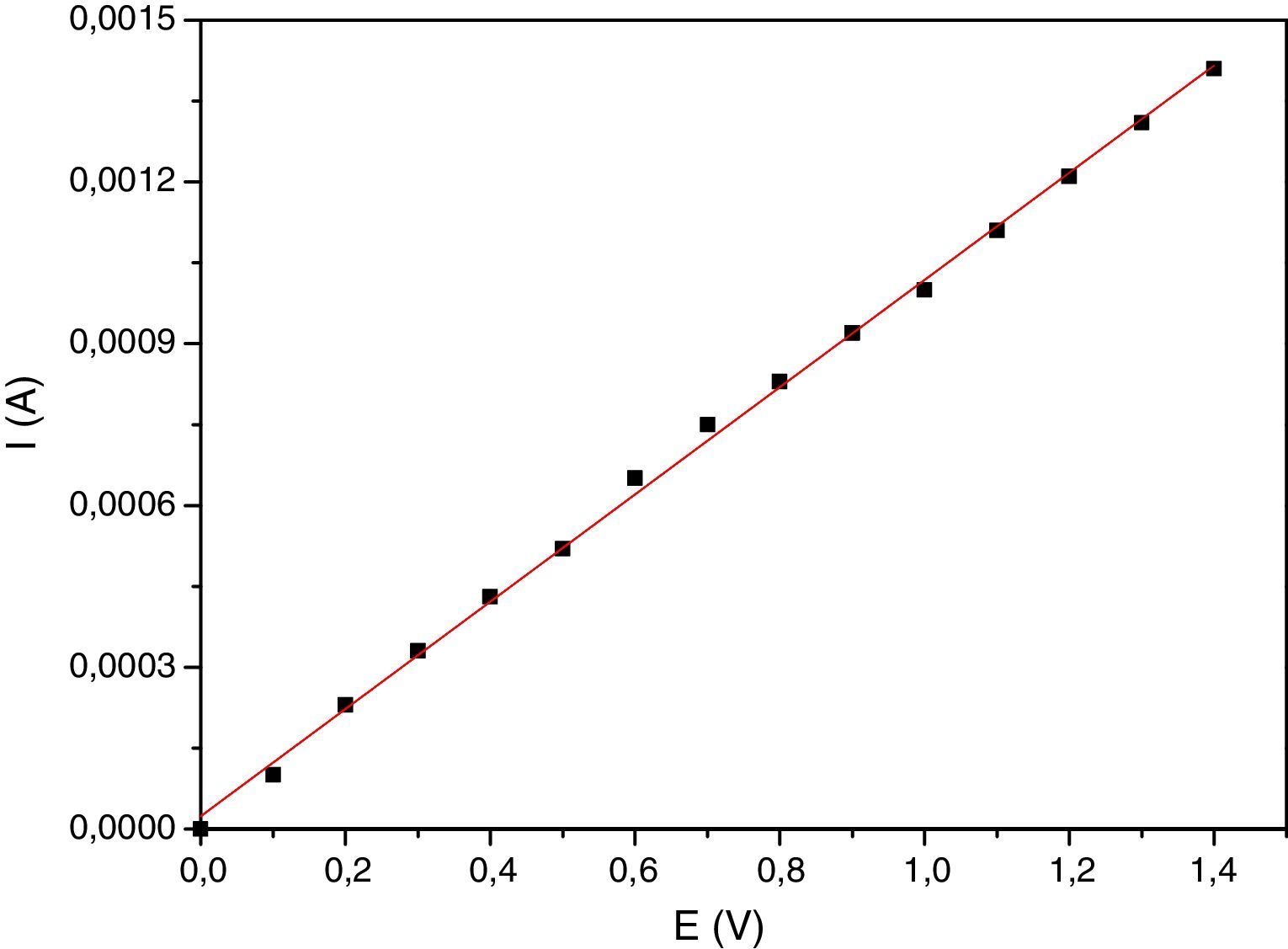
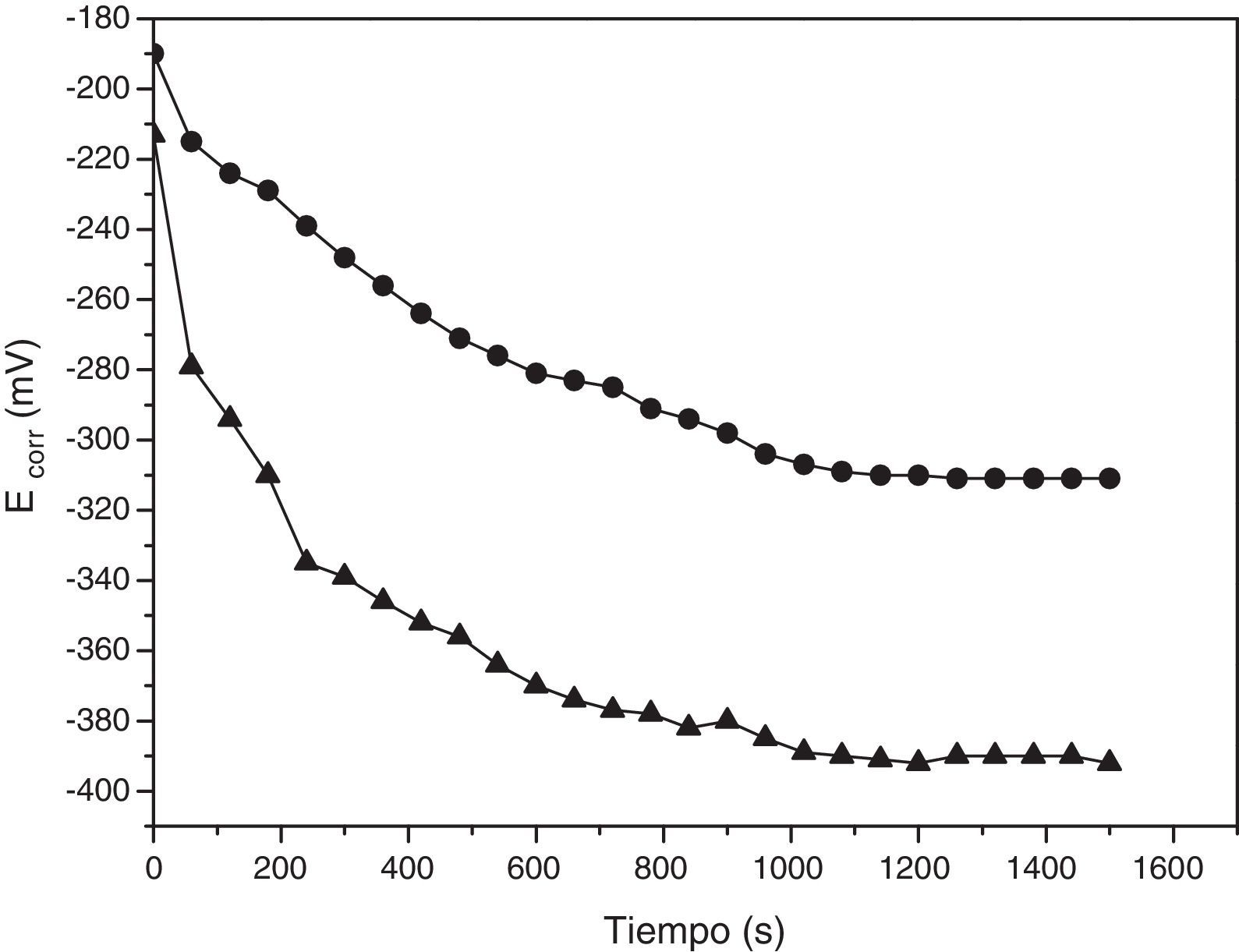
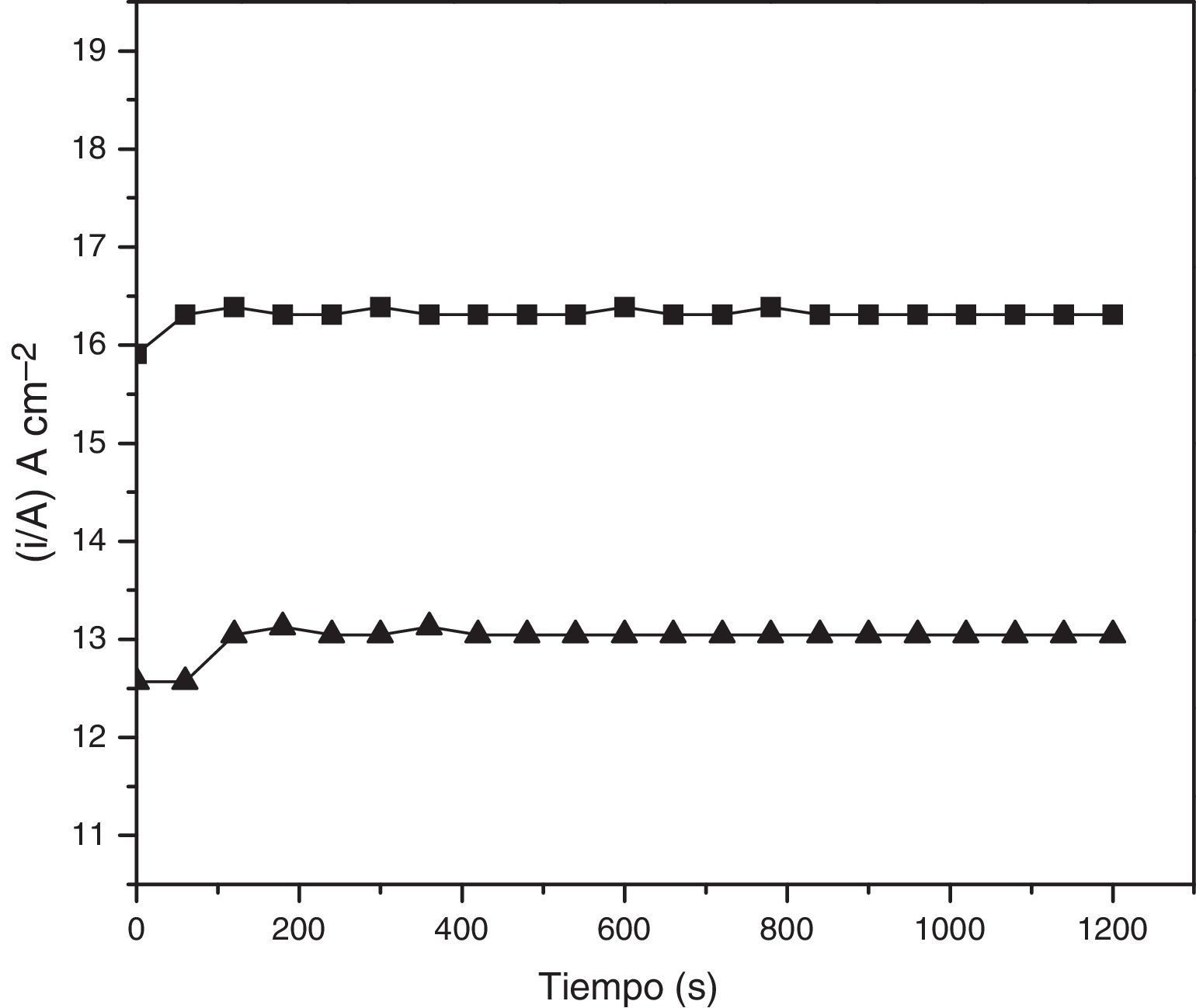
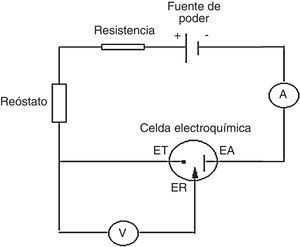
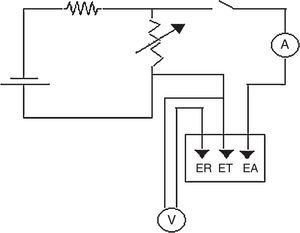
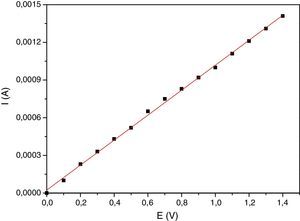
ExperimentalLa figura 2 muestra el esquema del montaje experimental del potenciostato de bajo costo, el cual se compone de una fuente de poder de 12V y 3A Impotec, una resistencia de 5kΩ, un potenciómetro en función reóstato de 10kΩ, un voltímetro de alta resistencia UNI-T UT151 (Modern Digital Multimeters), la celda electroquímica de 3 electrodos, la cual está compuesta por el electrodo auxiliar, el electrodo de referencia y el electrodo de trabajo, y un amperímetro Nagachi DT830B (Digital Multimeter). El amperímetro se colocó entre el electrodo de trabajo y el electrodo auxiliar para que el equipo funcione como potenciosato, esto es que mida la corriente entre estos 2 electrodos a un potencial fijo (Kaesche, 2003). Todo el circuito fue montado en la caja metálica de una fuente de poder de un computador en desuso, siguiendo el procedimiento descrito por Vilasó (2014). La figura 3 muestra el diagrama eléctrico del potenciostato. Como electrodo de trabajo se empleó un disco estacionario de acero al carbono SAE 1010 cuya composición en peso fue de 98.5Fe, 0.2C, 0.6Mn y trazas de P, S, Si, Sn, Cu, Ni, Cr, y Mo; se denominó así para aclarar que no se trataba de un electrodo de disco rotatorio. Se optó por este tipo de electrodo dada su facilidad de construcción y bajo costo. El electrodo se construyó utilizando un cilindro de acero al carbono SAE 1010 de 5cm de longitud, el cual se embebió en resina epóxica, dejando su base expuesta con un área de 0.1257cm2 (Alfaro, 2014). Como electrodo de referencia se empleó un microelectrodo de cobre inmerso en agua bidestilada Cu°|Cu(II)|H2O||, constituido por un alambre de cobre de 4.0cm de largo por 0.1cm de diámetro inserto en un tubo de acrílico cilíndrico de 3.0cm de largo y 1.0cm de diámetro fijado en este por un tapón de goma, utilizando una membrana de látex para separar el agua destilada de la solución y facilitar el intercambio iónico. Si se desea determinar el potencial de este electrodo de referencia, con respecto al electrodo normal de hidrogeno (ENH), se debe medir este con respecto a un electrodo de referencia de Calomelanos o Ag/AgClKCl0.1M utilizando un voltímetro de alta resistencia siguiendo el procedimiento descrito por Baeza (2017) y luego transformar este valor a ENH. Se optó por este electrodo de referencia y no por los electrodos de referencia de Calomelanos y Ag/AgCl en 0.1KClM pese a que la solución utilizada como medio corrosivo es NaCl, pensando en que el estudiante pudiese construir este electrodo en una sesión previa de laboratorio y que el énfasis del práctico estaba en el cambio del potencial de corrosión y la densidad de corriente de corrosión debido al inhibidor de corrosión (sulfato de atropina). Y como electrodo auxiliar, un alambre de platino (Alfaro, 2014); si no se dispone de platino se puede usar grafito o acero inoxidable. Los 3 electrodos se montaron en un recipiente de plástico de 50mL de capacidad; el conjunto conformó la celda electroquímica estándar de 3 electrodos (Kaesche, 2003). La diferencia de esta celda con la de 2 electrodos es que la de 2 electrodos solo puede medir el potencial de corrosión del electrodo de trabajo (electrodo de acero al carbono) versus un electrodo de referencia, siendo el más utilizado el electrodo de referencia de Cu/CuSO4.saturado en la determinación del potencial de corrosión de barras de acero en estructuras de concreto. La interpretación de estos valores de potencial de corrosión se puede hacer con base en la Norma ASTM C876-91. En cambio, la celda de 3 electrodos permite efectuar mediciones cronoamperométricas del electrodo de acero en solución acuosa a un potencial fijo (Baeza, 2017; Baltazar, Almeraya, Nieves, Borunda, Maldonado y Ortiz, 2007). Debe tenerse especial cuidado en la colocación de los 3 electrodos en la celda, debiendo quedar estos en posiciones fijas separados por no más de 1cm para que no se produzca interferencia entre ellos (Cáceres, 2017), ya que, como se muestra en la figura 3, la corriente entra en la solución de electrólito (medio corrosivo) por el electrodo de trabajo y sale de la solución de electrólito por el electrodo auxiliar. Como medio corrosivo se utilizó una solución de NaCl al 0.9% en volumen (suero fisiológico), se optó por esta solución debido a su bajo costo y fácil adquisición en comparación con NaCl p.a. (reactivo calidad para análisis) y porque esta concentración ya ha sido utilizada en estudios de corrosión de acero al carbono (Cáceres et al., 2007). Y como inhibidor de corrosión, sulfato de atropina (atropina 1%. Solución oftálmica estéril 10mL Oftalmer Nicolich SAVAL. Cada mL contiene: atropina sulfato 0.01g y excipientes), los cuales fueron comprados en una farmacia local. La calibración del potenciostato se efectuó utilizando el método de la celda ficticia reportado por Vilasó (2014), siguiendo el procedimiento descrito por Hernéndez (2017). Se prefirió este método, en lugar de utilizar el método de calibración por voltamperometría de ferricianuro de potasio (K3Fe(CN)6), por su simplicidad y bajo costo. La figura 4 muestra la relación corriente-potencial utilizando una celda ficticia, conformada por una resistencia de 1.0kΩ. El comportamiento que presenta es lineal y sigue la ley de Ohm, lo que permite corroborar el funcionamiento adecuado del potenciostato. El coeficiente de correlación lineal fue de 0.9993; esto significa que la relación entre el potencial aplicado y la corriente que circula es lineal, por lo que el circuito es completamente funcional. La pendiente de esta gráfica fue de 0.0009943 y representa el inverso de la resistencia utilizada en la construcción de la celda ficticia coincidiendo con la resistencia utilizada de 1.0kΩ. La figura 5 muestra la variación del potencial de corrosión de acero al carbono con el tiempo de inmersión en una solución de NaCl al 0.9% en volumen, en presencia y ausencia de sulfato de atropina. Se observa que los potenciales de corrosión versus el electrodo de referencia se modifican aumentando conforme aumentó el tiempo de inmersión en ambas soluciones, lo cual es concordante con lo reportado por Chen, Chen, Xiao, Cheng, Zhang y Yi (2005) para acero al carbono en una solución al 3.5% en peso de NaCl. El potencial de corrosión del acero al carbono en ausencia de sulfato de atropina evolucionó rápidamente hasta un valor constante alrededor de los 1,200s, en forma análoga al potencial de corrosión de acero al carbono en presencia de sulfato de atropina en una concentración de 8.58*10−5M, lo que es concordante con los resultados de Raja y Sethuraman (2008) para el sulfato de atropina en medio ácido. Estos resultados muestran que la adición de sulfato de atropina cambió significativamente el potencial de corrosión, el cual se vuelve más positivo con el tiempo de inmersión. La figura 6 muestra las curvas cronoamperométricas del electrodo de acero al carbono en solución de NaCl 0.9% en volumen en el tiempo en presencia y ausencia de sulfato de atropina a un potencial aplicado de –180mV versus el electrodo de referencia. El criterio escogido para elegir este potencial obedeció a que a ese potencial lo que se buscó fue inhibir la reacción de catódica (Raja y Sethuraman, 2008). La observación de burbujas en el electrodo auxiliar confirman que la reacción que ocurre a este potencial es la reacción de reducción del agua, debido a que la reacción ocurre al pH en que se encuentra el suero fisiológico, el cual es de 5.4 (Reid, Lobo, Williams, Rowlands y Allison, 2003). Después de 2min de inmersión del electrodo de acero al carbono en ausencia de sulfato de atropina, disminuyó la densidad corriente. La densidad de corriente del acero al carbono en presencia de sulfato de atropina fue estable durante todo el período experimental. La adsorción del sulfato de atropina sobre el electrodo inhibió fuertemente los sitios de corrosión en la superficie del acero inhibiendo la reacción catódica y por ende el proceso de corrosión (Wagner y Traud, 1938; Raja y Sethuraman, 2008).
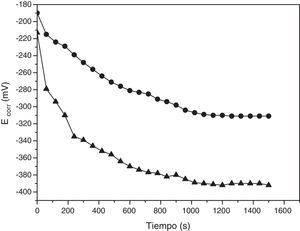
Variación del potencial de corrosión (Ecorr) de acero al carbono SAE 1010 con el tiempo de inmersión en la solución de cloruro de sodio al 0.9% en volumen. a) Sin adición de sulfato de atropina (triangulo negro). b) Con adición de sulfato de atropina en una concentración 8.58*10−5M (círculo negro).
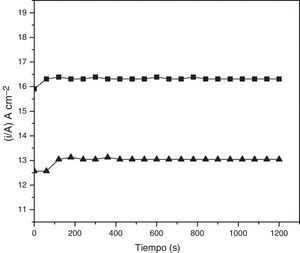
Curvas cronoamperométricas para acero al carbono SAE 1010 a un potencial aplicado de –180mV versus electrodo de referencia en la solución de cloruro de sodio al 0.9% en volumen. a) Sin adición de sulfato de atropina (triangulo negro). b) Con adición de sulfato de atropina en una concentración 8.58*10−5M (cuadrado negro).
Estos resultados obtenidos en una práctica de laboratorio con un potenciostato de bajo costo proporcionan al alumno no solo conocimientos y habilidades en cinética electroquímica, sino que también logran que aplique conceptos de química orgánica y química analítica instrumental al interpretar sus resultados utilizando un instrumento con datos reales. Es decir, se cumpliría con todas las expectativas de la docencia en el laboratorio (Lagos y Camus, 2016). En este caso, el alumno comprende el concepto potencial de corrosión y la técnica de medida utilizando un potenciostato (Alfaro, 2014), incluso conocerá el lenguaje de las características de los electrodos de trabajo (tipo de electrodo, corrosión en solución acuosa, inhibición de la corrosión, etc.), es decir, está ingresando al mundo de los instrumentos modernos de laboratorio al utilizar un equipo que es capaz de medir potencial de corrosión y efectuar mediciones cronoamperométricas con un bajo costo, que en este caso permitirán resolver un problema relacionado con la investigación de las propiedades de inhibición de corrosión de acero. Al entender el funcionamiento básico de un potenciostato, el estudiante está capacitado para entender cualquier configuración similar que se le presente en otros cursos o en la industria, es decir, el estudiante no solo está integrando conocimientos de diversas áreas de la química, sino que también está realizando una experiencia práctica en cinética electroquímica. Y, además, la práctica de laboratorio propuesta permite realizar posteriores experimentos, con otros compuestos orgánicos para determinar sus propiedades anticorrosivas, y así el alumno podría relacionar el potencial de corrosión y el comportamiento cronoamperométrico del acero en presencia del inhibidor con la estructura molecular de este.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Los autores agradecen el apoyo de la Dirección de Investigación de la Universidad de La Serena, Chile y especialmente al Dr. Eduardo Notte.
La revisión por pares es responsabilidad de la Universidad Nacional Autónoma de México.