El PET/TC Ga68-DOTATOC es una técnica de diagnóstico por la imagen, de reciente introducción en nuestro medio, para el diagnóstico y seguimiento de tumores neuroendocrinos.
Estudio observacional prospectivo de 7 pacientes a quienes se les realizó un estudio PET/TC Ga68-DOTATOC. Los pacientes tenían sospecha de lesiones tumorales neuroendocrinas activas, en diagnóstico inicial o con posible recidiva y/o progresión de tumores ya conocidos. Los resultados de los estudios de imagen realizados previamente (RM, TC toracoabdominal, octreotida…) habían sido negativos o no concluyentes.
Todos los PET Ga68-DOTATOC positivos fueron verdaderos positivos, confirmándose por anatomía patológica. No se obtuvieron resultados falsos positivos. Solo se obtuvo un falso negativo.
PET/TC Ga68-DOTATOC es más sensible y específico en la detección de lesiones tumorales primarias neuroendocrinas, permite un estudio de extensión más completo y detecta recidivas en estadios más precoces, condicionando cambios en la estadificación y el tratamiento quirúrgico. Aporta información adicional sobre la sobreexpresión de receptores de somatostatina, esencial para la indicación de PRRT (terapia con péptidos marcados con radionúclidos) con Lu177-Dotatate.
Ga-68-DOTATOC PET/CT is a recently introduced imaging technique for the diagnosis and follow-up of neuroendocrine tumors.
A prospective observational study was conducted in seven patients who underwent a Ga-68-DOTATOC PET/CT study. They were suspected of active neuroendocrine tumor lesions, either on initial diagnosis or as a possible recurrence and/or progression of already known tumors. The results of prior imaging studies (MRI, thoracoabdominal CT scan, octreotide...), had been negative or inconclusive.
All positive Ga-68-DOTATOC PETs were true positives, confirmed by pathological examination. There were no false positive results. Only one false negative result was found.
Ga-68-DOTATOC PET/CC is more sensitive and specific for the detection of primary neuroendocrine tumor lesions, allows for a more complete extension study, and detects recurrences in earlier stages, conditioning changes in staging and surgical treatment. It provides additional information on somatostatin receptor overexpression, which is essential for the indication of PRRT (peptide receptor radionuclide therapy) with Lu177 dotatate.
Los tumores neuroendocrinos son un grupo heterogéneo de tumores derivados de la cresta neural y del endodermo con diferenciación neuroendocrina. Dependiendo de su diferenciación histológica y grado de proliferación será distinto su comportamiento y evolución.
A pesar de su heterogeneidad la mayoría de estos tumores (80%) se caracterizan por la sobreexpresión de receptores de somatostatina, especialmente del subtipo 2. La expresión de receptores de somatostatina tiene implicaciones clínicas relevantes: por un lado, la propia función reguladora que ejercen en el tumor (secreción de hormonas, crecimiento tumoral y angiogénesis) con las correspondientes implicaciones terapéuticas, y por otro lado, juegan un importante papel en la identificación y tipificación de estos tumores1. La sobreexpresión de receptores de somatostatina es la base fisiopatológica del diagnóstico de estos tumores utilizando las técnicas de medicina nuclear (gammagrafía y PET), así como del tratamiento con análogos de la somatostatina fríos (lanreotida, octreotida, etc.) o marcados con isótopos como el lutecio177.
En el año 2017 la Organización Mundial de la Salud, en un intento de homogeneizar la denominación de este variado grupo de tumores, publicó una nueva clasificación basada en criterios histopatológicos: grado de diferenciación celular, grado de proliferación (Ki67) e índice mitótico2. Los tumores neuroendocrinos se clasificaron dependiendo de su Ki67 o índice mitótico en: G1, G2 y G3. Por otro parte, hablaremos de carcinomas neuroendocrinos cuando son tumores mal diferenciados y con un índice mitótico alto.
Se consideran tumores raros, con una incidencia en nuestro país de 5-6 por cada 100.000 habitantes. El 60% se localiza en el tracto gastrointestinal (siendo los tumores más prevalentes después del cáncer de colon) y el 27% en el árbol traqueobronquial3. La mayoría de ellos son tumores no secretores y el 50% presentan metástasis al diagnóstico.
En los últimos años se ha identificado un incremento en el diagnóstico de estos tumores, difícil de confirmar si se debe a un aumento real en su incidencia o a un mayor conocimiento y a una mayor sensibilidad y disponibilidad de técnicas para su diagnóstico.
En el año 2018 la Agencia Española del Medicamento (AEMPS)4,5 aprobó el uso del PET/TC con análogos de la somatostatina: 68Ga-edotreotida (SomaKit TOC®)5 en nuestro país.
Edotreotida (DOTATOC) es una molécula análoga a la somatostatina que unida al 68Ga permite, mediante la técnica PET, identificar aquellas células con sobreexpresión de receptores de somatostatina, especialmente del subtipo 2 y 5. Este tipo de receptores se identifican en el 80-85% de los tumores neuroendocrinos, por lo que es una técnica con una alta sensibilidad en el diagnóstico de estas neoplasias6,7. Pese a su reciente incorporación en nuestro país, el PET-TC con análogos de la somatostatina llega avalado por más de 10 años de experiencia en otros países europeos. La literatura publicada es extensa y muestra unos valores de sensibilidad y especificidad superiores a los de otras exploraciones, del 90% y 90-92% respectivamente, para el diagnóstico de los TNE (tumores neuroendocrinos) bien diferenciados G1, G2 y G3. Estos resultados son superiores a los del octreoscan, 60-80%6,7, y a los de otras técnicas radiológicas.
La aprobación tan reciente por parte de la AEMPS del uso de este radiofármaco hace que la experiencia en nuestro país sea muy incipiente8,9.
Creemos importante validar en nuestro medio los prometedores resultados descritos en la literatura internacional.
El objetivo de este trabajo es presentar los primeros 7 pacientes a quienes se les realizó un PET con análogos de la somatostatina en nuestra área sanitaria. Se hará hincapié en las indicaciones y la justificación de la realización del estudio, la comparación con el resto de estudios de imagen realizados con anterioridad, la correlación con los hallazgos anatomopatológicos (si los hubiera), y por último, se valorará la repercusión clínica del PET a través de las modificaciones en el diagnóstico y/o extensión de la enfermedad, así como de los cambios en la terapia inicialmente prevista.
Material y métodosEstudio descriptivo prospectivo de 7 pacientes con sospecha de un tumor neuroendocrino a quienes se les realizó un estudio PET/TC Ga68-DOTATOC. Los pacientes procedían de 2 centros, el Hospital del Mar y el Hospital Quironsalud de Barcelona, y los estudios se realizaron en el periodo comprendido entre marzo de 2018 y noviembre de 2018.
Se seleccionaron pacientes en estudio por sospecha de tumor primario de probable origen neuroendocrino y/o pacientes con sospecha de recidiva o progresión de tumores neuroendocrinos ya diagnosticados. A todos ellos se les habían realizado con anterioridad las pruebas de imagen habituales en el protocolo diagnóstico de estos tumores (ecografías, RM, TC toracoabdominal, gammagrafía con octreotida y/o PET/TC F18-FDG), con resultados negativos o no concluyentes. Se definían como no concluyentes cuando los hallazgos obtenidos no establecían un diagnóstico que permitiese adoptar una actitud terapéutica.
Los motivos del estudio fueron: confirmar la etiología neuroendocrina de la lesión, estadificación y valoración de recidivas de pacientes con diagnóstico de tumor neuroendocrino. Por otro lado, la prueba permitió seleccionar a los pacientes candidatos a tratamientos con análogos de la somatostatina tanto farmacológicos como marcados con isótopos radiactivos (PRRT).
La decisión definitiva de realizar el estudio PET con análogos de la somatostatina fue tomada de manera multidisciplinar en los comités donde eran estudiados estos pacientes. Las indicaciones del PET con análogos estaban basadas en las guías americana y europea de las respectivas sociedades de tumores neuroendocrinos10–12.
El estudio PET/TC se realizó tras la administración intravenosa de 1,5MBq/kg (100-185MBq) de Ga68-edotreotida (Somakit®, Advanced Accelerator Applications). La adquisición de las imágenes se llevó a cabo tras 60min en reposo físico y sensorial y posmicción, en el tomógrafo Siemens Biograph 6, situado en el Servicio de Medicina Nuclear del Hospital Quirón Barcelona.
Se efectuaron imágenes desde el cráneo hasta el tercio proximal del muslo de manera sistemática en todos los pacientes, añadiéndose el estudio de extremidades superiores y/o inferiores si fueran zonas susceptibles de ser la situación tumoral.
TC de 80 a 150mA (care dose), con contraste yodado intravenoso si no existía contraindicación. Imagen PET de emisión 3D de 3min×bed. Reconstrucción iterativa. Matrix 128×128, con tamaño de píxel de 2-4mm. Corrección de la atenuación mediante las imágenes de transmisión TC.
Se reconstruyó el estudio obteniéndose imágenes en los ejes transversal, coronal y sagital del PET corregido, PET no corregido y de la fusión PET/TC.
Análisis de las imágenes PET/TCLas imágenes PET/TC fueron evaluadas visualmente por 2 médicos nucleares experimentados, de forma independiente, uno de cada uno de los centros participantes. El informe definitivo se realizó por consenso entre ambos.
Para la evaluación del PET se consideró positivo cuando existían áreas de hipercaptación del radiofármaco no identificables como fisiológicas (hipófisis, tiroides, bazo, hígado, glándulas adrenales, proceso uncinado pancreático y tracto urinario), con intensidad superior al fondo del órgano o región donde estaba ubicada y superior a la esperable fisiológicamente.
El resultado del PET/TC Ga68-DOTATOC se correlacionó con la histopatología en aquellos casos en que se dispuso de ella (6 de los 7 casos), con la actitud terapéutica tomada tras la realización del PET y con el seguimiento clínico mínimo de 9 meses. Los estudios PET fueron considerados como verdadero positivo, verdadero negativo, falso positivo o falso negativo. Se valoraron estadísticamente dichos resultados.
La utilidad clínica del PET/TC Ga68-DOTATOC se analizó mediante el impacto clínico en el manejo del paciente. Para ello se evaluó si los resultados del PET provocaron modificaciones en el manejo clínico-terapéutico del paciente: indicaciones o variación en la actitud quirúrgica, cambios en el tratamiento farmacológico, variaciones en la planificación de la radioterapia, así como selección de pacientes candidatos a PRRT.
ResultadosSiete pacientes (2 mujeres y 5 varones) con un rango de edad de entre 45 y 77 años (media: 60,7) se incluyeron en el estudio.
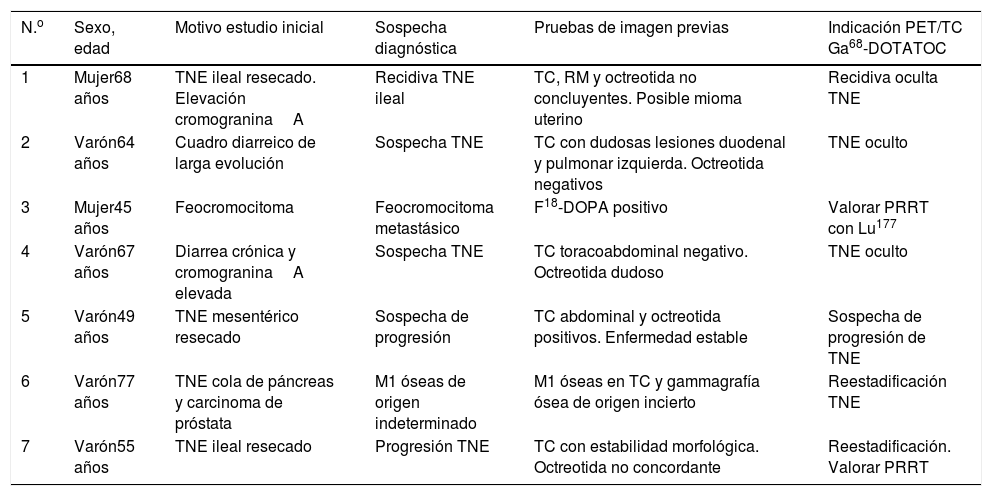
Todos los pacientes presentaban sospecha fundamentada de tumor neuroendocrino o sospecha de recidiva/progresión de tumores neuroendocrinos ya diagnosticados, con pruebas de imagen no concluyentes. Los motivos individuales por los que los pacientes estaban siendo estudiados, la sospecha diagnóstica del episodio en curso, así como el resto de datos y seguimiento clínicos, y las pruebas complementarias realizadas (principalmente pruebas diagnósticas de imagen), aparecen resumidos en la tabla 1.
Detalles de los pacientes. Indicación PET/TC Ga68-DOTATOC
| N.o | Sexo, edad | Motivo estudio inicial | Sospecha diagnóstica | Pruebas de imagen previas | Indicación PET/TC Ga68-DOTATOC |
|---|---|---|---|---|---|
| 1 | Mujer68 años | TNE ileal resecado. Elevación cromograninaA | Recidiva TNE ileal | TC, RM y octreotida no concluyentes. Posible mioma uterino | Recidiva oculta TNE |
| 2 | Varón64 años | Cuadro diarreico de larga evolución | Sospecha TNE | TC con dudosas lesiones duodenal y pulmonar izquierda. Octreotida negativos | TNE oculto |
| 3 | Mujer45 años | Feocromocitoma | Feocromocitoma metastásico | F18-DOPA positivo | Valorar PRRT con Lu177 |
| 4 | Varón67 años | Diarrea crónica y cromograninaA elevada | Sospecha TNE | TC toracoabdominal negativo. Octreotida dudoso | TNE oculto |
| 5 | Varón49 años | TNE mesentérico resecado | Sospecha de progresión | TC abdominal y octreotida positivos. Enfermedad estable | Sospecha de progresión de TNE |
| 6 | Varón77 años | TNE cola de páncreas y carcinoma de próstata | M1 óseas de origen indeterminado | M1 óseas en TC y gammagrafía ósea de origen incierto | Reestadificación TNE |
| 7 | Varón55 años | TNE ileal resecado | Progresión TNE | TC con estabilidad morfológica. Octreotida no concordante | Reestadificación. Valorar PRRT |
M1: metástasis; PRRT: terapia con péptidos marcados con radionúclidos; TNE: tumor neuroendocrino.
La paciente n.o1, de 68años, fue intervenida de un tumor neuroendocrino ileal en 2010 (Ki67 2%) que incluyó exéresis incompleta de implantes mesentéricos, iniciando tratamiento con análogos de la somatostatina. Se objetivó elevación progresiva de cromograninaA (357ng/ml) y gastrina (143pg/ml). Se realizaron estudios de imagen de RM y octreotida que no fueron concluyentes de persistencia de enfermedad. El PET/TC Ga68-DOTATOC mostró una lesión en fondo de saco de Douglas, retrouterina, varias lesiones nodulares peritoneales y afectación ganglionar retroperitoneal. Ante la extensión de la enfermedad se descartó la cirugía de rescate y se decidió aumentar la dosis del tratamiento con análogos de la somatostatina y control evolutivo.
El caso n.o2, un varón de 64años, presentaba pérdida de 7kg de peso en 3 meses con cifras elevadas de gastrina (143pg/ml) y cromogranina (540ng/ml). Los estudios realizados (ecografía, TC toracoabdominal, octreotida y endoscopias) fueron no concluyentes. El TC mostró una imagen infracentimétrica en la 3.a porción duodenal y un nódulo sólido de 11mm en el lóbulo inferior del pulmón derecho, difícil de tipificar. El PET 68Ga-DOTATOC confirmó la etiología neuroendocrina de la lesión duodenal y la descartó en la lesión pulmonar. Se practicó resección quirúrgica de la lesión duodenal. El estudio histológico confirmó la existencia de un tumor neuroendocrino en la mucosa duodenal, infracentimétrico con un Ki67 del 2%, TNEG1. Dieciocho meses después el paciente está libre de enfermedad y asintomático. En TC de control el nódulo pulmonar ha desaparecido.
A la paciente n.o3, de 34 años, se le detectó un nódulo adrenal izquierdo sospechoso durante el estudio de hipertensión arterial. Se realizó adrenalectomía izquierda con diagnóstico anatomopatológico de feocromocitoma. En el control evolutivo se observó elevación de catecolaminas y adenopatías subcentimétricas retroperitoneales paraórticas izquierdas. Se completó el estudio con un PET 18F-DOPA que mostró múltiples adenopatías milimétricas hipercaptantes supra- e infradiafragmáticas. Ante la posibilidad de realizar tratamiento sistémico con Lu177-Dotatate se solicitó estudio PET/TC Ga68-DOTATOC, siendo este negativo y por tanto contraindicando dicha terapia. Se realizó tratamiento con 150mCi de MIBG con mejoría de la sintomatología hipertensiva, pero sin cambios significativos en el PET 18F-DOPA de control.
El paciente n.o4, de 67 años, consultaba por diarrea crónica con empeoramiento en el último mes, dolor abdominal y vómitos. Cifras de cromograninaA elevadas (1.600ng/ml). Las pruebas de imagen convencionales fueron negativas, así como también el estudio PET/TC Ga68-DOTATOC. Se descartó tumor neuroendocrino y se manejó como diarrea secundaria a malabsorción de sales biliares. Tras 6 meses en tratamiento farmacológico la diarrea mejoró significativamente. El estudio TC posterior seguía siendo negativo.
El paciente n.o5, de 49 años, presentaba desde mayo de 2017 una lesión espiculada mesentérica central y metástasis hepáticas múltiples descritas en TC y RM abdominal, SPECT con octreotida y PET 18F-FDG. En octubre se realizó resección de la lesión del meso, con anatomía patológica definitiva de TNE de bajo grado (G1) peritoneal. CromograninaA, sinaptofisina, CD56, CDX2 positiva intensa y difusa, TTF1 negativo y Ki67 del 1-2%. Los estudios de imagen de control, angio-TC abdominal, RM abdominal y PET/TC 18F-FDG, en mayo de 2018, mostraban estabilidad de la enfermedad, persistiendo la sospecha clínica de progresión. Se solicitó estudio PET/TC Ga68-DOTATOC que mostró la presencia de lesión nodular en la raíz del mesenterio, metástasis hepáticas y adenopatías retroperitoneales hipercaptantes, sospechosas de progresión del proceso tumoral de origen neuroendocrino. Se continúa tratamiento con lanreotida 120mg/28 días y se remite para valoración de PRRT con Lu177-Dotatate.
El paciente n.o6, de 77 años, tenía antecedentes de neoplasia de próstata intervenida mediante prostatectomía radical y un adenocarcinoma de colon tratado con cirugía y con quimioterapia adyuvante. Ambos procesos neoplásicos, en remisión completa desde el año 2013. Durante el estudio de extensión del tumor neuroendocrino pancreático mediante PET 18F-FDG se observó, además de la presencia de la lesión primaria pancreática, múltiples lesiones óseas metastásicas no pudiendo concretarse su origen (neuroendocrino vs. prostático). El estudio PET/TC Ga68-DOTATOC mostró captación en la lesión pancreática, en una adenopatía paraórtica izquierda y en múltiples lesiones óseas, lo que indicaba su origen neuroendocrino. La biopsia ósea percutánea de sacro no fue concluyente inicialmente, pero tras estudios inmunohistoquímicos se confirmó el origen neuroendocrino de las lesiones óseas.
El paciente n.o7, de 55 años, con antecedentes de tumor neuroendocrino ileal, había sido intervenido en noviembre de 2015. Desde entonces recibía tratamiento de primera línea con lanreotida 90mg/28 días. En la actualidad presentaba valores normales de cromogranina (basal de 89ng/ml), con elevación de la serotonina de 293μg/l (menor que la basal [660μg/l]). El TC de control de noviembre de 2018 mostraba estabilidad radiológica de ganglios retroperitoneales y la gammagrafía con octreotida mostraba adenopatías supra- e infradiafragmáticas sin lesiones de nueva aparición respecto a estudios previos. Se indicó la realización del estudio PET Ga68-DOTATOC para obtener una correcta estadificación actual del proceso tumoral neuroendocrino, para valorar el mantenimiento de la terapia con lanreotida o indicar cambio terapéutico (posible PRRT). El PET/TC Ga68-DOTATOC evidenció progresión, con muy extensa afectación adenopática supra- e infradiafragmática sugestiva de progresión tumoral. El paciente se derivó al centro de referencia para valorar la posibilidad de inclusión en un ensayo clínico.
Presentando los resultados de manera agrupada podemos resumir:
De los 7 PET Ga68-DOTATOC realizados, 5 fueron verdaderos positivos (casos 1, 2, 5, 6 y 7) confirmándose todos ellos por anatomía patológica. No se obtuvieron resultados falsos positivos. De los 2 PET con resultados negativos, uno fue un verdadero negativo (caso 4) y el resultado del otro paciente se consideró un falso negativo del PET/TC Ga68-DOTATOC (caso 3), si bien fue positivo con PET 18F-DOPA. Los resultados de sensibilidad y especificidad fueron del 86% y 100%, respectivamente.
En todos los pacientes, los hallazgos del PET/TC Ga68-DOTATOC supusieron un cambio significativo en el diagnóstico del proceso en curso y tuvieron un efecto directo sobre el seguimiento y/o el tratamiento de los mismos (tabla 2).
Hallazgos PET/TC Ga68-DOTATOC. Impacto clínico. Modificaciones de la terapia
| N.o | PET/TC Ga68 edotreotida | Hallazgos PET/TC Ga68-DOTATOC | Variación seguimiento/terapia | Actitud terapéutica final |
|---|---|---|---|---|
| 1 | Positivo | Lesión pélvica retrouterina. Nódulos peritoneales. Adenopatías retroperitoneales | Sí | Se descartó cirugía de rescate. Análogos somatostatina |
| 2 | Positivo | TNE duodenal | Sí | Cirugía |
| 3 | Negativo | Lesiones sin expresión SSR | Sí | No PRRT |
| 4 | Negativo | Sin lesiones | Sí | Seguimiento |
| 5 | Positivo | Tumoración en raíz del mesenterio. M1 hepáticas. M1 adenopáticas múltiples | Sí | Análogos somatostatina. PRRT si progresión |
| 6 | Positivo | Masa pancreática, adenopatías múltiples y M1 óseas con expresión de SSR | Sí | Análogos somatostatina. PRRT si progresión |
| 7 | Positivo | Adenopatías múltiples supra- e infradiafragmáticas con expresión de SSR | Sí | Candidato a ensayo clínico con PRRT |
M1: metástasis; PRRT: terapia con péptidos marcados con radionúclidos; SSR: receptores de somatostatina; TNE: tumor neuroendocrino.
El trabajo que presentamos es la experiencia inicial en el uso del PET/TC Ga68-DOTATOC en nuestro país. Exponemos los primeros 7 casos clínicos en los que se indicó el uso de este nuevo radiofármaco. Todos los pacientes estaban clínicamente valorados por médicos experimentados en este tipo de tumores, existiendo dudas razonables de la presencia de lesiones de origen neuroendocrino, en la extensión y/o en la planificación terapéutica a realizar.
El PET/TC Ga68-DOTATOC aportó información relevante en todos y cada uno de los pacientes, si bien cabe descartar que la selección de los mismos fue muy minuciosa, con una indicación estricta y consensuada en los diferentes comités médicos.
Cinco de nuestros 7 pacientes con estudios de imagen previos no concluyentes mostraron un estudio PET/TC Ga68-DOTATOC positivo, todos ellos verdaderos positivos. Se confirma, por tanto, una mayor sensibilidad para la detección de tumor neuroendocrino de pequeño tamaño y/o en localizaciones atípicas que pueden pasar desapercibidas por otras pruebas diagnósticas, tanto en el diagnóstico de tumor primario neuroendocrino como ante la sospecha de recidiva. Igualmente, en el mismo estudio, se puede realizar una estadificación más exhaustiva del proceso tumoral13,14.
La ausencia de falsos positivos permitió obtener una especificidad del 100%. Este resultado se debe, en parte, a la cuidadosa selección de los pacientes, lo que incrementa la especificidad. Pese a no tener un poder estadístico adecuado por el pequeño tamaño de la muestra, creemos incide en la necesidad de que la decisión de la realización del PET/TC Ga68-DOTATOC sea tomada en el seno de comités multidisciplinares.
Así mismo presenta un valor predictivo negativo superior, otorgando una mayor confianza al descartar la presencia de tumoraciones de origen neuroendocrino bien diferenciadas. Los tumores neuroendocrinos de grado alto pueden presentar un alto metabolismo glicolítico, siendo por tanto el PET con F18-FDG la prueba de mayor sensibilidad. Ambos radiofármacos PET, Ga68-DOTATOC y F18-FDG, tienen su importancia en el estudio y seguimiento de los tumores neuroendocrinos, dependiendo del grado de desdiferenciación tumoral, pudiendo ser necesarios ambos según la heterogeneidad tumoral. Son pruebas complementarias y no excluyentes13-15.
El PET Ga68-DOTATOC detecta significativamente más lesiones que los estudios SPECT/TC con octreotida y la suma de TC y RM, tanto si están situadas en intestino como en páncreas, hígado, pulmón y adenopatías supra- e infradiafragmáticas16-19. En nuestro estudio se aumentó la estadificación en 5 de los 7 casos en comparación con la suma del resto de estudios diagnósticos.
Su mayor sensibilidad hace posible así mismo la detección precoz de recidivas tumorales, permitiendo iniciar las terapias adecuadas con mayor rapidez y con un volumen tumoral teóricamente menor17.
Nuestro paciente n.o2 fue un paciente en estudio por diarrea crónica de larga evolución con cifras elevadas de cromograninaA. Un estudio TC toracoabdominal previo describió una imagen nodular en la base pulmonar izquierda y una nodularidad no concluyente de etiología infiltrativa en el duodeno. La localización mural duodenal, el pequeño tamaño y la captación fisiológica intestinal de FDG dificultaron la detección precoz por TC y PET/TC 18F-FDG16. Sin embargo, el PET Ga68-DOTATOC pudo confirmar la naturaleza neuroendocrina de la, en principio dudosa, lesión duodenal. La ausencia de captación de la lesión nodular pulmonar desestimó la etiología neuroendocrina de la misma (alto valor predictivo negativo). Estos hallazgos permitieron tomar una decisión terapéutica correcta, en este caso cirugía con finalidad curativa con confirmación anatomopatológica del proceso neuroendocrino y mostrar el alto valor predictivo positivo del PET Ga68-DOTATOC. Dieciocho meses después el paciente está libre de enfermedad y asintomático. En TC de control el nódulo pulmonar había desaparecido.
Se podría recomendar un estudio PET/TC Ga68-DOTATOC para la estadificación tumoral neuroendocrina inicial, ya que la información adicional que aporta puede llegar a cambiar los planes quirúrgicos hasta en el 47% de los casos7,15,17.
En nuestro estudio, en todos los casos, los resultados del PET/TC Ga68-DOTATOC modificaron la actitud terapéutica inicialmente prevista. Estos cambios se concretaron en la indicación quirúrgica de una lesión tumoral no detectada con seguridad por otras pruebas diagnósticas, se descartó cirugía de rescate en un caso, se indicó tratamiento con análogos de la somatostatina en 2 pacientes, se descartó con seguridad la presencia de tumor neuroendocrino en un caso, se propuso PRRT a un paciente, y por último se descartó PRRT en otro caso.
En la actualidad, se encuentra disponible la radioterapia o terapia metabólica de receptor peptídico (PRRT) con Lu177-Dotatate con resultados muy prometedores en los tumores neuroendocrinos avanzados20. La condición básica para la indicación de dicha terapia es la constatación de la expresión de receptores de somatostatina en la membrana celular tumoral. Tanto el SPECT/TC con octreotida como el PET/TC Ga68-DOTATOC permiten evidenciar dichos receptores e indicar la PRRT, pero la sensibilidad del PET es significativamente mejor7,18, lo que incrementa el número de pacientes con indicación de PRRT.
En nuestro estudio 3 de los pacientes con tumores neuroendocrinos avanzados fueron valorados para un posible tratamiento con Lu177-Dotatate, inmediato o diferido, dada su alta expresión de receptores de somatostatina detectada por Ga68-DOTATOC, pese a que 2 de ellos no habían presentado captación significativa de octreotida.
Así mismo el valor predictivo negativo es significativamente mejor con Ga68-edotreotida, excluyendo únicamente aquellos pacientes sin receptores de somatostatina. Uno de nuestros pacientes, feocromocitoma metastásico, fue descartado para PRRT dada la negatividad del Ga68-DOTATOC. Si bien se ha validado la utilidad del PET Ga68-DOTATOC en el diagnóstico y el estudio de extensión de feocromocitomas y paragangliomas21,22, en nuestro caso la revaloración inmunohistoquímica tras negatividad del PET mostró ausencia de receptores de somatostatina, SDHB; SDHD; SDHC y SDHA activos. Se ha descrito la ausencia de captación de Ga68-DOTATOC en estos casos23, quedando por tanto la terapia con Lu177-Dotatate contraindicada.
Las limitaciones del estudio son varias. Se trata de un trabajo descriptivo con un número limitado de pacientes. Los casos fueron muy seleccionados, lo que podría sesgar los resultados. Entendemos que la implantación de la técnica en nuestro país está siendo muy laboriosa y de ahí que, al menos en esta etapa inicial, los casos deben ser muy seleccionados con la finalidad de por un lado obtener la mayor rentabilidad diagnóstica y por otro lado conseguir impactar el manejo de estos pacientes.
Sabemos que aún queda un largo camino por recorrer y muchas preguntas por responder. Sin embargo, creemos que el trabajo multidisciplinar y la disponibilidad del PET/TC Ga68-DOTATOC impactarán muy positivamente en el manejo de estos pacientes.
ConclusiónPET/TC Ga68-DOTATOC es una técnica con un gran potencial en el estudio de tumores neuroendocrinos, que abre las puertas a una nueva aproximación tanto en el diagnóstico como en la estadificación, el manejo terapéutico y el seguimiento de los mismos. Los resultados de este trabajo son aún muy preliminares, si bien están acordes con la bibliografía internacional publicada. El trabajo multidisciplinar y la disponibilidad del PET con nuevos trazadores creemos impactarán positivamente en el manejo de estos pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.