Evaluar los impactos clínicos y económicos de largo plazo de la terapia con bomba de insulina integrada a sistema de monitorización continua de glucosa (MCG) vs. inyecciones múltiples diarias de insulina (MDI) en pacientes con diabetes tipo 1 (DT1) en Colombia.
MétodosSe usó el CORE Diabetes Model con el fin de simular una cohorte hipotética de pacientes con DT1. Las características promedio de línea base fueron tomadas de un estudio clínico local. La perspectiva fue desde del pagador y se aplicó una tasa de descuento del 5% para los costes y los resultados.
ResultadosLa bomba de insulina integrada al sistema de MCG mejoró la expectativa de vida media en 3,51 años y 3,81 años de vida ajustados por calidad adicionales. En comparación con MDI hubo un retraso en el inicio de complicaciones relacionadas con la DT1, y el tiempo promedio de sobrevida y libre de cualquier complicación se aumentó en 1,74 años. Los costes relacionados con la bomba de insulina integrada al sistema de MCG fueron compensados con los ahorros por la disminución en las complicaciones relacionadas con la DT1. La relación de coste efectividad incremental fue de 23.200 dólares americanos por años de vida ajustados por calidad.
ConclusionesEl mejor control glucémico asociado con bomba de insulina integrada al sistema de MCG conduce a una disminución en la incidencia de las complicaciones relacionadas con DT1 y aumenta la esperanza de vida cuando se compara con MDI. De acuerdo a los umbrales recomendados por la Organización Mundial de la Salud, esta es una estrategia coste-efectiva cuando se compara con MDI en el tratamiento de la DT1.
To assess the long-term clinical and economic impact of integrated pump/CGM technology therapy as compared to multiple daily injections (MDI), for the treatment of type 1 diabetes (T1D) in Colombia.
MethodsThe CORE Diabetes Model was used to simulate a hypothetical cohort of patients with T1D. Mean baseline characteristics were taken from a clinical study conducted in Colombia and a healthcare payer perspective was adopted, with a 5% annual discount rate applied to both costs and outcomes.
ResultsThe integrated pump/CGM improved mean life expectancy by 3.51 years compared with MDI. A similar increase occurred in mean quality-adjusted life expectancy with an additional 3.81 quality-adjusted life years (QALYs). Onset of diabetes-related complications was also delayed as compared to MDI, and mean survival time free of complication increased by 1.74 years with integrated pump/CGM. Although this increased treatment costs of diabetes as compared to MDI, savings were achieved thanks to reduced expenditure on diabetes-related complications. The estimated incremental cost-effectiveness ratio (ICER) for SAP was Colombian Pesos (COP) 44,893,950 (approximately USD$23,200) per QALY gained.
ConclusionsImproved blood glucose control associated to integrated pump/CGM results in a decreased incidence of diabetes-related complications and improves life expectancy as compared to MDI. Using recommended thresholds from the World Health Organization and previous coverage decisions about health technologies in Colombia, it is a cost-effective alternative to MDI for the treatment of type 1 diabetes in Colombia.
La diabetes mellitus es un importante problema de salud en Colombia y representa un creciente desafío para el sistema de salud, con una prevalencia de 9,6% (8,6-10,7%) en edades entre los 20 y los 79 años, y se calcula un niño (0-14 años) con DMT1 por 1.000 habitantes1. Así mismo, al nivel de Sur y Centroamérica, Aschner y Aguilar encontraron una prevalencia para diabetes del 8,0% y los niños con diabetes tipo 1 representan el 0,2% del total de la población con diabetes2. En Colombia Aschner encontró una prevalencia que oscila entre el 4% y el 8% en función del rango de edad de la población estudiada, y estimó la prevalencia para diabetes mellitus tipo 1 en niños menores de 15 años en 0,07%3.
Barcelo et al. estimaron la carga total de la enfermedad para diabetes tipo 1 (DT1) y 2 en 2.500millones de dólares americanos para el año 2003, lo cual representa una carga relativamente baja cuando se hace una comparación per cápita con otros países latinoamericanos4. Barcelo et al., en The cost of diabetes in Latin America and the Caribbean. Bulletin of the World Health Organization. 2003, relacionan esta baja carga de la enfermedad con una baja frecuencia en la población colombiana en la utilización del servicio de consulta externa (0,7%) y hospitalización (6,1%)4.
La DT1 está asociada con un incremento en el riesgo de numerosas complicaciones serias, y la enfermedad cardiovascular asociada es la causa atribuible de muerte en el 47% de los hombres y en el 41% de las mujeres con DT15. Más allá del impacto clínico, las complicaciones relacionadas con la DT1 tienen importantes implicaciones en la calidad de vida (Quality of Life [QoL]) de los pacientes. Solli et al. evaluaron los resultados del cuestionario EuroQol 5-Dimensiones (EQ-5D), que permite valorar la calidad de vida de un determinado estado de salud entre 0 y 1, siendo 0 muerte y 1 el pleno estado de salud. Los investigadores encontraron que los pacientes con DT1 tuvieron, en una escala de 0 a 1, un promedio de 0,9 si estaban libres de complicaciones y de 0,68 si las complicaciones relacionadas con la DT1 estaban presentes6. Al evaluar los principales determinantes de una reducida QoL dentro de los subdominios del EQ-5D, los autores determinaron que el «miedo a la hipoglucemia» fue un importante determinador de «ansiedad/depresión», una de las 5 dimensiones del instrumento.
Las complicaciones relacionadas con la DT1 también tienen una importante influencia en los gastos en salud, y los costes relacionados con las complicaciones generalmente sobrepasan aquellos atribuidos directamente al tratamiento. Optimizar el manejo de los niveles de glucosa sanguíneos a través de un efectivo autocontrol de la enfermedad ha mostrado que reduce el riesgo de desarrollar las complicaciones relacionadas. El tratamiento efectivo de la DT1 es generalmente coste-efectivo7. A pesar de los beneficios de la auto-monitorización de la glucosa sanguínea (AMGS) en DT1, la evidencia indica que hasta el 63% de los pacientes no lo hacen regularmente8. Esto puede deberse a la complejidad y a los requerimientos de tiempos asociados. En una revisión de la literatura relacionada con adherencia a los diferentes regímenes de tratamiento de la DT1, Delamater et al. reportaron que los pacientes tienen mejor adherencia a regímenes más simples que a regímenes más complejos, y que menores tasas de AMGS fueron observadas entre hispanos que en la población general9.
Una gran ventaja puede ser obtenida a través del uso de monitorización continua de la glucosa (MCG) en tiempo real, la cual es más fácil de usar y facilita la adherencia. Un estudio clínico aleatorizado y controlado comparando MCG con AMGS encontró que la adherencia al primero fue más alta con un 83% de los pacientes de 25 o más años de edad usándolo por 6 días o más a la semana10. El beneficio de MCG sobre el AMGS y las inyecciones múltiples diarias de insulina (MDI por sus siglas en inglés) ha sido demostrado en varios estudios publicados10–16. Desafortunadamente los eventos hipoglucémicos pueden ocurrir incluso con MCG, y el número de eventos hipoglucémicos es frecuentemente subestimado. En el año 2013 Ly et al. demostraron que un sistema de automatizado de inyección de insulina que suspenda la inyección de esta hasta por 2h si el MCG detecta un valor de glucosa debajo de 60mg/dl, significativamente reduce la tasa de hipoglucemias sintomáticas y severas14. Bergenstal et al. encontraron que los eventos hipoglucémicos nocturnos ocurrieron un 31,8% menos frecuentemente en el grupo con umbral de suspensión que en el grupo control (1,5±1,0 vs. 2,2±1,3 por paciente por semana, p<0,001)12. Esta terapia de la bomba de insulina integrada a sistema de MCG tiene el potencial de reducir la hemoglobina glucosilada (HbA1c) y la frecuencia de eventos hipoglucémicos comparados con MDI10,12–15.
A través de la evaluación de la carga económica actual y futura de la DT1 en el sistema de salud de Colombia, se puede calcular el impacto de los diferentes tratamientos. Tales evaluaciones son de ayuda a los tomadores de decisiones del sistema de salud en el proceso de optimización de los recursos17. En este análisis evaluamos el impacto clínico y económico de la bomba de insulina integrada en el sistema de MCG comparado con MDI.
MétodosModeloPara el análisis de coste-efectividad se consideró un modelo de Markov que permitiera proyectar en el largo plazo los resultados clínicos, incluyendo las complicaciones asociadas, así como los costes médicos directos. Para ello, se consideró la utilización del IMS CORE Diabetes Model (CDM) versión 8.5, desarrollado por imshealth, debido a su alto nivel de validación y a su amplia utilización en muchos países del mundo.
El CDM es un modelo utilizado para simular la progresión de la diabetes y sus resultados asociados18,19. Está construido como un modelo de Markov con varios submodelos que corren en paralelo para simular la incidencia de complicaciones. Lo anterior basado en la progresión de la HbA1c y los esquemas de tratamiento. En este análisis hacemos una simulación de Montecarlo de segundo orden con 1.000 pacientes y 1.000 iteraciones. Las ecuaciones de riesgo para infarto de miocardio y accidente cerebrovascular fueron derivadas del United Kingdom Prospective Diabetes Study, al tiempo que las ecuaciones del estudio Framingham fueron usadas para estimar los riesgos de angina y fallo cardiaca.
El desarrollo de complicaciones (incidencia acumulada y tiempo hasta la presentación), expectativa de vida ajustada por calidad medida en años de vida ajustados por calidad (QALY), costes médicos directos y costes indirectos fueron modelados para cada una de las opciones de tratamiento18.
Beneficios clínicosCon el fin de parametrizar el impacto clínico de insulina integrada a sistema de MCG en Colombia se tomaron datos del estudio de Gómez et al.20. Este estudio reportó una reducción significativa en HbA1c, con una reducción media de 1,5% (16mmol/mol) para los 217 pacientes en el estudio. Los autores también reportaron una reducción significativa en la tasa anual de hipoglucemia severa, pasando de 5,22 episodios por año a 0,37 episodios por año (p=0,0009).
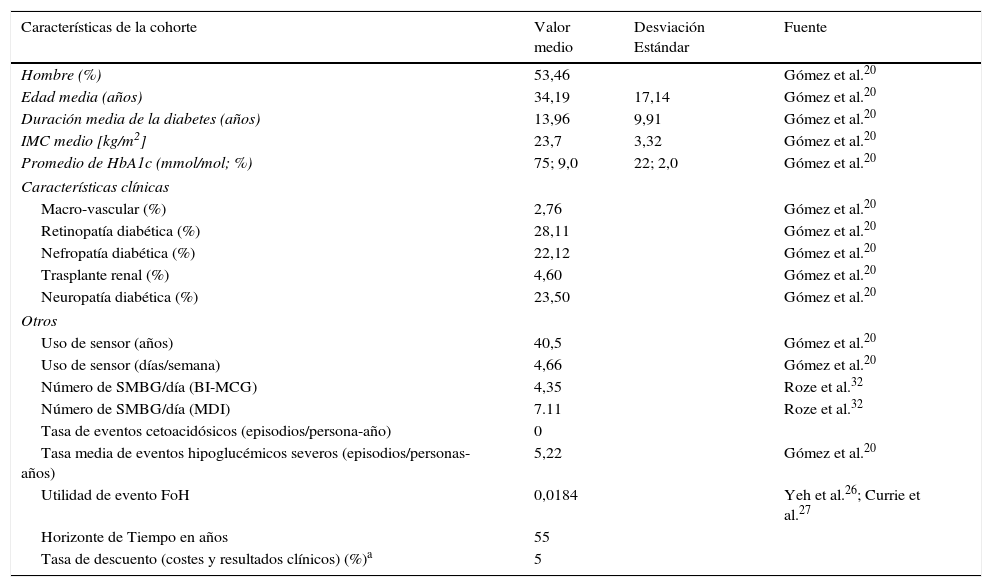
CohorteLas características basales de la cohorte para el análisis fueron tomadas del reciente estudio clínico de Gómez et al., que pueden ser encontradas en la tabla 120. Aunque el promedio del uso del sensor no fue reportado, el valor calculado a partir de los datos disponibles fue de 66,6 equivalente a 4,66 días-sensor por semana. La frecuencia relativa de AMGS fue tomada de un estudio observacional realizado por Personss et al., en el cual fue reportado que el uso del AMGS fue menor con la bomba de insulina integrada en el sistema de MCG en comparación con MDI21.
Características poblacionales
| Características de la cohorte | Valor medio | Desviación Estándar | Fuente |
|---|---|---|---|
| Hombre (%) | 53,46 | Gómez et al.20 | |
| Edad media (años) | 34,19 | 17,14 | Gómez et al.20 |
| Duración media de la diabetes (años) | 13,96 | 9,91 | Gómez et al.20 |
| IMC medio [kg/m2] | 23,7 | 3,32 | Gómez et al.20 |
| Promedio de HbA1c (mmol/mol; %) | 75; 9,0 | 22; 2,0 | Gómez et al.20 |
| Características clínicas | |||
| Macro-vascular (%) | 2,76 | Gómez et al.20 | |
| Retinopatía diabética (%) | 28,11 | Gómez et al.20 | |
| Nefropatía diabética (%) | 22,12 | Gómez et al.20 | |
| Trasplante renal (%) | 4,60 | Gómez et al.20 | |
| Neuropatía diabética (%) | 23,50 | Gómez et al.20 | |
| Otros | |||
| Uso de sensor (años) | 40,5 | Gómez et al.20 | |
| Uso de sensor (días/semana) | 4,66 | Gómez et al.20 | |
| Número de SMBG/día (BI-MCG) | 4,35 | Roze et al.32 | |
| Número de SMBG/día (MDI) | 7.11 | Roze et al.32 | |
| Tasa de eventos cetoacidósicos (episodios/persona-año) | 0 | ||
| Tasa media de eventos hipoglucémicos severos (episodios/personas-años) | 5,22 | Gómez et al.20 | |
| Utilidad de evento FoH | 0,0184 | Yeh et al.26; Currie et al.27 | |
| Horizonte de Tiempo en años | 55 | ||
| Tasa de descuento (costes y resultados clínicos) (%)a | 5 | ||
BI-MCG: bomba de insulina integrada en el sistema de monitorización continua de glucosa; MDI: inyecciones múltiples diarias de insulina.
La tasa de descuento está tomada de la Guía metodológica para la realización de evaluaciones económicas en el marco de guías de práctica clínica, versión 10/03/2014 [consultada 9 Ene 2015]. Disponible en: www.iets.org.co
El estudio considera los costes directos de la DT1 desde una perspectiva del pagador, los cuales fueron calculados en pesos colombianos del año 2013 y convertidos a dólares americanos para facilitar la comparación internacional, a la tasa vigente a 31 de diciembre de ese año, de 1.869.16 pesos colombianos por dólar americano. Los costes totales corresponden al tratamiento de la diabetes y sus complicaciones. Para el cálculo de estos costes se tuvo en cuenta el manual tarifario oficial para Colombia (SOAT) y los datos de facturación de pagadores públicos y privados. Los costes de intervención para la bomba de insulina integrada en el sistema de MCG fueron definidos a partir del precio de venta del precel Enlite® Sensor, de Enlite® Specific Serter, el MinilinkTM transmisor, baterías, lancetas y tirillas (paquete de 50), provistos por el fabricante. Un total de 40,5 Enlite® Sensor fueron usados para el caso base. Los costes de intervención para inyecciones diarias de insulina incluyeron los costes de las lancetas y las tirillas.
UtilidadesLos diferentes valores de utilidades de los estados de salud fueron tomados de varias fuentes previamente publicadas22–25, y cuando fue necesario aplicar múltiples valores de utilidades de forma simultánea se escogió el del estado con el menor valor. Si un paciente experimentaba infarto de miocardio, accidente cerebrovascular, amputaciones o eventos hipoglucémicos se le descontaban valores de utilidad del total de los QALY.
Yeh et al. reportaron que el MCG reduce el miedo a la hipoglucemia (Fear of Hypoglycemic [FoH]) comparado con AMGS26. En su estudio, la diferencia media entre los grupos en la encuesta de miedo a la hipoglucemia fue de –2,3 (IC 95% –8,2 a 3,6) a favor de MCG. En términos de utilidad se ha reportado que el EQ-5D disminuye en 0,008 unidades por cada unidad de aumento en el FoH en la encuesta de miedo a la hipoglucemia27. La utilidad de FoH que se aplicó en el presente trabajo fue de +0,0184 (2,3×0,008) en pacientes con la bomba de insulina integrada en el sistema de MCG, y refleja los beneficios derivados de la disminución del FoH.
Tasa de descuentoTal como fue recomendado para las condiciones colombianas, se aplicó una tasa de descuento del 5% tanto para los resultados clínicos como económicos (tabla 1). Para asegurarnos de que todos los impactos en términos de resultados en salud y en costes de las alternativas de tratamiento fueran capturados dentro del modelo, se asumió un horizonte de análisis para toda la vida.
Análisis de sensibilidadCon el fin de evaluar el nivel de robustez del modelo y construir las curvas de aceptabilidad a pagar, se realizó un análisis de sensibilidad probabilístico con muestreo de las distribuciones describiendo las incertidumbres en los parámetros de las variables.
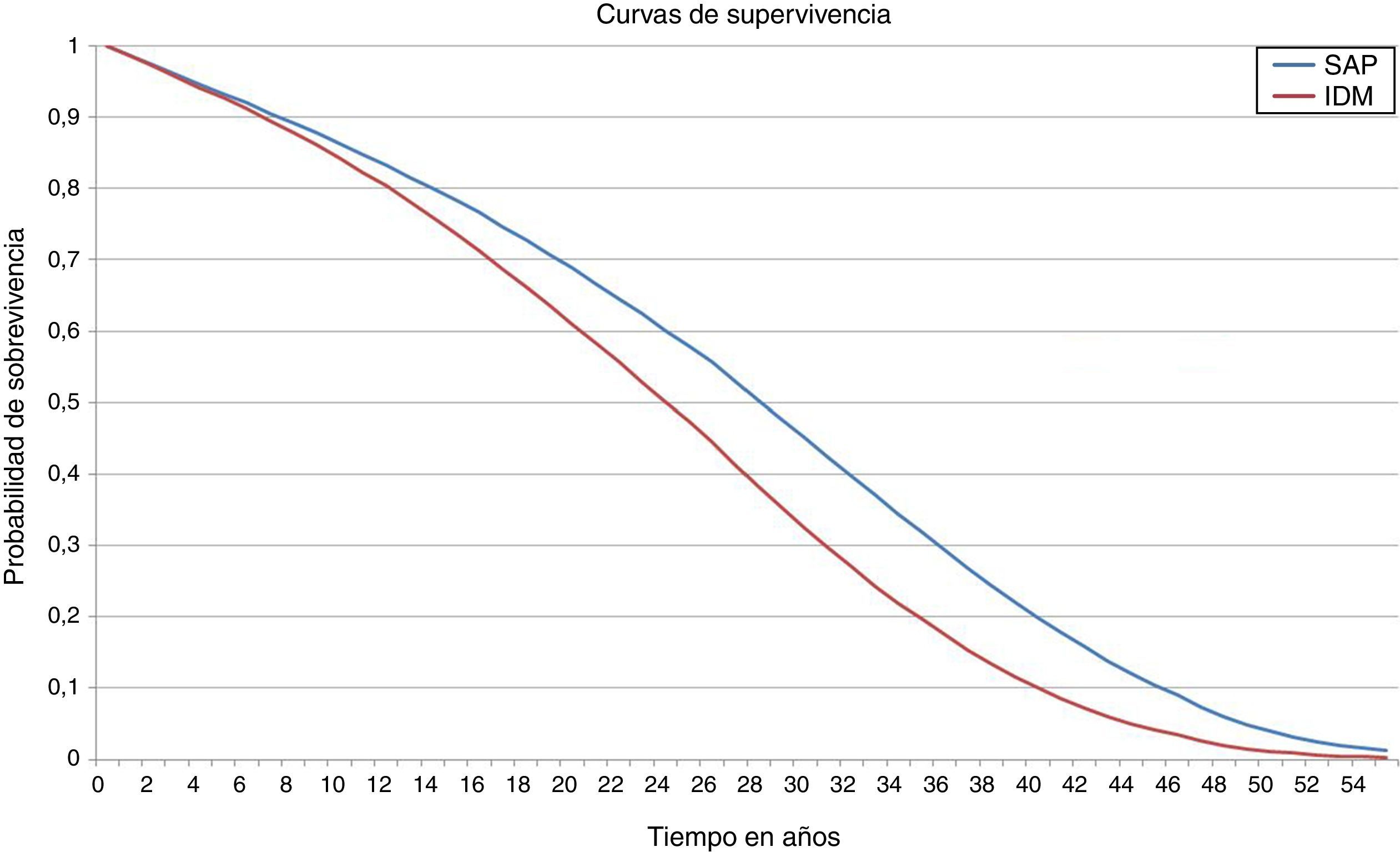
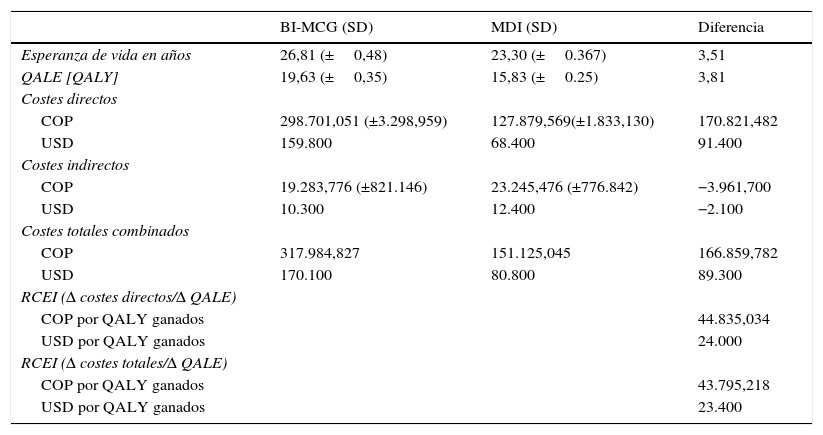
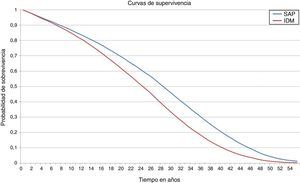
ResultadosEn el análisis del caso base el tratamiento de la DT1 con la bomba de insulina integrada en el sistema de MCG aumentó la esperanza de vida en 3,51 años (IC 95%: 3,47-3,55) comparado con las MDI (fig. 1 y tabla 2). La esperanza de vida media del grupo con bomba de insulina integrada en el sistema de MCG fue de 26,81±0,48 años comparado con 23,30±0,38 años para el grupo con MDI. Adicionalmente el grupo con bomba de insulina integrada en el sistema de MCG, logró 19,63±0,35 QALY vs. 15,83±0,25 para el grupo con MDI, lo que representa una diferencia de 3,81 QALY.
Resultados del caso base
| BI-MCG (SD) | MDI (SD) | Diferencia | |
|---|---|---|---|
| Esperanza de vida en años | 26,81 (±0,48) | 23,30 (±0.367) | 3,51 |
| QALE [QALY] | 19,63 (±0,35) | 15,83 (±0.25) | 3,81 |
| Costes directos | |||
| COP | 298.701,051 (±3.298,959) | 127.879,569(±1.833,130) | 170.821,482 |
| USD | 159.800 | 68.400 | 91.400 |
| Costes indirectos | |||
| COP | 19.283,776 (±821.146) | 23.245,476 (±776.842) | −3.961,700 |
| USD | 10.300 | 12.400 | −2.100 |
| Costes totales combinados | |||
| COP | 317.984,827 | 151.125,045 | 166.859,782 |
| USD | 170.100 | 80.800 | 89.300 |
| RCEI (Δ costes directos/Δ QALE) | |||
| COP por QALY ganados | 44.835,034 | ||
| USD por QALY ganados | 24.000 | ||
| RCEI (Δ costes totales/Δ QALE) | |||
| COP por QALY ganados | 43.795,218 | ||
| USD por QALY ganados | 23.400 |
BI-MCG: bomba de insulina integrada en el sistema de monitorización continua de glucosa; MDI: inyecciones múltiples diarias de insulina.
Conversión de pesos colombianos (COP) a dólares americanos (USD) (redondeado al porcentaje más cercano) a una tasa de cambio de 1 COP por 0,000535 USD.
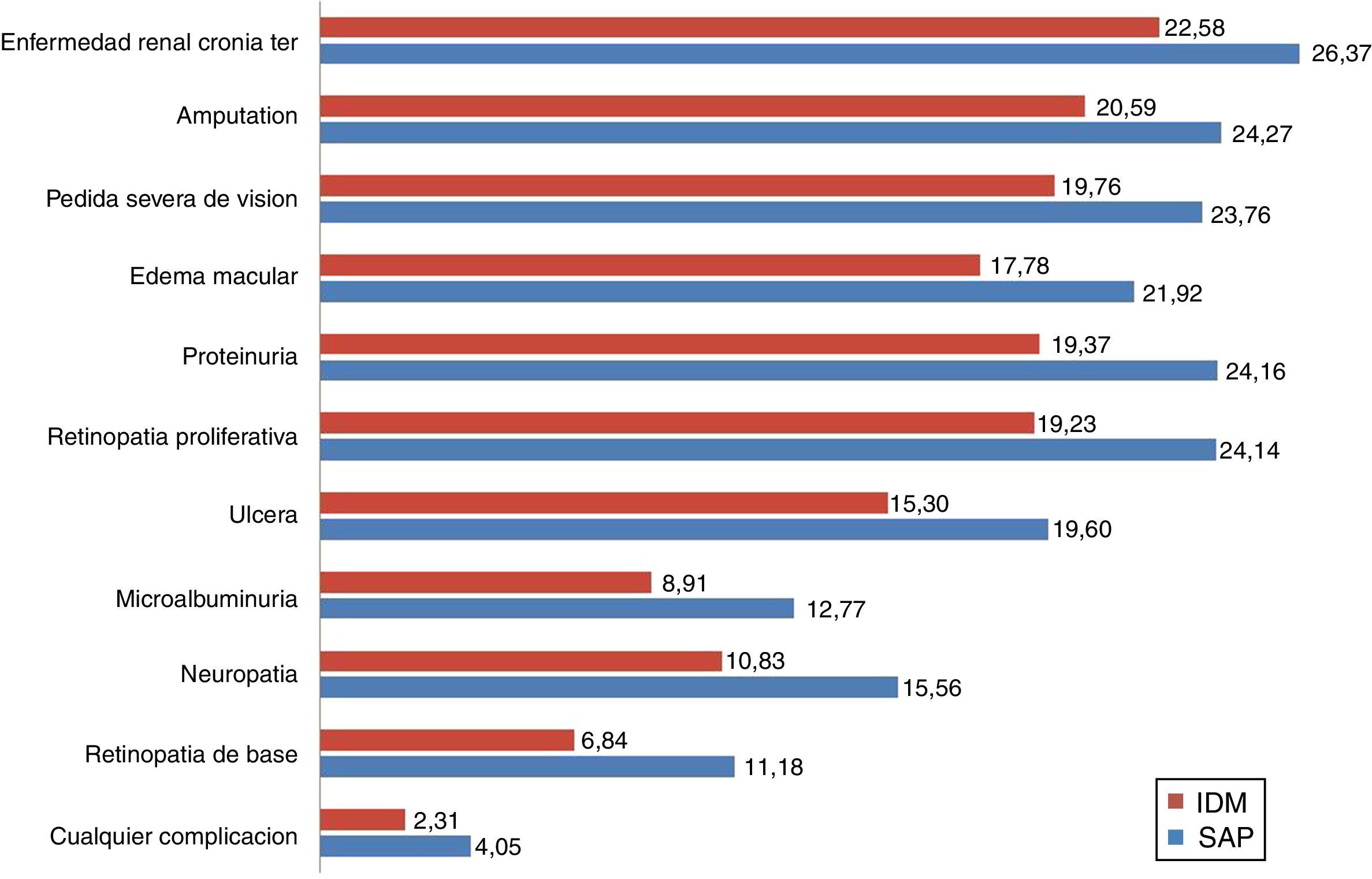
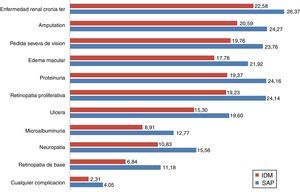
Considerando las complicaciones relacionadas con la DT1, la bomba de insulina integrada en el sistema de MCG retardó el tiempo medio de ataque de la primera complicación en cerca de 1,74 años. El tiempo medio de vida libre de cualquier complicación fue de 4,05 años vs. 2.38 con MDI (fig. 2).
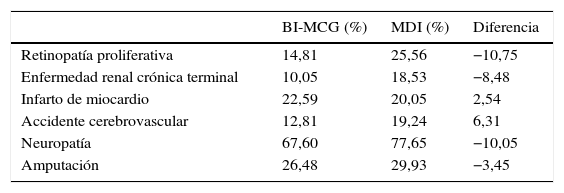
El grupo de la bomba de insulina integrada en el sistema de MCG tuvo un retardo medio de 4,5 años en el inicio de 3 complicaciones: neuropatía (4,73 años), proteinuria (4,79 años) y retinopatía proliferativa (4,91 años). Adicionalmente al retardo en el inicio de las complicaciones, la incidencia acumulada a lo largo de la vida de las complicaciones relacionadas con la DT1 fue menor cuando se comparó con el grupo de MDI y la incidencia acumulada de enfermedad renal terminal fue de 10,1% vs. 18,5% para MDI (tabla 3). Sin embargo, debido al aumento en la esperanza de vida con la bomba de insulina integrada en el sistema de MCG, se presentó una incidencia acumulada mayor en ciertas complicaciones relacionadas con la mayor edad cuando se comparó con el grupo de MDI, lo que corresponde a la llamada «paradoja de la supervivencia», como puede observarse en la tabla 3.
Incidencia acumulada de complicaciones relacionadas con la DT1
| BI-MCG (%) | MDI (%) | Diferencia | |
|---|---|---|---|
| Retinopatía proliferativa | 14,81 | 25,56 | −10,75 |
| Enfermedad renal crónica terminal | 10,05 | 18,53 | −8,48 |
| Infarto de miocardio | 22,59 | 20,05 | 2,54 |
| Accidente cerebrovascular | 12,81 | 19,24 | 6,31 |
| Neuropatía | 67,60 | 77,65 | −10,05 |
| Amputación | 26,48 | 29,93 | −3,45 |
BI-MCG: bomba de insulina integrada en el sistema de monitorización continua de glucosa; MDI: inyecciones múltiples diarias de insulina.
Los costes directos medios asociados con la bomba de insulina integrada en el sistema de MCG fueron proyectados en 159.800 dólares americanos, en comparación con 68.400$ para MDI (tabla 2). La relación de coste efectividad incremental fue de 24.000$. Asumiendo una disponibilidad a pagar de 26,750$ (aproximadamente 3 PIB per cápita) por QALY ganado28, la curva de aceptabilidad a pagar demostró que la bomba de insulina integrada a sistema de MCG sería coste efectiva en el 99% de los casos.
Evaluando los componentes de los costes directos, los principales determinantes fueron los costes de los tratamientos con el 86% y el 61% para la bomba de insulina integrada en el sistema de MCG y para MDI respectivamente. Los costes de tratamiento durante toda la vida fueron de 137.867$para la bomba de insulina integrada en el sistema de MCG comparado con 41,847$ para MDI. El incremento en la esperanza de vida asociado con la bomba de insulina integrada en el sistema de MCG fue responsable de un incremento del 13% en los costes. El resto del coste directo se relacionó con el manejo y tratamiento de las complicaciones relacionadas con la DT1. Diferencias sustanciales entre los 2 grupos fueron encontradas en el coste del tratamiento de las complicaciones. Aunque los componentes más importantes del coste de las complicaciones en las 2 cohortes hipotéticas fueron atribuidos al tratamiento de úlceras, amputaciones y neuropatía, este participó con el 6% de los costes directos con la bomba de insulina integrada en el sistema de MCG y el 18% con los costes directos con inyecciones diarias múltiples. En promedio el coste de tratar las complicaciones fue menor que con MDI (20.987$ vs. 25.638$), con una disminución en los costes atribuida a una incidencia acumulada menor de complicaciones.
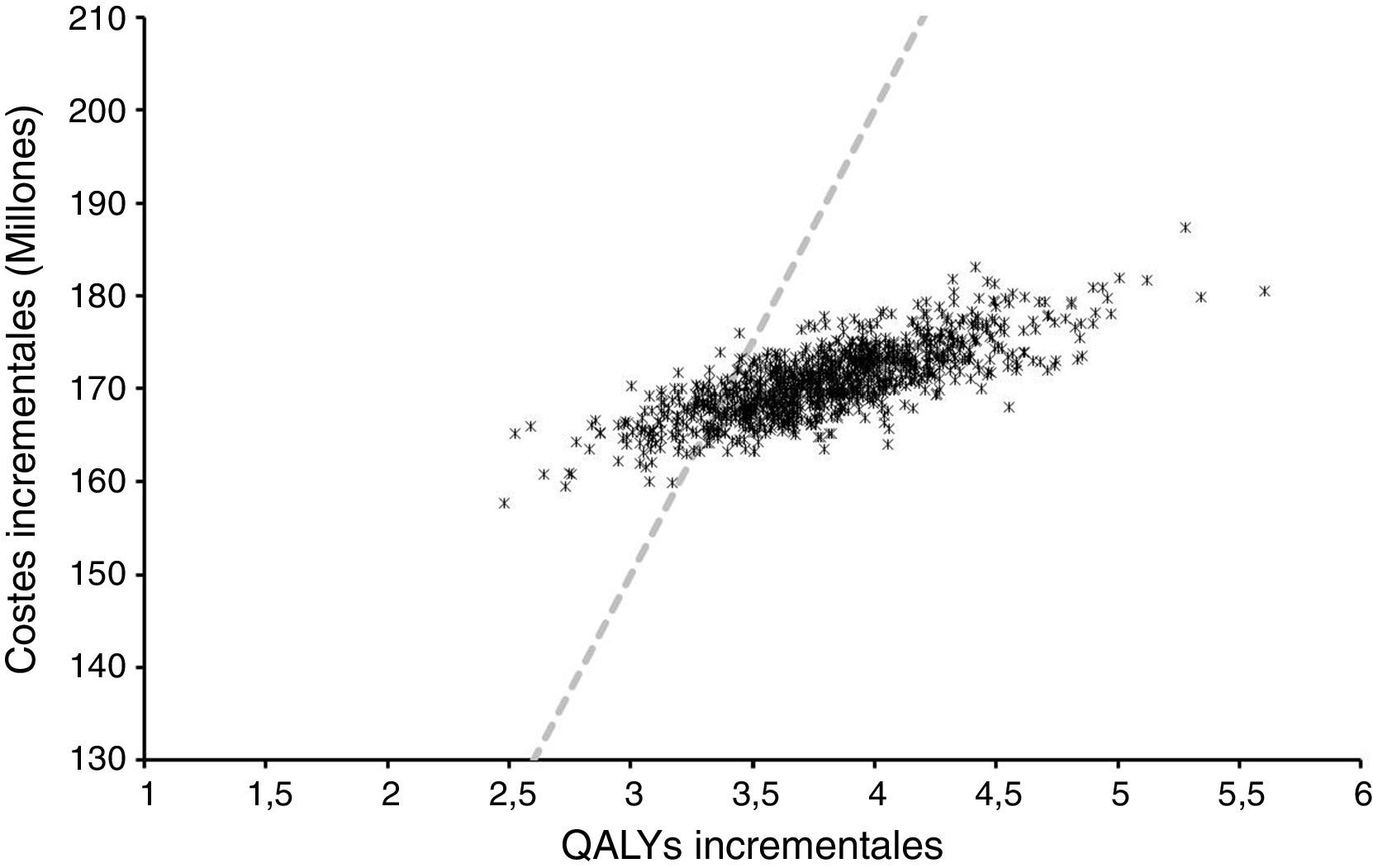
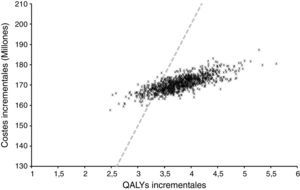
Análisis de sensibilidadEl análisis de sensibilidad probabilístico permitió explorar la variación en los resultados debido a la incertidumbre en el modelo y sus parámetros. La figura 3 muestra la distribución del coste incremental y de los QALY incrementales de la bomba de insulina integrada en el sistema de MCG respecto de las MDI a partir de 1.000 simulaciones.
En todos los casos está asociado con un aumento en la esperanza de vida ajustada por calidad y a un aumento en los costes directos. Los hallazgos de este estudio pueden entonces ser considerados robustos e interpretados con confianza. El RCEI promedio de estas simulaciones fue de 24.269$ por QALY con percentiles 25 y 75 de 22.680$ y 25.652$ por QALY ganado respectivamente. Si los costes indirectos, aquellos no relacionados con los costes médicos y más con el paciente, también fueran considerados el RCEI se incrementaría. Cuando se estimó el RCEI usando costes directos e indirectos, este alcanzó los 23.400$ por QALY.
DiscusiónEn el largo plazo los análisis de coste efectividad indican que el tratamiento con la bomba de insulina integrada en el sistema de MCG está asociado con mejores resultados clínicos e incidencia reducida de complicaciones relacionadas con la DT1 cuando se compara con MDI. La bomba de insulina integrada en el sistema de MCG se asoció con mayores costes médicos directos, lo cual fue parcialmente compensado por la disminución en la incidencia de las complicaciones. El RCEI indica que la bomba de insulina integrada en el sistema de MCG es probablemente coste-efectivo comparado con MDI en el tratamiento de la DT1 en las condiciones colombianas. De acuerdo a la recomendación de la OMS de una disponibilidad a pagar con un umbral de 3 PIB per cápita28,29, habría una probabilidad del 99% de que la bomba de insulina integrada en el sistema de MCG fuera considerada coste efectiva en Colombia. Si los costes indirectos fueran también considerados esta probabilidad se aumentaría.
Otros análisis de coste-efectividad comparando las 2 alternativas de acción y realizados en otros entornos han llegado a conclusiones similares. En una comparación con el manejo estándar AMGS, McQueen et al. estimaron que el uso de MCG en el tratamiento de la DT1 fue coste-efectivo con un RCEI de 45,033$ por QALY ganado30. Similarmente Huang et al. estimaron el RCEI de MCG comparado con la monitorización de glucosa estándar en DT1 fue de 78.943$ por QALY ganado31. El RCEI estimado en el presente trabajo es favorable, y puede reflejar la línea de base alta en HbA1c, la cual da una oportunidad adicional para mejores resultados. En este contexto el metaanálisis por Pickup et al. demostró que mayores reducciones en HbA1c estuvieron relacionadas con mayores valores de línea base15. Adicionalmente la evaluación del impacto de la bomba de insulina integrada en el sistema de MCG en FoH puede proveer beneficios adicionales. Ly et al. demostraron que la bomba de insulina integrada en el sistema de MCG fue de gran ayuda en la reducción de las tasas a las cuales los pacientes con baja consciencia de hipoglucemia experimentaban episodios hipoglucémicos severos14.
En el estudio de coste-efectividad realizado por Kamble et al.33, publicado en 2012, encontraron que la bomba de insulina tenía un ICER de 168.104$ por QALY ganado para un escenario de uso de sensor por 6 días, y concluye que todavía no es económicamente atractivo en EE. UU. A pesar de que este estudio utilizó el CORE Diabetes Model, no está claro en la utilización de los costes de las complicaciones de largo plazo de la DMT1, y solo menciona aquellos costes relacionados con los insumos y la insulina requeridos en el tratamiento en cada una de las 2 ramas, así como los eventos de hospitalización y urgencias relacionados directamente con la diabetes. Igualmente, los estimados de efectividad fueron tomados de datos del estudio STAR 3, los cuales son inferiores a la disminución de 1,2%, utilizado por St. Charles et al.34 a partir de un metaanálisis.
Un especial cuidado se tuvo en asegurar que este análisis fuera una representación precisa del uso de la bomba de insulina integrada en el sistema de MCG en el entorno colombiano. Sin embargo, como con todos los estudios de modelamiento en economía de la salud, el análisis presentado aquí provee estimados de las implicaciones clínicas y económicas basadas en simulaciones a partir de datos publicados y supuestos propios de los autores. La falta de estudios en el largo plazo en DT1 obliga al uso de datos de corto plazo para proyectar los resultados. Para minimizar las potenciales limitaciones en este estudio una búsqueda extensiva y sistemática en la literatura mundial fue realizada, y de acuerdo a la disponibilidad en el entorno local. En nuestro caso las particularidades demográficas y epidemiológicas de las cohortes hipotéticas fueron tomadas de literatura específica en la bomba de insulina integrada en el sistema de MCG en Colombia.
Una limitación del presente trabajo radica en que el CORE Diabetes Model se basa en datos del United Kingdom Prospective Diabetes Study, del Diabetes Control and Complications Trial, del Framingham Heart Study y del Wisconsin Epidemiologic Study of Diabetic Retinopathy, y aunque estos datos epidemiológicos son ampliamente utilizados para modelar los resultados de salud de los pacientes con diabetes, no siempre son representativos de la progresión de complicaciones de los pacientes más recientemente diagnosticados con DT1 tratados en la era moderna. Sin embargo, los estudios de validación han mostrado que las simulaciones con el CDM han producido valores estadísticos R2 de 0,9. Para estudios de validación con seguimiento para DMT1 se han encontrado valores R2 de 0,9 para periodos de menos de 15 años y de 0,72 para seguimientos a 30 años (DCCT)35.
FinanciaciónEste estudio recibió soporte financiero de Medtronic PLC.
Conflicto de interesesTodos los autores contribuyeron a la investigación y desarrollo del manuscrito y cumplen con los criterios de autoría. SR and RS son empleados de la empresa consultora y reciben pagos por su participación en la investigación. PML, JEV y JO son empleados de Medtronic PLC. RAC y AMG no han recibido honorarios de Medtronic PLC por el presente trabajo. Los autores declaran su completa independencia durante todo el proceso de investigación y son los únicos responsables por los métodos, resultados y conceptos contenidos en este manuscrito.