El abordaje diagnóstico-terapéutico de los pacientes transexuales solo puede desarrollarse en unidades funcionales de Identidad de Género, con la provisión de servicios de alta calidad asistencial, desarrollo de guías de práctica clínica y grupos de trabajo interdisciplinarios. El proceso terapéutico consta de 3 pilares fundamentales: evaluación diagnóstica psicológica inicial y psicoterapia, evaluación endocrinológica y terapia hormonal y cirugías de reasignación sexual. El tratamiento hormonal cruzado es un elemento importante en el proceso de transición anatómica y psicológica de los pacientes apropiadamente seleccionados. Las hormonas contribuyen a optimizar el proceso de vida real en el sexo identitario, mejoran la calidad de vida y limitan las comorbilidades psiquiátricas que muchas veces se asocian a la falta de este tratamiento. La elaboración de esta guía de práctica clínica responde a la necesidad de implantación de un protocolo de actuación coordinado para la atención sanitaria integral a las personas transexuales en el Sistema Nacional de Salud.
Transsexual patients can only be diagnosed and treated at functional gender identity Units with provision of high quality care, development of clinical practice guidelines, and interdisciplinary working groups. The therapeutic process has three mainstays: initial psychological diagnostic evaluation and psychotherapy, endocrinological evaluation and hormone therapy, and sex reassignment surgery. Cross-sex hormone therapy is essential for the anatomical and psychological transition process in duly selected patients. Hormones help optimize real-life sex identity, improve quality of life, and limit psychiatric co-morbidities often associated to lack of treatment. Development of this clinical practice guideline addresses the need for implementing a coordinated action protocol for comprehensive health care for transgender people in the National Health System.
La transexualidad o transexualismo se considera la situación más extrema dentro de las discordancias entre la identidad de género y el sexo biológico (DIG) y se define como un malestar intenso o disforia con el sexo anatómico e identificación con el otro sexo. Esta identidad cruzada suele conducir a una serie de cambios adaptativos físicos y sociales en la vida cotidiana (hábito externo, elección de un nombre acorde con su identidad, rol genérico, etc.), que constituyen el test de vida real o experiencia de la vida real (EVR)1.
La asistencia de los pacientes que experimentan una DIG constituye un excelente ejemplo de la necesidad de un equipo multidisciplinar. Los pacientes deben participar en el proceso terapéutico y la toma de decisiones tras una información correcta por parte de los clínicos. El tiempo de espera para acceso a este servicio debería estar en línea con la demora propia de otros servicios de un hospital de tercer nivel, lugar donde suele estar ubicada la unidad multidisciplinar. El paciente debería ser informado tras la valoración inicial de los tiempos de espera aproximados, de modo que sea consciente de que su tratamiento progresa de acuerdo con la escala temporal establecida en el protocolo.
El abordaje diagnóstico-terapéutico solo puede desarrollarse en unidades funcionales de Identidad de Género (UIG), donde va a ser fundamental el principio de accesibilidad a los recursos, evitando periodos de espera innecesarios, así como la provisión de servicios de alta calidad asistencial con el desarrollo de guías de práctica clínica y grupos de trabajo interdisciplinarios. El proceso terapéutico consta de 3 pilares fundamentales: evaluación diagnóstica psicológica inicial y psicoterapia, evaluación endocrinológica y terapia hormonal y cirugía de reasignación sexual (CRS). El tratamiento hormonal cruzado (THC) es un elemento importante en el proceso de transición anatómica y psicológica de adultos con alteraciones de identidad de género apropiadamente seleccionados. Las hormonas contribuyen a optimizar el proceso de vida real en el sexo identitario, mejoran la calidad de vida y limitan las comorbilidades psiquiátricas que muchas veces se asocian a la falta de este tratamiento.
La elaboración de esta guía de práctica clínica responde a la necesidad de implantación de un protocolo de actuación coordinado para la atención sanitaria integral a las personas transexuales en el Sistema Nacional de Salud. Esta guía es acorde con los consensos internacionales de manejo de esta entidad clínica.
DefinicionesExisten 2 manuales internacionales utilizados por los profesionales clínicos en los que constan los criterios que se deben cumplir para diagnosticar la transexualidad; el Diagnostic and Statistical Manual of Mental Disorders (DSM-IV) y el Código Internacional de Enfermedades (CIE-10). Ambos incluyen en el apartado de problemas mentales las alteraciones de la identidad de género, siendo en la actualidad controvertida esta inclusión, ya que la mayoría de los pacientes, aunque manifiestan una dificultad adaptativa y por tanto gran sufrimiento por su condición de transexual, no padecen otra patología mental específica2.
Trastorno de identidad de género (DSM IV). Pacientes con una identificación fuerte y consistente con el género opuesto, con una incomodidad persistente con su sexo y un sentimiento de desempeñar un rol de género inapropiado. A su vez se subdivide en función de la edad de diagnóstico en trastorno de identidad de género de niñez, adolescencia o del adulto. Las personas que no se encuadran dentro de estos criterios se identifican como trastorno misceláneo no especificado de identidad de género; en este apartado podían ser considerados los trastornos de identidad sexual que acompañan con cierta frecuencia a los trastornos de diferenciación sexual (anteriormente llamados estados intersexuales)2.
La CIE-10 incluye 5 diagnósticos dentro del trastorno de identidad de género (F 64): transexualidad, travestismo de papeles duales, trastorno de identidad de género de niñez, otros trastornos de identidad de género y trastorno misceláneo no especificado de identidad de género.
Transexualidad (CIE-10, F64.0). Tiene que cumplir 3 criterios: el deseo de vivir y ser aceptado como el sexo opuesto, generalmente acompañado por el deseo de hacer el cuerpo lo más similar posible al del sexo preferido por medio de cirugía y tratamientos hormonales; la identidad transexual ha estado presente persistentemente durante por lo menos 2 años; y la entidad no es un síntoma de un trastorno mental ni de una anomalía cromosómica.
Es la forma más extrema de la disforia sexual, manifestando, la persona que lo padece, un sentimiento constante y una convicción persistente de pertenecer al otro sexo, hecho que le crea un permanente conflicto de identidad sexual, siendo este el aspecto cardinal del fenómeno.
Disforia de género. La experiencia de la discordancia entre la apariencia sexual, y el sentimiento personal de ser hombre o mujer.
Transexual hombre a mujer (THM). La paciente THM (mujer transexual), se siente e identifica interiormente como mujer, aunque se sabe anatómicamente varón, en consecuencia realiza todos los esfuerzos posibles para que su cuerpo se adecue a esta identidad. Estas personas presentan una preocupación persistente por ocultar sus características sexuales primarias y secundarias, y en su mayoría solicitan tratamiento hormonal y quirúrgico para cambiar el sexo.
Transexual mujer a hombre (TMH). La persona TMH (hombre transexual), es anatómicamente mujer pero muestra actitudes, conductas, y aficiones típicamente de varón. La adopción de comportamiento, ropa y movimientos masculinos se efectúa en diferentes grados. Estas personas manifiestan un intenso deseo de adoptar el papel social de varón, ser aceptados como tal y, de adquirir un aspecto físico masculino, por ello desde la adolescencia tienden a llevar ropa ambigua o masculina ocultando sus mamas mediante prendas de compresión.
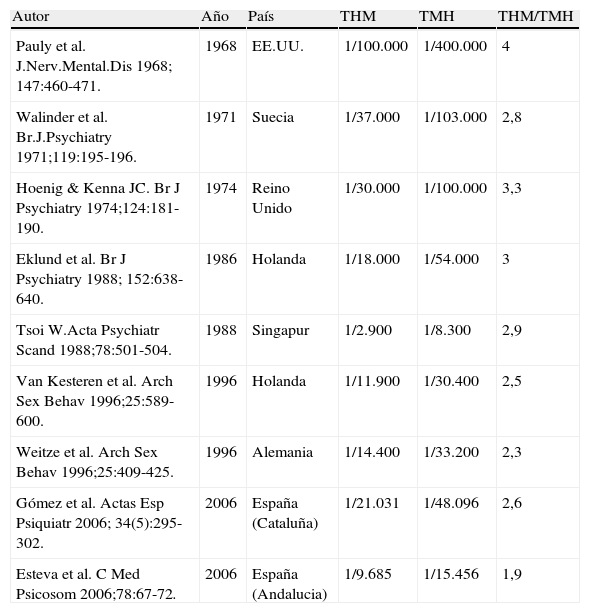
EpidemiologíaLas estimaciones de la prevalencia del DIG varían de forma considerable (tabla 1)3. En Europa, los estudios más recientes son el escocés que estima una prevalencia del 1:12.225 habitantes4, el holandés 1:11.900 varones biológicos y 1:30.400 mujeres biológicas5, y el inglés6 (registro Gender Identity Research and Education Society (GIRES) 2008) 1:4.000 habitantes. El cociente THM/TMH se sitúa entre 3:1 y 4:1. El GIRES asume una incidencia del DIG en 3 por cada 100.000 habitantes mayores de 15 años. En España la prevalencia se sitúa en THM de 1:9.685 - 1:21.031 varones biológicos y en TMH de 1:15.456 - 1:48.096 mujeres biológicas7–9. La extrapolación de estas prevalencias a la población española conlleva un total de 3.865 THM y 1.513 TMH, si bien estas cifras estén probablemente infraestimadas (ver más adelante referencia sobre datos en España).
Prevalencia y proporción entre sexos de la transexualidad en diversos estudios nacionales e internacionales (3)
| Autor | Año | País | THM | TMH | THM/TMH |
| Pauly et al. J.Nerv.Mental.Dis 1968; 147:460-471. | 1968 | EE.UU. | 1/100.000 | 1/400.000 | 4 |
| Walinder et al. Br.J.Psychiatry 1971;119:195-196. | 1971 | Suecia | 1/37.000 | 1/103.000 | 2,8 |
| Hoenig & Kenna JC. Br J Psychiatry 1974;124:181-190. | 1974 | Reino Unido | 1/30.000 | 1/100.000 | 3,3 |
| Eklund et al. Br J Psychiatry 1988; 152:638-640. | 1986 | Holanda | 1/18.000 | 1/54.000 | 3 |
| Tsoi W.Acta Psychiatr Scand 1988;78:501-504. | 1988 | Singapur | 1/2.900 | 1/8.300 | 2,9 |
| Van Kesteren et al. Arch Sex Behav 1996;25:589-600. | 1996 | Holanda | 1/11.900 | 1/30.400 | 2,5 |
| Weitze et al. Arch Sex Behav 1996;25:409-425. | 1996 | Alemania | 1/14.400 | 1/33.200 | 2,3 |
| Gómez et al. Actas Esp Psiquiatr 2006; 34(5):295-302. | 2006 | España (Cataluña) | 1/21.031 | 1/48.096 | 2,6 |
| Esteva et al. C Med Psicosom 2006;78:67-72. | 2006 | España (Andalucia) | 1/9.685 | 1/15.456 | 1,9 |
THM: transexual hombre a mujer; TMH: transexual mujer a hombre.
(3) Esteva I et al. Transexualismo. Manual del residente en endocrinología y nutrición. 2009 (ISBN 978-84-692-1374-2).
El tratamiento de la DIG basado en la combinación de terapia hormonal y habitualmente una combinación de intervenciones quirúrgicas de reasignación sexual, asociadas a una valoración y soporte psicológico adecuado, conlleva excelentes resultados, con una tasa de éxito definido como satisfacción personal tras el proceso superior al 90% y unas tasas de arrepentimiento muy bajas, del 0,5-3%10,11. Los factores que predicen el mal pronóstico y el arrepentimiento, tras la realización de cambios irreversibles, son la pérdida de apoyo familiar y social, la inestabilidad personal, los trastornos de la personalidad, la presencia de trastornos psicóticos y la aparición de eventos traumáticos como las complicaciones quirúrgicas, rupturas emocionales y pérdidas de trabajo. Los factores que predicen la mejoría posquirúrgica incluyen: edad más temprana, diagnóstico certero de la entidad, buen funcionamiento social y psíquico previo a la intervención quirúrgica y presencia de apoyo social.
EtiologíaLa identidad de género (sentimiento de ser un hombre o una mujer) evoluciona gradualmente durante la infancia y la juventud. Este proceso de aprendizaje cognitivo y afectivo ocurre en interacción con los familiares, compañeros y el entorno, desconociéndose cuándo cristaliza la identidad de género o qué factores contribuyen al desarrollo de una identidad de género atípica12,13. Los estudios genéticos sobre trastornos del comportamiento en la infancia sugieren un componente hereditario14, sin embargo, salvo la disforia de género que se presenta como secundaria a ciertos trastornos de la diferenciación sexual, no hay información clara sobre la etiopatogenia de las alteraciones de identidad sexual en la infancia y, dado que en la mayoría de los niños la disforia no persiste durante la adolescencia y la edad adulta, estos datos no son extrapolables a los de adultos. No existe un conocimiento adecuado acerca de los efectos de los esteroides sexuales en el desarrollo y funcionamiento cerebral, que identifique las bases biológicas de la formación de la identidad de género en humanos14–16. En resumen, ni los estudios biológicos, ni los psicológicos proporcionan una explicación satisfactoria de la aparición de esta situación en estas edades.
Calidad asistencialDisponibilidad, accesibilidad, recursosLa Unidad de DIG debe ser competente y eficiente, accesible a una región geográfica determinada o a una distancia de viaje prudencial, que permita una adecuada adherencia al proceso. El tiempo de espera, la vía de acceso y el protocolo a seguir debe ser comunicado a cada paciente según los estándares1,17, el diagnóstico y tratamiento se debería llevar a cabo en unidades especializadas y con abordaje multidisciplinar (es decir, en el que participen todos los especialistas implicados en el proceso, con proximidad física entre sus miembros y reflexionando en torno a sesiones clínicas sobre los casos en estudio y seguimiento). Siendo a su vez importante la implicación en el proceso asistencial de los especialistas en medicina familiar y comunitaria y salud mental del área mediante el desarrollo de actividades formativas.
Paciente y flexibilidadLos profesionales deben respetar en todo momento la autonomía del paciente en la toma de decisiones en cualquier estadio del proceso. El tratamiento debería estar centrado en el paciente individual, reconociendo las preferencias, necesidades y circunstancias individuales. El tratamiento no debe ser prescrito sin más, sino que se deberían ofertar al sujeto distintas opciones apropiadas para él, informar de los beneficios y riesgos para su salud, acordando la progresión del mismo y la secuencia temporal dentro de unos estándares establecidos. Para ello es fundamental el consentimiento informado en cada uno de los pasos del proceso. En caso de desacuerdo entre el facultativo y el sujeto, el paciente tendrá derecho a una segunda opinión independiente de otro especialista que trabaje en esta área.
Protocolo de actuación clínicaEn la evaluación de las personas afectas de las alteraciones de la identidad de género es aconsejable seguir los estándares internacionales de la Asociación Internacional Harry Benjamin (HBIGDA) (actualmente llamada World Professional Association for Transgender Health WPATH)1, y The Endocrine Society16, estas recomendaciones articulan los parámetros y las instrucciones, en forma de consenso internacional, para el diagnóstico y tratamiento de las DIG. Este tratamiento, como ya ha sido comentado previamente, se debería llevar a cabo en unidades especializadas y con abordaje multidisciplinar2. Dentro de estos equipos multidisciplinares son los especialistas en salud mental (psicólogos o psiquiatras) los encargados de confirmar el diagnóstico inicial y de llevar a cabo la tarea psicoterapéutica en el seguimiento del proceso de reasignación sexual (PRS). El paciente desarrolla el tratamiento en 3 fases conocidas como tríada terapéutica que incluye: 1) el diagnóstico y experiencia de vida real, 2) el tratamiento hormonal cruzado, y 3) las cirugías de reasignación sexual.
Diagnóstico y experiencia de vida realEvaluación inicial. Psicoterapia y soporte terapéuticoNo todas las personas que solicitan reasignación de sexo son transexuales18. No es infrecuente confundir transexualidad con otras formas de trastornos de la identidad de género y otras situaciones que no son subsidiarias de tratamiento hormonal o quirúrgico. La evaluación diagnóstica es un proceso prolongado y complejo que debe ser controlado de manera rigurosa, y que se debe realizar de forma extensiva y utilizando todo el tiempo que sea necesario2,18–21. La DIG puede ir acompañada de problemas psicológicos o psiquiátricos22–24. Será responsabilidad del profesional de salud mental (PSM) el diagnóstico de la DIG. Esta fase inicial se continuará, a lo largo del proceso de cambio de sexo, con evaluación periódica del caso, psicoterapia y terapia familiar si se considera necesaria y coordinación con el resto del equipo (endocrinólogos y cirujanos). La evaluación diagnóstica precisa de un mínimo de 4-6 meses, durante el que se mantendrá un contacto regular con el profesional. Es necesario realizar un adecuado diagnóstico diferencial, ya que la falta de certeza en esta fase está asociada a un incremento del arrepentimiento tras la realización del tratamiento de reasignación sexual y es un factor predictivo negativo de la evolución posterior10,25.
Experiencia de la vida realUna vez realizados el diagnóstico de certeza, y si el paciente aún no ha iniciado la experiencia de la vida real (EVR), se le sugiere la conveniencia de empezarlo en los diferentes ambientes sociales donde se relacione, salvo en situaciones claramente difíciles u hostiles. La EVR significa que la persona viva, trabaje y se relacione en todas las actividades de su vida, de acuerdo al sexo deseado y durante el mayor tiempo posible.
Previo a cualquier procedimiento quirúrgico de reasignación de sexo el PSM debe reevaluar la situación, lo que permite confirmar el diagnóstico de DIG y que se ha completado con éxito la EVR. En el caso de la mastectomía en TMH no es necesario cumplir los 12-24 meses de terapia hormonal para la indicación de la cirugía, dado que la presencia de las mamas puede hacer inviable la progresión de la EVR, pero sí es imprescindible el diagnóstico confirmado y el inicio de terapia hormonal cruzada al menos 6 meses antes.
Valoración endocrinológica e intervención hormonalEvaluación inicialHistoria clínica completa, hábitos de vida, antecedentes familiares de neoplasias, enfermedad cardiovascular precoz y fenómenos trombóticos, intervenciones quirúrgicas. Desarrollo puberal e historia sobre función gonadal. Empleo de THC previo (nombre, dosis del fármaco y duración del tratamiento) y si existiesen se aportarán estudios analíticos complementarios previos al inicio de dicha terapia. Se reflejan también en esta parte de la historia los resultados clínicos obtenidos y el grado de satisfacción conseguido. Métodos empleados para eliminar caracteres sexuales secundarios: depilación, electrolisis, plastias, etc2.
Durante la entrevista se observa el lenguaje autorreferencial empleado por el paciente y se refleja también la situación sociolaboral y el apoyo familiar y social así como datos sobre el test de vida real y las estrategias de la persona para su adaptación a la situación.
Es necesario investigar en el interrogatorio la posibilidad de que estos pacientes presenten un cuadro de transexualismo secundario en el curso de una hiperplasia suprarrenal congénita, tumor virilizante, resistencia androgénica, cromosomopatía, agenesia testicular o hipogonadismo de cualquier tipo que pudiera haber condicionado su DIG2. Aunque estas situaciones no son habituales obligan a un enfoque diferente desde el punto de vista diagnóstico y terapéutico26.
Exploración física, caracteres sexuales secundarios (estadios de Tanner), exploración mamaria, genital (incluyendo volumen testicular y longitud peneana), antropometría y cifras de presión arterial. Auscultación cardiopulmonar. Exploración abdominal. Signos de insuficiencia venosa crónica. Índice cintura/cadera y bioimpedanciometría, siempre que sea posible.
El objetivo de las exploraciones complementarias es descartar la presencia de alteraciones hormonales o cromosómicas que puedan condicionar algún tipo de trastorno conductual, así como otros procesos asociados que contraindiquen o condicionen la terapia hormonal. Se recomienda la realización de un análisis de bioquímica general, perfil hepático, perfil lipídico completo, ácido úrico, antígeno específico de la próstata, hemograma, cariotipo, estudio hormonal basal (tabla 2). En caso de toma no supervisada de hormonas sexuales se intentará proceder a un periodo de lavado de al menos un mes (dependiendo del preparado empleado), previo a la realización de las exploraciones complementarias27.
Valoración inicial y monitorización de la terapia hormonal en adultos con discordancia entre la identidad de género y el sexo biológico (29)
| Determinaciones comunes | THM | TMH |
| Estudio inicialAnamnesisExploración: caracteres sexuales secundarios, somatometría, tensión arterial, exploración mamaria.Analítica: bioquímica completa, perfil lipídico (LDLc, HDLc, TG), ácido úrico, función hepática.CariotipoHormonas basales: FSH, LH, E2, Testosterona SHBG, DHEA-S, 17OH-progesterona, PRL, TSH.Serologías: VHB, VHC, VIH y LúesHemograma y coagulaciónEstudio de hipercoagulabilidad | PSA.Hormonas basales: prolactinaExploración completa | Hormonas basales: DHEA, androstenediona, 17OH-ProgesteronaExploración completa |
| Visita trimestral-semestralEventos adversos.Somatometría, tensión arterial.Bioquímica completa, perfil lipídico (LDLc, HDLc, TG), función hepática, hemograma, Hormonas Basales: FSH, LH, E2, Testosterona, SHBG | Prolactina (visita sexto mes). | |
| Visita anualSomatometría, tensión arterial.Bioquímica completa, perfil lipídico (LDLc, HDLc, TG), a.úrico, función hepática, hemograma, Hormonas Basales: FSH, LH, E2, testosterona, SHBG.Coagulación básicaSerologías: VHB, VHC, VIH y Lúes | PSA, prolactina. Exploración mamaria, testicular (hasta CRS) | Exploración mamaria (hasta CRS)Revisión ginecológica, ecografía pélvica, citología (hasta CRS) |
| Otras determinacionesDensitometría osea (DEXA). Si factores de riesgo, incumplimiento terapéutico tras gonadectomía o en mayores de 60 añosRadiografía de tórax inicial y electrocardiograma (anual-bianual) | Despistaje rutinario de cáncer de mama para mujer biológica, cáncer de próstata y colon para varón biológico | Síntomas compatibles con SAOS (escala Epworth) |
DEXA: Dual energy X-ray absorptiometry; E2: estradiol; TT: testoterona total; PSA: antígeno prostático específico; CRS: cirugía reasignación desexo; SAOS: síndrome de apnea obstructiva del sueño; THM: transexual hombre a mujer; TMH: transexual mujer a hombre.
(29) Modificado de: Moreno-Pérez O. Transexualidad: control del tratamiento, en Función androgénica en el laboratorio. Editado por: Comité de Comunicación de la Sociedad Española de Bioquímica Clínica y Patología Molecular, 2010 (ISBN: 84-89975-40-X).
La prevalencia de seropositividad para VIH en un metaanálisis reciente, con una prevalencia del 27,7% en THM en determinadas poblaciones, hace recomendable descartar el VIH en estos pacientes28; la prevalencia de seropositividad para VIH es baja en TMH. La evaluación periódica de VHB, VHC y sífilis, es recomendable.
Pese a que las guías clínicas disponibles1,17 no se pronuncian acerca de la necesidad de realizar estudios de hipercoagulabilidad antes de iniciar el tratamiento hormonal, en opinión de los autores, el riesgo aumentado de fenómenos tromboembólicos en THM bajo tratamiento estrogénico y la accesibilidad de la técnica en los centros hospitalarios, hace aconsejable este estudio para que el paciente realice un adecuado consentimiento informado, asumiendo el posible incremento de riesgo o incluso beneficiándose de los tratamientos profilácticos si estuviesen indicados, antes del inicio de la terapia hormonal cruzada29,30.
Contraindicaciones a la terapia hormonalTHM-estrógenos: enfermedad tromboembólica, cardiopatía isquémica, accidente cerebrovascular, hepatopatía activa (transaminasas más de 3 veces límite superior normalidad), insuficiencia renal, hipertrigliceridemia grave, obesidad mórbida, diabetes mal controlada, migrañas graves, historia familiar de cáncer de mama, prolactinoma.
TMH-andrógenos: hepatopatía activa, insuficiencia renal, cardiopatia isquémica, hipertrigliceridemia grave, obesidad mórbida, diabetes mellitus mal controlada17,30,31.
Criterios de elegibilidadSon los criterios específicos mínimos que deben documentarse antes de iniciar el tratamiento; para la instauración de la terapia hormonal deben cumplirse los siguientes criterios1:
- 1.
Informe favorable de la evaluación diagnóstica del PSM según criterios DSM-IV o CIE-10.
- 2.
EVR documentada de al menos 3 meses o desarrollar un periodo de psicoterapia especificado por el profesional de salud mental del equipo después de la evaluación inicial (normalmente un mínimo de 3 meses).
- 3.
Conocimiento por parte del paciente de las distintas opciones terapéuticas con sus beneficios (expectativas reales) y riesgos para la salud, elección de la más apropiada, compromiso del paciente a realizar el seguimiento psicológico-endocrinológico establecido.
Otros criterios aplicables por cada unidad de disforia de género suelen ser: mayor de 18 años, o en su defecto mayor de 16 años y tener el consentimiento del tutor, no contraindicación a la terapia tras la revisión de las exploraciones complementarias solicitadas y firma de consentimiento informado.
Todos los pacientes deben de ser informados y aconsejados acerca de las opciones de fertilidad previa al inicio de la supresión hormonal en adolescentes o previo al tratamiento con hormonas sexuales del sexo deseado tanto en adolescentes como adultos2,17.
Se debe insistir antes de iniciar la terapia hormonal en el cese del hábito tabáquico, realizar ejercicio físico regular, dieta saludable y no consumir más de 14 unidades de bebida estándar de alcohol por semana.
Intervención hormonalLos 2 objetivos principales de la terapia hormonal son reducir la concentración de hormonas endógenas, y por tanto, las características sexuales secundarias del sexo biológico (genético), así como reemplazar estas por aquellas propias del sexo de identificación, empleando en principio terapia hormonal similar a la de los pacientes hipogonadales32,33. La desaparición total de estas características no es posible. En los THM no hay forma de revertir el desarrollo del esqueleto si se ha completado la maduración puberal, tampoco hay respuesta completa en la eliminación del vello facial, feminización de la voz ni siempre se consigue un desarrollo mamario del grado deseado; por el contrario la cirugía genital feminizante obtiene resultados adecuados estéticos y funcionales. En los TMH es más sencillo conseguir caracteres masculinos y sin embargo la genitoplastia masculinizante no logra por ahora resultados estéticos y funcionales totalmente satisfactorios2.
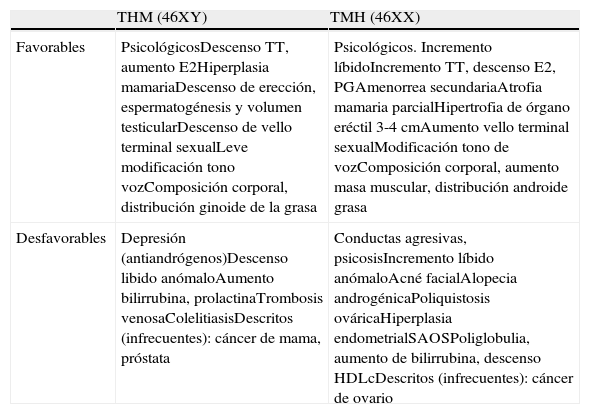
Los cambios físicos y psicológicos esperados con la terapia hormonal cruzada quedan recogidos en la tabla 317,29,34. El efecto máximo en determinados aspectos puede que no se manifieste hasta después de 2 o 3 años del tratamiento. La herencia influye en la respuesta de los tejidos diana a la terapia hormonal, con una gran variabilidad interindividual y no se puede superar su efecto administrando dosis suprafisiológicas.
Efectos favorables (deseados) y desfavorables de la terapia hormonal cruzada en adultos con discordancia entre la identidad de género y el sexo biológico (29)
| THM (46XY) | TMH (46XX) | |
| Favorables | PsicológicosDescenso TT, aumento E2Hiperplasia mamariaDescenso de erección, espermatogénesis y volumen testicularDescenso de vello terminal sexualLeve modificación tono vozComposición corporal, distribución ginoide de la grasa | Psicológicos. Incremento líbidoIncremento TT, descenso E2, PGAmenorrea secundariaAtrofia mamaria parcialHipertrofia de órgano eréctil 3-4cmAumento vello terminal sexualModificación tono de vozComposición corporal, aumento masa muscular, distribución androide grasa |
| Desfavorables | Depresión (antiandrógenos)Descenso libido anómaloAumento bilirrubina, prolactinaTrombosis venosaColelitiasisDescritos (infrecuentes): cáncer de mama, próstata | Conductas agresivas, psicosisIncremento líbido anómaloAcné facialAlopecia androgénicaPoliquistosis ováricaHiperplasia endometrialSAOSPoliglobulia, aumento de bilirrubina, descenso HDLcDescritos (infrecuentes): cáncer de ovario |
CRS: Cirugías de reasignación sexual; síndrome de apnea obstructiva del sueño;
THM; transexual hombre a mujer; TMH: transexual mujer a hombre.
La mayoría de los efectos favorables se inician entre 3 y 6 meses del inicio de la terapia, con efecto máximo entre 2 y 5 años.
Estos tratamientos deben ser indicados y monitorizados por un endocrinólogo con experiencia en el manejo de esteroides sexuales. La elección del preparado hormonal, método de liberación y dosificación, debe ajustarse al principio de mínimo riesgo para la salud y máxima eficacia.
En el anexo B se aportan documentos de información para los pacientes empleados en 2 centros nacionales. Es importante explicar verbalmente y por escrito las modificaciones corporales que se van a producir con la utilización del tratamiento hormonal.
El paciente y el endocrinólogo responsable firmarán en esta fase el consentimiento informado en el que quede reflejado no solo los posibles efectos secundarios de la terapia sino el compromiso a cumplir los plazos terapéuticos fijados y a asumir indicaciones y contraindicaciones2.
Tratamiento hormonal cruzado en transexuales THM
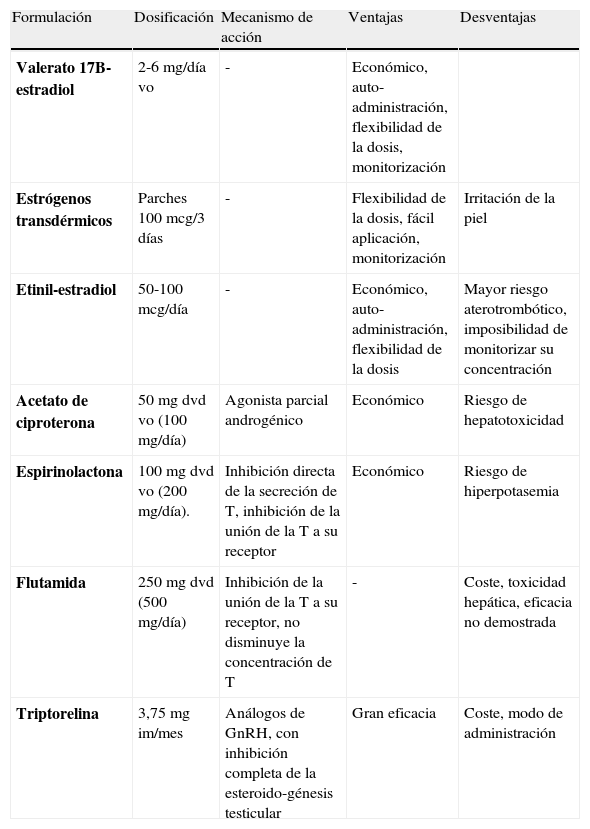
El régimen terapéutico en las mujeres transexuales (THM) es más complejo que en los TMH. La combinación de compuestos que suprimen la producción endógena de andrógenos o su acción, junto con la administración de estrógenos es la terapia más eficaz (tabla 4)11,29,35. El objetivo es eliminar el crecimiento del vello sexual, inducir la formación de mamas y una distribución femenina de la grasa corporal.
Farmacología clínica y monitorización del tratamiento hormonal cruzado en THM (29)
| Formulación | Dosificación | Mecanismo de acción | Ventajas | Desventajas |
| Valerato 17B-estradiol | 2-6mg/día vo | - | Económico, auto-administración, flexibilidad de la dosis, monitorización | |
| Estrógenos transdérmicos | Parches 100 mcg/3 días | - | Flexibilidad de la dosis, fácil aplicación, monitorización | Irritación de la piel |
| Etinil-estradiol | 50-100 mcg/día | - | Económico, auto-administración, flexibilidad de la dosis | Mayor riesgo aterotrombótico, imposibilidad de monitorizar su concentración |
| Acetato de ciproterona | 50mg dvd vo (100mg/día) | Agonista parcial androgénico | Económico | Riesgo de hepatotoxicidad |
| Espirinolactona | 100mg dvd vo (200mg/día). | Inhibición directa de la secreción de T, inhibición de la unión de la T a su receptor | Económico | Riesgo de hiperpotasemia |
| Flutamida | 250mg dvd (500mg/día) | Inhibición de la unión de la T a su receptor, no disminuye la concentración de T | - | Coste, toxicidad hepática, eficacia no demostrada |
| Triptorelina | 3,75mg im/mes | Análogos de GnRH, con inhibición completa de la esteroido-génesis testicular | Gran eficacia | Coste, modo de administración |
Objetivo terapéutico. Las concentraciones de estradiol deberían mantenerse en los valores medios normales de una mujer premenopáusica (200pg/mL) o en el límite superior de la fase folicular normal para cada laboratorio de referencia, junto unas concentraciones de T en los límites femeninos (< 0,8ng/mL)
Monitorización. Determinación de E2, cada 3 meses (1.er año), luego semestral-anual. El momento de la determinación de la misma dependerá del preparado de E2 empleado: a las 24 horas de la última dosis de estrógeno vo o a las 48 horas de la aplicación del estrógeno trandérmico
DHT: dihidrotestosterona; dvd, 2 veces al día; E2: estradiol; im: intramuscular; s, semana; T: testosterona; THM: transexual hombre a mujer; vo, vía oral.
Los estrógenos son aconsejables vía oral (estrógenos conjugados o valerato de estradiol) o como estrógenos transdérmicos. El empleo de estrógenos transdérmicos y estrógenos no sintéticos vo, va a permitir monitorizar sus concentraciones. Las concentraciones de estradiol deberían mantenerse en los valores medios normales de una mujer premenopáusica o en el límite superior de la fase folicular normal para cada laboratorio de referencia (estradiol 100pg/mL determinado por radioinmunoanálisis), junto a unas concentraciones de testosterona total en los límites femeninos (inferior a 0,5-0,8ng/mL por inmunoanálisis de quimioluminiscencia).
Preparados estrogénicos actuales: de elección el valerato estradiol o estrógenos transdérmicos. Valerato de 17β-estradiol vo (2-6mg/día); Estrógenos transdérmicos (100μg/3-7 días). El uso de estrógenos transdérmicos podría conferir una ventaja en THM de mayor edad, los cuales presentan un mayor riesgo de enfermedad tromboembólica29.
Los estrógenos equinos conjugados son más difíciles de monitorizar y el etinilestradiol no debería emplearse por presentar un mayor riesgo aterotrombótico17,29–31.
La supresión de la secreción o acción de los andrógenos se basa en compuestos con efecto antiandrogénico y análogos de la hormona liberadora de gonadotropinas (GnRH)32. El acetato de ciproterona (Androcur® 50mg), de elección, es un esteroide sintético con efecto doble, bloqueador del receptor androgénico e inhibidor de la secreción gonadotropa29. La posología habitual es de 50mg 2 veces al día, aunque la dosis y duración del tratamiento debe ser ajustada dependiendo del grado de impregnación androgénica de cada paciente y sobre todo de la edad de comienzo del tratamiento. Aunque infrecuente, hay casos que sin antiandrogenización y solo con el tratamiento estrogénico consiguen una buena feminización y disminución de las erecciones a lo largo del seguimiento2. Como efecto secundario es habitual cierto incremento ponderal y retención hídrica moderada debida al propio fármaco y potenciada por la asociación de estrógenos. Se ha descrito hepatotoxicidad y dificultad de visión nocturna33,34.
La espironolactona (Aldactone® 100) es un diurético con propiedades antiandrogénicas, al inhibir directamente la secreción de testosterona y su unión con el receptor androgénico32; a dosis de 200mg/día. No es de uso habitual. Otros antiandrógenos disponibles son la flutamida y el finasteride, que impiden la acción final de la testosterona, pero no disminuyen sus concentraciones, su eficacia no ha sido demostrada.
El empleo de análogos de GnRH (Decapeptyl ®) por su elevado coste y la falta de aprobación con esta indicación en nuestro medio, debe reservarse como uso compasivo para DIG en adolescentes por conllevar una gonadectomía química reversible y para aquellos pacientes refractarios a preparados antiandrogénicos2,32.
Tras la gonadectomía no será necesaria la terapia antiandrogénica
El uso de progestágenos es controvertido y en principio se desaconseja su uso, dado que pueden aumentar los riesgos tromboembólicos, alteraciones hepáticas, hipertensión arterial, cambios de humor y potenciar el resto de efectos negativos posibles del tratamiento estrogénico. Podrían ser utilizados en caso de requerir una disminución en la dosis de estrógenos o presentar intolerancia a estos2. En estos casos se recomendaría medroxiprogesterona a dosis de 2,5 a 10mg/día (presentación en comprimidos de 5-10mg) o noretisterona a la misma dosis (presentación en comprimidos de 5-10mg).
El tratamiento estrogénico ha de mantenerse tras la cirugía genital a dosis adecuadas para evitar clínica de hipogonadismo y pérdida de masa ósea1.
Tratamiento hormonal cruzado en transexuales TMH
El objetivo en los hombres transexuales es detener la menstruación e inducir virilización, incluyendo un patrón de vello sexual y un morfotipo masculino e hipertrofia del órgano eréctil. El tratamiento hormonal también conlleva un aumento en la masa muscular, un descenso de la masa grasa y un incremento de la libido.
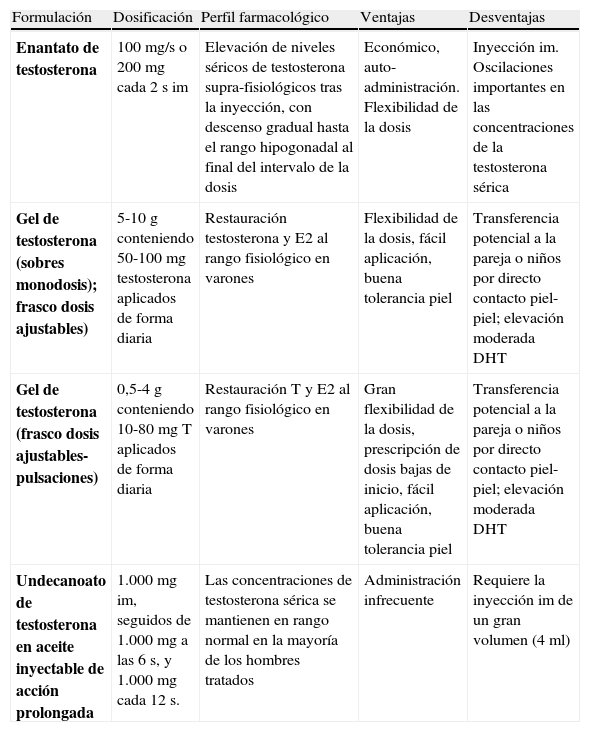
Los preparados androgénicos más frecuentemente empleados35 (tabla 5), son los ésteres de testosterona administrados de forma intramuscular o en gel de aplicación tópica (los parches aunque aconsejados no están actualmente disponibles en el mercado español). El objetivo será mantener las concentraciones de testosterona total dentro de los valores de referencia para la población masculina (320-1.000ng/dL). El momento oportuno para la determinación de las concentraciones de testosterona, dependerán del preparado (tabla 5). El efecto virilizador de los andrógenos y su capacidad de inhibición de las gonadotrofinas permite el no tener que utilizar de forma obligada fármacos antigonadotrópicos para el cese de las menstruaciones. Salvo en casos aislados se logra amenorrea tras 2-3 meses de tratamiento androgénico, en muy raras ocasiones hay que recurrir a utilizar análogos de GnRH o progestágenos si persiste el periodo menstrual.
Farmacología clínica y monitorización del tratamiento hormonal cruzado en TMH (29)
| Formulación | Dosificación | Perfil farmacológico | Ventajas | Desventajas |
| Enantato de testosterona | 100mg/s o 200mg cada 2 s im | Elevación de niveles séricos de testosterona supra-fisiológicos tras la inyección, con descenso gradual hasta el rango hipogonadal al final del intervalo de la dosis | Económico, auto-administración. Flexibilidad de la dosis | Inyección im. Oscilaciones importantes en las concentraciones de la testosterona sérica |
| Gel de testosterona (sobres monodosis); frasco dosis ajustables) | 5-10g conteniendo 50-100mg testosterona aplicados de forma diaria | Restauración testosterona y E2 al rango fisiológico en varones | Flexibilidad de la dosis, fácil aplicación, buena tolerancia piel | Transferencia potencial a la pareja o niños por directo contacto piel-piel; elevación moderada DHT |
| Gel de testosterona (frasco dosis ajustables-pulsaciones) | 0,5-4g conteniendo 10-80mgT aplicados de forma diaria | Restauración T y E2 al rango fisiológico en varones | Gran flexibilidad de la dosis, prescripción de dosis bajas de inicio, fácil aplicación, buena tolerancia piel | Transferencia potencial a la pareja o niños por directo contacto piel-piel; elevación moderada DHT |
| Undecanoato de testosterona en aceite inyectable de acción prolongada | 1.000mg im, seguidos de 1.000mg a las 6 s, y 1.000mg cada 12 s. | Las concentraciones de testosterona sérica se mantienen en rango normal en la mayoría de los hombres tratados | Administración infrecuente | Requiere la inyección im de un gran volumen (4ml) |
Monitorización. Determinación de testosterona total, cada 3 meses (primer año), luego semestral-anual. El momento de la determinación de la misma dependerá del preparado de testosterona empleado: enantato de testosterona im medición a mitad de camino entre inyecciones, gel de T en cualquier momento tras haber recibido al menos una semana de terapia, undecanoato de testosterona im de acción prolongada justo antes de la siguiente inyección
Objetivo terapéutico. Mantener testosterona 3-10ng/ml (rango medio de la normalidad para varón biológico según laboratorio de referencia). Estradiol2<50pg/ml (límite superior de la normalidad para varón biológico según laboratorio de referencia)
DHT: dihidrotestosterona; im: intramuscular; s: semana;TMH, transexual mujer a hombre.
El tratamiento androgénico ha de mantenerse tras la cirugía genital a dosis adecuadas para evitar sofocos y pérdida de masa ósea2.
Eventos adversos y seguridad del tratamiento hormonal cruzado
La terapia hormonal cruzada a priori presenta los mismos riesgos que la terapia hormonal sustitutiva en pacientes hipogonadales, si bien el empleo de dosis supra-fisiológicas que se requiere en muchas ocasiones puede conllevar un mayor riesgo de complicaciones2,11,34. Es más probable que los pacientes con problemas médicos o con riesgo elevado de enfermedades cardiovasculares experimenten efectos serios o fatales del tratamiento con hormonas del sexo opuesto. Los riesgos y efectos secundarios de tratamiento hormonal pueden aumentarse a causa de tabaquismo, obesidad, vejez, cardiopatías, hipertensión, anomalías de coagulación, malignidades y algunas anormalidades endocrinológicas. El paciente y el médico deben considerar juntos el balance entre beneficios y riesgos. Los eventos adversos potenciales quedan recogidos en la tabla 3.
Densidad mineral ósea. Una adecuada dosificación del tratamiento hormonal es importante para el mantenimiento de la masa ósea en las personas transexuales. No existe mucha información en la literatura acerca del riesgo de fractura en estos pacientes, pero la suspensión del tratamiento supervisado tras la gonadectomía, es un factor de riesgo para la aparición de osteoporosis. En los TMH el efecto protector de la testosterona parece mediado por la conversión periférica a estradiol, mientras que en THM los estrógenos exógenos preservan la densidad mineral ósea36,37.
Enfermedad cardiovascular. Hay escasa información bibliográfica, a plazo medio-largo, sobre la repercusión de la terapia hormonal cruzada en la enfermedad cardiovascular11. Algunas observaciones publicadas refieren que la deprivación androgénica, junto al ambiente estrogénico, en THM asocia mayores efectos deletéreos, que la inducción de un medio androgénico en los TMH9, sin embargo la UTIG de Andalucía está objetivando un incremento de síndrome metabólico, con el paso del tiempo, especialmente en el grupo de TMH38. Para reducir el riesgo de síndrome metabólico y enfermedad cardiovascular, se deben potenciar medidas higiénico-dietéticas saludables en estos pacientes.
Riesgo de neoplasias. Existen pocos casos descritos de cáncer hormonodependiente en pacientes con DIG, sin embargo la probabilidad de aparición se incrementa con la duración de la exposición de la terapia cruzada y la edad de este colectivo33,39. Existen pocos casos reportados en la literatura de la aparición de cáncer de mama en THM. Los estudios en población general sugieren que la terapia estrogénica a medio plazo (20-30 años) no incrementa el riesgo de cáncer de mama40,41, no obstante es necesaria la realización de exámenes físicos regulares por parte de la paciente y el clínico. El cáncer de próstata es infrecuente antes de los 40 años, y aunque no parece existir un mayor riesgo de desarrollar patología prostática en THM, la existencia de casos aislados en la literatura de hipertrofia benigna de próstata y 3 casos de cáncer de próstata en THM con inicio de la terapia a partir de los 50 años, hacen obligatorio la determinación de PSA y valorar según este un examen digital rectal en THM de avanzada edad, con tratamiento hormonal cruzado tardío o intermitente17. En los TMH cuando se retrasa la histerectomía, existe riesgo potencial de cáncer de endometrio, lo que justificaría la revisión ginecológica anual33,39,40, sugerencia no siempre bien aceptada por los pacientes.
Seguimiento clínico-analíticoEl seguimiento endocrinológico será más exhaustivo durante el primer año de terapia hormonal, pudiéndose espaciar tras la reasignación quirúrgica. En la tabla 2 queda reflejada una monitorización estándar para estos pacientes. De forma inicial los pacientes serán evaluados cada 3-4 meses el primer año y posteriormente con carácter semestral de por vida. Es necesaria la monitorización del peso, presión arterial, hemograma, función renal y hepática, metabolismo de la glucosa, ácido úrico y perfil graso. La monitorización periódica (cada 2-3 años) de la densidad mineral ósea, es necesaria tras la gonadectomía realizada en la genitoplastia a THM o tras la histerooforectomía en TMH. Durante la fase de tratamiento médico es también el momento de ir evaluando la satisfacción o no por los cambios físicos experimentados, siendo este un requisito o condición obligada para ratificar la situación de transexualidad2. En las fases iniciales las modificaciones fisonómicas y funcionales son reversibles total o parcialmente, no así cuando el tratamiento ha sido utilizado largo tiempo.
Transexual hombre mujerEl objetivo es mantener las concentraciones de estrógenos y andrógenos en los límites fisiológicos de una mujer biológica, para evitar la aparición de fenómenos tromboembólicos, disfunción hepática o hipertensión arterial. Hasta el 20% de mujeres transexuales experimentan elevaciones en la cifras de prolactina, asociados o no con agrandamiento de la glándula hipofisaria42,43, por el estímulo crónico de la terapia con estrógenos en las células lactotropas o por interferencia directa con el factor inhibidor de la prolactina44,45. Dado que los síntomas asociados a esta elevación no serán valorables en THM (hipogonadismo, ginecomastia), es fundamental la monitorización de su concentración plasmática. La reducción de dosis o suspensión de los estrógenos suele ser suficiente para la resolución del proceso.
Como hemos comentado, existe evidencia limitada acerca del posible beneficio o riesgo cardiovascular asociado a la terapia estrogénica en THM46. Los cambios favorables en el perfil lipídico, con aumento del colesterol HDL y descenso del colesterol LDL, parecen verse contrarrestados por el aumento ponderal, tensión arterial y cambios en la homeostasis de la insulina38,47. Es necesario por tanto un evaluación continua del riesgo cardiovascular en estos pacientes.
Se sugiere que los THM en tratamiento con estrógenos sigan las guías clínicas de enfermedad prostática y cáncer de próstata recomendadas para un varón biológico, así como las de despistaje de cáncer de mama para una mujer biológica17,33,34.
Transexual mujer hombreEl objetivo es mantener la testosterona en los límites fisiológicos de un varón biológico evitando la aparición de los eventos adversos asociados a la terapia crónica con andrógenos35, fundamentalmente la aparición de eritrocitosis, disfunción hepática, hipertensión, ganancia ponderal excesiva, cambios lipídicos, aparición de acné grave y alteraciones psicológicas17,30,34,46. Las concentraciones de LH podrían servir en fase pregonadectomía como indicador de la idoneidad de la administración de esteroides sexuales para preservar la masa ósea17,36,37.
No existe evidencia concluyente a favor de un menor o mayor riesgo cardiovascular asociado a la terapia androgénica a dosis fisiológicas en TMH48. No parecen comparables los datos aplicados a población general, donde se ha objetivado una relación inversa entre las concentraciones de testosterona endógena y la mortalidad49,50, con los cambios inducidos por la hiperandrogenización en estos pacientes. La testosterona influye en la distribución de la grasa corporal mediada por la expresión de receptores de esteroides sexuales específicos en tejido adiposo, y por el metabolismo local de las hormonas esteroideas51. A nivel celular, los andrógenos actúan sobre los adipocitos, estimulando la lipolisis, reduciendo los depósitos grasos. Sin embargo, la administración de testosterona en TMH suele conllevar un perfil lipídico más aterogénico, con descenso del colesterol HDL y aumento de los triglicéridos2,52. La repercusión en la homeostasis de la insulina de los TMH es controvertida38,47. El aumento en la masa muscular asociado a los andrógenos podría tener efectos beneficiosos, dado que el músculo esquelético es el lugar principal de captación de glucosa bajo condiciones de estímulo insulínico, captando hasta el 75% de la glucosa disponible en el periodo posprandial52.
Si bien son necesarios nuevos estudios que evalúen el riesgo cardiovascular en TMH, estos datos justifican la necesidad de evaluación continua de dichos factores de riesgo en estos pacientes.
Se sugiere también evaluar el metabolismo del ácido úrico ya que sufre modificaciones importantes, tanto en TMH como en THM, con el THC53.
En TMH es necesaria una revisión ginecológica anual hasta histerectomía y doble anexectomía, por el riesgo potencial de neoplasias.
En ambos grupos de pacientes, tras un período de al menos 2 años de tratamiento hormonal (para lograr la mejor respuesta tisular a los estrógenos o andrógenos) y, con adherencia constatada al protocolo de seguimiento psicológico y endocrinológico, los pacientes pueden ya solicitar cambio de documentación registral de acuerdo a la reciente Ley BOE 3/2007, 15 de marzo.
No está bien definida en estos pacientes la edad máxima de mantenimiento del tratamiento hormonal cruzado. No hay series descritas de personas transexuales de edad avanzada en seguimiento. Se recomendaría seguimiento prospectivo estricto con control de factores de riesgo cardiovasculares y de tumores dependientes de esteroides sexuales, sin olvidar la evaluación de la masa ósea.
Actitud ante la disforia de género en niños y adolescentesAl igual que en los adultos la evaluación diagnóstica de la identidad sexual y de la salud mental a esta edad es fundamental. La terapia sexológica y psicoterapia estará dirigida a resolver cualquier comorbilidad existente y a reducir el malestar que el paciente experimente en relación a su problema de identidad sexual. Es necesario un tratamiento conservador dado que la identidad sexual puede sufrir variaciones inesperadas en esta edad6,54–57, por lo que no se debe influir de forma directa en el rol de género, ni iniciar tratamiento hormonal en niños prepuberales. La experimentación por parte de los individuos de los primeros cambios en relación a su pubertad espontánea es trascendental, dado que su forma de interpretar los primeros cambios físicos posee valor diagnóstico.
Los criterios de elegibilidad para el inicio de cualquier intervención hormonal son superponibles a los del adulto, pero con requerimientos adicionales en adolescentes: es necesario alcanzar un estadio Tanner 2 de desarrollo puberal, así como un soporte psicológico y social adecuado. Esto va a condicionar el desarrollo de psicoterapia familiar y orientación a los padres para afrontar la toma de decisiones.
Si se confirmara la permanencia de la disforia la intervención médica, de forma precoz mediante la supresión del eje gonadal en los estadios iniciales del desarrollo puberal en pacientes con DIG, podría prevenir el daño psicológico asociado al desarrollo de los caracteres sexuales secundarios propios de su sexo biológico, conllevando una adaptación psicosocial más adecuada y mejores resultados físicos17. Esta intervención es reversible, permitiendo en el futuro el desarrollo puberal del sexo biológico si fuese necesario.
Esta intervención precoz va a requerir un seguimiento estrecho por parte de endocrinólogo, no será recomendado ningún tratamiento sin haber alcanzado el estadio 2 de Tanner y si se prescribe, se hará con análogos de GnRH (Decapeptyl 11,25mg® IM/12 semanas). Las características sexuales en estadios iniciales puberales regresarán, mientras que la instauración en estadios más avanzados conllevara su detención, con atrofia parcial de la mama y ausencia de menstruación en las niñas y paro de la virilización y descenso del volumen testicular y peneano en niños58. Es necesaria la monitorización de las gonadotropinas y de las concentraciones de esteroides sexuales, para confirmar la correcta supresión del eje gonadal y acortar el intervalo terapéutico si fuese necesario. En cuanto a los eventos adversos potenciales, aunque se produce una detención inicial de la mineralización ósea no existen datos concluyentes acerca de la posible repercusión de esta inducción de «pubertad retrasada» en la densidad mineral ósea adulta de estos pacientes.
Otras alternativas como el empleo de progestágenos, antiestrógenos o antiandrógenos, son menos eficaces y presentan más eventos adversos17,58.
La asociación de THC en adolescentes se iniciará a partir de los 16 años induciendo una pubertad del sexo deseado con una titulación progresiva del tratamiento, superponible a la de otros individuos adolescentes hipogonadales:
Transexual THM 17β Estradiol, 5 mcg/kg/día con ascenso semestral durante 2 años hasta dosis adulta (2mg/día).
TMH, testosterona 25mg/m2/cada 2 semanas con ascenso semestral durante 2 años hasta dosis adulta (Testogel® 50mg/día cutáneo, Reandron ® 1g cada 12 semanas IM).
En la actualidad la tendencia es a mantener de forma prolongada el uso de análogos de GnRH, desde su inicio en estadio 2 de Tanner hasta los 18 años, asociando a los 16 años dosis progresivas de estrógenos o andrógenos y continuar directamente el proceso de reasignación de sexo con la genitoplastia al llegar a la mayoría de edad y tras al menos 1-2 años de THC59.
Otras terapiasTerapia del vello sexualEl tratamiento de reasignación sexual ya sea hormonal o quirúrgico, conlleva una reducción sustancial del crecimiento del vello sexual, aunque existe una variabilidad interindividual. En la actualidad solo existen 2 métodos depilatorios que son potencialmente permanentes, la electrodepilación y el láser. La electrodepilación (destrucción individual de cada folículo por energía térmica o electrolítica) es lenta y tediosa, requiere tratamientos de repetición durante meses o años, aunque se obtiene buenos resultados en manos expertas, es adecuada para áreas limitadas como el labio superior. La depilación por láser (absorción por la melanina de la energía lumínica con destrucción del folículo piloso), es más rápida porque permite tratar varios folículos a la vez, es más efectiva en el vello oscuro, pero es una técnica más cara y también requiere varias sesiones, no asegurando la permanencia.
Terapia del habla y lenguaje
Necesaria en ocasiones dado el efecto limitado en los cambios de voz en los THM y la respuesta variable en TMH. Puede ser impartida por un foniatra de forma individual o terapia grupal.
Cirugía de reasignación de sexoPara la mayoría de los pacientes con DIG la reasignación quirúrgica genital es un paso necesario para conseguir una vida plenamente satisfactoria en el rol del sexo de identificación. En los últimos años estas intervenciones han evolucionado, siendo la genitoplastia con preservación de la sensibilidad neurológica la técnica estándar. Se debe valorar cada caso de forma individual, para lo cual es necesario reevaluar al paciente, en fechas próximas a la cirugía, por una persona del equipo de psicología/psiquiatría que no conozca previamente el caso y ser comentado en sesión clínica por todos los miembros de la unidad (endocrinólogos, profesionales de salud mental, y los profesionales del campo de la cirugía involucrados en las intervenciones, urólogos, ginecólogos y cirujanos plásticos).
Criterios de disposición: son aquellos específicos que se fundamentan en la evaluación del clínico para continuar la secuencia terapéutica (en este caso para pasar a cirugía desde endocrinología)1,2:
- 1.
El paciente ha aumentado la consolidación de su identidad de género durante la experiencia de vida real o la psicoterapia.
- 2.
El paciente ha realizado progresos en el dominio de sus problemas de identidad que conducen a la mejora o continuidad de su estabilidad mental.
- 3.
Las hormonas son tomadas de forma responsable.
Los criterios de intervención serían:
- -
Ser mayor de 18 años; haber realizado la EVR con éxito, con participación responsable en la psicoterapia si fuese necesario, durante al menos 12 meses.
- -
Terapia hormonal supervisada durante al menos 12 meses.
- -
Conocimientos del tipo de intervención, irreversibilidad de la misma, tiempo de hospitalización, posibles complicaciones y rehabilitación, a través de consentimientos informados.
- -
Aprobación por el comité multidisciplinar.
- -
En caso de la presencia de contraindicaciones a la terapia hormonal podría indicarse la cirugía directa.
Cirugía genital para THM. Consiste en la penectomía, gonadectomía y creación de una neovagina a partir de la piel del pene, empleando la piel del escroto para la creación de los labios mayores, preservando el paquete neurovascular del glande como tejido para elaborar el clítoris60.
El tratamiento estrogénico en THM debe suspenderse entre 2 y 3 semanas previas a la intervención por el riesgo de trombosis venosa y reiniciar una vez que la paciente comience la deambulación.
Cirugía genital para TMH. La intervención quirúrgica genitoplástica es menos satisfactoria. La apariencia cosmética del neopene puede llegar a ser adecuada pero requiere múltiples intervenciones en manos experimentadas, y la erección del mismo solo puede obtenerse en contadas ocasiones mediante sistemas protésicos. La histerectomía más doble anexectomía es aconsejable no demorarla más de 2-3 años tras el inicio del tratamiento, dado que el uso prolongado de andrógenos se ha asociado a la aparición de neoplasia ovárica61. En la actualidad es habitualmente realizada vía laparoscópica. La genitoplastia masculinizante no debe realizarse antes de 2-3 años de tratamiento androgénico para objetivar la máxima hipertrofia del órgano eréctil sobre el que se aplicará con posterioridad la técnica de metaidoioplastia, salvo que el paciente y el cirujano del equipo opten por otras técnicas quirúrgicas2.
Cirugía mamaria. En THM, dado que el efecto estrogénico máximo sobre la glándula mamaria se objetiva a partir de 2 años del tratamiento estrogénico, no es hasta este momento cuando la paciente debe plantearse una mamoplastia de aumento. Puede realizarse antes o después de la cirugía genital. Sin embargo en TMH, la mastectomía debe indicarse de forma más precoz una vez iniciada la terapia hormonal y la EVR (6-12 meses después de estos pasos).
Circuito de prestación de servicios y derivación de pacientesCada unidad debe establecer su modelo de derivación de pacientes, en general se remiten desde el médico de atención primaria o profesional de salud mental del área pero no es infrecuente la demanda de información o asistencia directa por parte del propio paciente. La situación también dependerá de si el equipo es centro referencial del área sanitaria o incluso si la unidad acepta casos remitidos de otras comunidades autónomas.
Hay protocolos establecidos en los que la valoración del caso en primera visita se hace de forma conjunta por el equipo de psicólogos/psiquiatras y endocrinólogos, en otros equipos los profesionales de salud mental de la unidad atienden en primera instancia a los pacientes y en otros es el coordinador el que establece la secuencia de citación asociadas y tratamiento médico actual2,3,8.
Proyectos de investigaciónEs deseable el desarrollo de proyectos de investigación a nivel nacional en coordinación con las distintas UIG, con el objetivo de avanzar en el conocimiento de la entidad clínica y mejorar los cuidados y calidad de vida de estos pacientes. Algunas unidades han establecido ya protocolos de evaluación y recogida de datos de forma conjunta, fruto de ello han surgido diversas publicaciones recientes62–65.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Albero, Ramón (Aragón), Almaraz, María Cruz (Andalucía), Álvarez-Diz José Antonio (Asturias), Audí, Laura (Barcelona), Becerra, Antonio (Madrid), Castaño, Luis (País Vasco), Esteva, Isabel (Andalucía), Fernández Sánchez-Barbudo, Miguel (Canarias), Gómez-Balaguer, Marcelino (Comunidad Valenciana), Gómez-Gil, Esther (Cataluña), Hurtado Felipe (Comunidad Valenciana), López-Siguero, Juan Pedro (Andalucía), Martínez-Tudela, Juana (Andalucía), Moreno-Pérez, Óscar (Comunidad Valenciana), Sanisidro, Carmen (Aragón), Toni, Marta (Navarra), Vázquez-San Miguel, Federico (País Vasco) y Vidales Angelines (País Vasco).
Servicio de Endocrinología y Nutrición
Unidad de Transexualidad e Identidad de Género
Hospital Civil, Pabellón 7, 2.ª planta (PabellónC, HRU Carlos Haya). Málaga
Los siguientes efectos del tratamiento se producen de forma gradual y no siempre de forma idéntica en cada persona. Suele empezar a notarse su acción a partir de 2-4 meses de tratamiento, siendo algunos de sus efectos irreversibles tras 6-12 meses de uso. No se deben utilizar dosis altas de estrógenos, ya que sus resultados a plazo medio y largo son similares con dosis menores y también son menores los efectos secundarios con una correcta utilización.
Los resultados pueden ser menos evidentes si no se ha realizado la cirugía para extirpar los testículos.
- 1.
En la actividad sexual: se produce disminución en la capacidad de erección hasta desaparecer casi totalmente. Al disminuir la secreción de semen los orgasmos eyaculatorios son menos intensos.
La satisfacción sexual es variable y subjetiva dependiendo mucho de cada persona.
Los testículos y la próstata se atrofian.
- 2.
Disminuye la fertilidad al descender la producción de semen. En algunas ocasiones puede ser reversible al suspender el tratamiento, pero puede ocurrir esterilidad permanente tras 6 meses de uso de estrógenos.
- 3.
Aumento del tamaño mamario, no siempre el crecimiento es simétrico en ambas glándulas ni se puede elegir un tamaño deseado concreto aumentando la dosis de estrógenos.
- 4.
Se redistribuye la grasa aumentando en la zona de las caderas y variando también en la cara.
- 5.
Disminuye el pelo corporal (no siempre desaparece del todo el de la cara, aunque se hace menos denso y menos oscuro).
- 6.
La voz sufre pocos cambios, ya que es poco sensible la laringe adulta a estas hormonas.
- 7.
Cambio de carácter con incremento de la emotividad, dependiendo mucho de las características psicológicas de cada persona.
Otros posibles efectos secundarios (poco frecuentes): retención de líquido ocasional, alteración de la función hepática en aproximadamente 4 de cada 100 pacientes, cálculos en la vesícula (1% de los pacientes), y tromboflebitis o tromboembolismo pulmonar en casos muy excepcionales.
En caso de no solicitar la extirpación de sus testículos deberá hacer exploraciones periódicas en su especialista ante la posibilidad, aunque escasa, de que aparezcan lesiones degenerativas.
Los siguientes efectos del tratamiento se producen de forma gradual y no siempre de forma idéntica en cada persona. Suele empezar a notarse su acción a partir de las primeras dosis de Andrógenos, siendo sus efectos prácticamente irreversibles casi desde el principio. No se deben utilizar dosis altas de andrógenos, ya que sus resultados a plazo medio y largo son similares con dosis menores y también son menores los efectos secundarios con una correcta utilización.
- 1.
Disminuye la fertilidad, desaparecen los ciclos menstruales.
- 2.
Aumenta la actividad sexual, puede haber en ocasiones dolor en el órgano eréctil (clítoris), este aumenta su tamaño en varios cm.
- 3.
El vello facial y corporal aumenta haciéndose más grueso y oscuro.
Puede aparecer acné.
- 4.
Aumenta la masa muscular. Se distribuye la grasa de forma masculina.
- 5.
La voz puede hacerse más grave aunque no siempre llega al tono masculino clásico.
- 6.
Cambios de carácter, con mayor agresividad, dependiendo mucho de las características psicológicas de cada persona.
- 7.
No disminuye apenas el tamaño de las glándulas mamarias, aunque pueden ablandarse.
Algunos posibles efectos secundarios o cambios metabólicos que debe Vd. conocer son: retención ocasional de líquido, dolor de cabeza, aumento de las cifras de tensión arterial, elevación de la glucemia (azúcar en sangre) y elevación de las cifras de colesterol.
DE TODO ELLO RECIBIRÁ INFORMACIÓN EN NUESTRA UNIDAD
Resultados del Tratamiento Hormonal de Adultos
Puede que no se manifiesten los máximos efectos físicos de las hormonas hasta después de 2 años de tratamiento continuo. La herencia influye la respuesta de los tejidos a las hormonas, y no se puede superar esto administrando dosis más altas. El grado de efectos que realmente se logra varía de paciente en paciente.
Efectos deseados de las hormonas
Los varones biológicos tratados con estrógenos pueden esperar efectivamente que el tratamiento resulte en algún crecimiento de los senos, alguna redistribución de grasa corporal hacia la forma más femenina, una disminución de la fuerza del cuerpo superior, un ablandamiento del piel, una disminución del vello corporal, una disminución o cesación de la calvicie, una disminución de fertilidad y del tamaño testicular, y erecciones menos frecuentes y firmes. Son reversibles la mayoría de estos cambios, aunque no se revertirá completamente el aumento de los senos al descontinuar el tratamiento.
Las mujeres biológicas tratadas con testosterona pueden esperar los cambios permanentes siguientes: que la voz se hace más grave, el crecimiento del clítoris, la atrofia moderada de los senos, el aumento de vello facial y corporal y la calvicie típica del varón. Los cambios reversibles incluyen un aumento de la fuerza del cuerpo superior, un aumento de peso, un aumento de interés social y sexual y de excitación sexual, y la disminución de grasa de las caderas.
El potencial de efectos médicos secundarios negativos
Es más probable que los pacientes con problemas médicos o tendencia a enfermedades cardiovasculares experimenten efectos serios o fatales del tratamiento con hormonas del sexo opuesto. Los riesgos y efectos secundarios de tratamiento hormonal pueden aumentarse a causa de tabaquismo, obesidad, vejez, cardiopatías, hipertensión, anormalidades de coagulación, malignidades y algunas anormalidades endocrinológicas. Por eso, puede que algunos pacientes no toleren el uso de hormonas del sexo opuesto. Por otro lado, las hormonas pueden dotar beneficios a la salud tanto como riesgos. El paciente y el médico deben considerar juntos el balance entre beneficios y riesgos.
Los efectos secundarios en varones biológicos tratados con estrógenos y progestágenos pueden incluir una tendencia aumentada a coagulación (trombosis venosa con riesgo de embolismo pulmonar fatal), desarrollo de prolactinomas benignos de la hipófisis, infertilidad, aumento de peso, inestabilidad emocional, enfermedades del hígado, formación de cálculos biliares, somnolencia, hipertensión y diabetes mellitus.
Los efectos secundarios en las mujeres tratadas con testosterona pueden incluir infertilidad, acné, inestabilidad emocional, aumento de deseo sexual, cambio de perfil lipídico hacia el patrón masculino (lo que aumenta el riesgo de enfermedades cardiovasculares), y la predisposición a desarrollar tumores benignos y malignos del hígado y malfuncionamiento hepático.
El motivo por el que Vd. está siendo atendido en este servicio es una condición clínica llamada disforia de género, reconocida también como transexualidad (CIE F64.0).
Se trata de un problema cuya causa no es bien conocida, pero en el que existe una disociación entre el sexo genético de nacimiento y su identidad actual psicológica y social.
Vd. está siendo atendido/a también por otros servicios médicos con el fin de abordar de manera integral este conflicto entre identidades. El estudio y seguimiento conjunto por Endocrinología y Psicología se realizará al menos durante los 6 meses previos a iniciar ningún tratamiento hormonal, para confirmar el diagnóstico y descartar contraindicaciones de dicho tratamiento.
Desde esta fase inicial se le realizará en Endocrinología (UTIG) una historia clínica y una serie de exploraciones periódicas con el fin de evaluar su situación física. Estos estudios contemplan la realización de un estudio cromosómico (cariotipo), análisis rutinarios de sangre y orina, estudio hormonal y estudios genéticos que se realizarán dentro de un proyecto de investigación con el fin de estudiar la contribución a su diagnóstico o a su respuesta al tratamiento hormonal en el seguimiento.
Posteriormente a la realización de su diagnóstico recibirá tratamiento hormonal con el fin de suprimir sus actuales hormonas y utilizar aquellas otras que produzcan cambios en su cuerpo de acuerdo al sexo que su situación clínico-psicológica aconseja:
- ▪
TRANSEXUALISMO de HOMBRE a MUJER
- ▪
TRANSEXUALISMO de MUJER a HOMBRE.
Los efectos que se producirán en su cuerpo serán notados por Vd. de forma gradual sin poder precisar con exactitud el tiempo o los resultados finales, ya que a veces estos no coinciden exactamente con las expectativas iniciales de Vd., por ello, se le explicará cada paso, pero debe conocer que gran parte de estos cambios son irreversibles una vez que se inicia el tratamiento.
Tras la fase de tratamiento psicológico y hormonal si así lo desea se le ofrecerá la posibilidad de tratamiento quirúrgico para extirpación de sus órganos sexuales y reconstrucción de estos de acuerdo a su identidad sexual.
CONSENTIMIENTO:
Yo...................................................., declaro que he leído este documento y que me han sido explicados de forma satisfactoria la naturaleza y propósitos del proyecto así como las complicaciones más frecuentes y/o más importantes del tratamiento. También me han expuesto las fases de este, asumiendo estos plazos y el riesgo de posibles consecuencias desfavorables que no sean debidas a conducta profesional negligente.
Firma: Firma médico: Fecha:
http://www.san.gva.es/comun/ciud/docs/pdf/Castellano_201109_4.pdf
http://www.san.gva.es/comun/ciud/docs/pdf/Castellano_201109_5.pdf