La acromegalia es una enfermedad diagnosticada cada vez con mayor frecuencia1 y cuya edad promedio de presentación coincide en una proporción considerable con la vida fértil de la mujer2. Los tratamientos disponibles actualmente incluyen la cirugía, la terapia farmacológica y, en determinados casos, la radioterapia. Dichas herramientas consiguen el control del crecimiento tumoral y minimizar las consecuencias clínicas del hipersomatotropismo en la mayoría de nuestros pacientes3.
A pesar del impacto positivo de los tratamientos actuales en la supervivencia y calidad de vida, el embarazo en la acromegalia continúa siendo una eventualidad infrecuente y un reto para el clínico: la serie de casos más numerosa publicada requirió una colaboración multicéntrica en Francia y agrupó 59 embarazos4, y otros casos publicados agrupan apenas un centenar de embarazos4. La carencia de datos retrospectivos dificulta anticipar las posibles complicaciones. Dicha información es necesaria para proporcionar un consejo informado a las pacientes con acromegalia cuando desean tener descendencia. Por ello presentamos una paciente con acromegalia activa tras cirugía que llevó a término una gestación en nuestro servicio.
Mujer de 31 años de edad que acudió a consulta de Ginecología en el año 2005 por oligomenorrea y galactorrea de aproximadamente un año de evolución, sin hirsutismo ni otros síntomas. En las determinaciones bioquímicas disponibles destacaba una prolactina de 86,22ng/ml (4,8-23,3ng/ml) sin fármacos que afectaran a dicha medición. La resonancia magnética hipofisaria (RM) describió un macroadenoma hipofisario con extensión supraselar e invasión del seno cavernoso derecho. La paciente fue remitida al Servicio de Neurocirugía para tratamiento quirúrgico, que se realizó en 2006 por vía transesfenoidal sin complicaciones. Posteriormente fue evaluada en nuestro servicio para seguimiento postoperatorio. La paciente en ningún momento había manifestado engrosamiento acral, prognatismo, diaforesis, cefalea, artralgias, hipertensión arterial, hiperglucemia u otros datos sugestivos de acromegalia. Sin embargo, en el estudio hipotálamo-hipofisario basal (tabla 1) destacaban unas concentraciones de IGF-I consistentemente elevadas y la ausencia de supresión de la hormona de crecimiento (GH) en la sobrecarga oral de glucosa. En el resto del perfil hipofisario destacaban concentraciones disminuidas de cortisol sérico, por las cuales la paciente recibió tratamiento con hidrocortisona oral. Se efectuaron ecocardiograma, estudio polisomnográfico y colonoscopia, y ninguna de estas pruebas sugirieron alteraciones asociadas a la acromegalia. En la RM posquirúrgica persistía un resto tumoral intraselar y en seno cavernoso derecho por lo que se decidió conjuntamente con el Servicio de Neurocirugía reintervenir a la paciente.
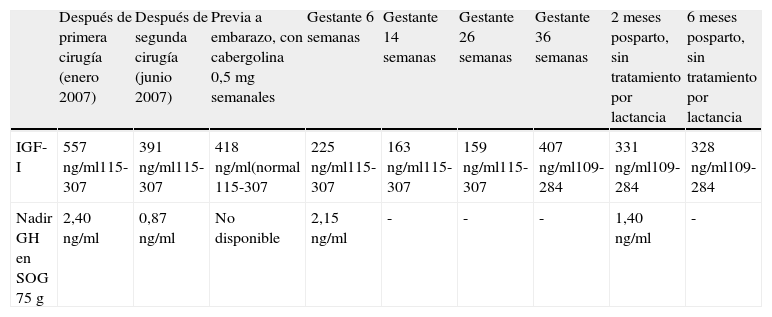
datos analíticos de la paciente
| Después de primera cirugía (enero 2007) | Después de segunda cirugía (junio 2007) | Previa a embarazo, con cabergolina 0,5mg semanales | Gestante 6 semanas | Gestante 14 semanas | Gestante 26 semanas | Gestante 36 semanas | 2 meses posparto, sin tratamiento por lactancia | 6 meses posparto, sin tratamiento por lactancia | |
| IGF-I | 557ng/ml115-307 | 391ng/ml115-307 | 418ng/ml(normal 115-307 | 225ng/ml115-307 | 163ng/ml115-307 | 159ng/ml115-307 | 407ng/ml109-284 | 331ng/ml109-284 | 328ng/ml109-284 |
| Nadir GH en SOG 75g | 2,40ng/ml | 0,87ng/ml | No disponible | 2,15ng/ml | - | - | - | 1,40ng/ml | - |
GH: hormona de crecimiento; IGF-I: insulin growth factor-I; SOG: sobrecarga oral de glucosa.
Se realizó cirugía transesfenoidal endoscópica en nuestro hospital, consiguiendo una disminución importante de las concentraciones de IGF-I y una reducción de la masa tumoral. La anatomía patológica describió un adenoma con inmunohistoquímica positiva para GH, negativa para prolactina y con un índice Ki 67 del 5%. Después de la cirugía la paciente consiguió tener menstruaciones regulares y no había datos de hipopituitarismo. Sin embargo (tabla 1), persistían criterios bioquímicos de actividad de la enfermedad y restos tumorales macroscópicos. Dadas las concentraciones discretamente elevadas de IGF-I, se intentó tratamiento con cabergolina con lo que se mejoró el control bioquímico de la enfermedad. Al inicio del tratamiento se le había aconsejado que evitara la gestación hasta no asegurar la normalización bioquímica y la estabilidad tumoral.
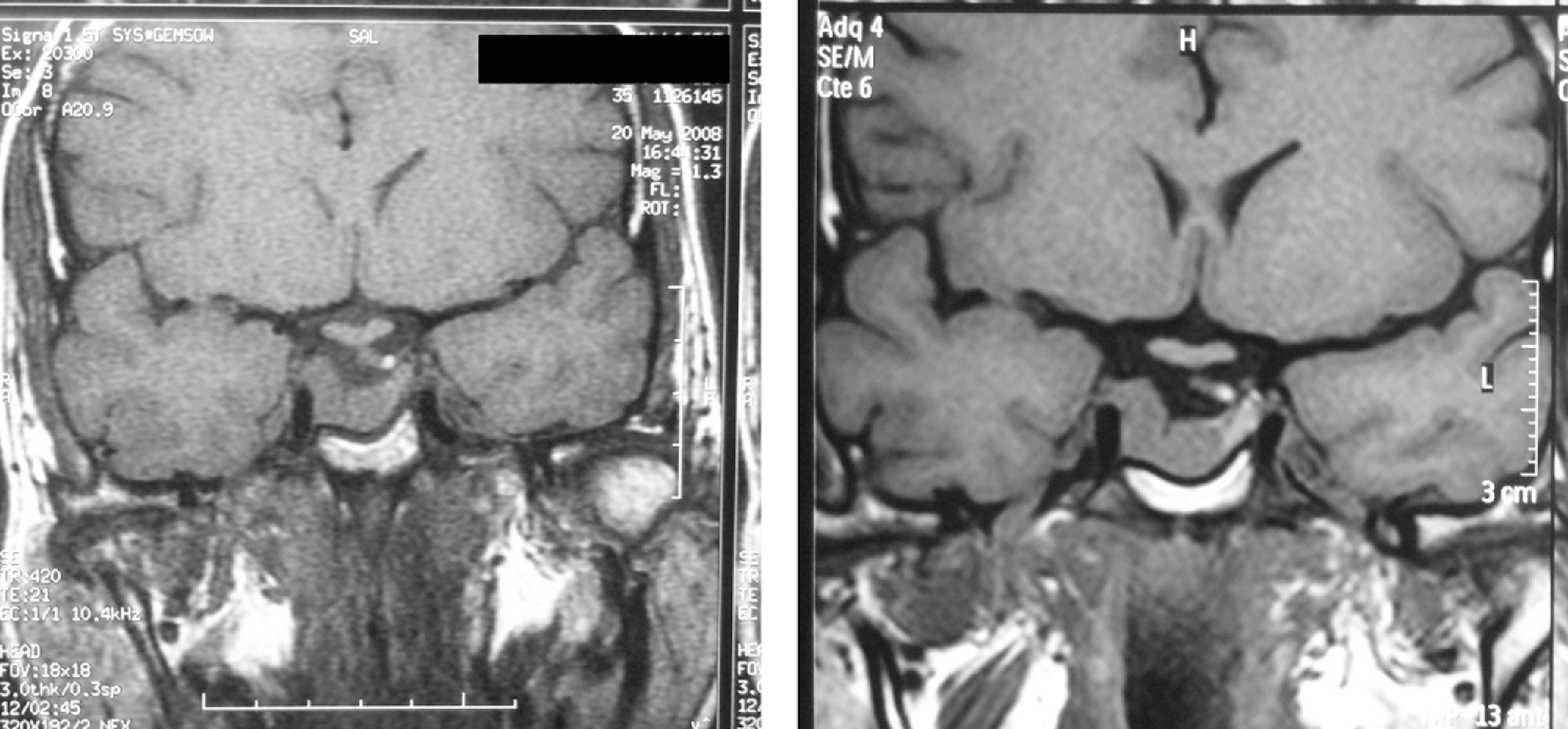
En 2008, 3 meses después de la última revisión y con 35 años de edad, la paciente contactó con nuestro servicio por gestación de 5 semanas con la que deseaba continuar. En ese momento se interrumpió el tratamiento con cabergolina, se programaron revisiones neuroftalmológicas trimestrales, y seguimiento en la consulta de embarazo de alto riesgo. Asimismo, se le recordó la conveniencia de abandonar el hábito tabáquico, que decidió mantener. Durante la gestación permaneció asintomática hasta dar a luz a las 39 semanas un neonato sano. En las revisiones efectuadas (tabla 1) las concentraciones de IGF-I disminuyeron durante el embarazo hasta niveles normales para su edad excepto la última determinación. El test de O'Sullivan fue normal en el primer y tercer trimestres y la tensión arterial no precisó tratamiento. La RM efectuada al término del embarazo mostró estabilidad tumoral (fig. 1). Sin embargo, las concentraciones de IGF-I posparto volvieron a superar los límites fisiológicos, sin que la paciente aquejara síntoma alguno. Con objeto de disminuir la morbilidad asociada al exceso de GH la paciente inició tratamiento con cabergolina con mejoría gradual de los parámetros bioquímicos y estabilidad del tumor.
La acromegalia es un síndrome con una alta morbimortalidad asociada. Afortunadamente, disponemos de un arsenal terapéutico cada vez mayor para mejorar el pronóstico y la calidad de vida del paciente. Sin embargo, a pesar de estos avances, existe escasa experiencia en el seguimento del embarazo en las pacientes con acromegalia. Diversas razones podrían justificar esta carencia:
- -
La hiperactividad del eje somatotropo puede alterar los ciclos hormonales que conducen a la ovulación. Esto, junto con la mayor frecuencia de hiperandrogenismo funcional ovárico y mayor resistencia a la insulina en pacientes con acromegalia2,3,5, puede dificultar la ovulación y, en consecuencia, la gestación. Asimismo, puede coexistir un hipogonadismo hipogonadotropo por compresión tumoral o yatrogénico (cirugía y radioterapia), que obligaría a la inducción hormonal externa de la ovulación para lograr la gestación.
- -
La carga sintomática de la enfermedad y la escasa experiencia con la mayoría de los fármacos disponibles para la acromegalia en el embarazo puede desalentar el mismo en las pacientes con acromegalia y en sus clínicos. En la actualidad, se recomienda suspender los análogos de somatostatina y la cabergolina al confirmar la gestación, aunque los casos clínicos publicados no han demostrado estos fármacos sean teratogénicos ni aumenten el riesgo materno-fetal. Asimismo, la intervención quirúrgica conlleva riesgo de interrupción de la gestación y la radioterapia está directamente contraindicada en pacientes gestantes.
- -
La mayor dificultad del seguimiento clínico y bioquímico de la enfermedad: durante el embarazo se sustituye fisiológicamente la secreción de GH hipofisaria (GH1) por la variante placentaria (GH-V); las pacientes sanas suprimen la secreción de GH1, mientras que la gestante acromegálica mantiene concentraciones estacionarias de GH1. Además, el hiperestrogenismo gestacional bloquea la secreción hepática de IGF-I, lo cual explica la disminución de la misma en nuestra paciente5,6. Por otra parte, las distintas variantes de GH y la IGF-I no traspasan la barrera placentaria, lo cual impide que tengan un efecto nocivo directo sobre el feto7. Los cambios fisiológicos mencionados no permiten un seguimiento fiable de la acromegalia en el embarazo con estos parámetros bioquímicos, y los cambios físicos propios del embarazo (edemas, tumefacción acra, etc.) pueden confundirse con síntomas de la enfermedad. Al mismo tiempo, la RM debe efectuarse sin contraste y únicamente en casos con síntomas de posible afectación visual, lo cual aumenta la incertidumbre sobre el curso clínico.
En línea con lo descrito en estos apartados, se deben incluir las siguientes consideraciones cuando una paciente con acromegalia consulta sobre la viabilidad de un futuro embarazo:
- 1)
Debe vigilarse la posibilidad de crecimiento tumoral durante la gestación, y tener en cuenta los riesgos específicos para la gestación de los tratamientos disponibles (cirugía, análogos de somatostatina y cabergolina)
- 2)
Debe vigilarse con atención la posibilidad de diabetes gestacional e hipertensión inducida por el embarazo, cada cual con un riesgo materno-fetal específico, particularmente en pacientes con enfermedad activa
- 3)
No hay datos de que el exceso de hormona de crecimiento e IGF-I por sí mismos empeoren el riesgo materno-fetal
- 4)
El seguimiento bioquímico pierde validez en la gestación, y los datos clínicos son más difíciles de interpretar, dado que los cambios propios del embarazo pueden ser muy similares
A pesar de lo descrito anteriormente, la experiencia publicada hasta ahora ha sido mayoritariamente favorable, aunque no es descartable un sesgo de publicación. En la mayor serie descrita hasta la fecha4, con 59 gestaciones, la mayoría de las pacientes pudieron suspender con seguridad el tratamiento farmacológico, se encontraron 6 fetos microsómicos, 2 fetos macrosómicos y una incidencia discretamente mayor de diabetes gestacional e hipertensión arterial inducida por el embarazo, particularmente en las pacientes que permanecieron con actividad de la enfermedad. El volumen tumoral permaneció estable en la mayoría de las pacientes. No obstante a estos datos positivos, la experiencia disponible hoy día sobre el embarazo en la acromegalia es escasa, y es por ello preciso que los datos de futuros embarazos sean analizados de forma consistente y exhaustiva, preferiblemente en el marco de colaboraciones multicéntricas. Dichos estudios informarían más rigurosamente el consejo sobre la viabilidad del embarazo en las pacientes con acromegalia, un consejo que debiera formar parte del tratamiento integral de una paciente con cualquier patología en edad fértil.