La colonoscopia es el «estándar de oro» para la detección de pólipos y lesiones precancerosas. Un adecuado nivel de limpieza es crítico para una colonoscopia efectiva. Los preparados intestinales deben ser eficaces, seguros y con adecuada tolerancia por parte del paciente.
ObjetivoComparar la eficacia, tolerancia y costo de 2 preparaciones colónicas: 4l polietilenglicol vs. 2l polietilenglicol+10mg de bisacodilo.
Material y métodosSe realizó un estudio transversal, prolectivo, comparativo y analítico. Se incluyeron pacientes enviados a colonoscopia por cualquier indicación de 18-85 años de edad. Se excluyeron a pacientes con antecedente de alergia a las fórmulas utilizadas, falla cardiaca, resección de algún segmento de colon. Se formaron en forma aleatoria simple 2 grupos: el grupo 1 recibió la preparación estándar al ingerir 4l de polietilenglicol y el grupo 2 recibió 2l de polietilenglicol y 10mg de bisacodilo.
ResultadosSe incluyeron 92 pacientes, de los cuales se eliminaron 18. Se incluyeron 74 pacientes, 37 (50%) hombres y 37 (50%) mujeres. El grupo 1 estuvo formado por 39 pacientes (53%), el grupo 2 por 35 pacientes (47%), la edad media fue de 50 años de edad. La tolerancia de la preparación fue medida con la escala de Likert obteniendo una media de 4 puntos en ambos grupos. La eficacia se midió con la escala de Boston con un valor en el grupo 1 de 7.36 y en el grupo 2 de 7.43 (RR 0.063).
ConclusionesEn nuestro estudio no hubo diferencia significativa en la limpieza colónica y tolerancia entre ambos grupos. La preparación con bisacodilo es más económica.
Colonoscopy is the “gold standard” for the detection of polyps and precancerous lesions. Adequate cleansing is essential for an effective colonoscopy. Intestinal preparations should be effective, safe and well tolerated by the patient.
ObjetiveTo compare the bowel cleansing efficacy, tolerability and cost of 2 colonic preparations: 4l polyethylene glycol vs. 2l polyethylene+10mg bisacodyl.
Material and MethodsA cross-sectional, prolective, comparative and analytical study was conducted including patients referred for colonoscopy due to any indication, aged between 18 and 85 years. We excluded patients with a history of allergy to the formulations used, heart failure and resection of a segment of the colon. Two groups were formed by simple randomisation: group 1 received the standard preparation of 4 litres of polyethylene glycol (PEG), and group 2 received 2l PEG and 10mg bisacodyl.
ResultsThe study included a total of 92 patients, of which 18 were ruled out. Out of the final 74 patients, 37 (50%) were male and 50% were female. Group 1 included 39 patients (53%) and group 2 included 35 patients (47%), and the mean age was 50 years. Tolerance to the preparation was measured using a Likert scale, with a mean result of 4 points in both groups. Efficacy was measured using a Boston scale, with a value of 7.36 in group 1 and of 7.43 in group 2 (RR 0.063).
ConclusionsThe study found no significant differences in colon cleansing and tolerance between groups. The preparation containing bisacodyl was less expensive.
La Agencia Internacional de Investigación de cáncer publicó que el cáncer colorrectal (CCR) ocupa mundialmente la cuarta causa de muerte1. El CCR representa en México el segundo tipo de cáncer más prevalente2. La detección de CCR en una fase temprana se asocia con una supervivencia a 5 años del 90%. La colonoscopia sigue siendo el «estándar de oro» para la detección de pólipos y lesiones precancerosas3. La precisión diagnóstica de la colonoscopia requiere la visualización completa de la mucosa colónica4,5. Un adecuado nivel de limpieza es crítico para una colonoscopia efectiva6,7.
Los diferentes preparados intestinales deben de cumplir con las siguientes características: eficacia, seguridad y tolerancia del paciente8,9. La eficacia es evaluada por el endoscopista a través de escalas como la escala de Boston, la cual fue desarrollada para limitar la variabilidad inter-observador en la calificación de la calidad de la preparación intestinal, mientras que preserva la capacidad para distinguir diferentes grados de limpieza del intestino4. Cada región del colon (colon derecho, transverso e izquierdo) recibe una «puntuación del segmento» de 0-3 y son sumados, los valores van del 0-94,8. La seguridad: se refiere a los eventos adversos del procedimiento y de la ingesta de los fármacos. La tolerancia es un concepto complejo y subjetivo10,11, presentando síntomas como náuseas, distensión abdominal o dolor abdominal, pudiendo ser estimada con la escala de Likert9.
Al paso del tiempo se han desarrollado soluciones osmóticamente balanceadas hasta llegar a soluciones más seguras como las osmóticas no fermentables tales como el polietilenglicol (PEG)6.
PolietilenglicolEs una molécula inerte, se disuelve de forma completa en cualquier solución, contiene electrolitos y sulfato de sodio para lograr un avance osmótico4, su característica principal es la ausencia de sulfato de sodio9,12. La preparación tradicional requiere la ingesta de 4l, lo cual se asocia a pobre tolerancia y mal apego por parte del paciente y efectos adversos11,12. Se ha optado por reducir el volumen de PEG a 2l y añadir un complemento de laxante tales como ácido ascórbico, bisacodilo, sen o magnesio para mejorar la tolerancia del paciente13.
Polietilenglicol más bisacodiloEste último es un derivado de difenilmetano, tiene pobre absorción en el intestino delgado. Dos tabletas de bisacodilo estimulan la motilidad colónica6. El bisacodilo de 10mg tiene un mejor perfil de seguridad, con una reducción significativa del dolor, náuseas y malestar general13. El fosfato de sodio es una molécula osmóticamente activa ha demostrado ser segura y efectiva, pero dado sus características hiperosmóticas, puede causar alteraciones electrolíticas6,17. Diferentes metaanálisis han comparado la preparación (PEG o FS con o sin simeticona)7,9,14.
El bisacodilo se ha combinado con PEG+Gatorade, con lo que se ha informado mayor número de eventos adversos y no demostró ser una mejor preparación para limpieza del colon16. Como parte de la preparación intestinal se recomienda una dieta baja en fibra en el día anterior a la colonoscopia15.
El presente trabajo tuvo como objetivo primario comparar la eficacia de limpieza colónica de la combinación de PEG más bisacodilo frente a la preparación de PEG tradicional (4l). Como objetivos secundarios se compararon la tolerancia de la combinación de PEG+bisacodilo vs. PEG preparación tradicional y el costo entre ambas preparaciones.
Material y métodosSe realizó un estudio transversal, prolectivo, comparativo y analítico. Se incluyeron pacientes que acudieron al servicio de Endoscopia Gastrointestinal del «Hospital General de México Dr. Eduardo Liceaga» de junio de 2013 a mayo 2014 enviados con solicitud de colonoscopia y que cumplieran con los siguientes criterios de inclusión: a) hombres o mujeres de 18-85 años de edad, b) pacientes enviados a colonoscopia por cualquier indicación, c) que aceptaran participar previa firma de consentimiento informado; se excluyeron a) mujeres embarazadas o lactando, b) antecedente de alergia a las fórmulas utilizadas, c) obstrucción intestinal que impidiera la limpieza intestinal, d) megacolon tóxico, e) falla cardiaca en clase funcional III o IV, f) resección de algún segmento de colon, f) enfermos psiquiátricos, g) falla renal crónica, h) cirróticos descompensados, i) diabéticos.
Las colonoscopias se realizaron con colonoscopios Olympus CF-H 180 AL (Olympus American Corp Melville, NY, EE. UU.). Se utilizó equipo videorreproductor Toshiba para grabar los estudios en disco DVD. Se formaron en forma aleatoria simple 2 grupos: el grupo 1 recibió la preparación estándar al ingerir 4l de PEG un día previo al estudio iniciando la primera toma a las 17:00h un litro por hora. El grupo 2 recibió la preparación combinada con 10mg de bisacodilo a las 13:00h y 2l de PEG desde las 17:00h, un litro por hora.
Análisis estadísticoSe utilizó estadística descriptiva, mediante cálculo de medias y desviaciones estándar para variables cuantitativas o semicuantitativas; así como frecuencias y porcentajes para variables cualitativas. Se realizó prueba T de Student para comparar los valores de las escalas de Boston total para el tipo de preparación, así como la escala de Likert para tolerancia de las mismas. Se consideró el p valor<0.05 como significativo. Se empleó el software SPSS 21.0 para Windows (IBM).
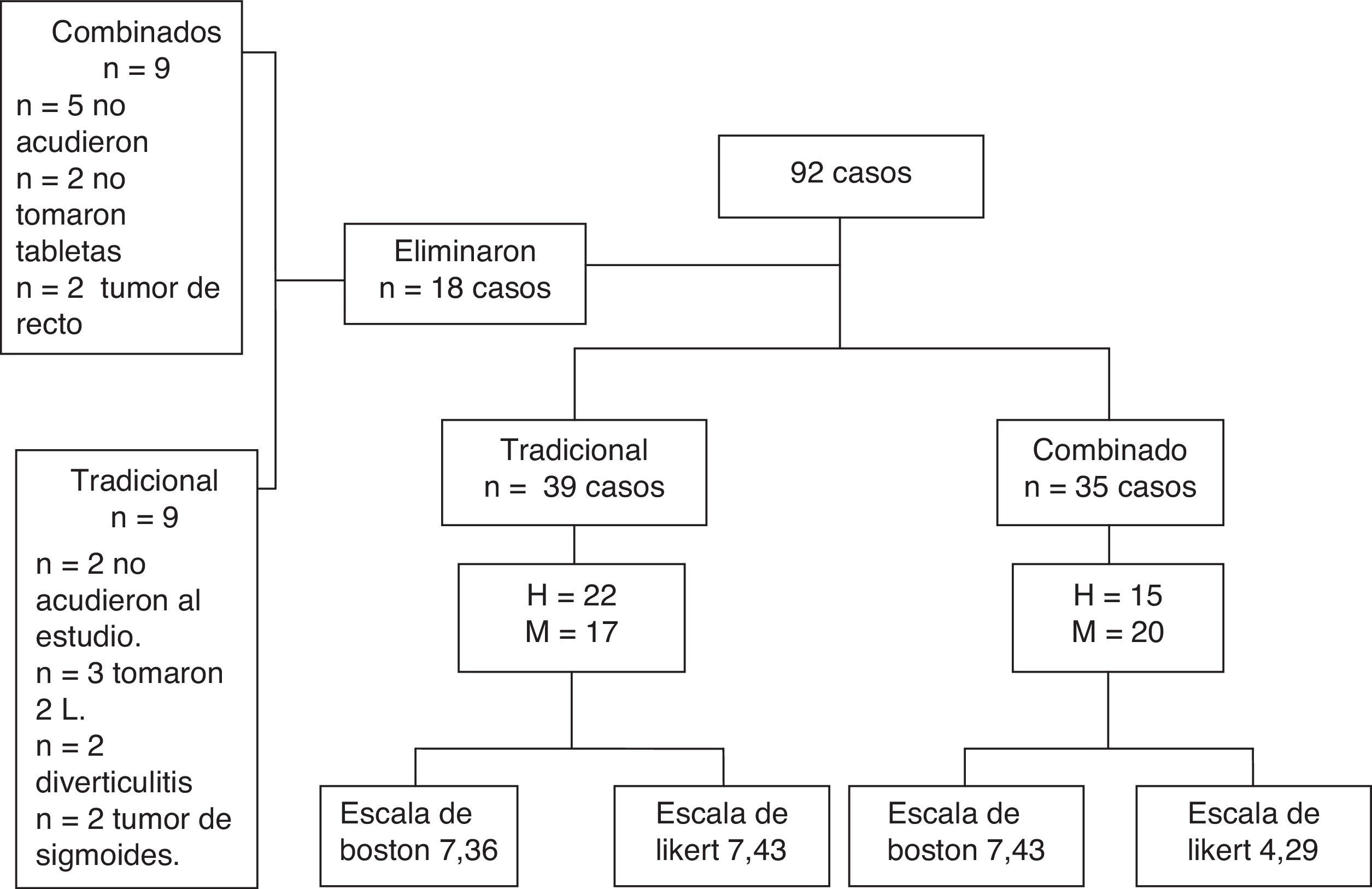
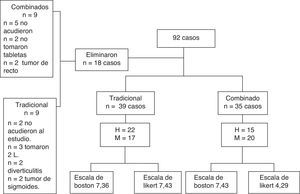
ResultadosSe incluyeron 92 pacientes, de los cuales se eliminaron 18 por las siguientes razones: 5 que no cumplieron con el esquema de preparación, 7 no se presentaron el día del estudio y en 6 no se llegó al ciego (fig. 1).
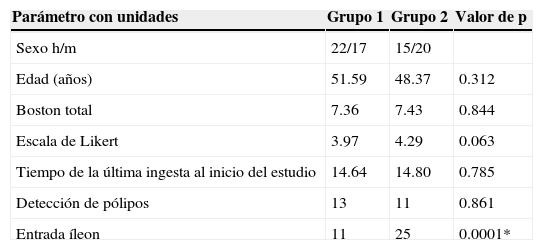
Por lo tanto se consideraron 74 pacientes, 37 (50%) hombres y 37 (50%) mujeres. Los principales diagnósticos de envio para realización del estudio fueron: hemorragia de tubo digestivo bajo en 39 (52.7%) y estreñimiento 14 (18.9%). Los principales diagnósticos finales endoscópicos fueron: 24 (32.4%) con estudio normal y 18 (24.3%) con pólipos colónicos. En la tabla 1 se observan las diferencias entre los grupos incluidos en el estudio en relación con las características generales de los pacientes. El grupo 1 estuvo formado por 39 pacientes (53%), el grupo 2 por 35 pacientes (47%), la edad media fue de 50 años de edad con una desviación de±13 años (rango 21-80 años de edad).
Características generales diferenciadas entre los grupos de los pacientes incluidos en el estudio
| Parámetro con unidades | Grupo 1 | Grupo 2 | Valor de p |
|---|---|---|---|
| Sexo h/m | 22/17 | 15/20 | |
| Edad (años) | 51.59 | 48.37 | 0.312 |
| Boston total | 7.36 | 7.43 | 0.844 |
| Escala de Likert | 3.97 | 4.29 | 0.063 |
| Tiempo de la última ingesta al inicio del estudio | 14.64 | 14.80 | 0.785 |
| Detección de pólipos | 13 | 11 | 0.861 |
| Entrada íleon | 11 | 25 | 0.0001* |
La tolerancia de la preparación fue medida con la escala de Likert en una escala de 1-5, (1=seriamente preocupante, 2=angustiante, 3=muy molesto, 4=leve, 5=no hubo molestias). Obteniendo una media de 4 en ambos grupos (fi. 1). Se comparó la tolerancia obteniendo en grupo 1 una media de 3.97 (±0.749) en el grupo 2 una medida de 4.29 (±0.66), sin encontrar diferencia en la tolerancia en ambos grupos.
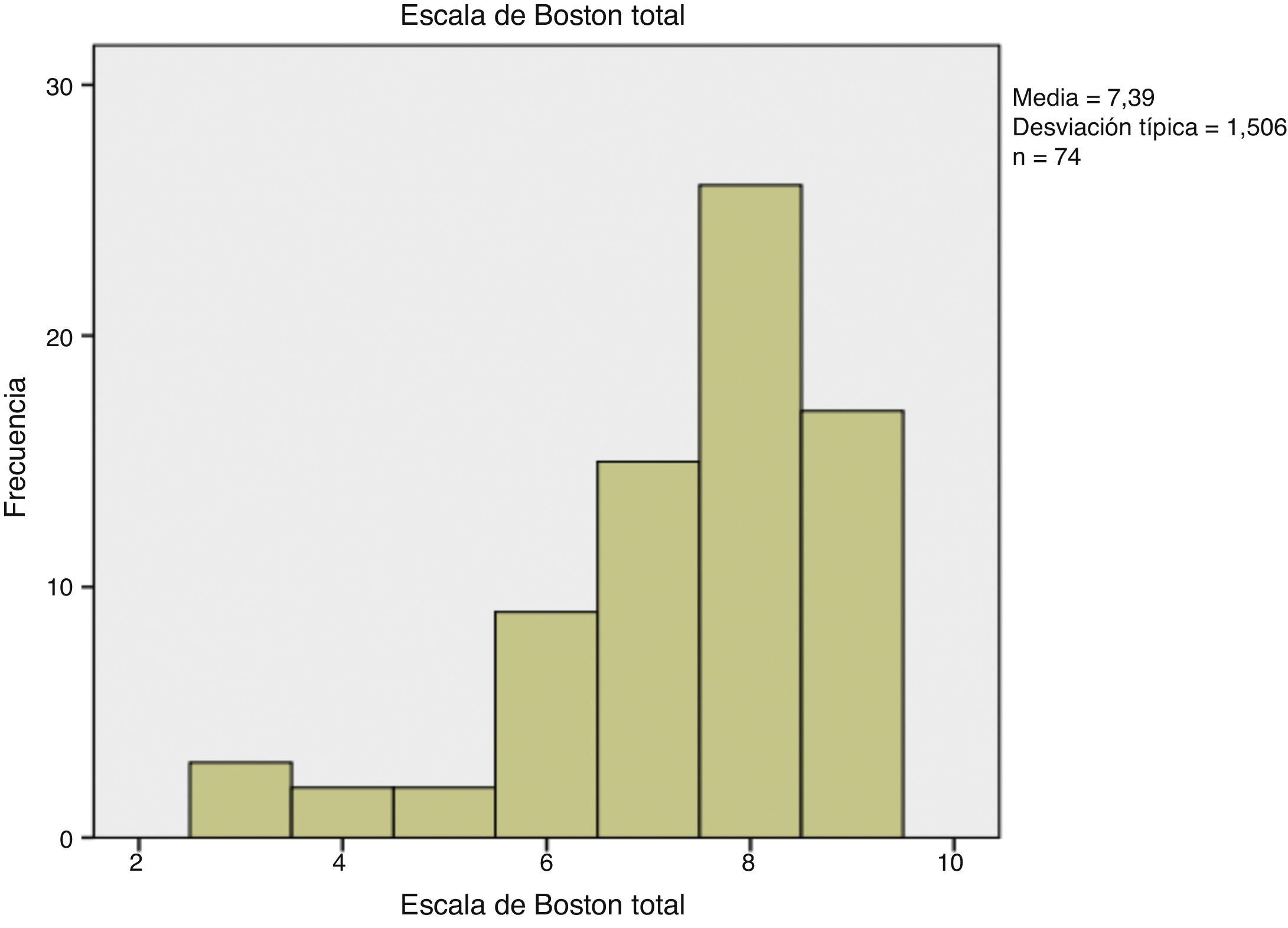
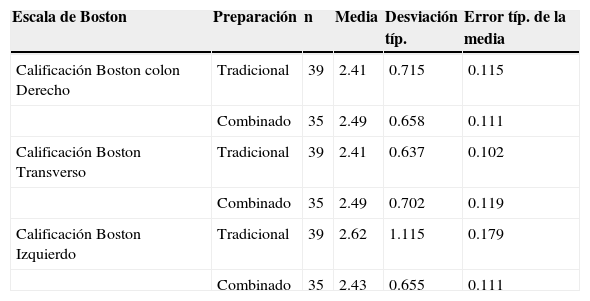
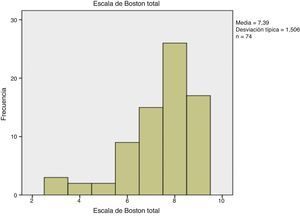
Se comparó la calidad de la preparación entre los grupos, con la escala de Boston el total por tipo preparación donde el grupo 1 obtuvo una media de 7.36 (±1.64), el grupo 2 presentó una media de 7.43 (±1.35) (fig. 2). Se midió la escala de Boston por segmento colónico teniendo los siguientes resultados: grupo 1, colon derecho una media de 2.41, colon transverso 2.41 e izquierdo 2.62; grupo 2, colon derecho una media de 2.49, colon transverso 2.49 e izquierdo 2.43 (tabla 2). No encontrando diferencia en la escala de Boston en promedio y por segmento en ambos grupos.
Clasificación de Boston en los diferentes grupos de acuerdo al segmento colónico estudiado
| Escala de Boston | Preparación | n | Media | Desviación típ. | Error típ. de la media |
|---|---|---|---|---|---|
| Calificación Boston colon Derecho | Tradicional | 39 | 2.41 | 0.715 | 0.115 |
| Combinado | 35 | 2.49 | 0.658 | 0.111 | |
| Calificación Boston Transverso | Tradicional | 39 | 2.41 | 0.637 | 0.102 |
| Combinado | 35 | 2.49 | 0.702 | 0.119 | |
| Calificación Boston Izquierdo | Tradicional | 39 | 2.62 | 1.115 | 0.179 |
| Combinado | 35 | 2.43 | 0.655 | 0.111 |
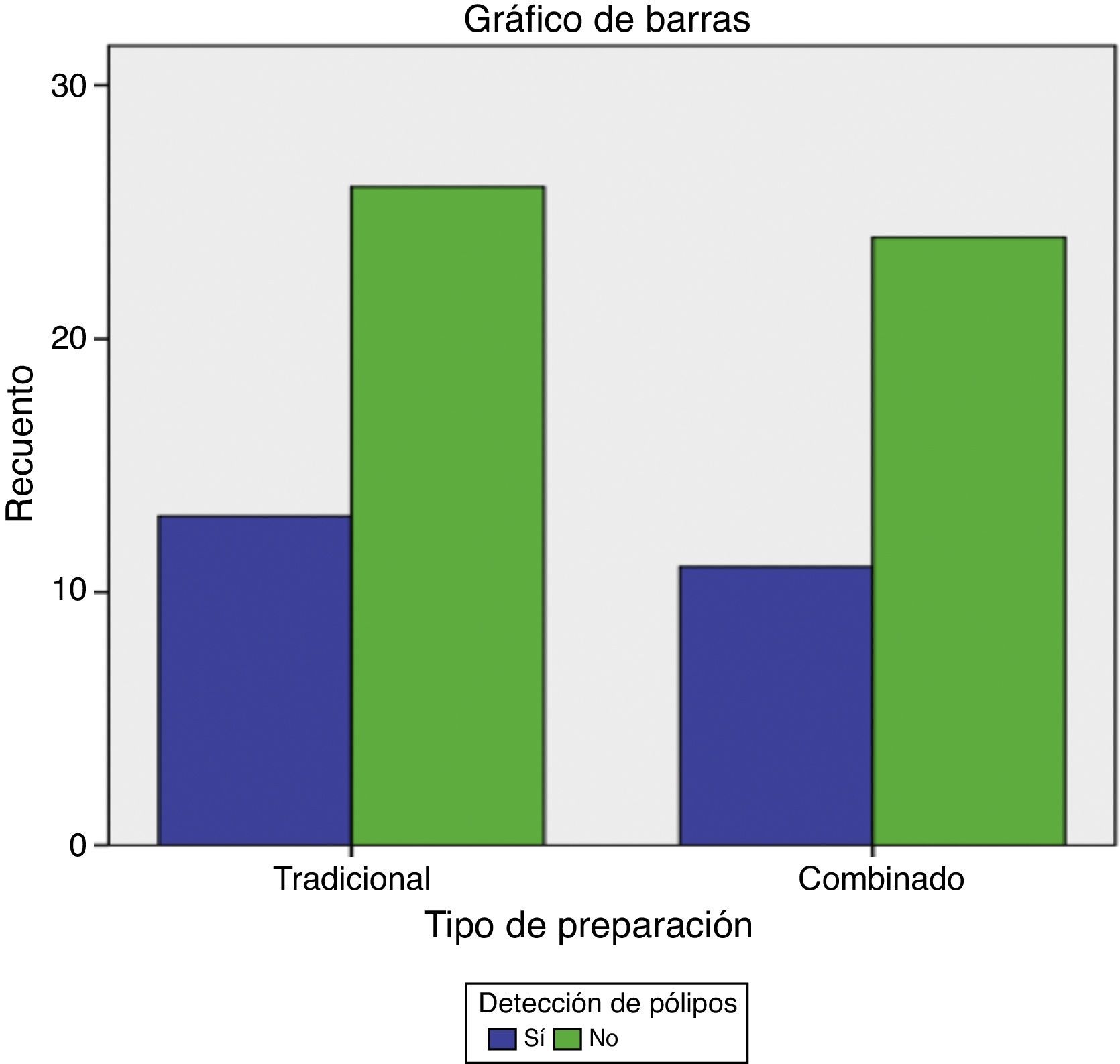
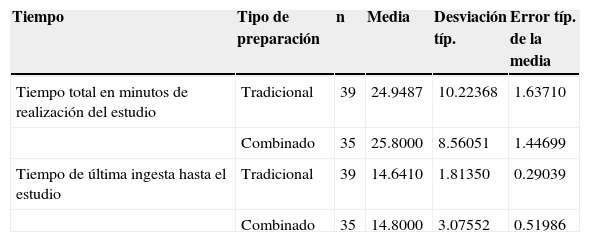
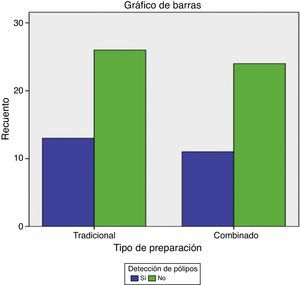
El tiempo promedio en que se realizó cada estudio fue de 25±9min. El tiempo trascurrido desde la última toma del medicamento hasta la realización del estudio presentó una media de 15±2h. El tiempo total en que realiza el estudio es igual en ambos grupos y el tiempo en que trascurre de la última ingesta de cualquiera de las 2 preparaciones a la realización del estudio presentaron una media de 14h (tabla 3). Se comparó la tasa de detección de pólipos colónicos en los pacientes incluidos divididos de acuerdo a la preparación recibida sin encontrar diferencia estadísticamente significativa (fig. 3). Se comparó entrada al íleon con cada uno de los grupos encontrando diferencia estadísticamente significativa en el tipo de preparación, observando mayor entrada a íleon en el grupo 2 (tabla 1).
Tiempo total del estudio. Tiempo de la última ingesta de la fórmula a la realización de estudio
| Tiempo | Tipo de preparación | n | Media | Desviación típ. | Error típ. de la media |
|---|---|---|---|---|---|
| Tiempo total en minutos de realización del estudio | Tradicional | 39 | 24.9487 | 10.22368 | 1.63710 |
| Combinado | 35 | 25.8000 | 8.56051 | 1.44699 | |
| Tiempo de última ingesta hasta el estudio | Tradicional | 39 | 14.6410 | 1.81350 | 0.29039 |
| Combinado | 35 | 14.8000 | 3.07552 | 0.51986 |
No se documentaron complicaciones secundarias al uso de los 2 esquemas de preparación evaluados.
DiscusiónEn nuestro estudio encontramos que la fórmula de 10mg de bisacodilo más 2l PEG es efectiva en la limpieza colónica para realización de colonoscopia. El bajo volumen (2l) de la fórmula se asocia a una mejor aceptación y apego por parte del paciente como se ha demostrado en estudios previos7,18.
Valiante et al. compararon el esquema 4l PEG vs. dosis de PEG 2l + bisacodilo 10mg concluyeron que es una combinación mejor tolerada y aceptada por los pacientes, encontraron mayor detección de pólipos19. En nuestro estudio se detectaron más pólipos con la preparación tradicional vs. combinada aunque esta diferencia no fue estadísticamente significativa. Sharma et al. compararon la eficacia y tolerancia de las 2 preparaciones encontrando que es mayor la tolerancia en el grupo de PEG+bisacodilo21. Clarckston y Smith encontraron que fue superior la combinación de 2l PEG+bisacodilo 10mg vs. PEG 4l en eficacia, pero en tolerabilidad y aceptación no hubo diferencias, al igual que el estudio presentado por Di Palma, mientras que Wang y Lin no encontraron diferencias en tolerancia y eficacia21 semejante a nuestros resultados.
La sociedad Americana de Endoscopia Gastrointestinal (ASGE) recomienda la utilización de bisacodilo y PEG20. Church et al. demostraron que la administración de las fórmulas el mismo día del estudio proporciona una mejor preparación colónica en comparación con la preparación de un día antes utilizando la misma cantidad de solución de PEG21.
La visualización del ciego e íleon terminal forma parte de los estándares de calidad de la colonoscopia22, en nuestro estudio encontramos una diferencia significativa en la visualización de íleon terminal en pacientes con la preparación combinada, sin embargo, al analizar otros posibles factores encontramos que estuvo más relacionado al tipo de supervisión del procedimiento por médico adscrito.
Estudios han demostrado que la preparación que se realiza el mismo día del estudio tiene mejor eficacia en la limpieza colónica así como en la detección de adenomas colonicos20,21. En nuestro estudio el tiempo promedio de la última toma del laxante y el inicio del estudio fue de 14h siendo un factor que podría afectar una adecuada limpieza. No todas las dosis Split o la preparación de «el mismo día» es posible llevarse en centros hospitalarios, ya que la mayoría de los estudio endoscópicos se llevan a cabo en el primer turno donde se cuenta con anestesiólogos, por lo que estos esquemas se encuentran limitados en hospitales públicos.
Los costos de 4 sobres de PEG es de 380 pesos mientras que el costo de 2 tabletas de bisacodilo de 5mg+2 sobres de PEG es de 200 pesos. Teniendo en cuenta que ambas fórmulas tienen la misma eficacia en la limpieza colónica y una de ellas es más económica se convierte en una alternativa de preparación en los pacientes del «Hospital General de México Dr. Eduardo Liceaga».
ConclusionesEn nuestro estudio no hubo diferencia significativa en la limpieza colónica y tolerancia entre ambos grupos. Sí se encontró diferencia significativa en la entrada a la válvula ileocecal siendo mayor en pacientes que tomaron 2 PEG+10mg de bisacodilo. La preparación de bisacodilo es bien tolerada y aceptada por los pacientes teniendo una adecuada limpieza colónica, permitiendo mayor adherencia a las indicaciones por parte del paciente traduciendo en mejorar los estándares de calidad.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciamientoLos autores no recibieron patrocinio para llevar a cabo este artículo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.