Introducción
La lesión de Dieulafoy (LD), conocida también como exulceratio simplex o arteria de calibre persistente, es una causa de sangrado digestivo, frecuentemente no reconocida, que potencialmente pone en peligro la vida.1 En cerca de 5% de los pacientes con sangrado gastrointestinal oscuro, los estudios estándar de diagnóstico (angiogramas viscerales, endoscopia y exploraciones quirúrgicas), fallan en demostrar el origen del sangrado.2 Esta lesión fue descrita por Gallard en 1884 y caracterizada por Dieulafoy en 1898; en 1953, Rider describió la ectasia vascular del antro gástrico y Jabari en 1984. En 1991, Franko informó la lesión de Dieulafoy en recto.3
Aspectos generales de la fisiopatología, diagnóstico y presentación clínica
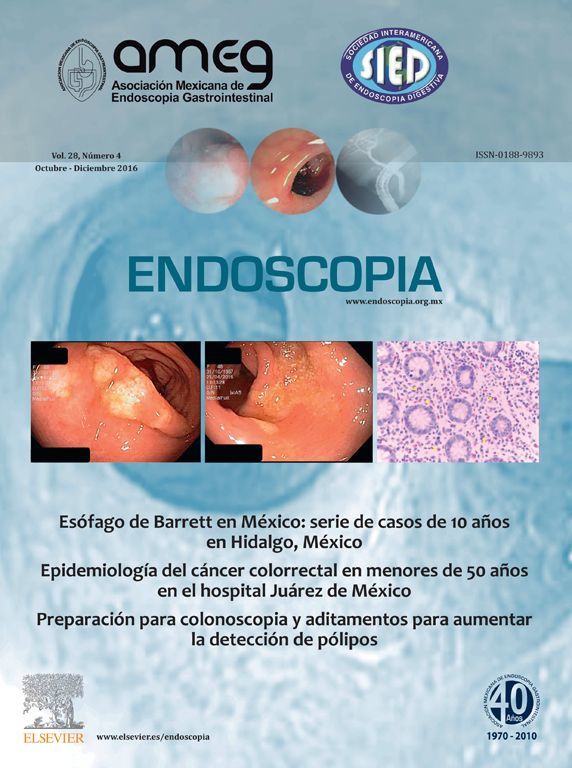
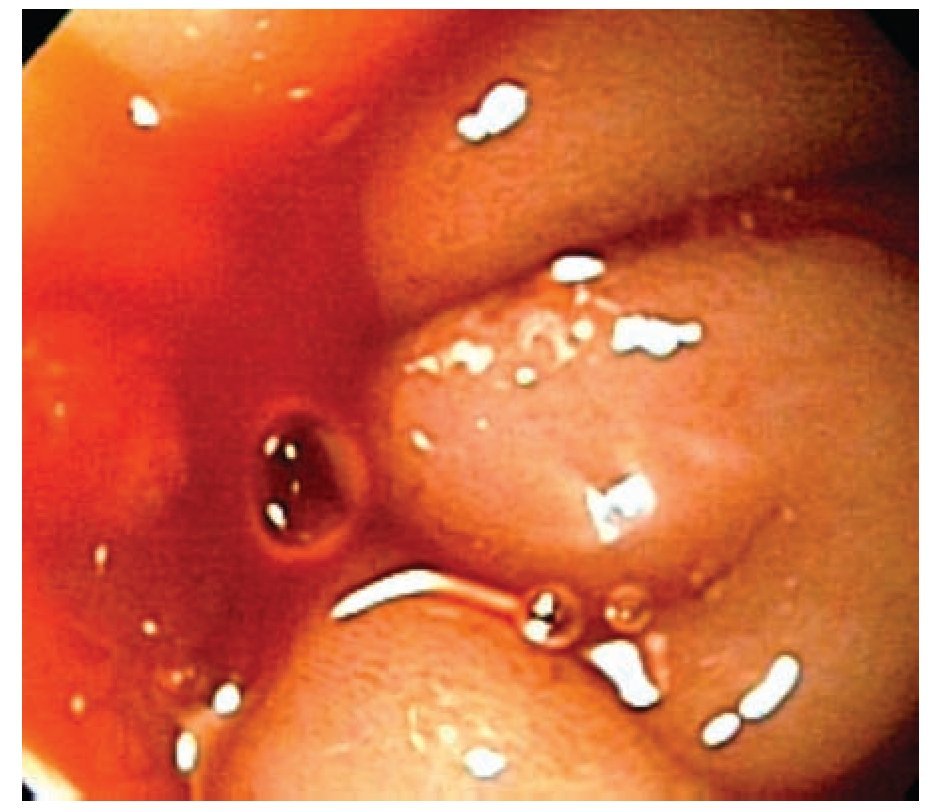
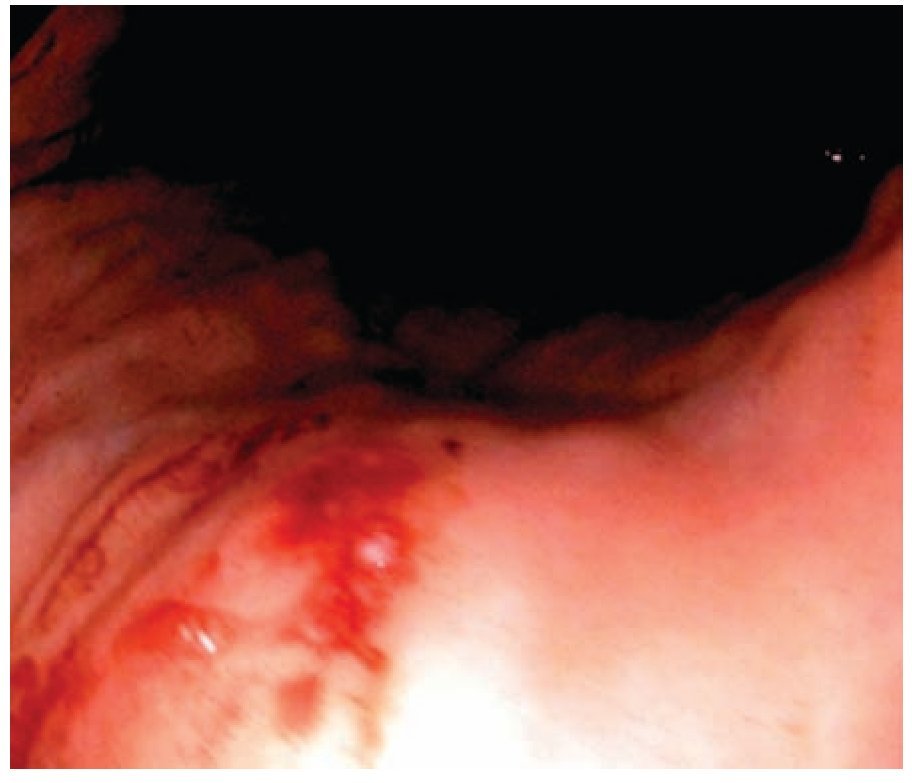
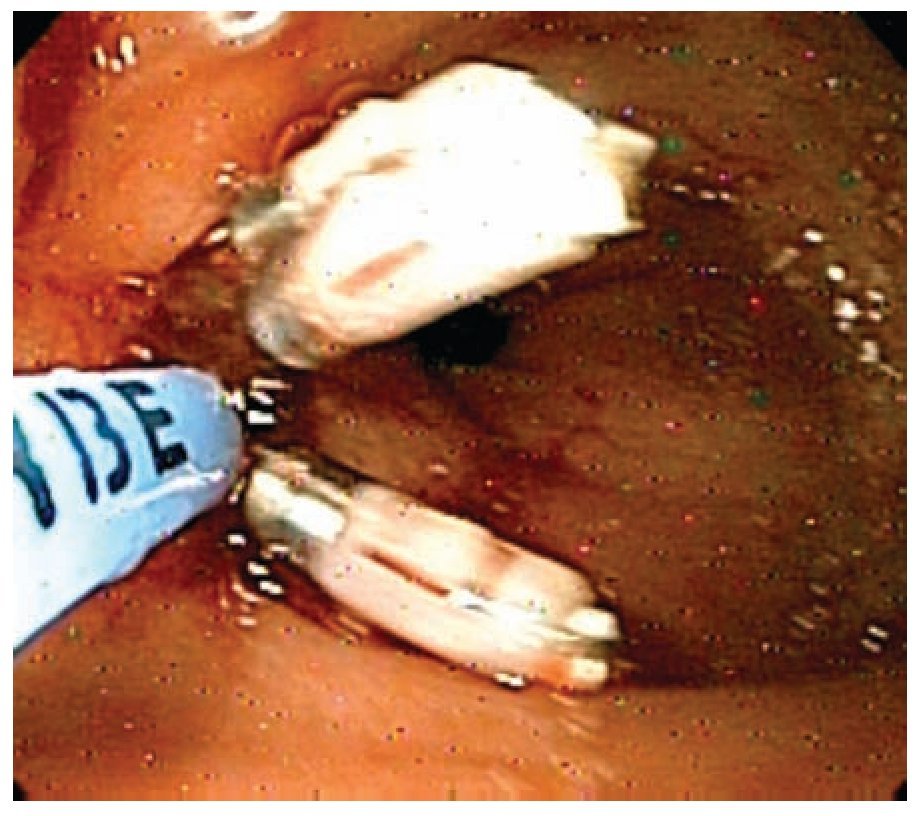
La LD representa aproximadamente 1% a 2% de las hemorragias digestivas superiores no variceales. La mayoría de estas lesiones se localizan en la cavidad gástrica; sin embargo, pueden estar presentes en otras localizaciones del tracto digestivo como duodeno, yeyuno o recto (Figuras 1 a 4). Ésta entidad es poco frecuente, pero puede alcanzar altos índices de morbi-mortalidad.4
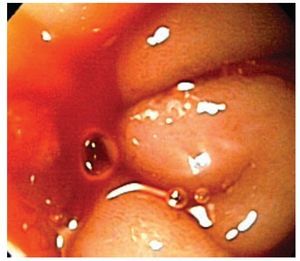
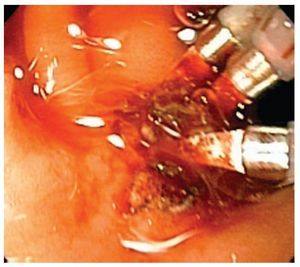
Figura 1. Sangrado activo.
Figura 2. Detalle de la lesión.
Figura 3. Lesión de Dieulafoy imagen en banda
Figura 4. Lesión de Dieulafoy con luz blanca angosta.
La LD es una arteria de calibre persistente, expuesta, de trayecto aberrante, que no sigue las ramificaciones habituales desvaneciéndose hasta llegar a
una microvasculatura capilar. La arteria de calibre persistente mide entre uno y tres milímetros y está situada sub-epitelialmente. Está usualmente asociada a un defecto de la mucosa de dos a cinco milímetros de tamaño, sin evidencia de inflamación, esclerosis o dilatación aneurismática.
La patogénesis de la LD es oscura; sin embargo, se ha descrito que la ectasia vascular en el antro está asociada en su génesis a los siguientes trastornos:3
Trastornos de la motilidad antral (hiperplasia muscular).
Disminución del flujo sanguíneo del antro en comparación con el fondo.
Presencia de células neuro-endócrinas.
Trombosis espontánea y ruptura de la arteria. También se ha querido explicar la LD a través de la teoría de Scott-Boyle (obstrucción intermitente del drenaje venoso).5 La LD puede permanecer silente por muchos años. Entre las causas que pueden precipitar sangrado, están los traumas a los que la mucosa gástrica es objeto, por ejemplo: prolapso de la mucosa del antro gástrico hacia el píloro, contracciones intensas frecuentes, gastritis reactiva y otros mecanismos que comprometen la pared del vaso.6
Existen varios diagnósticos diferenciales de hemorragia digestiva superior además de la LD (Tabla 1).7
La localización más común es en el estómago, con presencia de lesiones a seis u ocho centímetros del cardias, en su mayoría. Esto puede ser debido al hecho de que el aporte de flujo arterial en ésta área emerge directamente de la arteria gástrica izquierda. La LD es responsable de 2% de las hemorragias gastrointestinales altas y se encuentra en 1% a 2% de los pacientes llevados a cirugía por sangrado de tubo digestivo alto. La LD es difícil de identificar y comúnmente se requiere de una endoscopia de repetición.7
En otros casos, la angiografía, la cirugía, la broncoscopia y la tomografía computarizada multi-detector, ofrecen apoyo para el diagnóstico en un caso de LD en recto.8,9
La ecoendoscopia, ha sido señalada como un recurso tecnológico útil que puede apoyar en el diagnóstico de ésta entidad, ya que se localiza con gran exactitud el vaso submucoso.4 Otros sitios de localización de LD menos frecuentes son: intestino delgado, colon, recto y bronquios.8,9
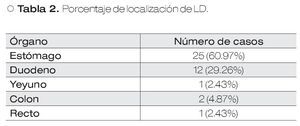
En un estudio realizado por Ibañez y colaboradores,10 revisaron de forma retrospectiva todos los casos de hemorragia digestiva por LD entre los años 2000 y 2006; identificaron 41 pacientes: 26 hombres y 15 mujeres. En este estudio, la LD fue la causa de 1.55% de los casos de hemorragia digestiva aguda. La incidencia de hemorragia digestiva por LD fue de 2.2 casos por cada 100 000 habitantes por año. La localización más frecuente fue: el estómago (61%), seguida del duodeno (29%) (Tabla 2).10 La mayoría de éstos pacientes presentaron hemorragia activa en el momento de la endoscopia (85%). En este estudio, se documentaron como co-morbilidades frecuentes a la hipertensión arterial, seguida de insuficiencia renal crónica y enfermedad pulmonar obstructiva crónica.
En otros estudios se han descrito otras comorbilidades asociadas como: enfermedad de von Willebrand, enfermedades cardiacas (estenosis aórtica, enfermedad vascular y cardiomiopatía isquémica congestiva), poliposis intestinal, colestásis intrahepática, trastornos autoinmunes, páncreas ectópico, diabetes mellitus tipo 2, tirotoxicosis, atrofia gástrica y en algunos casos cirrosis hepática.10
Por histología, en la LD se ha encontrado: hipertrofia y arterias tortuosas a nivel de la submucosa; también, se ha descrito ectasia vascular del antro gástrico, hiperplasia foveolar, presencia de capilares dilatados debajo de la submucosa, trombos e hiperplasia de la lámina propia.3,6
El cuadro clínico habitualmente está enmarcado en hemorragia digestiva que incluso llega a pérdidas de volemia del orden de la clase II a IV del American College of Surgeons. Esta enfermedad es de inicio súbito, con episodios intermitentes e indoloros de sangrado del tubo digestivo alto. En una serie de revisión de 177 casos, 28% de los pacientes presentó hematemesis, 51% estaba acompañada de melena y 18% sólo de melena.1
Tratamiento
Al igual que en otras condiciones de hemorragia de tubo digestivo, una parte fundamental para el tratamiento, incluye la reposición volumétrica aguda y el monitoreo de las constantes vitales.11
Si la lesión está documentada por endoscopia, se debe hacer el intento de lograr hemostasia a través de este método, utilizando técnicas como electrocoagulación multipolar endoscópica, heater probe, fotocoagulación con laser, inyección con adrenalina, hemo-clips, ligadura con banda, argón plasma, inyección de polidocanol o etanolamina, cirugía y angiografía con embolización selectiva. Los dos últimos métodos se recomiendan en pacientes con inestabilidad hemodinámica, que impida el intento endoscópico para diagnóstico y tratamiento así como para los pacientes con fracaso diagnóstico y terapéutico endoscópico.
En la revisión realizada por Reilly y Al-Kawas, se trataron 79 casos por vía endoscópica y se logró hemostasia permanente con la endoscopia inicial en 85% de los casos. Del resto de los pacientes (15%), en ocho se logró hemostasia definitiva con la segunda endoscopia.12
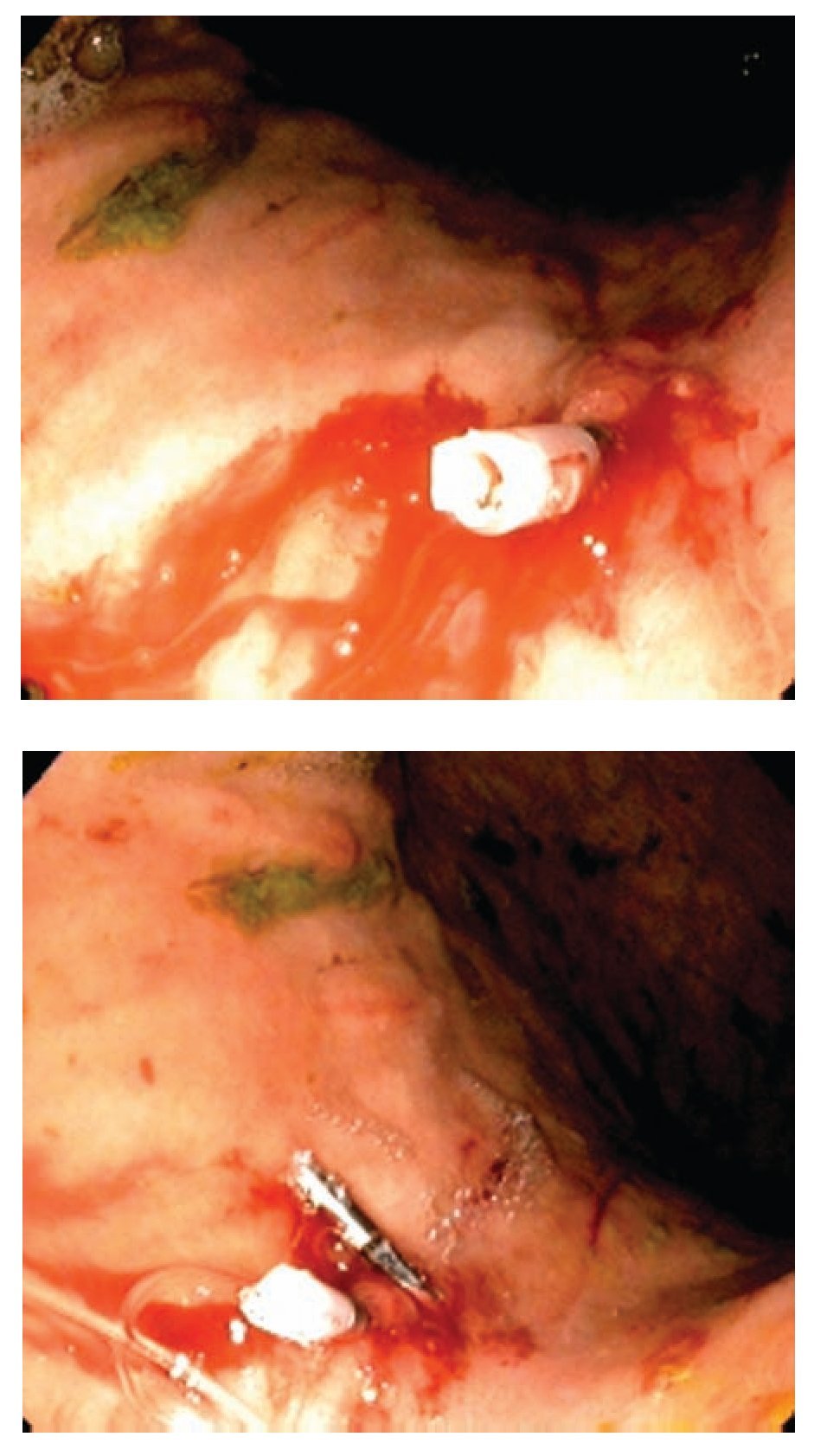
En el estudio de Ibañez y colaboradores, se utilizaron cinco técnicas diferentes para lograr hemostasia. La técnica más frecuentemente usada fue inyección con adrenalina combinada con argón plasma. También se usó la inyección con adrenalina sola o en combinación con polidocanol o etanolamina. En 6.8% de los casos se utilizó la inyección combinada con hemoclips y la coagulación con argón sola en 4.5% de los pacientes (Figuras 5 a 8).10 La hemostasia primaria se logró en 100% de los casos, con recurrencia de 7.3%; no se requirió tratamiento quirúrgico en ningún caso. En éste estudio, los tres casos con recurrencia fueron pacientes tratados inicialmente con inyección endoscópica exclusivamente. El porcentaje de recurrencia para la inyección endoscópica es de 27% vs 0% para el resto de las técnicas endoscópicas. Este fenómeno de recurrencia ha sido explicado por falla en la trombosis definitiva del vaso arterial de gran calibre.13 El tatuaje endoscópico previo a la cirugía y la endoscopia transoperatoria son dos factores a considerar como coadyuvantes del tratamiento quirúrgico. La mayoría de los cirujanos prefieren realizar una resección amplia en cuña, ya que se ha visto que la ligadura simple o con suturas transfrictivas tiene un alto índice de recidiva hemorrágica.
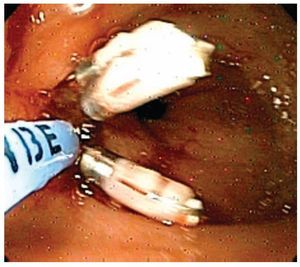
Figura 5. Utilización de hemoclips
Figura 6.Hemoclips mas argón plasma.
Figuras 7 y 8. Detalle de los Hemoclips.
Conclusiones
La LD es una entidad que potencialmente pone en peligro la vida y debe ser sospechada en pacientes con inicio súbito de sangrado digestivo o episodios recurrentes del mismo. Existen métodos útiles para su diagnóstico y terapia multimodal endoscópica, quirúrgica o angiográfica.
Aún se necesitan estudios controlados y de grandes series de casos para definir de manera más precisa el mejor abordaje endoscópico para el tratamiento de la LD. La experiencia del endoscopista y los recursos materiales disponibles influyen en forma directa con el la eficacia en el diagnóstico, tratamiento y sobrevida de los enfermos con esta patología.
Correspondencia: Dr. Carlos Benjamín González Sánchez.
Camino a Sta. Teresa 1055. Consultorio 817, Torre Ángeles. Col. Héroes de Padierna. México, D. F. 10700. Delegación Magdalena Contreras.
Correo electrónico:carlosbenjamings@hotmail.com