La colonoscopia es el método recomendado para la prevención del cáncer colorrectal. La visualización y evaluación óptima de la mucosa dependen de una adecuada preparación colónica. El método ideal de preparación del colon debe ser seguro, bien tolerado y efectivo, sin embargo ninguna de las opciones actuales cumple todas estas características. El Polietilenglicol (PEG) y el Fosfato Sódico (FS) son las dos soluciones más utilizadas, ya sean solas o asociadas a otro fármaco para mejorar la calidad de la preparación y su tolerabilidad. Ambas han demostrado ser efectivas. El FS es mejor tolerado, mientras que PEG es más seguro. El FS se ha asociado a falla renal aguda por fosfatos y alteraciones electrolíticas severas por lo debe usarse con precaución en pacientes con riesgo. Este artículo revisa las diferentes opciones de preparación previo a la realización de una colonoscopia.
Colonoscopy is the recommended method for colorrectal cancer (CCR) screening. Proper visualization and optimal evaluation of colonic mucosa depend on adequate cleansing The ideal bowel cleansing method should be safe, well tolerated and effective. However, none of those presently available meet these characteristics. Polyethyleneglycol with electrolytes (PEG) and Sodium Phosphate (FS) are the most commonly used bowel preparations, either alone, or associated with another drug to enhance their tolerability and cleansing capacity. Both have shown to be effective. FS preparation is better tolerated, while PEG is safer. FS has been associated with acute phosphate nephropathy and with severe electrolyte disturbances so it must be used with caution in patients at risk. This article reviews the options for bowel cleansing before colonoscopy.
Introducción
La colonoscopia es la estrategia preferida y recomendada para la prevención del cáncer colorrectal (CCR) mediante la detección oportuna de lesiones premalignas.1 La preparación colónica es fundamental para la evaluación óptima de la mucosa, se estima que alrededor del 20% de las colonoscopias tienen una preparación inadecuada. Lo anterior se asocia a varios eventos adversos, entre los que están: evaluación incompleta de la mucosa, incremento del tiempo del procedimiento, mayor número de complicaciones, malestar del paciente por exceso de insuflación, menor detección de adenomas, etc.2 El Colegio Americano de Gastroenterología y la Sociedad Americana de Endoscopía Gastrointestinal definen como "inadecuada" a una preparación colónica, si no permite visualizar pólipos menores de 5mM.3 Varios estudios retrospectivos, han demostrado que la disminución del riesgo para la incidencia y mortalidad por cáncer de colon, se ha mantenido sin cambios en los tumores que afectan el colon derecho. Si bien este fenómeno es multifactorial, es posible que la inadecuada preparación sea uno de los principales implicados.4,5
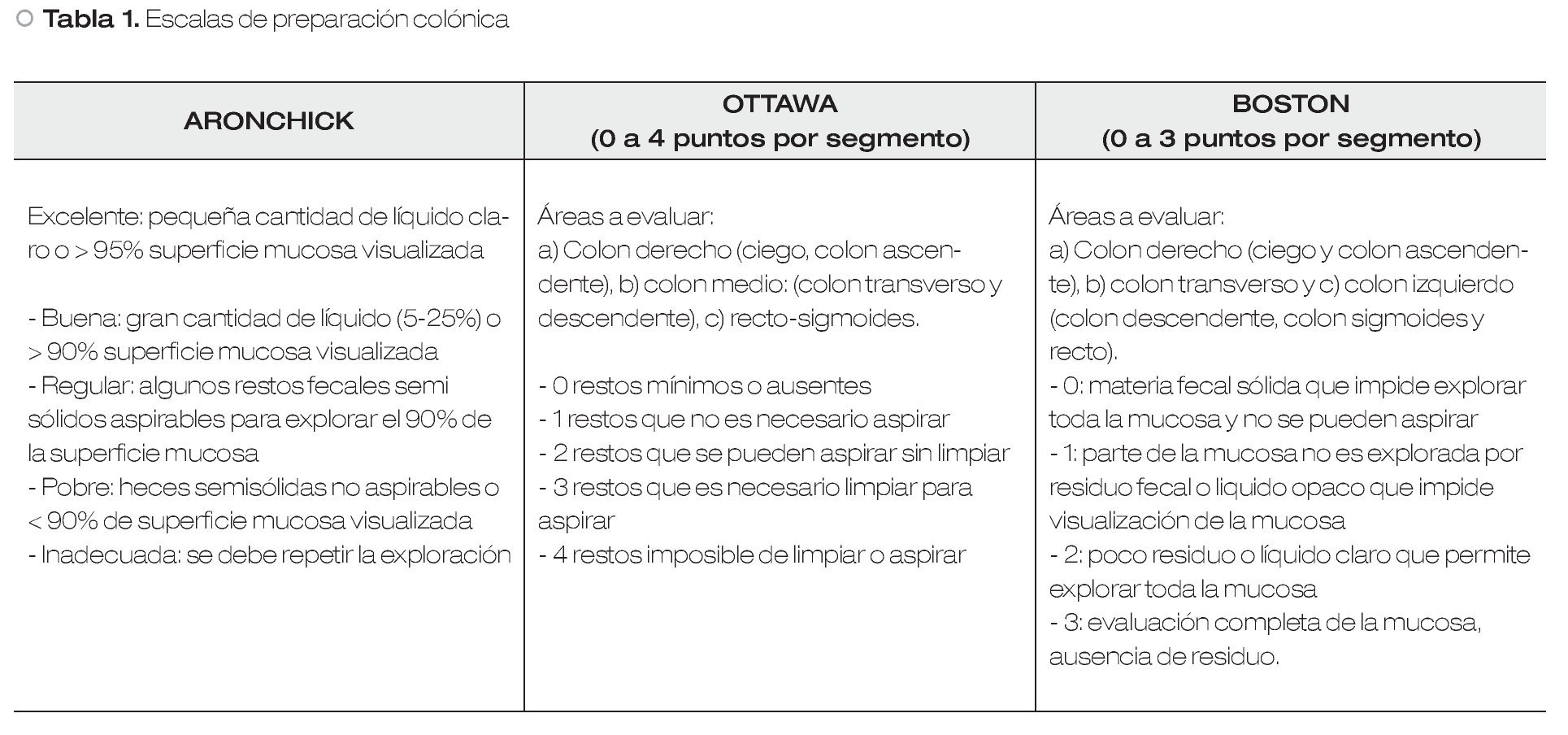
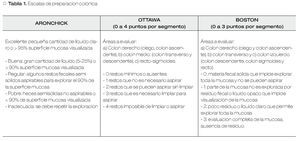
La calidad de la preparación debe ser evaluada y documentada de manera rutinaria, en el reporte del procedimiento.6 Desafortunadamente, esta evaluación no es uniforme pues existen varios sistemas de calificación. Los tres más utilizados son: Aronchick, Ottawa y Boston (Tabla 1). Todas han sido validadas y han mostrado confiabilidad interobservador (kappa > 0.7). Una de las ventajas de las escalas Ottawa y Boston, es que evalúan la preparación colónica dividiendo al colon por segmentos (colon derecho, transverso y colon izquierdo). De todas ellas, la que parece más sencilla de aplicar en la práctica cotidiana es la de Boston, pues sus variables a evaluar son menores y más sencillas de memorizar.7-9
Es difícil predecir que pacientes tendrán una preparación inadecuada, sin embargo se ha asociado a: pacientes hospitalizados, procedimientos matutinos tardíos, periodos largos entre última ingesta preparación e inicio de la colonoscopia, falta de apego a las instrucciones por parte del paciente, género masculino, constipación habitual, cirrosis, diabetes, uso de antidepresivos tricíclicos, demencia, enfermedad vascular cerebral, entre otros.2
En general, los pacientes consideran a la preparación colónica como la peor parte del proceso, lo cual es una limitante principal para que acepten su realización inicial y posteriores procedimientos periódicos en caso necesario.10 Las preparaciones iniciales para colonoscopia, fueron adoptadas de aquellas realizadas por los cirujanos, en pacientes sometidos a procedimientos abdominales o radiológicos. Originalmente incluían restricción dietética, así como la administración de laxantes y enemas, además de ayuno.11 Estas preparaciones intestinales, requerían la ingesta de un gran volumen de líquido (siete a 12 litros) durante varios días, lo cual generaba poca tolerancia, además de ganancia de peso por retención hídrica y alteraciones electrolíticas. Por esta razón, se fueron desarrollando soluciones osmóticamente balanceadas, en un afán de disminuir la cantidad del preparado a ingerir.12 Una de las primeras, fueron aquellas que contenían Manitol. Éste es un oligosacárido no absorbible, que ejerce un efecto osmótico intraluminal sin generar alteraciones hidroelectroliticas.13 El problema principal es que, al no ser absorbido, es fermentado por las bacterias del colon generando gas metano e hidrógeno, con el consecuente riesgo de explosión.14 Posteriormente, se fueron desarrollando soluciones más seguras como son las osmóticas no fermentables, tales como el Polietilenglicol (PEG) y el Fosfato Sódico (FS).
Hoy en día, éstas representan las dos soluciones más utilizadas existiendo múltiples esquemas de administración y combinación entre ellas. Así mismo hay otros métodos entre los que se encuentra la restricción dietética asociada a catárticos.15 Es indispensable que el médico gastroenterólogo y/o endoscopista, se encuentre familiarizado con las opciones existentes para preparación colónica, así como su dosificación, tolerabilidad, seguridad y efectividad.
Polietilenglicol
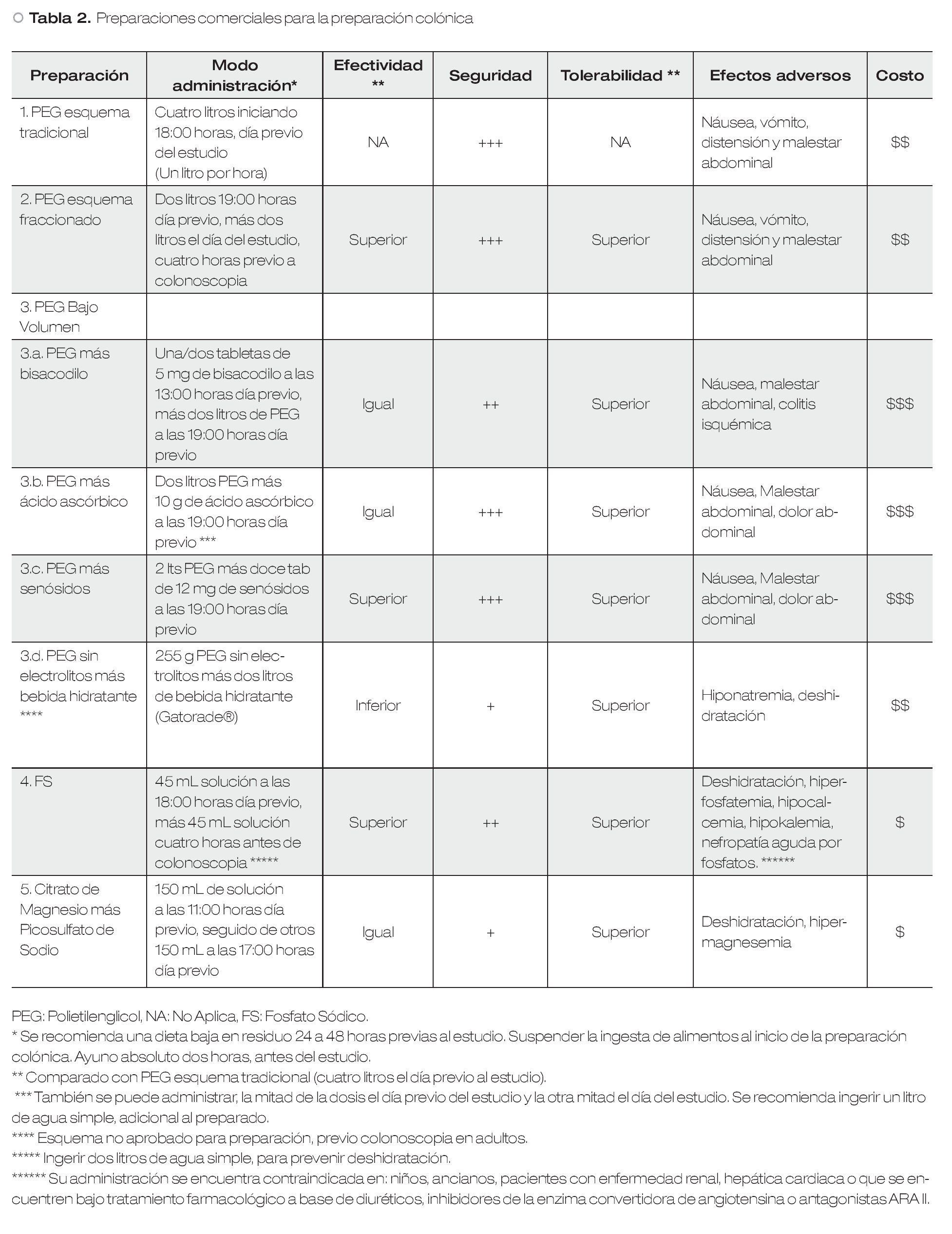
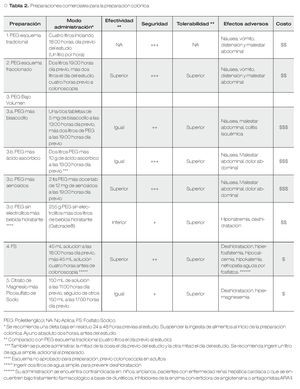
El PEG es una molécula inerte con alto peso molecular (3350 daltons), que se disuelve completamente en cualquier solución. La fórmula original desarrollada a mediados de los ochentas incluía PEG, electrolitos y sulfato de sodio, para lograr un balance osmótico (Golytely®). Esto permite que la preparación, pase a lo largo del tracto gastrointestinal sin ocasionar absorción o secreción neta de líquidos o electrolitos. En general es bastante segura, y debido a que no existe fermentación, el PEG no produce gases combustibles.16 Existen múltiples presentaciones comerciales que varían en la composición (Tabla 2).
Los estudios iniciales mostraron amplia superioridad del PEG en dosis de cuatro litros, la tarde previa al estudio, comparado con los métodos previamente utilizados (restricción dietética, catárticos, laxantes) logrando así un mayor porcentaje de limpieza excelente-buena (92 vs 69%).17
PEG libre de sulfato (PEG-SF)
El PEG-SF (Nulytely®) es posiblemente, la preparación más difundida en nuestro medio. Su característica principal es la ausencia del sulfato de sodio. Esto se hizo con la intención de disminuir el sabor salado y el olor desagradable, haciendo más tolerable su ingesta. Existen además presentaciones saborizadas artificialmente (cereza y limón).18 Su efectividad y seguridad para limpieza colónica, no es diferente a Golytely® y los pacientes refieren menos náusea que su similar sulfatado.19
Desafortunadamente, la preparación con PEGSF requiere la ingesta de cuatro litros, lo cual se ha asociado a pobre tolerabilidad y mal apego, por parte del paciente. Los efectos adversos más comunes son náusea, vómito, sensación de plenitud y distensión abdominal.20 Tradicionalmente se ha recomendado ingerir la totalidad del preparado, el día previo al estudio. Sin embargo, no existe un argumento científico fundamentado. Recordemos que la preparación para colonoscopia, inició imitando aquella de los pacientes que serían sometidos a procedimientos quirúrgicos abdominales y que necesitaban ayuno prolongado, razón por la cual recibían la totalidad de la preparación la tarde previa.
PEG: esquema fraccionado "split dose"
En los años noventas, fueron realizados estudios en busca de lograr una mejor tolerabilidad, por lo que la dosis de la preparación fue fraccionada (dos litros el día previo más dos litros cuatro a seis horas antes del estudio). Interesantemente, este esquema fraccionado, logró mejor tolerabilidad, apego y mayor tasa de detección de adenomas y lesiones planas en la mucosa colónica, en comparación con el esquema tradicional (cuatro litros día previo al estudio).21-23 Un meta-análisis reciente ha confirmado lo anterior.24
Pese a la evidencia a favor, la dosis fraccionada no es muy utilizada por temores poco fundamentados. Uno de ellos, es que la dosis matutina del esquema fraccionado, pudiera contraindicar la sedación por posibilidad de un residuo gástrico alto, con riesgo de broncoaspiración para el paciente. La Sociedad Americana de Anestesiología permite un periodo de ayuno de dos horas para líquidos claros y seis horas para comidas ligeras, previo a una sedación.25 Un estudio prospectivo y aleatorizado, no encontró diferencia en la cantidad de residuo gástrico entre pacientes con ayuno de dos horas vs. ayuno mayor de seis horas (19mL vs. 21 mL).26
Otro de los temores por parte de los médicos y pacientes, es que la dosis ingerida el día del estudio, genere evacuaciones inesperadas o involuntarias durante su trayecto al hospital. Estudios aleatorizados no han encontrado diferencia. en la necesidad de evacuar durante el trayecto al hospital (16.3% vs. 9.1%, valor p no significativo).27
PEG: Esquema de bajo volumen
Debido a la necesidad de ingerir gran volumen de los preparados con PEG, para lograr una adecuada limpieza, se han desarrollado estrategias de preparación con menor volumen (dos litros).
PEG más bisacodilo
Consiste en dos litros de PEG, asociado a bisacodilo. El bisacodilo es un derivado de difenilmetano, con pobre absorción en intestino delgado. Es hidrolizado por esterasas endógenas, liberando su metabolito activo que estimula la motilidad colónica.20 Se recomienda ingerir el bisacodilo, seis horas antes de los dos litros de PEG, el día previo a la colonoscopia. Se ha estudiado la dosis ideal del bisacodilo, estableciendo mayor tolerabilidad y menores molestias gastrointestinales (náusea, dolor), con dosis de 10 mg vs. 20 mg.28
Existe una preparación comercial que incluye dos litros de PEG-SF, combinado con bisacodilo (Halflytely®). Es importante mencionar que la dosis de bisacodilo del Halflytely® fue reducida de 20 mg a 5 mg debido a reportes de colitis isquémica, con dosis de 20 y 10 mg.29 Cuando PEG-SF más bisacodilo, se ha comparado con la preparación tradicional de cuatro litros de PEG-SF, no se ha demostrado inferioridad en la capacidad de lograr una limpieza excelente-buena.28
PEG más ácido ascórbico
Los dos litros de PEG están asociados a 10.6g de ácido ascórbido (MoviPrep®). El ácido ascórbico es absorbido, solo en un 10% por el intestino proximal, y el resto genera un gradiente osmótico potenciando el efecto del PEG. Además, mejora el sabor e inhibe la reproducción bacteriana y por ende, la producción de gas.20 Si bien la mezcla final del preparado es de dos litros, el paciente requiere ingerir un litro adicional de agua simple. La ingesta en una sola toma se asocia a malestar y retortijones, por lo que se recomienda dar la mitad el día previo al examen y el restante, el día del estudio. Existen dos estudios, que comparan este esquema con el tradicional de cuatro litros de PEG. Ambos han demostrado eficacia similar y mejor tolerabilidad de PEG más ácido ascórbico.30.31
PEG más senósidos
Los senósidos son derivados de las antraquinonas. Su efecto laxante es producto de la estimulación de la motilidad intestinal e inhibición de la reabsorción de agua y electrolitos.20 Han sido utilizados incluso sin asociación a PEG en dosis altas (24 tabletas de 12 mg fraccionadas), mostrando superioridad en la calidad de preparación, en comparación con PEG-SF, cuatro litros esquema tradicional.32
Un estudio reciente comparó dosis alta de senósidos, 24 tabletas de 12 mg vs. dos litros PEG-SF, más 12 tabletas de senósidos. No hubo diferencia, en la calidad de la preparación entre ambos grupos (excelente/buena 90%).33 El inconveniente para dosis alta de senósidos, es la producción de cólicos intensos.
PEG sin electrolitos más bebida hidratante
PEG sin electrolitos (Miralax®) está aprobada por la FDA, como tratamiento para el estreñimiento y para preparación colónica en niños.34 Esto generó interés para probar su efectividad en adultos.23 El preparado es un compuesto de 255 g de PEG, sin electrolitos (Miralax®), asociado a dos litros de una bebida hidratante (Gatorade®). En relación a eficacia y tolerabilidad, un estudio reciente demostró inferioridad de dos litros del preparado con MiraLAX®, dosis fraccionada vs. cuatro litros de PEG sulfatado (Golytely®), administrado el día previo al estudio.35 En cuanto a la seguridad, el compuesto de PEG sin electrolitos más bebida hidratante, no es iso osmótico sino más bien hipotónico, existen reportes de casos de hiponatremia sintomática asociada.36 A la luz de la evidencia actual, en cuanto a efectividad y seguridad, este esquema no deberá seguir siendo utilizado.
Fosfato de Sodio (FS)
El FS surgió como una alternativa de preparación con bajo volumen. Es una molécula osmóticamente activa, que genera movimiento de agua y electrolitos del plasma a la luz intestinal, favoreciendo así la limpieza digestiva. Existen dos presentaciones: solución y tabletas.20
La forma líquida se desarrolló en los noventas (Fleet®, Fosfosoda®), contiene 45mL con 29.7g de FS. El régimen de preparación clásico, consiste en la ingesta de 45mL del preparado de FS la tarde previa, y 45mL el día del estudio cuatro a seis horas antes de la colonosocopia. Se recomienda de manera adicional complementar cada ingesta de la solución de FS, con un mínimo de 500mL de agua simple por toma.37
En la presentación en tabletas, cada una contiene 1.5g de FS. El régimen de preparación consiste en la ingesta de 40 o 32 tabletas (OsmoPrep®), en dosis dividida la tarde previa y el día del estudio. Se recomienda la ingesta de agua simple, en una cantidad aproximada de dos litros para prevenir deshidratación.38
Ambas presentaciones con FS han demostrado ser igual de efectivas que PEG. Un estudio europeo reciente, comparó la calidad de la preparación de la solución de FS con diferentes regímenes de PEG: 1) dosis tradicional (cuatro litros) y 2) esquema PEG de bajo volumen (dos litros más ácido ascórbico). La calidad de la preparación fue equivalente entre los grupos, aunque con una tolerabilidad discretamente mejor para la solución de FS (93% vs. 87%) (p=0.03).39 Sin embargo, un meta-análisis demostró que la tolerabilidad entre FS cuando se compara con PEG "split dose", es similar.40
Dado su característica hiperosmótica, una de las limitantes para el uso del FS es que puede causar alteraciones electrolíticas.20 Las evaluaciones iniciales demostraron que existia hiperfosfatemia, hipocalcemia e hipokalemia significativa hasta en el 20% a 40% de sujetos sanos, lo cual generó preocupación de su uso en pacientes con enfermedad cardiaca, renal y hepática.41 Posteriormente, aparecieron reportes sobre el particular riesgo de desarrollar una rara forma de nefropatía aguda asociada a fosfatos.42 Por este motivo la FDA anunció una alerta "black box warning", informando de este riesgo y prohibiendo su uso en niños, ancianos, pacientes bajo tratamiento con diurético, inhbidores de la ECA o antagonistas ARAII, así como en aquellos con enfermedad renal, cardiaca o hepática. Como consecuencia de estas restricciones, la empresa productora de FS en presentación líquida retiró su producto del mercado estadounidense, quedando disponible solo el FS en tabletas. En México, aún se comercializa la solución de FS.43
Otro inconveniente de los fosfatos son los cambios macro y microscópicos, que puede producir sobre la mucosa intestinal. Estos consisten en lesiones aftoides, que semejan aquellas de la enfermedad inflamatoria intestinal.44 Por tal motivo, se ha desaconsejado su uso como preparación en pacientes con sospecha de patología inflamatoria intestinal.45
Enemas
Estos eran parte de la preparación habitual en los pacientes, cuando aún no se desarrollaban soluciones actuales (PEG, FS). Su uso hoy en día, no está científicamente fundamentado.3 La evidencia existente demuestra, que los enemas no mejoran la calidad de la limpieza colónica. Tanto la calidad de la preparación, la visualización mucosa y el volumen de líquido retenido en el colon, no difiere al agregar enemas a la preparación oral con PEG, y por el contrario puede haber efectos negativos asociados a su uso, como son trauma anorectal, inflamación e incluso mayor rechazo a realizarse una colonoscopia subsecuente.46
Citrato de magnesio
El citrato de magnesio es un laxante osmótico. No ha demostrado ser efectivo como agente único en la preparación de colonoscopia, sin embargo se ha utilizado en asociación con un derivado del bisacodilo, el picosulfato de sodio. Este último es hidrolizado por las bacterias del colon, generando su metabolito activo ejerciendo efecto laxante estimulante.20 La combinación de ambos laxantes (Picolax®) se ha comparado con PEG y FS solución, mostrando ser igualmente efectivo con una tolerancia discretamente mejor a PEG en cuanto a náusea. La dosis utilizada de Picolax® es 150 mL, la mañana previa al estudio, y 150 mL seis horas después de la primera dosis.47.48
En lo que se refiere a seguridad, uno de los principales inconvenientes de esta opción, para preparación colónica es debida a su mecanismo de acción osmótico, que favorece deshidratación y alteraciones electrolíticas, particularmente en pacientes ancianos o con falla renal.20
Dieta
Las restricciones dietéticas por sí solas no son suficientes, sin embargo han demostrado su utilidad en combinación con PEG o laxantes.15 Las recomendaciones habituales, incluyen dieta con líquidos claros o dieta baja en residuo.
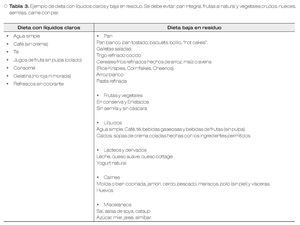
Los líquidos claros son aquellos alimentos, que son líquidos a temperatura corporal. Estos dejan poco residuo y son fáciles de absorber. Evitan una carga osmolar alta en el tracto gastrointestinal y por lo general, contienen carbohidratos pero poca proteína y grasa. Por otro lado, la dieta baja en residuo, se utiliza para reducir el tamaño y número de deposiciones. Si bien esta dieta es baja en fibra, técnicamente no significa lo mismo. La fibra es la parte no digerida de los vegetales y permanece en el tracto intestinal, contribuyendo al bolo fecal. El residuo incluye la fibra y cualquier otro tipo de alimento que pueda incrementar el bolo fecal.49
La evidencia científica es escasa para determinar el efecto de la dieta, sobre la calidad de preparación en la colonoscopia. Uno de los primeros estudios al respecto, fue realizado en la década de los ochentas, durante el desarrollo de los laxantes iso osmóticos. Este estudio, comparó la efectividad de laxantes estimulantes asociados a dieta con líquidos claros por tres días (grupo uno), dieta baja en residuo por uno y tres días (grupo dos y grupo tres, respectivamente) contra cuatro litros de PEG (grupo cuatro). Además de evidenciar una mejor calidad de preparación, en el grupo que utilizó PEG, este estudió mostró que la dieta baja en residuo por uno o tres días, era más efectiva, que la de líquidos claros, en lo que a limpieza colónica se refiere.17
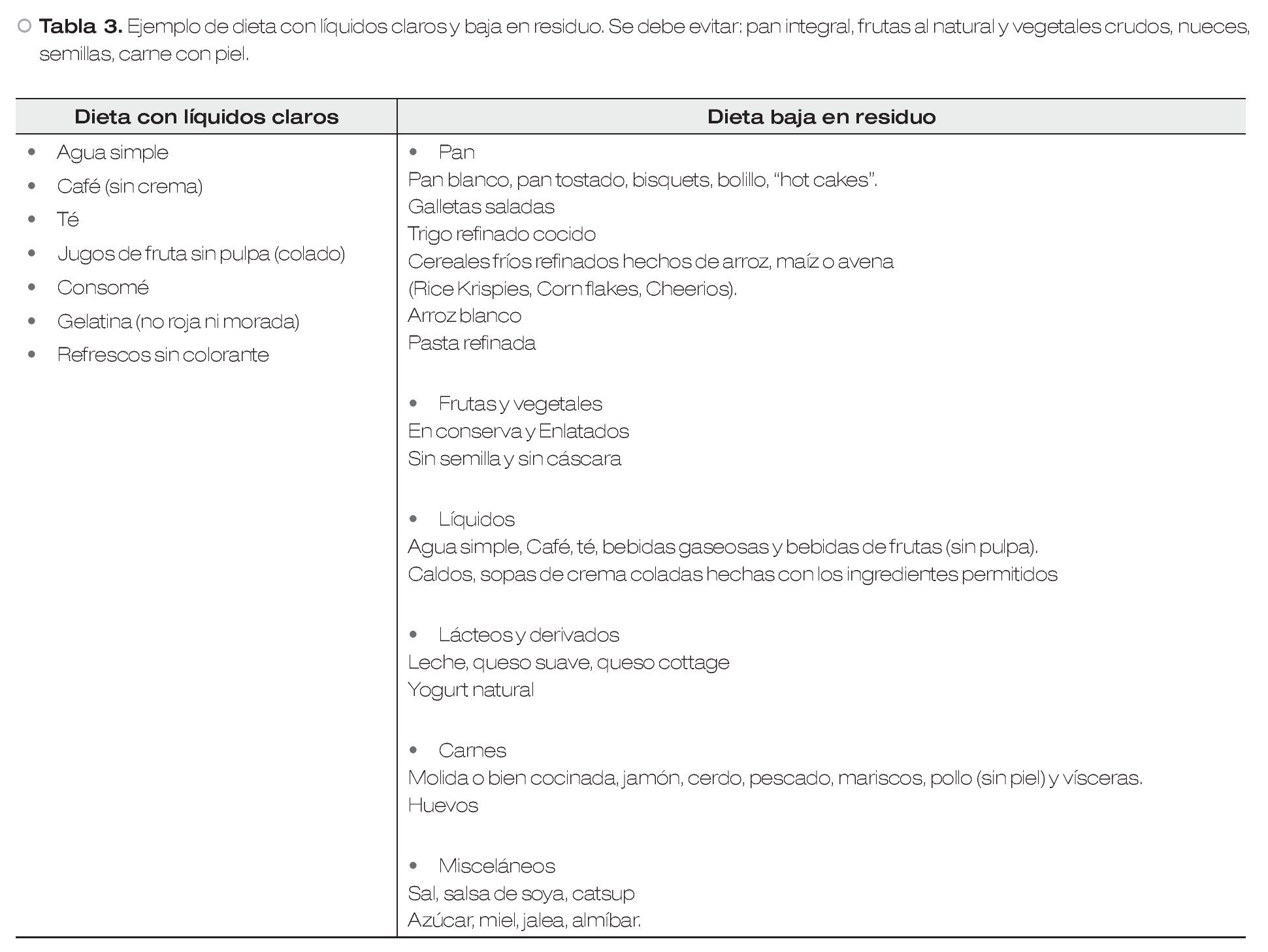
Un estudio reciente, evaluó el impacto de la dieta baja en residuo por dos días asociado a PEG cuatro litros, día previo al estudio. Los resultados nuevamente mostraron, una mejor calidad de la preparación con dieta baja en residuo, sin embargo evidenció una mala adherencia de los pacientes a este tipo de dieta (44%).50 Esto hace necesario poner énfasis en las instrucciones dietéticas dadas al paciente, previo al procedimiento (Tabla 3).
Preparación inadecuada
La preparación subóptima, ocurre en alrededor del 20% de las colonoscopias realizadas. Los predictores de mala preparación son: estreñimiento habitual, procedimientos matutinos tardíos, periodos largos entre última ingesta preparación e inicio de la colonoscopia, falta de apego a las instrucciones por parte del paciente, género masculino, constipación habitual, cirrosis, diabetes, uso de antidepresivos tricíclicos, demencia, enfermedad vascular cerebral, entre otros.2
En aquellos pacientes con preparación inadecuada, que son evaluados mediante realización de nueva colonoscopia, se reporta que la falla en la de detección de adenomas es del 40% para todos los adenomas y del 27% para adenomas avanzados.51
Por lo tanto, cuando ocurre un evento de este tipo, es importante determinar la causa de la preparación inadecuada. Se ha encontrado que en el 80% de los casos, se debe a que los pacientes no siguieron adecuadamente las instrucciones de preparación, por lo que el primer paso es repetir el procedimiento utilizando la misma preparación, haciendo énfasis en el paciente acerca de la importancia del apego a la misma. Se sugiere esperar un intervalo de 24 horas, para repetir el procedimiento en aquellos pacientes que hubieran utilizado preparaciones con efecto osmótico (FS, citrato de magnesio), por el mayor riesgo de toxicidad.52
Desafortunadamente, para el resto de los pacientes con preparación inadecuada, las recomendaciones son más bien empíricas con un nivel de evidencia bajo (reportes de caso),por lo tanto, lo más prudente es tomar la decisión, de acuerdo al problema de cada paciente en particular. Por ejemplo, si un paciente tuvo mala tolerancia a la preparación tradicional de cuatro litros, se puede optar por un esquema de bajo volumen con PEG o FS, si no hay contraindicación. En el caso de pacientes con mala preparación pese a buena tolerancia y apego, se puede dar mayor tiempo de preparación (48 horas), con dieta baja en residuo y esquema con PEG de bajo volumen asociado a laxantes.3
Conclusión
Existen múltiples métodos para la preparación colónica. Los dos más utilizados son PEG (asociado o no a laxantes) y FS. Ninguno de ellos, ha demostrado ser el ideal. Actualmente, los enemas no tienen fundamento científico que lo avale como preparación previo a colonoscopia. La dieta impacta positivamente sobre una mejor calidad de preparación, aunque el apego del paciente a ésta es malo. El análisis particular de cada caso, permitirá elegir el esquema de preparación y decidir que hacer cuando esta sea inadecuada.
Correspondencia: Dr. Enrique Murcio Pérez.
Departamento de Endoscopia. Instituto Nacional de Ciencias Médicas y Nutrición "Salvador Zubirán". Mexico D.F.
Teléfono: (525) 55487 0900, ext 2150.
Correo electrónico: murcio@hotmail.com.